Les biomarqueurs peuvent-ils contribuer au diagnostic?
Nos interlocuteurs:
Dr méd. Alexander Ritter
Klinik für Nephrologie und Transplantationsmedizin, Kantonsspital St. Gallen
PD Dr méd. Harald Seeger
Chefarzt Nephrologie, Kantonsspital Baden
Interview menée par Dre méd. Felicitas Witte
Journaliste médicale
La néphrite lupique est une atteinte d’organes fréquente et sévère du lupus érythémateux disséminé (LED). Les lésions des podocytes sont considérées comme l’un des facteurs essentiels. Les biomarqueurs urinaires, qui indiquent précocement les lésions, pourraient constituer une nouvelle méthode non invasive pour poser un diagnostic précoce et intervenir à temps, comme le montrent des chercheurs chinois dans un article de synthèse récemment publié (voir encadré).1
Que pensez-vous des biomarqueurs urinaires?
A. Ritter: Je pense qu’il est fondamentalement adéquat de rechercher de nouveaux biomarqueurs, car les biomarqueurs actuels, tels que la protéinurie, l’albuminurie, les auto-anticorps et les facteurs du complément, sont déficitaires pour évaluer l’activité et la chronicité de la maladie. Les résultats de la plupart des marqueurs présentés dans l’article de synthèse sont toutefois en partie très préliminaires et, de mon point de vue, les auteurs sont un peu trop euphoriques à l’heure actuelle. Un marqueur idéal est très sensible et spécifique, et fournit en outre des informations sur l’activité/la chronicité de la maladie ainsi que la réponse thérapeutique. De plus, il est facile à obtenir, stable dans l’analyse, bon marché et facilement disponible.
H. Seeger: La plupart des marqueurs individuels sont sans doute loin de répondre à ces exigences, car ils en sont encore au stade expérimental. De plus, les nouveaux marqueurs doivent se concurrencer la biopsie rénale, l’examen de référence, et des études prospectives longitudinales doivent démontrer qu’ils sont équivalents ou supérieurs. La pathologie touchant plusieurs compartiments et cellules rénaux, il est probablement judicieux de prendre en compte et de combiner différents marqueurs. L’étude ReBioLup2 devrait apporter de nouvelles informations à ce sujet. Dans cette étude, des prélèvements séquentiels de biopsie sont réalisés, et des échantillons de sérum et d’urine sont prélevés chez des patients atteints de néphrite lupique et conservés. Ces échantillons permettent de corréler les anciens comme les nouveaux biomarqueurs urinaires et sanguins avec les résultats histologiques et cliniques.
Quel est l’avantage des marqueurs podocytaires?
A. Ritter: L’un des problèmes réside dans le fait que ces marqueurs dépendent notamment du nombre de podocytes. Si un rein présente déjà une lésion glomérulaire chronique importante, le nombre de podocytes peut également être réduit et moins d’antigènes podocytaires peuvent être détectés dans l’urine. Cela peut signifier que, malgré une lésion persistante des podocytes, moins d’antigènes podocytaires sont présents dans l’urine. Il en résulte une valeur faible qui donne une fausse impression de sécurité.
En quoi la podocytopathie lupique diffère-t-elle d’une néphrite lupique «normale»?
H. Seeger: Un faible pourcentage, soit moins de 2%, des patients atteints de lupus avec protéinurie du syndrome néphrotique présentent une podocytopathie lupique, une forme particulière de néphrite lupique.3 Celle-ci est causée par une lésion des podocytes, caractérisée par une fusion des pédicelles des podocytes, comme on le connaît dans la forme à lésions minimes. Dans ce cas, ce ne sont pas les dépôts de complexes immuns qui sont au premier plan. Les causes évoquées sont des auto-anticorps dirigés contre les protéines au niveau de la membrane des fentes et une lésion des podocytes par des cytokines ou des lymphocytes T. La prise d’anti-inflammatoires non stéroïdiens est également associée à la podocytopathie.
Pensez-vous que les biomarqueurs urinaires s’imposeront dans la pratique de routine?
A. Ritter: L’urine peut être obtenue facilement, de manière non invasive et, par définition, de partout. Le problème réside toutefois dans les méthodes d’analyse parfois complexes utilisées pour déterminer les biomarqueurs mentionnés. Bien que l’urine soit une source facilement accessible, les périodes de stockage prolongées, les temps de collecte, la contamination bactérienne et la nécessité d’une correction pour la dilution peuvent affecter la qualité des échantillons d’urine et donc celle des biomarqueurs.
H. Seeger: Il convient de préciser que jusqu’à présent, seuls quelques biomarqueurs urinaires se sont imposés en néphrologie, en plus de la protéinurie et de l’albuminurie. Dans d’autres domaines également, comme la médecine de transplantation, de nombreux efforts ont été déployés en ce sens, sans succès. De nouvelles technologies et méthodes d’analyse se développent cependant rapidement, il existe donc un espoir fondé.
A. Ritter: Je suis d’avis que les marqueurs podocytaires peuvent constituer un complément utile, notamment en combinaison avec des marqueurs d’inflammation et de fibrose. Il convient en outre de déterminer les marqueurs des lésions causées à d’autres cellules, telles que les cellules endothéliales glomérulaires et les cellules d’autres compartiments rénaux. Les marqueurs podocytaires seuls ne répondent probablement pas aux exigences d’un biomarqueur de qualité. Des recherches sur d’autres biomarqueurs sont déjà menées; à cet égard, je peux recommander un très bon article de synthèse de Brad Rovin et ses collègues.4
Quel est l’avenir du diagnostic précoce?
A. Ritter: Il n’y a pas vraiment de corrélation entre le système de classification histologique actuel de l’International Society of Nephrology/Renal Pathology Society (ISN/RPS) et les modèles d’expression génique. L’histologie ne semble donc pas être apte à bien refléter l’hétérogénéité des glomérulonéphrites lupiques. Je pense que les analyses moléculaires des tissus issus de la biopsie rénale pourraient jouer un rôle important à l’avenir – complétées par des biomarqueurs urinaires et sériques conventionnels et nouveaux.
H. Seeger: Sur cette base, un traitement ciblé pourrait alors être mis en place, à l’instar du traitement personnalisé des tumeurs en oncologie.
Les biomarqueurs vont-ils remplacer la biopsie rénale?
A. Ritter: Non, car une analyse moléculaire des tissus permettra probablement des approches thérapeutiques différenciées et ciblées. Des biomarqueurs appropriés, qui fournissent des informations fiables sur l’activité et la chronicité de la maladie ou le risque de récidive, sont toutefois un complément important et contribuent alors à un diagnostic précoce et à la gestion du traitement. D’ici là, un gros effort de recherche doit toutefois encore être fourni. Il est possible que les biomarqueurs nous permettent d’éviter les biopsies de progression.
Pourrons-nous réparer les lésions des podocytes à l’aide de médicaments ciblés et guérir ainsi la néphrite lupique?
H. Seeger: Les lésions ne se limitent pas aux podocytes, mais concernent également le mésangium, les cellules endothéliales et la membrane basale. Les lésions des podocytes sont généralement secondaires. Une telle approche serait uniquement pertinente en cas de podocytopathie lupique. Toutefois, les corticoïdes et/ou les inhibiteurs de la calcineurine ainsi que le traitement de la maladie sous-jacente – par exemple, par l’hydroxychloroquine et, le cas échéant, le mycophénolate – permettent généralement de bien les maîtriser. Je considère surtout le traitement des podocytes comme un traitement complémentaire dans le cadre d’une stratégie multimodale.
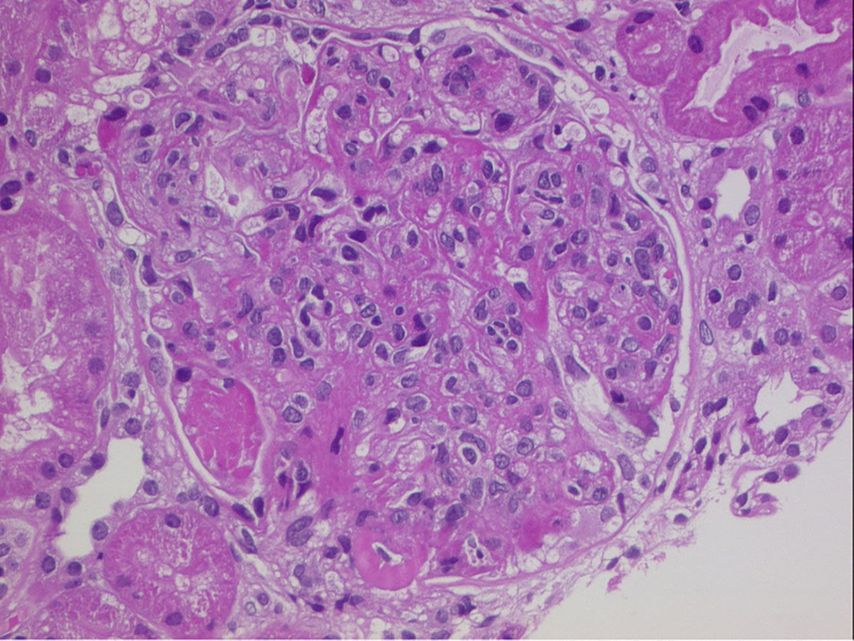
Fig. 1: Coloration HE: glomérule avec modifications typiques d’une néphrite lupique proliférative (hypercellularité mésangiale et endocapillaire, dépôts sous-endothéliaux et thrombus hyalins)
Comment procédez-vous dans la pratique?
A. Ritter: Une néphrite lupique est suspectée en cas de sédiment urinaire actif, de protéinurie et/ou de diminution du débit de filtration glomérulaire. Des titres élevés d’anticorps anti-ADNdb et une consommation de complément (C3, C4) indiquent une néphrite lupique. La sensibilité de la protéinurie pour l’activité histologique est bonne, celle des autres paramètres l’est moins. En revanche, la spécificité de ces marqueurs conventionnels est moins bonne. Par exemple, la protéinurie peut être élevée, d’une part, en cas de lésions rénales chroniques sans néphrite lupique active et, d’autre part, en cas de néphrite lupique active. Les anticorps anti-ADNdb et la consommation du complément sont des marqueurs modérément efficaces pour déterminer l’activité de la néphrite lupique. Ils sont encore moins appropriés pour évaluer la réponse thérapeutique des patients et le pronostic.
H. Seeger: Ces marqueurs sont néanmoins utilisés de manière combinée pour le suivi. Une biopsie rénale est importante pour confirmer le diagnostic, définir la classification de la néphrite lupique selon l’ISN/RPS, évaluer l’activité et la chronicité de la maladie, et exclure d’autres causes. Le tableau clinique seul ne reflète pas toujours la sévérité de la maladie.
Quand une biopsie est-elle indiquée?
A. Ritter: Conformément aux directives EULAR/ERA-EDTA et KDIGO5,6, la biopsie doit certainement être réalisée en présence d’une protéinurie supérieure à 500mg/j, de sédiment actif ou d’une augmentation inexpliquée de la créatinine. La prudence est néanmoins de mise chez les patients dont la protéinurie est <500mg/j mais ≥200mg/j. Ils doivent faire l’objet d’une surveillance étroite, car une progression avec augmentation de la protéinurie >500mg/j a été mise en évidence chez un patient sur deux dans les deux ans.7 De plus, il a été démontré qu’une proportion significative de patients atteints de LED avec protéinurie <500mg/j présentent une néphrite lupique proliférative de classe III, voire IV.4 C’est pourquoi je préconise dans certains cas aussi la réalisation d’une biopsie chez les patients présentant une protéinurie élevée persistante, mais qui reste <500mg/j, même si le débit de filtration glomérulaire est normal. Ceci est particulièrement important, car un traitement précoce en cas de néphrite lupique contribue à prévenir les lésions chroniques et permet également un traitement moins agressif.
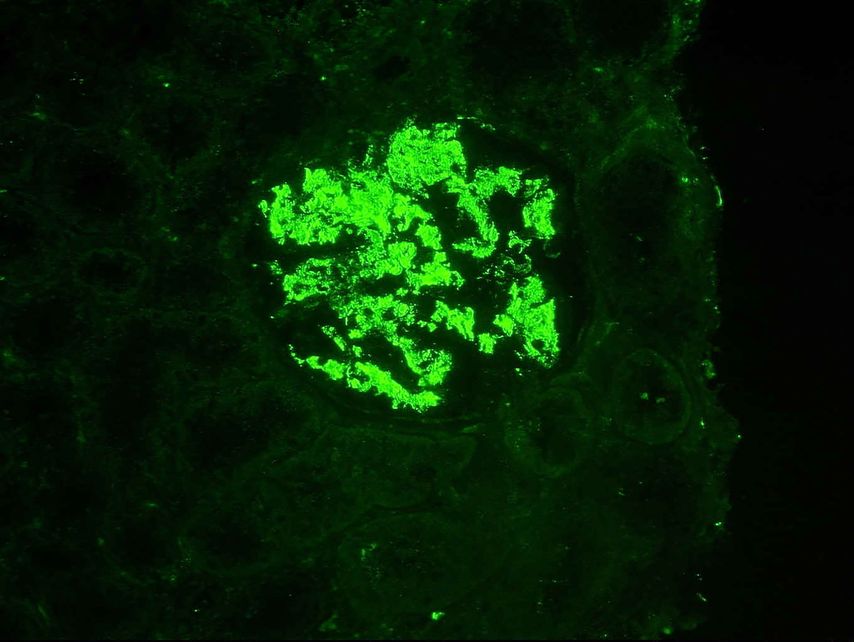
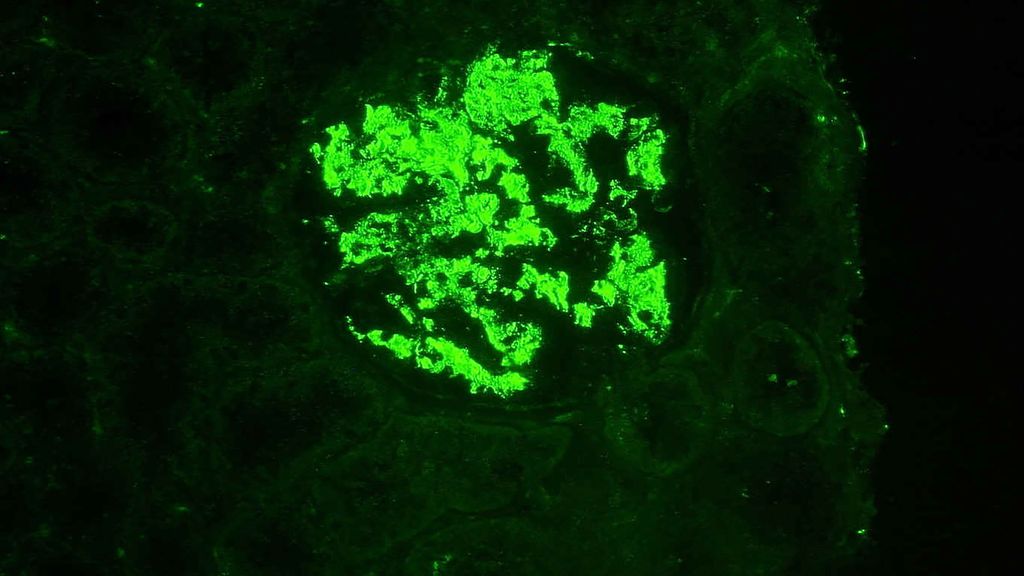
Fig. 2: Immunofluorescence: dépôts glomérulaires étendus du composant C1q du complément chez un patient atteint de néphrite lupique proliférative
Quelle est la durée de traitement de la néphrite lupique?
H. Seeger: Il est recommandé de traiter une néphrite lupique proliférative (classe ISN/RPS III/IV±V) pendant au moins trois ans, y compris le traitement d’induction initial. Il convient de réaliser une biopsie rénale avant de décider d’un arrêt du traitement, car le tableau clinique et l’histologie ne coïncident pas toujours, et elle permet d’évaluer le risque de récidive, notamment à l’aide de l’indice d’activité des National Institutes of Health (NIH),8 même si la pertinence de ces biopsies de progression n’a pas encore été prouvée par des essais randomisés contrôlés. Il ne faut pas oublier de surveiller attentivement les effets secondaires. Le traitement par des corticoïdes, en particulier, contribue à des séquelles à long terme, raison pour laquelle les glucocorticoïdes doivent être administrés à faible dose, le cas échéant, et arrêtés dès que possible. Les traitement combinés modernes par le belimumab ou la voclosporine, qui sont actuellement disponibles, permettent de réduire les corticoïdes sans augmenter les effets secondaires et sans diminuer l’efficacité du traitement. Au contraire, une trithérapie combinant la voclosporine au traitement de première ligne par des corticoïdes et du mycophénolate, ou combinant le belimumab au cyclophosphamide ou au mycophénolate et aux corticoïdes offre une chance significativement plus élevée de rémission complète ou partielle de la néphrite lupique.9,10
Littérature:
1 Guo Z et al.: Urinary biomarkers associated with podocyte injury in lupus nephritis. Front Pharmacol 2024; 15: 1324540 2 https://rebiolup.com 3 Hu W et al.: Clin J Am Soc Nephrol 2016; 11: 585-92 4 Mejia-Vilet JM et al.: Kidney Int 2022; 101: 242-55 5 Fanouriakis A et al.: Ann Rheum Dis 2020; 79: 713-23 6 Kidney Disease: Kidney Int 2024; 105(1S): S1-69 7Wang S et al.: Clin J Am Soc Nephrol 2022; 17: 1150-8 8 De Rosa M et al.: Kidney Int 2018; 94: 788-94 9 Furie R et al.: N Engl J Med 2020; 383: 1117-28 10 Rovin BH et al.: Lancet 2021; 397: 2070-80 11 Aringer
M et al.: Arthritis Rheumatol 2019; 71: 1400-12
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...