Behandlung der Sigmadivertikulitis
Autor:innen:
Prof. Dr. med. Robert Rosenberg,
FACS, Executive MBA
Francesca Cordera
Klinik Chirurgie & Viszeralchirurgie
Kantonsspital Baselland
Liestal
E-Mail:
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Divertikulitis gehört zu den häufigsten Krankheitsbildern bei akuten Bauchschmerzen. Die Inzidenz nimmt mit dem Alter stark zu und immer mehr jüngere Patienten erkranken an einer Divertikulitis. Die Krankheitsverläufe unterscheiden sich in Abhängigkeit vom Schweregrad erheblich in der Symptomatik. Lange Zeit galt die chirurgische Resektion des Entzündungsfokus auch schon in frühen Stadien als Therapiestandard. Heutzutage gibt es klare, evidenzbasierte Leitlinien zur Therapie und Operationsindikation. Die primäre Behandlung ist in der unkomplizierten Form konservativ. Die Indikation zur Chirurgie wird zunehmend zurückhaltender gestellt. Um eine optimale Therapie festzulegen, ist eine präzise Diagnostik mit akkurater Stadieneinteilung unabdingbar.
Keypoints
-
Die Diagnose der Divertikulitis sollte mittels einer Sonografie oder Computertomografie gesichert und anhand der CDD-Klassifikation eingeteilt werden.
-
Die akute unkomplizierte Divertikulitis (Stadium I) ohne Risikofaktoren kann ambulant und ohne antibiotische Therapie behandelt werden. Es besteht keine Operationsindikation bei vollständiger Beschwerderegredienz.
-
Die Behandlung der akuten komplizierten Divertikulitis (Stadium II) erfolgt stationär mit Antibiotika. Bei einem Makroabszess (>3cm) ist eine perkutane Drainage indiziert. Eine Sigmaresektion kann im entzündungsfreien Intervall angeboten werden. Bei freier Perforation und Peritonitis muss notfallmässig operiert werden, vorzugsweise laparoskopisch mit primärer Anastomose und protektivem Ileostoma, alternativ eine Hartmann-Operation (Diskontinuitätsresektion).
-
Bei chronisch-rezidivierender Divertikulitis (Stadium III) sollte die Operationsindikation individuell nach Nutzen-Risiko-Abwägung und Einschränkung der Lebensqualität gestellt werden. Studien zeigen, dass operierte Patienten eine bessere Lebensqualität aufweisen als solche mit langjähriger, konservativer Behandlung.
Mit einer Lebenszeitprävalenz von 50–60% und einem deutlichen Anstieg in der Population über 70 Jahre zählt die Divertikulose zu den häufigsten benignen Erkrankungen des Dickdarms. Zur Geschlechteraufteilung ist die Datenlage heterogen, jedoch scheinen Männer in jüngerem Alter bis etwa 60 Jahre häufiger betroffen zu sein als Frauen.1 Immer häufiger erkranken jüngere Patienten. Obgleich die Divertikulose in hohem Masse verbreitet ist, kommt es im Laufe der Lebenszeit nur bei etwa 4,3% zu einer Divertikulitis, und davon bei 15% zu einem komplizierteren Verlauf. Während das Rezidivrisiko mit jedem weiteren Entzündungsschub ansteigt, ist das Risiko für eine freie Perforation entgegen früherer Meinung bei Erstauftreten am höchsten und zeigt sich im weiteren Verlauf unabhängig von der Krankheitsprogression.
Zu den beeinflussbaren Risikofaktoren der Divertikulitis zählen Übergewicht, eine ballaststoffarme Ernährung, Alkoholkonsum und Rauchen, während eine gesunde Ernährung und körperliche Aktivität protektiv wirken. Nicht beeinflussbare Faktoren umfassen genetische Prädispositionen wie das Marfan- oder Ehlers-Danlos-Syndrom, Störungen des Metabolismus der Bindegewebsmatrix, enterische Neuropathien, das Alter und weitere Komorbiditäten.
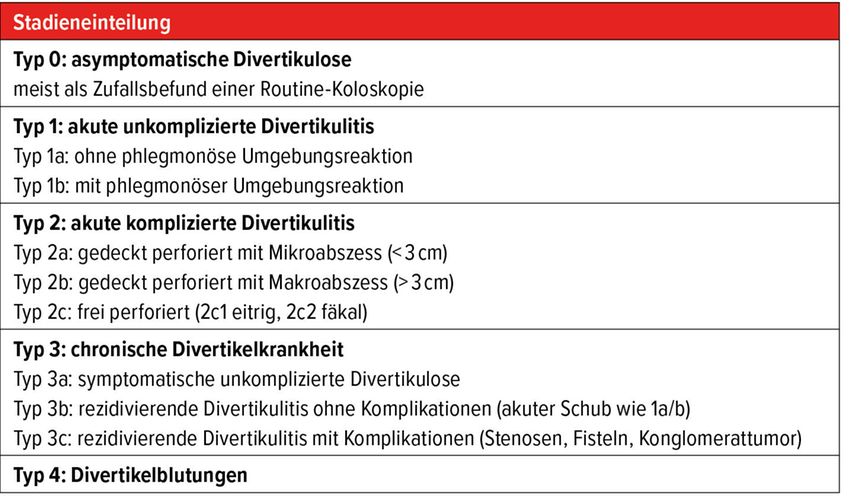
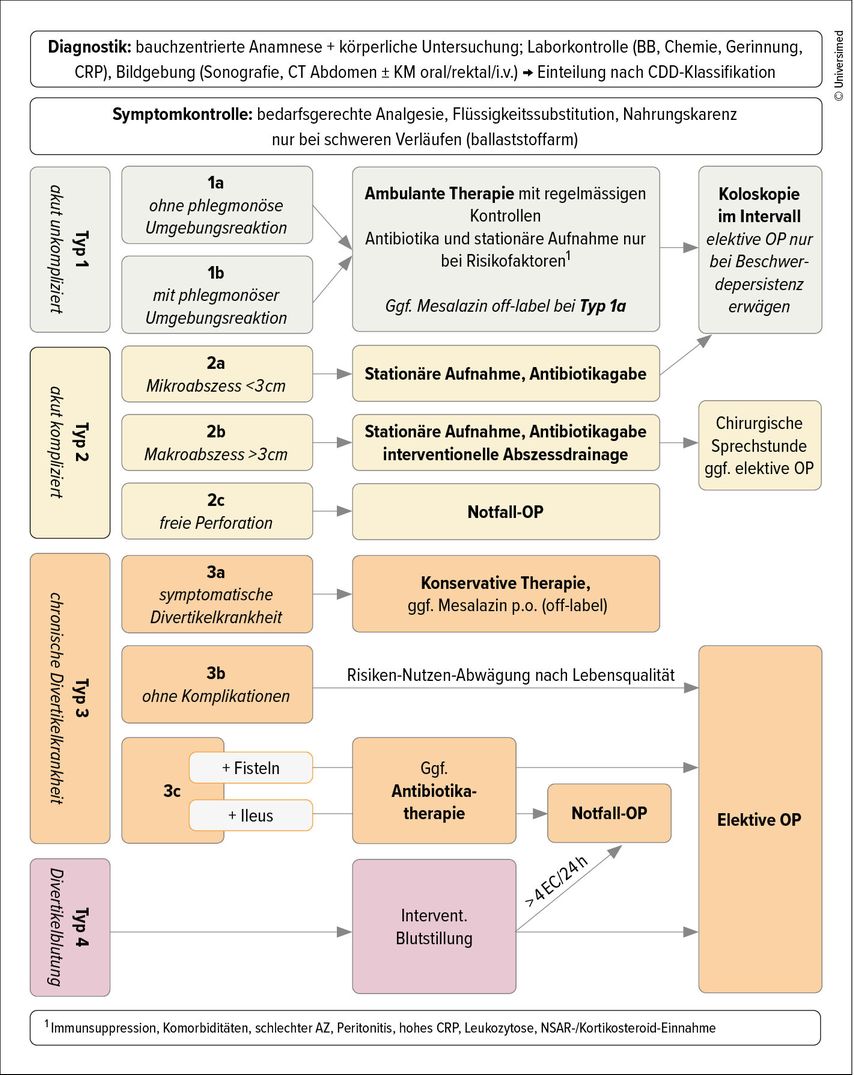
Einteilung nach Stadien: Diagnostik und Therapie
Zur Stadieneinteilung der Divertikelkrankheit hat sich vor allem im deutschsprachigen Raum die Classification of Diverticular Disease (CDD) als Standard etabliert (Tab. 1). Diese ging basierend auf Hinchey aus der Klassifikation nach Hansen und Stock hervor und teilt die Krankheit in fünf Typen mit Untertypen ein. Neben der abdomenfokussierten Anamnese und der klinischen körperlichen Untersuchung, einer Laborkontrolle der Entzündungsparameter und je nach Erfahrung des Untersuchers einer Abdomensonografie zählt das CT Abdomen als Goldstandard in der Diagnostik und zur Stadieneinteilung.
Typ 1 – akute unkomplizierte Divertikulitis
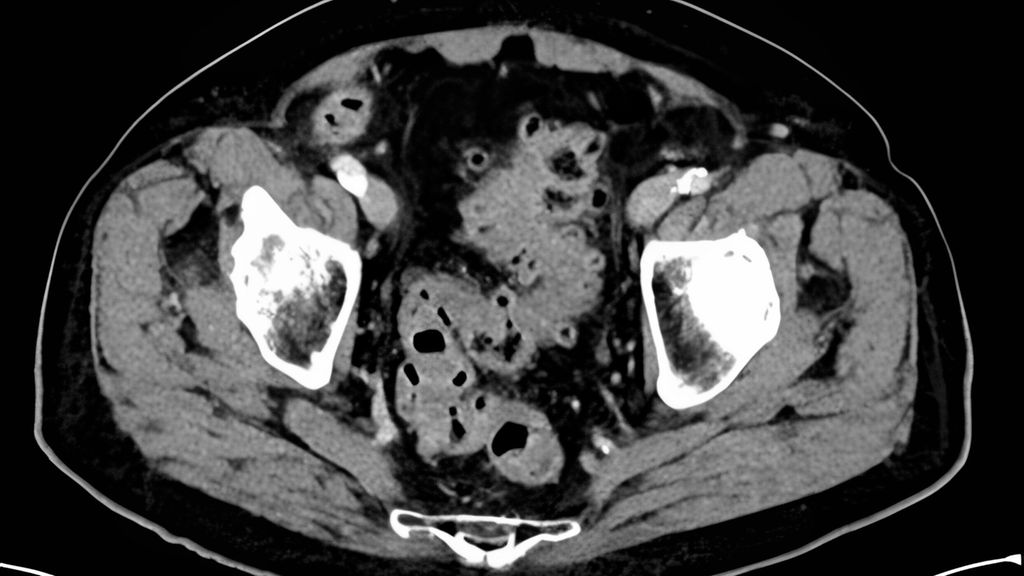
Klinisch imponiert hier meist eine milde Symptomatik mit dezent erhöhten Entzündungswerten, ohne Fieber, Sepsiszeichen oder Peritonitis. In der Bildgebung zeigt sich eine Entzündung der Divertikel, ggf. mit phlegmonöser Umgebungsreaktion (Abb. 1).
Abb. 1: CT einer Divertikulitis CDD 1b mit phlegmonöser Umgebungsreaktion
Therapie: Grundsätzlich werden bei der unkomplizierten Divertikulitis leitliniengerecht eine ambulante, symptomatische Therapie sowie eine Koloskopie nach Abklingen des Entzündungsschubes zum Ausschluss eines malignen Geschehens empfohlen. Eine antibiotische Therapie zeigte in diesem Stadium keinen signifikanten Benefit und sollte nicht mehr standardmässig verabreicht werden.2 Voraussetzung für den Verzicht auf Antibiotika und für eine ambulante Behandlung sind der Zugang zu engmaschigen ambulanten Verlaufskontrollen sowie ein Allgemeinzustand, der eine orale Nahrungs- und Flüssigkeitsaufnahme ermöglicht. Zudem entscheiden auch vorliegende Komorbiditäten wie arterielle Hypertonie, koronare Herzerkrankung, chronische Nierenerkrankung, Leberzirrhose, Immunsuppression oder ein schlechter Allgemeinzustand über die individuelle Risikokonstellation und die Notwendigkeit einer stationären Behandlung bzw. des Einsatzes von Antibiotika. Bei den genannten Risikofaktoren wird eine stationäre Behandlung mit Antibiotikagabe empfohlen. Die Indikation zur chirurgischen Resektion besteht nicht.
Typ 2 a/b – akute komplizierte Divertikulitis mit gedeckter Perforation
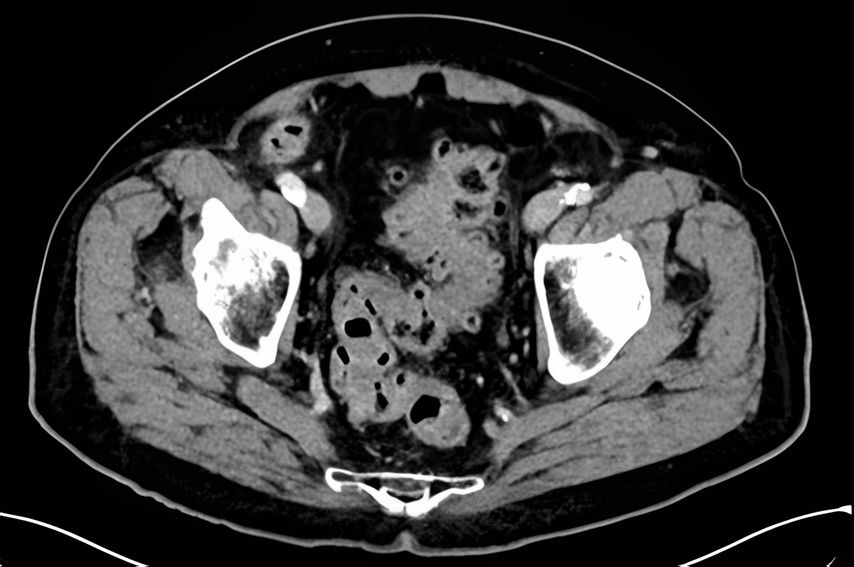
Während Patienten mit gedeckt perforierter Divertikulitis sich klinisch ähnlich präsentieren können wie Patienten mit unkomplizierten Divertikulitisverläufen vom Typ 1 (im Sinne einer Peridivertikulitis), zeigen sich die Entzündungsparameter hier in der Regel doch deutlicher erhöht. In der CT sehen wir einen Abszess, der je nach Grösse als Mikro- (<3cm) (Typ 2a) oder Makroabszess (>3cm) (Typ 2b) eingeteilt wird und für die weitere Therapie ausschlaggebend ist (Abb. 2). Das Rezidivrisiko weiterer Schübe korreliert zudem mit der Abszessgrösse.
Abb. 2: CT einer Divertikulitis CDD 2b mit interenterischem Makroabszess
Therapie: Für Patienten mit akuter komplizierter Divertikulitis Typ 2a/b besteht der Konsens zur stationären Aufnahme mit Beginn einer intravenösen Antibiotikatherapie sowie ggf. parenteraler Flüssigkeitszufuhr. Auch hier wird eine Koloskopie im entzündungsfreien Intervall empfohlen. Bei Vorliegen eines Mikroabszesses besteht nach den aktuellen Leitlinien die Indikation zur Operation nur bei Beschwerdepersistenz unter symptomatischer und antibiotischer Therapie. Im Falle eines Makroabszesses hingegen wird die interventionell-radiologische Abszessdrainage empfohlen mit anschliessender möglicher Evaluation einer elektiven Resektion nach Abklingen des akuten Entzündungsschubs. Üblicherweise eingesetzte Antibiotika sind je nach Schweregrad Amoxicillin/Clavulansäure (p.o./i.v.) oder Piperacillin/Tazobactam i.v. Auf Alternativen wie Ciprofloxacin mit Metronidazol sollte nur als 2. Wahl bei Allergien zurückgegriffen werden, aufgrund eines erhöhten Risikos für eine Clostridium-difficile-Infektion.3
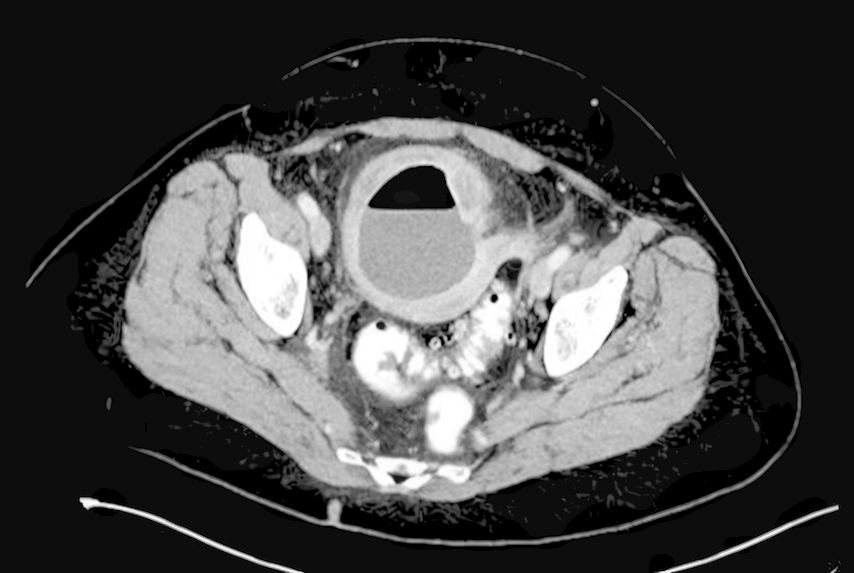
Typ 2c – akute komplizierte Divertikulitis mit freier Perforation
Patienten mit frei perforierter Divertikulitis imponieren meist mit einem deutlich reduzierten Allgemeinzustand, Kaltschweissigkeit sowie Sepsiszeichen. Oftmals lässt sich anamnestisch zunächst eine Phase subakuter diffuser Unterbauchschmerzen eruieren, die einem plötzlich eingetretenen, maximalen Schmerzereignis vorausgehen. In der körperlichen Untersuchung zeigt sich in der Regel ein akutes Abdomen mit diffuser Peritonitis. Die Entzündungswerte sind deutlich erhöht, in der CT Abdomen ist freie Luft und/oder Flüssigkeit sichtbar. Das klinische Beschwerdebild wird durch die eitrige (Typ 2c1) oder fäkale (Typ 2c2) Peritonitis mit Durchwanderung und Sepsis geprägt und entspricht einer absoluten Notfallsituation. Eine Antibiotikatherapie muss so rasch als möglich gestartet werden. Mit jeder verpassten Stunde bis zum Therapiebeginn steigt die Letalität signifikant.
Therapie:Das Vorliegen einer freien Darmperforation ist eine Indikation zur sofortigen Notfalloperation. Gemäss Leitlinie besteht der Konsens zur Resektion des betroffenen Kolonteils mit – falls möglich – standardmässiger primärer Anastomose und protektivem Ileostoma. Bei septischen und instabilen Patienten sollte, je nach intraoperativem Befund und Ermessen des Operateurs, jedoch eine Hartmann-Operation mit passagerem Kolostoma und Blindverschluss des (Rektum-)Stumpfes durchgeführt werden. Eine gross angelegte Multicenterstudie zeigte jedoch, dass in der Realität die Hartmann-Operation immer noch häufiger durchgeführt wird.4 In beiden Fällen gab es keine signifikanten Unterschiede in der Stomarückverlagerungsrate. Eine weitere Therapieoption, die in ersten Studien diskutiert wird, ist die alleinige laparoskopische Peritoneallavage, welche im 5-Jahres-Follow-up keinen signifikanten Unterschied im Auftreten schwerwiegender Komplikationen zeigte, jedoch eine deutlich höhere Wahrscheinlichkeit rezidivierender Divertikulitiden, bei signifikant niedriger Wahrscheinlichkeit eines Stomas.5,6 Angesichts der 28-Tage-Mortalität der abdominellen Sepsis von bis zu 42,9% bei fehlender chirurgischer Fokussanierung kann die alleinige Lavage bei frei perforierter Divertikulitis zum jetzigen Zeitpunkt nicht als Alternative zur Resektion empfohlen werden.7
Typ 3 – chronische Divertikelkrankheit
Die chronische Divertikelkrankheit lässt sich nochmals unterteilen: Typ 3a beschreibt das Auftreten persistierender bzw. wiederkehrender Beschwerden, durch eine Divertikulose bedingt und meist nach initialen Episoden einer akuten Divertikulitis, ohne eindeutige laborchemisch und CT-grafisch nachweisbare entzündliche Veränderungen. Sie stellt letztlich eine Ausschlussdiagnose dar und eine Abgrenzung zum Reizdarmsyndrom ist oft schwierig. Im Spital werden uns solche Fälle kaum vorgestellt. Typ 3b und c hingegen umfassen die «typischen» rezidivierenden Divertikulitiden, ohne (Typ 3b) und mit Komplikationen (Typ 3c) wie Fisteln (meist zur Harnblase), Stenosen oder Konglomerattumoren.
Therapie: Für Betroffene mit einer Typ-3a-Divertikelkrankheit besteht keine Indikation zur operativen Versorgung. Eine Therapie mit Mesalazin kann nach Leitlinie die Häufigkeit der symptomatischen Episoden sowie die Lebensqualität in diesen Fällen positiv beeinflussen.
Die lange geltende Empfehlung bei Typ 3b zur chirurgischen Resektion nach dem zweiten Schub ist nicht mehr gegeben. Entgegen früherer Meinung sind rezidivierende akute Divertikulitiden nicht mit einer höheren Komplikations- oder Versagensrate der konservativen Therapie assoziiert. Jedoch wird der weitere Verlauf durch die beeinträchtigte Lebensqualität von neu auftretenden Entzündungsschüben geprägt. Die Indikation zur Operation wird durch die individuelle Abwägung des Operationsrisikos gegen die subjektive Beeinträchtigung der Lebensqualität bestimmt. Im DIRECT-Trial und mittlerweile weiteren Studien zeigte sich nach elektiver Rektosigmoidresektion eine signifikant höhere Lebensqualität im Vergleich zur konservativen Behandlung.8 Zusammenfassend ist eine chirurgische Entfernung des Sigmas als Entzündungsfokus mit einer verbesserten Lebensqualität assoziiert.
Beim Vorliegen von Fisteln, symptomatischen Stenosen oder Konglomerattumoren im Rahmen einer Typ-3c-Divertikelkrankheit ist grundsätzlich eine Beschwerdebesserung nur durch die operative Behandlung zu erreichen. Jedoch gibt es auch Fallberichte, die die prinzipielle Möglichkeit einer konservativen Therapie bei Patienten mit kolovesikalen Fisteln unterstützen, unabdingbar hierfür ist jedoch der Ausschluss einer malignen Grunderkrankung.9,10 Wir empfehlen bei Fistelverdacht den Mohnsamentest mit anschliessender operativer Sanierung.
«Smoldering» Divertikulitis
Eine Sonderform der chronischen Divertikulitis stellt die «smoldering» Divertikulitis dar, die sich bei etwa 5% der Patienten entwickelt und bei der, nach einem akuten Schub, nie eine vollständige Beschwerdefreiheit erreicht wird. Die Entzündung zeigt sich zwar regredient, heilt jedoch nie vollends ab, vergleichbar mit einem «Schwelbrand». Die Konsequenz ist eine deutlich höhere Rezidivrate mit kürzeren Intervallen zwischen den akuten Entzündungsschüben.11 Bis dato bestehen kaum gesonderte Studiendaten zu dieser Unterform, jedoch scheint das zeitnahe operative Management am erfolgversprechendsten zu sein.12 Beim Auftreten einer «smoldering» Divertikulitis empfehlen wir die operative Entfernung des entzündeten divertikeltragenden Darmabschnitts.
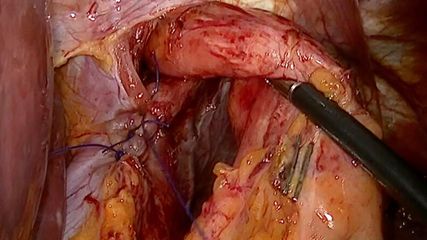
Operation
Die Operation im elektiven Setting erfolgt heutzutage in versierten Spitälern minimalinvasiv in laparoskopischer oder robotischer Technik. Entfernt werden muss bei der Sigmadivertikulitis das entzündete divertikeltragende Segment über eine Länge von circa 20cm. Die immer gestellte Frage der Patienten bzgl. der Länge des zu entfernenden Darmsegmentes wird vor allem durch das häufig vorhandene Colon elongatum mit deutlich elongierter Sigmaschlaufe bestimmt. Beruhigend kann man den Patienten mitteilen, dass wenig Darmlänge entfernt werden muss und die Darmentfernung wenig negativen Einfluss auf die Stuhlqualität haben sollte. Die Absetzung des Darmabschnitts muss im proximalen Rektum erfolgen, um das Rezidivrisiko niedrig zu halten. Die proximale Absetzung erfolgt in einem entzündungsfreien Darmabschnitt circa am Übergang Colon descendens zu Sigma. Die Spitalaufenthaltsdauer beträgt mit heutigen «Fast-track»-Behandlungen 3 bis 5 Tage bei unkomplizierten Verläufen. In guten Spitälern beträgt die Anastomoseninsuffizienzrate im elektiven Setting 3–5% (eigene Daten). Damit kann die Operation als sicher bezeichnet werden.
Nachsorge
Ernährungsempfehlungen
Nach aktuellen Leitlinien besteht keine Evidenz für eine spezifische ernährungsbasierte Sekundärprophylaxe über die allgemeingültigen Empfehlungen einer gesunden und ausgewogenen Ernährung hinaus.
Wertigkeit einer Endoskopie nach Divertikulitisschub
Zwar wird durch vermehrten Einsatz der hochauflösenden CT die traditionelle Empfehlung zur Koloskopie im entzündungsfreien Intervall zunehmend infrage gestellt, jedoch zeigte eine Metastudie ein signifikant häufigeres Auftreten von kolorektalen Adenomen und Karzinomen bei Status nach Divertikulitis, nicht aber Divertikulose.13 Während bei 0,3–0,4% der Normalbevölkerung ein kolorektales Karzinom durch Koloskopie gefunden wird, war dies nach stattgehabter Divertikulitis, unabhängig von der Krankheitsschwere, bei 2,0% der Fall, nach komplizierter Divertikulitis sogar bei 6,1%. Die Autoren gehen nicht von einem kausalen Zusammenhang aus, jedoch besteht weiterhin die Empfehlung zur Koloskopie 6 bis 8 Wochen nach Divertikulitisschub – bei medizinisch fitten Patienten, bei denen das Risiko den Nutzen nicht übersteigt.
Sonderfälle und Differenzialdiagnosen
Immunsupprimierte Patienten
Immunsupprimierte Patienten weisen eine erhöhte Inzidenz, Komplikations- und Mortalitätsrate bei Divertikulitis auf, insbesondere zeigte sich das nichtoperative Management in dieser Gruppe weniger erfolgversprechend.14 Weitere Studien fanden einerseits ein erhöhtes Risiko, notfallmässig operiert werden zu müssen, andererseits eine erhöhte Morbidität immunsupprimierter Patienten bei elektiven Operationen sowie eine erhöhte Mortalität bei Notfalloperationen.15,16 Ein wichtiger Unterschied in der Diagnostik der Divertikulitis bei immungeschwächten Patienten besteht zudem darin, dass die typische Symptomatik sowie klinische und laborchemische Entzündungszeichen abgeschwächt oder absent sein können, wodurch die Sensitivität und Spezifität der CT-Untersuchung verringert werden.17 Trotz uneindeutiger Studienlage bezüglich Operationsindikation differenziert die aktuelle S3-Leitlinie bei unkomplizierter Divertikulitis und beschwerdefreien Patienten nicht nach Vorerkrankungen und Immunstatus, sondern empfiehlt keine grundsätzliche elektive Sigmaresektion. Es sollte jedoch eine rasche Diagnosestellung mittels CT und die obligate Etablierung einer antibiotischen Therapie erfolgen.11 Die Operationsindikation sollte nach Abwägen der individuellen Risikofaktoren und des Rezidivrisikos gestellt werden. Beispielsweise zeigten sich bei therapeutisch gut eingestellten HIV-Patienten kaum erhöhte Komplikationen, während Patienten unter Kortikosteroidtherapie die schlechtesten Outcomes hatten.18,19 Patienten mit Status nach Transplantation, unter immunsuppressiver Therapie hatten ein besseres Outcome als solche vor der Transplantation.
Jüngere Patienten
Unter jüngeren Patienten, insbesondere in der Altersgruppe von 40- bis 49-Jährigen, ist ein deutlicher Trend der Inzidenzzunahme zu beobachten.20 Initial wurde von einem rezidiv- und komplikationsreicheren Verlauf bei jüngeren Patienten ausgegangen, dies scheint sich jedoch in Studien, die bei der Rezidivrate die Überlebensanalysen unter Einbezug der Nachbeobachtungsdauer berücksichtigten, nicht zu bestätigen. Auch fand sich kein signifikanter Unterschied im Anteil an komplizierten Verläufen.21 Demnach wird leitliniengerecht keine Anpassung der Therapie für Divertikulitis nach Alter empfohlen. Jedoch muss man jüngeren Patienten transparent sagen, dass weitere Schübe auftreten können und das Leben mitbestimmen werden.
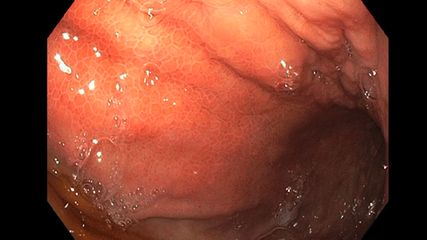
SCAD – segmentale Kolitis assoziiert mit Divertikulose
Eine seltene, jedoch an Relevanz gewinnende Differenzialdiagnose der Divertikulitis, insbesondere der «smoldering» Divertikulitis, stellt die segmentale Kolitis assoziiert mit Divertikulose dar. Unter Patienten mit Divertikulose sind circa 1% betroffen, der Verlauf kann oft asymptomatisch oder aber von Hämatochezie, Diarrhö oder abdominellen Schmerzen geprägt sein. Endoskopisch imponieren sichtbare inflammatorische Schleimhautläsionen interdivertikulär statt peridivertikulär, also in den divertikelfreien Zwischenarealen. Histologisch präsentiert sich die SCAD ähnlich einer chronisch-entzündlichen Darmerkrankung, während laborchemisch ein erhöhter TNF-alpha-Spiegel auffällt. Therapeutisch kommt bislang ausschließlich Mesalazin zum Einsatz.22,23
Fazit
Zusammenfassend haben wir in dieser Arbeit das breite Spektrum, welches die Divertikulitis als Erkrankung einnehmen kann, von milden unkomplizierten Verläufen bis hin zu lebensbedrohlichen Komplikationen, dargestellt (Abb. 3). Die Therapie ist stadienabhängig und umfasst die symptomatische Behandlung bis zur Notfalloperation. Eine präzise Diagnostik, Stadieneinteilung und daran ausgerichtete Wahl der Therapie ist die Grundvoraussetzung, um eine optimale Patientenversorgung zu gewährleisten und dem Patientenwohl gerecht zu werden. Die chirurgische Therapie ist deutlich zurückhaltender geworden, jedoch ist die Datenlage ausreichend, um Patienten, die nach mehreren Schüben in ihrer Lebensqualität eingeschränkt sind, die Operation zu empfehlen.
Literatur:
1 Leifeld L et al.: S3-Leitlinie Divertikelkrankheit/Divertikulitis. Gemeinsame Leitlinie der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS) und der Deutschen Gesellschaft für Allgemein- und Viszeralchirurgie (DGAV). Z Gastroenterol 2022; 60: 613-88 2 Poh CW et al.: Antibiotics vs observational therapy in acute uncomplicated diverticulitis, a systemic review and meta-analysis. Int J Colorectal Dis 2023; 38: 97 3 Gaber CE et al.: Comparative effectiveness and harms of antibiotics for outpatient diverticulitis: two nationwide cohort studies. Ann Intern Med 2021; 174: 737-46 4 Perrone G et al.: Goodbye Hartmann trial: a prospective, international, multicenter, observational study on the current use of a surgical procedure developed a century ago. World J Emerg Surg 2024; 19: 14 5 Azhar N et al.: Laparoscopic lavage vs primary resection for acute perforated diverticulitis: long-term outcomes from the Scandinavian diverticulitis (SCANDIV) randomized clinical trial. JAMA Surg 2021; 156: 121-7 6 Sciascia D et al.: Longer term outcomes of laparoscopic peritoneal lavage in the management of acute Hinchey III perforated diverticulitis: a systematic review and meta-analysis. Dig Surg 2025; 42: 36-47 7 Hecker A et al.: Intra-abdominal sepsis: new definitions and current clinical standards. Langenbecks Arch Surg 2019; 404: 257-71 8 van de Wall BJM et al.: Surgery versus conservative management for recurrent and ongoing left-sided diverticulitis (DIRECT trial): an open-label, multicentre, randomised controlled trial. Lancet Gastroenterol Hepatol 2017; 2: 13-22 9 Zizzo M et al.: Management of colovesical fistula: a systematic review. Minerva Urol Nephrol 2022; 74: 400-8 10 Radwan R et al.: How safe is it to manage diverticular colovesical fistulation non-operatively? Colorectal Dis 2013; 15: 448-50 11 Peery AF et al.: AGA clinical practice update on medical management of colonic diverticulitis: expert review. Gastroenterol 2021; 160: 906-11.e1 12 Rink AD et al.: [Smoldering diverticultis - still a type of chronic recurrent diverticulitis with good indication for surgery? - Surgery for smoldering diverticulitis]. Z Gastroenterol 2019; 57: 1200-8 13 Cao AMY et al.: Endoscopic findings after CT proven acute diverticulitis: a systematic review and meta-analysis. ANZ J Surg 2023; 93: 1150-8 14 Hwang SS et al.: Diverticulitis in transplant patients and patients on chronic corticosteroid therapy: a systematic review. Dis Colon Rectum 2010; 53: 1699-1707 15 Lee JG et al.: Comparative outcomes of acute colonic diverticulitis in immunocompromised versus immunocompetent patients: a systematic review and meta-analysis. Intest Res 2023; 21: 481-92 16 McKechnie T et al.: Operative management of colonic diverticular disease in the setting of immunosuppression: A systematic review and meta-analysis. Am J Surg 2021; 221: 72-85 17 de’Angelis N et al.: Emergency abdominal surgery after solid organ transplantation: a systematic review. World J Emerg Surg 2016; 11: 43 18 Cronley K et al.: Diverticulitis in HIV-infected patients within the United States. HIV Med 2016; 17: 216-21 19 Brandl A et al.: Diverticulitis in immunosuppressed patients: A fatal outcome requiring a new approach? Can J Surg 2016; 59: 254-61 20 Bharucha AE et al.: Temporal trends in the incidence and natural history of diverticulitis: a population-based study. Am J Gastroenterol 2015; 110: 1589 21 van Dijk ST et al.: A systematic review and meta-analysis of disease severity and risk of recurrence in young versus elderly patients with left-sided acute diverticulitis. Eur J Gastroenterol Hepatol 2020; 32: 547-54 22 Cassieri C et al.: How to differentiate segmental colitis associated with diverticulosis and inflammatory bowel diseases. J Clin Gastroenterol 2016; 50: 36 23 Sbarigia C et al.: Common diagnostic challenges and pitfalls in segmental colitis associated with diverticulosis (SCAD). J Clin Med 2023; 12: 6084
Das könnte Sie auch interessieren:
Antirefluxbarriere des LES – ein Auslaufmodell?
Hauptursache für das Auftreten einer gastroösophagealen Refluxerkrankung ist ein Defekt der sogenannten Antirefluxbarriere, zu der der untere Ösophagussphinkter (LES) zählt. Moderne ...
Wenn die Magensonde nicht fördert: der seltene Fall eines Magenabszesses
Der vorliegende Fallbericht soll die Aufmerksamkeit auf die seltene Pathologie des Magenwandabszesses lenken, die mit einem eindrucksvollen Ausprägungsgrad initial eine falsche ...
Perioperative Ernährung bei gastrointestinalen Eingriffen
Im Bereich der perioperativen Ernährung bei geplanten Operationen am Magen-Darm-Trakt wurden in den letzten Jahren einige Dogmen über Bord geworfen – mit dem Ziel, den Patienten ...
_A.jpg)
