Prostatakrebsfrüherkennung in der Schweiz
Autoren:
Anas Elyan
PD Dr. med. Ashkan Mortavezi
Urologie
Universitätsspital Basel
E-Mail: ashkan.mortezavi@usb.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine zeitgemässe Prostatakrebsfrüherkennung hat das Potenzial, die Überdiagnose von nicht lebensbedrohlichem Prostatakrebs zu reduzieren, Männer besser zu identifizieren, die tatsächlich eine Gewebeprobe benötigen, und die Mortalität an der Erkrankung zu senken. Basierend auf diesen neuen Erkenntnissen empfiehlt die Europäische Union ihren Mitgliedsländern, organisierte Programme zur Früherkennung zu evaluieren. Wie ist die Situation in der Schweiz?
Keypoints
-
Das Prostatakarzinom ist die häufigste Krebserkrankung und die zweithäufigste Krebstodesursache bei Männern in der Schweiz. Bisher gibt es jedoch keine landesweite Vorsorgestrategie, aufgrund der berechtigten Sorge um Überdiagnose und Übertherapie.
-
Eine zeitgemässe Prostatakrebsfrüherkennung kombiniert PSA, optional zusätzliche Bluttests und immer ein mpMRI, was die Anzahl der durchgeführten Biopsien reduziert und den Anteil an Überdiagnosen senkt. Es konzentriert sich auf die Erfassung von klinisch relevantem Prostatakarzinom.
-
Neue Biomarker, wie z.B. der Stockholm3-Test, bieten vielversprechende Möglichkeiten zur Verbesserung der Prostatakrebsvorsorge, indem sie unnötige Biopsien vermeiden und gleichzeitig klinisch relevanten Prostatakrebs effektiv erkennen.
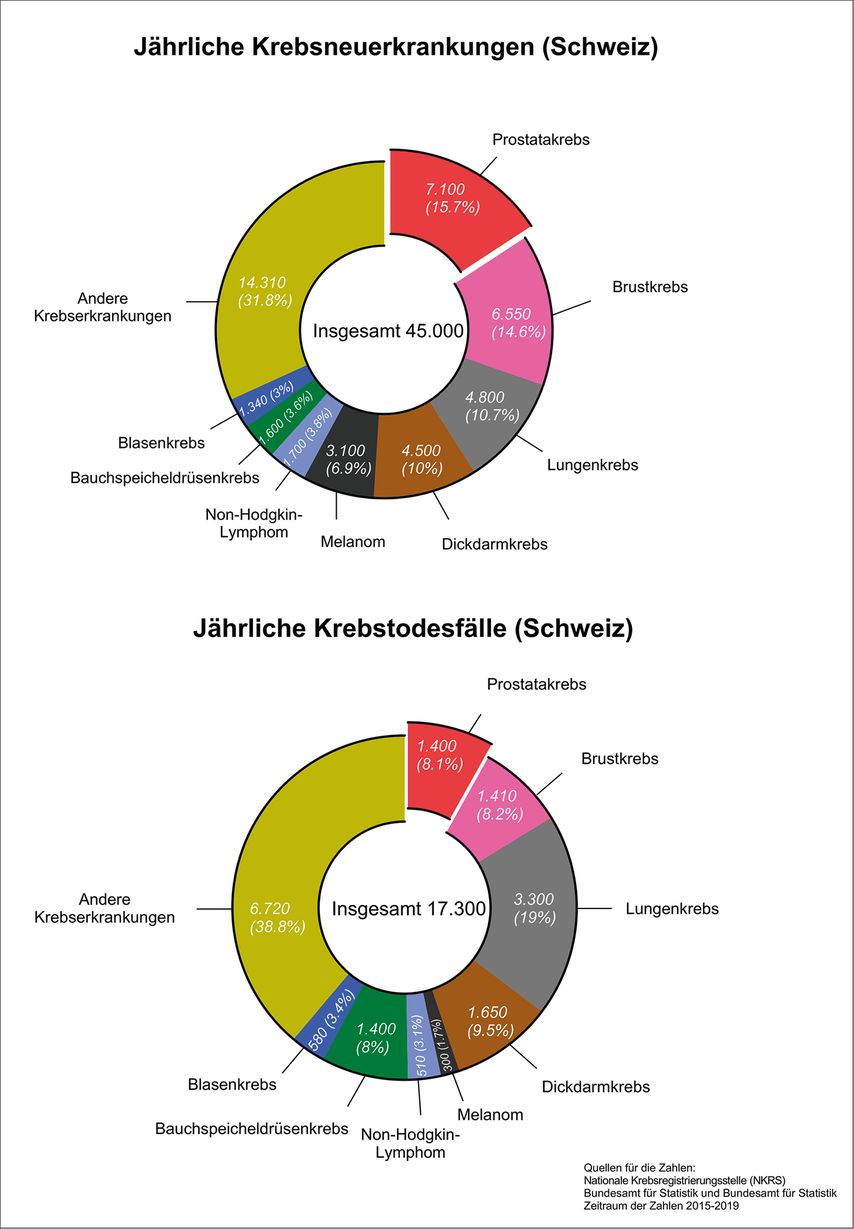
Das Prostatakarzinom ist die häufigste bösartige Krebserkrankung und die zweithäufigste onkologische Mortalitätsursache bei Männern in der Schweiz (Abb. 1).1 Bei der Diskussion um die Überdiagnose und Übertherapie dieses Leidens wird Letzterem oft nicht genügend Aufmerksamkeit zugesprochen. Hinzu kommt, dass die Zahl der Männer, welche bei der Diagnose bereits an einer metastasierten Erkrankung leiden, kaum Beachtung findet; für das Jahr 2019 gehen wir von mehr als 1100 Männern aus (NICER). Die dann notwendige Systemtherapie, welche aus einer Kombination von Hormonentzug, Antiandrogenen und neu auch Chemotherapie besteht, hat nicht nur signifikante negative Auswirkungen auf die Lebensqualität der Erkrankten, sondern aufgrund der hohen Behandlungskosten auch gesundheitsökonomische Implikationen. Die gesündere Lebensweise der Männer durch Abnahme des Nikotinkonsums, ausgewogenere Ernährung, Sport und nicht zuletzt die konsequente Behandlung von Bluthochdruck, Hypercholesterinämie und Blutzuckereinstellung führt gemäss Registerdaten zu einer stetigen Abnahme des Anteils kardiovaskulärer Todesursachen; Männer werden alt genug, um an Prostatakrebs zu erkranken und zu sterben.2
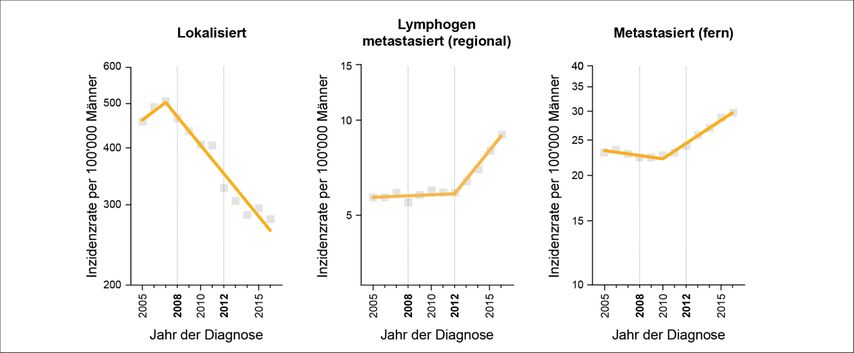
In der Schweiz gibt es organisierte Früherkennungsprogramme für Brust- und Darmkrebs. Gleichzeitig gibt es Bestrebungen für die Etablierung eines Programms für die Früherkennung von Lungenkrebs ( www.swisscancerscreening.ch ). Für den häufigsten Krebs beim Mann wurde bislang keine vergleichbare Initiative in Erwägung gezogen; es ist anzunehmen, dass die Diskussionen um Überdiagnose und Übertherapie aus dem letzten Jahrzehnt dazu geführt haben, dass Prostatakrebsfrüherkennung zur heissen Kartoffel in der Gesundheitspolitik geworden ist – dies zum Nachteil der in der Schweiz lebenden Männer. Im europäischen Ausland wurde das Thema der Prostatakrebsfrüherkennung in den letzten Jahren, nicht zuletzt aufgrund der Bestrebungen der Europäischen Urologischen Fachgesellschaft (EAU), sehr intensiv geführt. Im Dezember 2022 hat der Rat der Europäischen Union seine Empfehlungen zur Krebsvorsorge nach einem Vorschlag der Europäischen Kommission aktualisiert. Es wurde die Absicht bekannt gegeben, das gezielte Krebsscreening über Brust-, Darm- und Gebärmutterhalskrebs hinaus auf Prostatakrebs auszuweiten. Die Empfehlung fordert die Mitgliedsstaaten auf, die Durchführbarkeit und Wirksamkeit von organisierten Screening-Programmen für Prostatakrebs zu untersuchen. In Schweden wurde die Confederation of Regional Cancer Centres bereits 2018 damit beauftragt, alle Regionen bei der Etablierung von Programmen für die organisierte Prostatakrebstestung («organized prostate cancer testing») zu unterstützen.3 Die Pionierarbeit der Schweden ist unter anderem auch darauf zurückzuführen, dass die häufigste Todesursache bei Männern in Schweden der Prostatakrebs ist, und aufgrund der niedrigen Raucherrate nicht Lungenkrebs wie im restlichen Europa. Mittlerweile wurde ein solches Programm in fast allen schwedischen Regionen etabliert oder wird in Kürze initiiert werden. Basierend auf neuen epidemiologischen Daten aus Nordamerika haben sich dort die Meinungen hinsichtlich Prostatakrebsfrüherkennung ebenfalls geändert, nachdem die PSA-Testung im letzten Jahrzehnt deutlich zurückging. Die U.S. Preventive Services Task Force (USPSTF) hatte sich aufgrund fehlender Evidenz bezüglich Nutzens im Jahr 2008 zunächst gegen ein PSA-Screening für Männer ab 75 Jahren und dann 2012 gegen eine Testung für alle Altersgruppen ausgesprochen. Manch einer mag sich noch an diese Meldungen erinnern, welche damals auch den Umgang der Männer und Hausärzte mit PSA in der Schweiz nachhaltig beeinflussten. Es hat einige Jahre gedauert, bis man die tatsächlichen Effekte dieser Empfehlungen objektiv evaluieren konnte. Mittlerweile zeigten mehrere voneinander unabhängige Untersuchungen einen signifikanten Anstieg der nationalen Fälle von lokal fortgeschrittenen und metastasierten Prostatakarzinomen, welche nach Ausschluss anderer Einflussfaktoren («confounder») auf die reduzierte Früherkennung zurückgeführt werden (Abb. 2).4 Diese Entwicklung hat bereits dazu geführt, dass die USPSTF ihre Empfehlungen revidiert hat. Für die Schweiz liegen leider bisher keine Daten vor, da keine Erfassung auf dieser Ebene vor Initiierung der Krebsregister erfolgte. Erste Erkenntnisse können erst in 3 bis 4 Jahren erwartet werden.
Abb. 2: Aktuelle Trends in den altersadjustierten SEER-Inzidenzraten, 2000–2020 (USA). Im Jahr 2008 wurde durch die USPSTF eine Empfehlung gegen ein PSA-Screening für Männer ab 75 Jahren und im Jahr 2012 für alle Männer ausgesprochen (adaptiert gemäss Jemal et al., 2021)4
Wissenschaftliche Evidenz
Bei der Kontroverse um Prostatakrebsfrüherkennung geht es in der Regel um die niedrige Spezifität des PSA-Werts und die Übertherapie klinisch nicht relevanter Karzinome. Untersuchungen zeigen, dass im Kontext der klassischen Algorithmen (keine Bildgebung, transrektale Zufallsbiopsien) ein unorganisiertes Screening, so wie es in der Schweiz überwiegend praktiziert wurde, ein negatives Kosten-Nutzen-Verhältnis aufweist. Im Wissen um die Schwächen der Diagnostik beim Prostatakarzinom wurden in den vergangenen Jahrzehnten intensive Forschungsanstrengungen zur Entwicklung neuer diagnostischer Verfahren und Algorithmen durchgeführt. Diese sind speziell darauf ausgelegt, Männer mit klinisch relevantem Prostatakarzinom, definiert als Gleason Score ≥7 (neu: Grade Group ≥2), zu identifizieren. Sie umfassen im ersten Schritt neue Biomarker und Nomogramme für die Verbesserung der Sensitivität und Spezifität bei der initialen Triage. Im zweiten Schritt beinhalten sie die multiparametrische Magnetresonanztomografie (mpMRI) und Fusionssysteme für gezielte Gewebeentnahmen aus den detektierten Läsionen zur Reduktion benigner Biopsien, Überdetektion insignifikanter Karzinome, aber auch Vermeiden falsch negativer Befunde. Nicht zuletzt hat der definitive Wechsel von einem transrektalen Zugangsweg zu einem transperinealen die Häufigkeit infektiologischer Komplikationen drastisch senken können.
Screening zur Reduktion der Mortalität
Wichtig zu erwähnen ist hier vorgängig die «negative» Studie zum Prostatakrebsscreening, welche der Auslöser für die Empfehlung der USPSTF gegen PSA-Testung vor 10 Jahren war: die nordamerikanische PLCO-Studie (Prostate, Lung, Colorectal, and Ovarian Cancer Screening Trial).5 Nach einer 1:1-Randomisierung von 76685 Männern im Alter zwischen 55 und 74 Jahren zu einer jährlichen Einladung zur PSA-Testung oder zum Kontrollarm zeigte sich nach 13 Jahren kein Unterschied in der Prostatakarzinomsterblichkeit. Nachfolgende Analysen, welche leider erst nach mehreren Jahren durchgeführt wurden, zeigten jedoch, dass Screening doch die Mortalität reduzierte, und zwar um 32%. Nicht beachtet wurde bei der initialen Schlussfolgerung nämlich die signifikante Kontamination im Kontrollarm mit opportunistischem PSA-Screening (85% der Männer erhielten mindestens einmal während der Beobachtungsperiode einen PSA-Test).6 Auch wenn die Resultate der PLCO-Studie mittlerweile von den meisten Experten nicht mehr als relevant für die Beurteilung des Nutzens von PSA-Screening angesehen wird, bildet die initiale Interpretation bis heute die Grundlage für die PSA-Kontroverse.
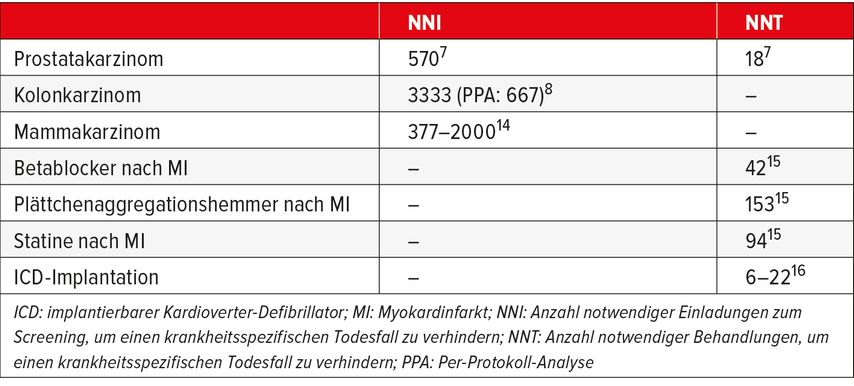
Ein anderes, «positives» Ergebnis zeigte die ERSPC-Studie (European Randomised Study of Screening for Prostate Cancer). Diese teilte 182000 Männer im Alter von 50 bis 74 Jahren zufällig in Gruppen ein, die entweder alle vier Jahre eine Einladung für ein PSA-Screening erhielten oder zur Kontrollgruppe gehörten. Nach 16 Jahren Follow-up zeigte sich eine 20%ige Reduktion der Sterblichkeit durch Prostatakrebs in der Screeninggruppe; in absoluten Zahlen waren es 570 Männer, welche zum PSA-Test eingeladen wurden, und 18 Fälle, welche diagnostiziert werden müssen, um einen Prostatakarzinom-spezifischen Todesfall zu verhindern.7 Zum Vergleich hierzu die neusten Daten der NordICC-Studie zur Darmkrebsvorsorge:8 Dort brauchte es allein 455 Einladungen, um nur einen Kolonkarzinomfall zu vermeiden. Die Darmkrebsmortalität konnte durch die Vorsorgespieglung nicht signifikant reduziert werden, auch wenn sich eine Tendenz zeigte (relatives Risiko: 0,90; 95% CI: 0,64–1,16). In einer analogen Kalkulation zur ERPSC-Studie wären somit 3333 Einladungen nötig, um einen Todesfall durch Darmkrebs zu verhindern; in einem hypothetischen Szenario, bei dem jeder Eingeladene zur Untersuchung erscheint (Per-Protokoll-Analyse) beträgt dieser Wert bestenfalls 667. Für das Brustkrebsscreening ist die Effektivität stark abhängig von der untersuchten Altersgruppe; dementsprechend ist die Streubreite der angegebenen Zahlen in der Literatur sehr gross (377–2000) und überschneidet sich bei den «optimistischeren» Szenarien mit denen beim Prostatakarzinom (Tab. 1).
Tab. 1: Anzahl notwendiger Einladungen (NNI) oder Behandlungen (NNT), um einen krankheitsspezifischen Todesfall zu vermeiden
Fortschritte bei der (Früh-)Erkennung
Der PSA-Wert zeigt zwar eine gute Sensitivität für die Detektion von Prostatakarzinom im Frühstadium, zeichnet sich aber durch eine niedrige Spezifizität aus. In den moderat erhöhten Bereichen (3–10ng/ml) ist hierfür die Ursache häufiger eine unspezifische Entzündung oder Hyperplasie als ein Karzinom. Dies führt dazu, dass viele Männer durch den Prozess der Diagnostik geführt werden, ohne am Ende eine Bestätigung für ein klinisch relevantes Prostatakarzinom zu erhalten. Während eine MRI-Untersuchung wenig invasiv ist ohne Strahlenbelastung, ist eine Prostatabiopsie, auch wenn sie lege artis transperineal durchgeführt wird, mit relevanten Risiken assoziiert. Beiden gemeinsam ist der psychologische Stress, dem gesunde und asymptomatische Männer ausgesetzt werden.
In den letzten Jahren konnten dank verbesserter Diagnostik die Raten an falsch negativen Biopsien und die Detektion klinisch irrelevanter Fälle deutlich gesenkt werden. Die Anwendung eines multiparametrischen Prostata-MRI zur Erkennung von Prostataläsionen in Kombination mit gezielten Prostatabiopsien resultierte in einer signifikanten Reduktion der Detektionsrate klinisch nicht relevanter Tumoren. Männer mit unauffälligem MRI müssen nicht mehr biopsiert werden. Gleichzeitig konnte die Detektionsrate klinisch signifikanter Erkrankungen, welche vormals (z.B. in der ERSPC-Studie) in relevanter Häufigkeit durch die transrektale Zufallsbiopsie verpasst wurden, durch die bildgesteuerte Fusionsbiopsie erhöht werden. Was sich in der Praxis schon bewährt hatte, musste sich noch auf Populationsebene beweisen. Und in der Tat, zwei neue prospektiv randomisierte Studien aus Schweden konnten diese Vorteile des MRI auch im Screening-Setting zeigen.9,10 Auch wenn bei beiden Studien ausschliesslich ein biparametrisches MRI ohne Kontrastmittel durchgeführt wurde, sind die für ein solches Programm, bei dem ausschliesslich PSA die Bildgebung triggert, notwendigen Ressourcen und damit assoziierten Kosten auf Populationsebene nicht zu vernachlässigen. Eine Möglichkeit, diese zu senken und die Effizienz des diagnostischen Algorithmus weiter zu erhöhen, ist die Durchführung eines zwischengeschalteten Triage-Tests für das MRI. Da dieser nur bei Überschreiten eines vordefinierten PSA-Cut-off-Werts durchgeführt werden würde, spricht man auch von einem Reflex-Test.
Reflex-Tests
Der PSA-Test ist günstig und ein Routinetest in den meisten Laboren in der Schweiz. Somit eignet er sich hervorragend als initialer Triage-Test im Screening. Wir wissen, dass unterhalb eines Werts von 1,5µg/l das Risiko für einen relevanten Prostatakrebs äusserst niedrig ist. Erfreulicherweise haben 65% der Männer (über alle Altersgruppen) einen Wert, der niedriger ist.11 Ab einem Wert von 1,5µg/l steigt das Risiko kontinuierlich an. Der häufig genutzte Toleranzwert von 3,0µg/l (manchmal sogar 2,5µg/l) ist ein Kompromiss zwischen Sensitivität und Spezifität, auch wenn wir eine relevante Anzahl signifikanter Karzinome im Graubereich von 1,5–3,0µg/l verpassen. Ein interessantes Konzept ist es, einen Reflex-Test zu entwickeln, der erst ab einem gewissen PSA-Wert, z.B. 1,5µg/l, durchgeführt wird. Dieser Test darf dann teurer und aufwendiger sein, solange er eine bessere Performance als PSA zeigt. Je nach Land sind bereits unterschiedliche Tests wie zum Beispiel der «Prostate Health Index» oder der «4Kscore Test» auf dem Markt verfügbar. Beide wurden zwar in Kohorten von Männern mit erhöhtem PSA vor einer Biopsie validiert, jedoch nicht im Screening-Setting im Sinne eines Tests zur Früherkennung. Besonders vielversprechend erscheint deshalb der Stockholm3-Test, der (wie der Name impliziert) in Schweden am Karolinska-Institut entwickelt wurde.12 Der Bluttest bestehend aus zwei Röhrchen kombiniert fünf Proteinbiomarker und 232 genetische Single-Nucleotid-Polymorphismen (SNP). Dies sind Variationen in der DNA-Sequenz, die an bestimmten Positionen innerhalb eines Genoms auftreten. SNP sind die häufigste Art von genetischen Variationen bei Menschen und zeigen Assoziationen mit dem Auftreten bestimmter Krankheiten. Der Vorteil des Stockholm3-Tests ist, dass er mit nur sehr wenigen klinischen Parametern, welche ohne fachärztliches Zutun erhebbar sind (Alter, Familienanamnese für Prostatakarzinom, vorherige unauffällige Prostatabiopsie, Einnahme eines 5-alpha-Reduktasehemmers), eine sehr präzise Angabe zum Risiko für das Vorliegen eines relevanten Prostatakrebses machen kann. Der Test wurde in zwei grossen populationsbasierten Studien in Schweden mit PSA verglichen. Bemerkenswerterweise wurde eine relevante Anzahl signifikanter Karzinome im PSA-Bereich 1,5–3,0µg/l gefunden. Je nach ausgewähltem Grenzwert (11% oder 15%) kann mittels Einsatzes des Stockholm3-Tests bei Männern mit einem PSA-Wert von >1,5µg/l die Anzahl der MRI fast halbiert oder die Detektion der signifikanten Karzinome um 20% erhöht werden12,13 – und dies ohne jegliche urologische Beurteilung oder Abklärung vor der Bildgebung.
Aufgrund der populationsspezifischen Heterogenität der SNP wurde der Test 2022 in einer multizentrischen Validierungsstudie in der Schweiz untersucht; er zeigte eine erhaltene Performance auch ausserhalb von Skandinavien in einer mitteleuropäischen Population.
Fazit
Die neuste Forschung hat gezeigt, dass ein moderner Ansatz zum Prostatakrebs-Screening, der eine Kombination aus PSA, zusätzlichem Bluttest und MRI vereint, die Überdiagnose von nicht lebensbedrohlichem Prostatakrebs reduziert und Männer besser identifiziert, die tatsächlich eine Gewebeprobe benötigen. Der diagnostische Wert dieser Zusatztests ist klar, es bedarf jedoch weiterer Forschung, um herauszufinden, wie sie am besten eingesetzt werden können. In Anbetracht des erheblichen Umfangs des laufenden opportunistischen Screenings in der Schweiz sollten die Kantone einen schrittweisen Ansatz in Betracht ziehen, einschliesslich Pilotprojekten und Studien, um die Durchführbarkeit und Wirksamkeit der Umsetzung organisierter Früherkennungsprogramme für Prostatakrebs zu bewerten. Diese sollten darauf abzielen, eine angemessene Behandlung und Qualität auf Grundlage des PSA-Tests, ggf. in Kombination mit einem Biomarker, jedoch zwingend mit MRI, sicherzustellen. Eine Stellungnahme der Schweizer Gesellschaft für Urologie (SGU) hinsichtlich einer solchen Bestrebung wird für den kommenden Herbst erwartet.
Literatur:
1 Cirillo P et al.: Schweizerischer Krebsbericht 2021. Neuchâtel: BFS, 2021 2 ReFaey K et al.: Cancer mortality rates increasing vs cardiovascular disease mortality decreasing in the world: future implications. Mayo Clin Proc Innov Qual Outcomes 2021; 5: 645-53 3 Bratt O: Organised prostate cancer testing. 2023. https://cancercentrum.se/samverkan/vara-uppdrag/prevention-och-tidig-upptackt/prostatacancertestning/organised-prostate-cancer-testing/ ; zuletzt aufgerufen am 15.8.2023 4 Jemal A et al.: Prostate cancer incidence 5 years after US Preventive Services Task Force recommendations against screening. J Natl Cancer Inst 2021; 113: 64-71 5 Andriole GL et al.: Mortality results from a randomized prostate-cancer screening trial. N Engl J Med 2009; 360: 1310-9 6 Shoag JE et al.: Reevaluating PSA testing rates in the PLCO trial. N Engl J Med 2016; 374: 1795-6 7 Hugosson J et al.: A 16-yr follow-up of the European randomized study of screening for prostate cancer. Eur Urolol 2019; 76: 43-51 8 Bretthauer M et al.: Effect of colonoscopy screening on risks of colorectal cancer and related death. N Engl J Med 2022; 387: 1547-56 9 Hugosson J et al.: Prostate cancer screening with PSA and MRI followed by targeted biopsy only. N Engl J Med 2022; 387: 2126-37 10 Eklund M et al.: MRI-targeted or standard biopsy in prostate cancer screening. N Engl J Med 2021; 385: 908-20 11 Crawford ED et al.: An approach using PSA levels of 1.5ng/mL as the cutoff for prostate cancer screening in primary care. Urol 2016; 96: 116-20 12 Grönberg H et al.: Prostate cancer screening in men aged 50-69 years (STHLM3): a prospective population-based diagnostic study. Lancet Oncol 2015; 16: 1667-76 13 Eklund M et al.: The Stockholm-3 (STHLM3) model can improve prostate cancer diagnostics in men aged 50-69 yr compared with current prostate cancer testing. Eur Urol Focus 2018; 4: 707-10 14 Gøtzsche PC, Nielsen M: Screening for breast cancer with mammography. Cochrane Database Syst Rev 2011; (1): CD001877 15 Ong HT: Beta blockers in hypertension and cardiovascular disease. BMJ 2007; 334: 946-9 16 Uhlig K et al.: Assessment on implantable defibrillators and the evidence for primary prevention of sudden cardiac death. Rockville (MD): Agency for Healthcare Research and Quality (US), 2013
Das könnte Sie auch interessieren:
Drogen und Anabolika: vom Sportplatz auf die Intensivstation
Anabolika und Drogen sind im Sport verboten. Athlet:innen nehmen dennoch immer wieder solche Substanzen ein – und riskieren neben Disziplinarverfahren vor allem auch ihre Gesundheit oder ...
Screening psychosozialer Faktoren in der Schmerzmedizin
Psychosoziale Faktoren beeinflussen in Interaktion mit biologischen Faktoren die Entstehung, Chronifizierung und Aufrechterhaltung von Schmerzen und sollten deshalb frühzeitig erfasst ...
Herpes zoster im Gesicht
Während ein Herpes zoster im Bereich des Thorax meist gut hausärztlich behandelt werden kann, empfiehlt sich bei einem Auftreten im Kopf-Hals-Bereich meist die interdisziplinäre ...