Modulation du microbiote dans le côlon irritable – pertinent ou non?
Auteur:
Prof. Dr méd. Peter C. Konturek
Thüringen-Kliniken «Georgius Agricola» GmbH Saalfeld
Akademisches Lehrkrankenhaus der Universitätsklinik Jena
E-mail: pkonturek@thueringen-kliniken.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Chez la plupart des patients atteints du syndrome du côlon irritable (SCI), une dysbiose intestinale, c’est-à-dire un déséquilibre qualitatif et quantitatif du microbiote intestinal, peut être mis en évidence. Il existe différentes possibilités ciblées pour la modulation du microbiote.
Keypoints
-
Le syndrome du côlon irritable (SCI) est la maladie gastro-intestinale fonctionnelle la plus fréquente.
-
La pathogenèse du côlon irritable est multifactorielle, la dysfonction de l’axe microbiote-intestin-cerveau jouant un rôle central. Il est désormais bien établi que le microbiote intestinal contribue de manière significative au maintien de l’homéostasie et d’une multitude de processus physiologiques différents.
-
Une modulation du microbiote intestinal par des probiotiques, des antibiotiques (rifaximine), une transplantation de microbiote fécal ou un régime FODMAP est pertinente et permet de soulager significativement les symptômes du SCI.
Le syndrome du côlon irritable (SCI) est le trouble fonctionnel du tractus gastro-intestinal le plus fréquent.1 Il s’accompagne d’un certain nombre de troubles physiopathologiques, tels qu’une augmentation de la perméabilité de la barrière intestinale, un trouble du système immunitaire local, une sécrétion anormale, une sensibilité viscérale accrue, une motilité intestinale pathologique, un déséquilibre du microbiote intestinal et, enfin, des comorbidités psychiatriques concomitantes, telles que la dépression ou le trouble anxieux.2
Origine du côlon irritable et dysbiose intestinale
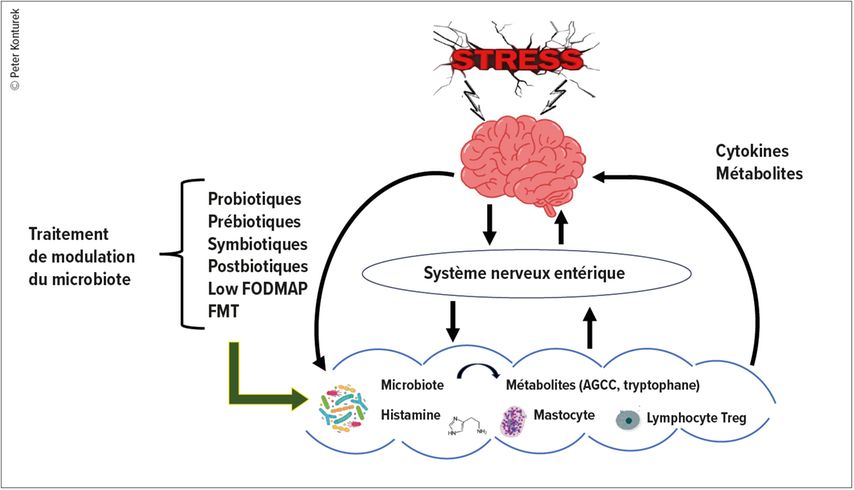
Le SCI se caractérise en premier lieu par une dysfonction de l’axe intestin-cerveau (AIC), c’est-à-dire une communication bidirectionnelle entre les systèmes nerveux entérique et central (Fig.1).3 La plupart des patients atteints du SCI présentent une dysbiose intestinale, c’est-à-dire un déséquilibre qualitatif et quantitatif du microbiote qui a un impact négatif sur l’activité de l’AIC. À cela s’ajoutent de nombreuses modifications du microenvironnement de la muqueuse intestinale (p.ex. l’activation des mastocytes avec augmentation de la libération d’histamine, troubles du système immunitaire inné et adaptatif). Suite à ces processus pathologiques, une micro-inflammation se développe dans la muqueuse des patients concernés. Tout cela peut entraîner l’apparition des symptômes du côlon irritable.4
Fig. 1: Influence de la dysbiose intestinale sur l’axe intestin-cerveau (AIC) et options thérapeutiques de modulation du microbiote
Cette apparition est multifactorielle. En premier lieu, de nombreuses études ont pu mettre en évidence des modifications quantitatives et qualitatives du microbiote intestinal dans le cas du côlon irritable. Les analyses du microbiome fécal des patients concernés montrent une réduction significative des bactéries commensales (p.ex. bifidobactéries, lactobacilles), mais une augmentation significative des taxons bactériens pro-inflammatoires, tels que les Enterobacteriaceae.5
Les conséquences de la dysbiose intestinale ne sont pas seulement des modifications structurelles du microbiote intestinal, mais aussi des changements significatifs dans la production de métabolites microbiens. Récemment, un groupe de travail de Göteborg a mis en évidence une différence significative entre les profils des métabolites chez les patients atteints du SCI et ceux des témoins sains.6
Les mécanismes exacts qui conduisent à la dysbiose intestinale n’ont pas été suffisamment clarifiés jusqu’à présent. Les études de ces dernières années fournissent une série de preuves démontrant que l’exposition des femmes enceintes ou des enfants, dans les premiers mois suivant la naissance, aux antibiotiques, au stress ou à une mauvaise alimentation, en plus de la prédisposition génétique, peut favoriser la survenue du SCI.7 D’autre part, les infections jouent également un rôle extrêmement important en tant qu’élément déclencheur; on parle de SCI post-infectieux.8 Environ 10% de tous les cas de côlon irritable peuvent être attribués à cette cause. Le SCI post-Covid en est un exemple. Il se caractérise par des douleurs abdominales récurrentes et réfractaires au traitement dues à une hypersensibilité viscérale accrue et à une modification de la motilité intestinale.9
Modulation du microbiote
La modulation du microbiote constitue une approche prometteuse du SCI (Fig.1). Il s’agit notamment de l’utilisation d’antibiotiques, de probiotiques, de prébiotiques, de symbiotiques, de postbiotiques et de la transplantation de microbiote fécal.10
Une option thérapeutique prometteuse est l’utilisation de la rifaximine. Il s’agit d’un antibiotique à large spectre non absorbable qui module positivement le microbiote intestinal et améliore les symptômes, surtout en cas de SCI avec diarrhée.11
D’autre part, les médecins ont également à leur disposition de nombreux probiotiques. Ces bactéries positives renforcent la fonction de barrière, ont une influence positive sur l’immunomodulation, présentent des effets anti-inflammatoires et inhibent également l’invasion de bactéries pro-inflammatoires.12 De nombreuses études randomisées menées avec des probiotiques par rapport à un placebo mettent en évidence un effet positif de ce traitement.13
Les aliments fermentés, appelés probiotiques naturels, tels que le kimchi, la choucroute, le miso, le natto, le réjuvélac, le kombucha, le kéfir ou le yaourt, peuvent également avoir une influence positive sur la composition et la fonction des bactéries intestinales.14
Outre les probiotiques, les prébiotiques jouent un rôle important dans le traitement des patients atteints du SCI. Ce sont des composants alimentaires non digestibles (p.ex. inuline, xylo-oligosaccharides ou fructo-oligosaccharides) qui ont un effet positif sur leur hôte en stimulant spécifiquement la croissance et/ou l’activité d’une ou de plusieurs espèces de bactéries dans le côlon, améliorant ainsi la santé de l’hôte. Ils stimulent la production d’acides gras à chaîne courte, augmentent la biomasse dans l’intestin, fournissent plus d’énergie aux cellules du côlon et, enfin, inhibent également la croissance des bactéries négatives et peuvent avoir un effet positif sur l’évolution du pH dans l’intestin. Les prébiotiques sont aussi présents dans différents aliments, tels que l’endive, le topinambour, l’artichaut, le poireau, l’oignon ou le salsifis. Les prébiotiques et les probiotiques peuvent être associés pour obtenir un symbiotique ayant un effet renforcé sur l’immunomodulation et les réactions métaboliques dans l’intestin.15
Les postbiotiques constituent une autre option pour la modulation du microbiote intestinal. Il s’agit de micro-organismes inanimés ou de leurs composants, ou de certains produits métaboliques (p.ex. butyrate). Le principal effet des postbiotiques est de renforcer le système immunitaire local et d’améliorer la fonction de la barrière intestinale.16
La transplantation de microbiote fécal (c’est-à-dire le transfert de selles d’un donneur sain dans l’intestin d’un patient malade par endoscopie ou capsules) est une autre possibilité pour modifier la composition du microbiote intestinal. La FMT permet en premier lieu d’améliorer la diversité du microbiote. Il s’agit toutefois d’une méthode complexe qui nécessite une préparation en laboratoire ainsi que la sélection d’un donneur sain approprié.17 Les méta-analyses montrent des résultats très variables, allant de négatifs à positifs, en fonction de la dose, de la durée du traitement et de la voie d’administration (voie gastro-intestinale supérieure par rapport à inférieure).18
Enfin, un régime pauvre en FODMAP (low FODMAP), c’est-à-dire en oligosaccharides, disaccharides, monosaccharides et polyols fermentescibles, constitue également une option importante pour la modulation du microbiote intestinal. Ce type de régime alimentaire a un effet favorable sur les symptômes du côlon irritable,19 son efficacité est d’ailleurs confirmée par les méta-analyses de nombreuses études. Il se déroule en trois phases: élimination, test de tolérance et alimentation à long terme. C’est pourquoi les patients concernées ont besoin de l’aide de diététiciens.
Littérature:
1 Sperber AD: Epidemiology and burden of irritable bowel syndrome: an international perspective. Gastroenterol Clin North Am 2021; 50: 489-503 2 Huang KY et al.: Irritable bowel syndrome: Epidemiology, overlap disorders, pathophysiology and treatment. World J Gastroenterol 2023; 29: 4120-35 3 Konturek PC, Zopf Y: Therapeutic modulation of intestinal microbiota in irritable bowel syndrome. From probiotics to fecal microbiota therapy. MMW Fortschr Med 2016; 158: 12-6 4 Simrén M: Targeting the gut microenvironment in IBS to improve symptoms. Nat Rev Gastroenterol Hepatol 2023; 20: 69-70 5 Pittayanon R et al.: Gut microbiota in patients with irritable bowel syndrome – a systematic review. Gastroenterol 2019; 157: 97-108 6 Ahluwalia B et al.: A distinct faecal microbiota and metabolite profile linked to bowel habits in patients with irritable bowel syndrome. Cells 2021; 10: 1459 7 Zhou GQ et al.: Early life adverse exposures in irritable bowel syndrome: new insights and opportunities. Front Pediatr 2023; 11: 1241801 8 Lupu VV et al.: Emerging role of the gut microbiome in post-infectious irritable bowel syndrome: A literature review. World J Gastroenterol 2023; 29: 3241-56 9 Marasco G et al.: Post COVID-19 irritable bowel syndrome. Gut 2022: gutjnl-2022-328483 10 Zhao Y, Zou DW: Gut microbiota and irritable bowel syndrome. J Dig Dis 2023; 24: 312-20 11 Goodoory VC, Ford AC: Antibiotics and probiotics for irritable bowel syndrome. Drugs 2023; 83: 687-99 12 Mazzawi T: Gut microbiota manipulation in irritable bowel syndrome. Microorganisms 2022; 10: 1332 13 Goodoory VC et al.: Efficacy of probiotics in irritable bowel syndrome: systematic review and meta-analysis. Gastroenterology 2023; 165: 1206-18 14 Garnås E: Fermented vegetables as a potential treatment for irritable bowel syndrome. Curr Dev Nutr 2023; 7: 100039 15 Simon E et al.: Probiotics, prebiotics and synbiotics: implications and beneficial effects against Iirritable bowel syndrome. Nutrients 2021; 13: 2112 16 Bednarska O et al.: A postbiotic fermented oat gruel may have a beneficial effect on the colonic mucosal barrier in patients with irritable bowel syndrome. Front Nutr 2022; 9: 1004084 17 Stallmach A et al.: Fecal Microbiota Transfer (FMT) in Germany – status and perspective. Z Gastroenterol 2023; doi: 10.1055/a-2075-2725 18 Myneedu K et al.: Fecal microbiota transplantation in irritable bowel syndrome: A systematic review and meta-analysis. United European Gastroenterol J 2019; 7: 1033-1041 19 Liu J et al.: Low-FODMAP Diet for Iirritable bowel syndrome: What we Know and what we have yet to learn. Annu Rev Med 2020; 71: 303-14 20 van Lanen AS et al.: Efficacy of a low-FODMAP diet in adult irritable bowel syndrome: a systematic review and meta-analysis. Eur J Nutr 2021; 60: 3505-22
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...