Long Covid
Autorinnen:
Dr. med. Schirin Frey
Oberärztin
KD Dr. med. Elisabeth Weber
Chefärztin
Klinik Innere Medizin Waid
Stadtspital Zürich
E-Mail: schirin.frey@stadtspital.ch
E-Mail: elisabeth.weber@stadtspital.ch
Die Covid-19-Pandemie mit schweren Verläufen brachte vielerorts das Gesundheitswesen an seine Grenzen. Nach Abklingen der Pandemie stellen Langzeitfolgen Betroffene wie auch Fachleute vor eine Herausforderung – sowohl Diagnose als auch Management der Post-Covid-19-Erkrankung ist komplex und erfordert einen interdisziplinären und interprofessionellen Ansatz.
Keypoints
-
Die Diagnose des Post-Covid-19-Syndroms beruht auf der typischen Anamnese (insbesondere Fatigue, PEM, unerholsamer Schlaf).
-
Die im Juni 2023 publizierten Schweizer Richtlinien26 sollen den Grundversorger:innen helfen, die Patient:innen zu begleiten und abzuklären.
-
Therapeutisch zentral sind edukative Massnahmen (Energiemanagement) durch alle im interprofessionellen Team tätigen Behandler:innen.
-
Es gibt keine medikamentöse kausale Therapie, allerdings können individuell je nach Symptomencluster Medikamente eingesetzt werden.
Anfang Mai 2023 erklärte die WHO den durch die Covid-19-Pandemie bedingten Gesundheitsnotstand als beendet. Während die Mehrheit der Genesenen in den normalen Alltag zurückkehren kann, gilt dies nicht für Patient:innen mit einem Post-Covid-19-Syndrom (PCS).
Bereits früh in der Pandemie häuften sich Berichte über länger andauernde Krankheitssymptome nach Abheilen der akuten Infektion mit SARS-CoV-2. Dies ist nicht neu, allerdings sind postinfektiöse Syndrome mit dem Hauptsymptom Fatigue selbst vielen Ärzt:innen kein Begriff. Beschrieben sind sie unter anderem nach mild verlaufenden Infektionen mit dem Epstein-Barr-Virus (EBV), dem humanen Herpesvirus Typ 6 (HHV6) und dem Parvovirus B19.1
Schwerpunkt dieses Artikels ist das PCS, welches nach mildem Verlauf auftreten kann. Davon abzugrenzen sind Folgekomplikationen durch Organschäden oder ein Post-ICU-Syndrom nach schweren Verläufen einer akuten Covid-19-Erkrankung.
Definition
Die Ende 2020 veröffentlichte Guideline des britischen National Institute for Health and Care Excellence (NICE)2 beschreibt die Erkrankung als Syndrom, das länger als 4 Wochen nach der Infektion andauert und nicht anders erklärt werden kann. Im Zeitraum zwischen 4 und 12 Wochen spricht die NICE-Definition von «Ongoing Symptomatic Covid-19», ab 12 Wochen von einem Post-Covid-19-Syndrom. Diese zeitliche Unterteilung von Long Covid (als Überbegriff) macht Sinn, da sich viele Patient:innen bis zum Ende des 3. Monats nach der Infektion erholen.
Die WHO3 prägte den Begriff «Post Covid Condition». Hier fliesst ein, dass die Symptome nach der akuten Erkrankung verschwinden können, aber innerhalb von 3 Monaten wieder auftreten können und dann mindestens 2 Monate anhalten. Da zu Beginn der Pandemie noch nicht und nach Ende nicht mehr breitflächig getestet wurde, ist eine nachgewiesene Infektion gemäss WHO-Definition nicht erforderlich. Anamnestische Angaben über eine mit Covid-19 vereinbare Symptomatik zu Beginn der Beschwerden können akzeptiert werden. Da auch asymptomatische Infektionen zu einem PCS führen können, muss selbst dann ein PCS in Betracht gezogen werden.3,4
Symptome
PCS-Symptome sind heterogen und betreffen praktisch alle Organsysteme. Typischerweise sind Beschwerden nicht konstant, können sich in der Intensität verändern, verschwinden und wieder auftreten.5
Alle Patient:innen sind mehr oder weniger ausgeprägt von Fatigue betroffen, die wahrscheinlich als pathognomonisches Symptom angesehen werden muss. Es gibt keine eindeutige Definition des Begriffs «Fatigue» und die Abgrenzung gegenüber Müdigkeit oder Erschöpfung ist unscharf. Fatigue bezeichnet am ehesten eine unverhältnismässig schwere Erschöpfung, welche durch längere Erholung nicht beseitigt werden kann.6
Zudem wird das Symptom «Post Exertional Malaise» (PEM) gefordert. Dabei handelt es sich um sogenannte «Crashs», die nach Belastungen an der neuen, deutlich niedrigeren Belastungsgrenze (physisch, kognitiv und emotional) im Sinne einer schwersten Fatigue auftreten.
Dieser Symptomenkomplex ist bereits gut bekannt und definiert im Rahmen von «Myalgic Enzephalomyelitis/Chronic Fatigue Syndrome» (ME/CFS). ME/CFS erfordert zur Diagnosestellung eine Beschwerdedauer >6 Monate – es muss wohl davon ausgegangen werden, dass bei vielen Patient:innen das PCS in ein ME/CFS übergeht.
Definition «Fatigue» nach CDC:7
-
Eine substanzielle Verschlechterung des möglichen Aktivitätslevels im Vergleich zu der Zeit vor der Erkrankung
-
Post-exertional Malaise (PEM)
-
Unerholsamer Schlaf
Die PEM kann folgendermassen definiert werden:8
-
Verschlechterung der Symptome nach physischer/kognitiver/emotionaler Anstrengung
-
Auftreten häufig verzögert 12 bis 48 Stunden nach der auslösenden Aktivität
-
Symptomschwere und -dauer überproportional zur auslösenden Aktivität
-
Dauer von Tagen, Wochen oder länger
-
Bei einigen Patienten kann Reizüberflutung (Licht, laute Umgebung) PEM auslösen.
Die CDC-Definition eignet sich im Alltag für ein erstes Bild – eine vertiefte Diagnostik, auch hinsichtlich eines Übergangs in ein ME/CFS, gelingt über die Canadian Consensus Criteria mit einem Fragebogen.9
Eine Übersichtsarbeit zeigt, dass neben dem Symptomcluster Fatigue mit Belastungsintoleranz und PEM vorwiegend über 2 weitere Symptomcluster berichtet wird: kognitive Probleme («brain fog» mit Gedächtnis-, Konzentrations-, Wortfindungsstörungen etc.) und respiratorische Beschwerden wie z.B. Kurzatmigkeit, Thoraxschmerzen und Husten.10 Die klinische Erfahrung aus der Sprechstunde bestätigt dies, es können jedoch beliebige Überlagerungen der Cluster auftreten und Zusatzsymptome hinzukommen. Diese sind vielfältig – hierzu gehören insbesondere Symptome des autonomen Nervensystems wie Tachykardien, das posturale orthostatische Tachykardie-Syndrom (POTS), Schwindel, orthostatische Intoleranz. Ausserdem treten immunologische Phänomene mit Krankheitsgefühl, Fieber, erhöhte Infektanfälligkeit und Halsschmerzen auf. Hinzu kommen neben weiteren allgemeinen Schmerzen (Muskeln, Kopf, Gelenke)11 Missempfindungen (Kribbeln, Vibrieren).12
In allen Fällen führen die Beschwerden zu einer schweren Beeinträchtigung der Funktionsfähigkeit bis hin zur Pflegebedürftigkeit und stellen damit für Primärversorger:innen, Gesundheitsinstitutionen, aber auch sozioökonomisch eine Herausforderung dar.
Epidemiologie
Die Datenlage zur Häufigkeit eines PCS ist heterogen, eine Metaanalyse beschreibt Inzidenzen von 7,5–41% bei nicht hospitalisierten Patient:innen.13 Limitationen, die eine korrekte Schätzung erschweren, sind grosse methodische Unterschiede der Studien, u.a. nur wenige Studien mit Kontrollgruppen, Unterschiede bei der Beobachtungsdauer, Schwere der Infektion mit/ohne Hospitalisation, Zusammensetzung der Studienpopulation, Erhebung der Funktionseinschränkungen.4
Auszugehen ist wahrscheinlich von einer Häufigkeit von ca. 6% (Hochrechnung).10,14,15 Wie viele der Erkrankten schwer und chronisch betroffen sein werden, muss der Verlauf zeigen. Zudem gibt es Hinweise, dass die Zahl der Betroffenen mit den neueren Virusvarianten abnimmt.15
Daten aus den USA zeigen eine präpandemische Prävalenz von ME/CFS von 0,4%.6 Nach den verfügbaren Daten zu PCS-Patient:innen, welche im Verlauf die Diagnose eines ME/CFS erfüllen (Canadian Consense Criteria),9 ist von einer Verdopplung6 bis Verdreifachung der aktuellen Prävalenz auszugehen.17
Risikofaktoren
Ein höheres Erkrankungsrisiko findet sich bei Frauen im jungen bis mittleren Alter.10 Neben Alter und Geschlecht scheint es weitere Risikofaktoren zu geben, es werden unter anderem das Vorhandensein von somatischen und psychischen Vorerkrankungen beschrieben, Adipositas, hohe Symptomlast während der akuten Infektion (>5 Symptome),13 ebenfalls werden Unterschiede bezüglich des sozioökonomischen Status und Ethnie genannt.18
Verlauf
Eine Metaanalyse über die Jahre 2020 und 2021 untersuchte Studien mit insgesamt 1,2 Millionen Covid-19-Genesenen. Bei 6% wurden 3 Monate nach der Infektion persistierende Symptome beschrieben, bei wiederum 15% davon bestanden nach 12 Monaten noch Beschwerden – wobei hier keine detaillierten Angaben zur Symptomschwere gemacht werden.10 Daten aus Grossbritannien (Beobachtung von 12 Symptomen bei über 20000 Covid-19-Erkrankten 2020–2021)19 kommen zu einem ähnlichen Resultat – nach 4 bis 6 Monaten stabilisiert sich der Anteil der Betroffenen im niedrigen zweistelligen Bereich, und wer nach 12 Monaten noch krank ist, scheint auch nach 2 Jahren noch auf einem ähnlichen Krankheitsniveau zu sein.15 Je nach Art der Symptome zeigt sich eine unterschiedliche Krankheitsdauer, insbesondere die Cluster Fatigue und Kognition haben auch nach 6 bis 12 Monaten noch einen relevanten Einfluss auf Befinden und Arbeitsfähigkeit.20 In unserer Sprechstunde zeigt sich genau dieses Bild: das Risiko einer Chronifizierung ist höher, je länger die Symptome andauern.
Pathomechanismus
Die Ursachen eines PCS sind nicht klar und Gegenstand intensiver Forschung. Erklärungsversuche lehnen sich an die bisher wenig untersuchten postinfektiösen Syndrome und die aktuellen Erkenntnisse zu SARS-CoV-2.
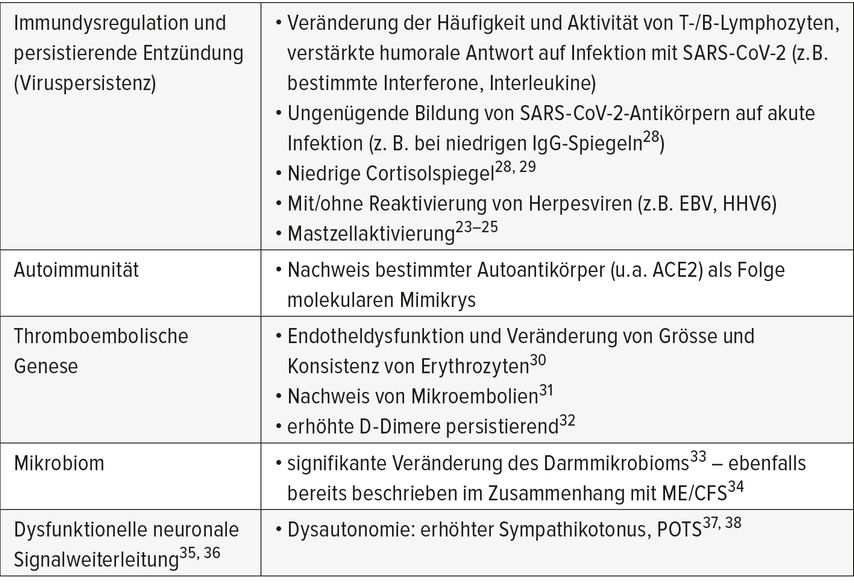
Die wichtigsten Hypothesen und eine Auswahl an Untersuchungsergebnissen verschiedener Studien zeigt Tabelle 1.
Darüber hinaus liefern mehrere Studien Hinweise auf eine Mitochondriendysfunktion.18 Eine Viruspersistenz wird ebenfalls diskutiert, in verschiedenen Studien konnten bis einige Monate nach der Infektion Virus oder Viruspartikel in Lunge und Darm nachgewiesen werden21 – jedoch auch bei asymptomatischen Patient:innen.22 Möglicherweise trägt diese Persistenz aber zur Immundysregulation bei.
Die Erklärungsansätze können sich überlagern. Interessant ist, dass sich diese Pathomechanismen auch bei anderen postviralen Syndromen wie ME/CFS beobachten lassen.18 Eine Übersichtsarbeit zu ME/CFS beschreibt die Erkrankung als «Multisystemerkrankung mit Dysregulation des Immunsystems, des autonomen Nervensystems, des Gefässsystems und des zellulären Stoffwechsels»6 – eine ebenfalls auf PCS zutreffende Beschreibung.
Weitere Überschneidungen finden sich zum Mastzellaktivierungssyndrom (MCAS). Eine frühe Studie mit PCS-Patient:innen zeigt identische Symptome wie solche mit bekanntem MCAS. Die Autor:innen schlussfolgern, dass eine Mastzellaktivierung pathophysiologisch bei der Entstehung von PCS-Symptomen eine Rolle spielt.23 Es gibt zudem die Vermutung, dass SARS-CoV-2 ein nicht diagnostiziertes MCAS triggern könnte.24,25 Entsprechend profitieren tatsächlich einige Patient:innen von einer probatorischen Therapie mit Antihistaminika.
Die gleichen Symptome wie bei einem PCS können sich auch nach Covid-19-Impfungen entwickeln, seriöse Angaben zur Häufigkeit eines «post-vaccination syndrome» gibt es nicht.
Diagnosestellung
Es gibt keinen spezifischen Marker zur Diagnosesicherung eines PCS. Die sorgfältige Anamnese (bezüglich Fatigue und PEM) und Abklärung der organbezogenen Beschwerden nach ärztlicher Massgabe ist wesentlich. Dabei ist die Diagnosestellung nicht exklusiv den Spezialsprechstunden vorbehalten – die Kenntnis der zum Teil langjährigen Patientengeschichte, wie es bei Hausärzt:innen der Fall ist, kann helfen, das Vorliegen eines PCS besser einzuschätzen.
Sinnvoll ist eine vollständige Erfassung der Symptome mittels Systemanamnese mit Augenmerk auf Fatigue, PEM und kognitiven Beschwerden, ausserdem Komorbiditäten, Medikation, Familien- und Sozialanamnese. Die ausführliche körperliche Untersuchung sollte ergänzt werden durch ein Basislabor, ausserdem können ein 6-Minuten-Gehtest oder ein Sit-to-stand-Test Hinweise auf eine zugrunde liegende pulmonale Erkrankung oder Dekonditionierung liefern. Spezialisierte Fragebögen eignen sich, um das Ausmass von Fatigue oder depressiven Symptomen zu erfassen.
Bei Hinweisen auf andere, möglicherweise erklärende Erkrankungen wie beispielsweise ein Asthma bronchiale oder ein obstruktives Schlafapnoesyndrom sollten diese fachärztlich abgeklärt werden.
Abbildung 1 zeigt einen möglichen Abklärungs- und Behandlungsalgorithmus.
Mittlerweile gibt es verschiedene Richtlinien zur Abklärung eines PCS. Im Juni 2023 sind die schweizerischen Empfehlungen für primärbehandelnde Ärzt:innen erschienen.26 Hilfreich wird es in Zukunft sein, wenn alle Behandler:innen sich an diese Guidelines halten (Fragebogen, Tests), damit die Verläufe vergleichbar werden.
Therapie
Die Betreuung von PCS-Patient:innen stellt eine Herausforderung dar. Nach wie vor existiert keine ursächliche Therapie, wobei der Leidensdruck durch eine symptomorientierte Therapie deutlich gemindert und eine gewisse Stabilisierung erreicht werden kann. Im Vordergrund stehende Beschwerden wie chronische Kopfschmerzen und Schlafstörungen sollten leitliniengerecht behandelt werden, dasselbe gilt für neu diagnostizierte Komorbiditäten wie eine Depression oder ein Asthma bronchiale.
Eine besondere Herausforderung ist der Umgang mit der Fatigue und der damit verbundenen Belastungsintoleranz/PEM. Im Gegensatz zur Fatigue bei nicht postviralen Syndromen und psychiatrischen Erkrankungen führt eine (übermässige) Aktivierung zur Verschlechterung der Symptome (PEM). Zentral ist daher bei allen PCS-Patient:innen die Vermeidung von Überbelastungen. Instrumente sind das Erlernen von Techniken, welche helfen, den Alltag an die reduzierten Energieressourcen anzupassen: Das sogenannte Pacing (Energie- und Pausenmanagement) nimmt eine zentrale Stellung ein. Bezüglich Fatigue erfahrene Physio- und Ergotherapeut:innen schulen Patient:innen im Erkennen individueller Grenzen und in Methoden zur Selbstwirksamkeit – sehr zurückhaltende Bewegung kann positive Auswirkungen haben und eine langsame Steigerung ermöglichen. Niederschwellig sollte ausserdem eine psychologische Anbindung zum Erlernen von Coping-Strategien erfolgen. Ergänzend helfen je nach Symptomatik Schlafhygiene, Atem- und Entspannungsübungen. Für eine Therapie mit Blutverdünnern oder antiviralen Medikamenten sowie für die hyperbare Sauerstofftherapie, Plasmapherese etc. ist die Evidenz noch dünn. Studien dazu sind im Gang.
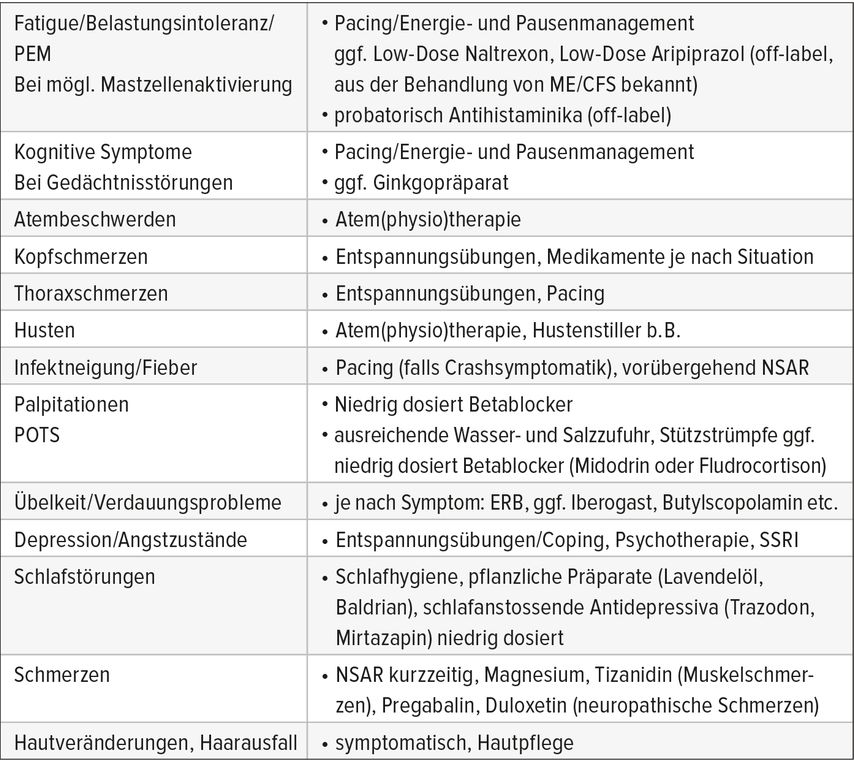
Eine Auswahl der wichtigsten Symptome und deren Management zeigt Tabelle 2.
Tab. 2: Häufigste Symptome und mögliches Management (nach Ausschluss anderweitiger Ursachen). Kein Anspruch auf Vollständigkeit
Zur Entlastung im Beruf ist eine frühe und hochprozentige Arbeitsunfähigkeit vielfach leider unumgänglich. Bei Stabilisierung der Symptomatik sollte das Pensum nur langsam und graduell gesteigert werden, um im längerfristigen Verlauf Symptomverschlechterungen zu vermeiden. Aus Erfahrung sind die Patient:innen höchst motiviert, in den Arbeitsprozess zurückzukehren, aber die reale Angst vor Crashs (PEM) ist dominant – und auch daran muss gearbeitet werden (edukativ, medikamentös, therapeutisch). Allerdings ist der Aufbau von psychosozialem Druck diesbezüglich meist kontraproduktiv.
In regelmässigen Hausarztkonsultationen sollten im Sinne des biopsychosozialen Krankheitsmodells neben den Veränderungen von körperlichen Symptomen ebenfalls Psyche und Bedingungen im Umfeld erfragt werden. Erfahrungen aus unserer Sprechstunde zeigen, dass die Unterstützung durch ambulante Pflege und Hausbesuche wertvoll sein können. Selbsthilfegruppen können sozialer Isolation und Ausgrenzung entgegenwirken6 und gegenseitiges Verständnis und Erfahrungsaustausch helfen, weitere Bewältigungsstrategien zu entwickeln.
Führen ambulante Massnahmen über mehrere Monate zu keiner Besserung, ist eine stationäre Rehabilitation zu erwägen – unterdessen bieten mehrere Kliniken in der Schweiz spezialisierte Post-Covid-19-Rehabilitationsprogramme an.
Aufgrund des langwierigen Verlaufs ist eine IV-Anmeldung zu evaluieren – diese kann bei der Wiedereingliederung bei empfohlenem niedrigem Pensum hilfreich sein.
Mittlerweile werden verschiedene Therapieansätze untersucht, ein Review zählt 388 Studien mit breit gefächerten und heterogen aufgebauten Studien (Stand 1. Januar 2023).27 Dazu zählen medikamentöse Versuche, beispielsweise mit Antihistaminika, niedrig dosiertem Naltrexon oder Aripiprazol. Auch in der Schweiz laufen Studien, beispielsweise mit Temelimab, einem Medikament aus der Multiple-Sklerose-Behandlung.
Neben verschiedenen Rehabilitationsmassnahmen werden Patientenedukation, psychotherapeutische Interventionen, komplementär- und alternativmedizinische Ansätze und weitere Massnahmen wie beispielsweise Vagusstimulationen und Sympathikusblockaden untersucht, ausserdem Plasmapherese, Kryotherapie, transkranielle Nervenstimulationen, Ernährungsumstellung.27
Wir machen die Erfahrung, dass die psychoedukativen Massnahmen, Geduld, empathische Begleitung, symptomatische medikamentöse Therapie und möglichst wenig Druck im System den Genesungsprozess am positivsten beeinflussen.
Literatur:
1 Rasa S et al.: J Transl Med 2018; 16: 268 2 Sivan M, Taylor S: BMJ 2020; 371: m4938 3 https://www.who.int/publications/i/item/WHO-2019-nCoV-Post_Covid-19_condition-Clinical_case_definition-2021.1 ; zuletzt aufgerufen am 11.6.2023 4 https://www.rki.de/SharedDocs/FAQ/NCOV2019/FAQ_Liste_Gesundheitliche_Langzeitfolgen.html ; zuletzt aufgerufen am 11.6.2023 5 Bahmer T et al.: eClinicalMedicine 2022; 51: 101549 6 Renz-Polster H, Scheibenbogen C: Innere Medizin 2022; 63: 830-39 7 https://www.cdc.gov/me-cfs/about/index.html ; zuletzt aufgerufen am 11.6.2023 8 Institute of Medicine: Beyond myalgic encephalomyelitis/chronic fatigue syndrome: redefining an illness. Washington, DC: The National Academies Press, 2015 9 Carruthers BM et al.: J Chronic Fatigue Syndr 2003; 11: 7-115 10 Global Burden of Disease Long COVID Collaborators et al.: JAMA 2022; 328: 1604-15 11 Lopez-Leon S et al.: medRxiv 2021; 01.27.21250617 12 Oaklander AL et al.: Neurol Neuroimmunol Neuroinflamm 2022; 9: e1146 13 Nittas V et al.: Health Rev 2022; 43: 1604501 14 Ballering AV et al.: Lancet 2022; 400: 452-6115 Ballouz T et al.: BMJ 2023; 381: e074425 16 Jason LA, Mirin AA: Fatigue: Biomed Health Behav 2021; 9: 9-13 17 Roessler M et al.: PLoS Medicine 2022; 19: e1004122 18 Davis HE et al.: Nat Rev Microbiol 2023; 21: 133-46 19 https://www.ons.gov.uk/peoplepopulationandcommunity/healthandsocialcare/conditionsanddiseases/bulletins/newonsetselfreportedlongcovidaftercoronaviruscovid19reinfectionintheuk/latest ; zuletzt aufgerufen am 11.6.2023 20 Qiangru H et al.: Value Health 2022; 26: 934-42 21 Benjamin Chen et al.: eLife 12: e86015 22 Gaebler C et al.: Nature 2021; 591: 639-44 23 Weinstock LB et al.: Int J Infect Dis 2021; 112: 217-26 24 Arun S et al.: Br J Hosp Med 2022; 83: 1-10 25 Batiha GES et al.: Virol J 2022; 19: 158 26 https://www.rafael-postcovid.ch/en/informations-sante/post-covid-recommendations ; zuletzt aufgerufen am 11.6.2023 27 Fawzy NA et al.: Clin Microbiol Infect 2023; 29: 570-7 28 Su Y et al.: Cell 2022; 185: 881-95.e20 29 Klein J et al.: medRxiv 2022; 2022.08.09.22278592 30 Kubánková M et al.: Biophys J 2021; 120: 2838-47 31 Pretorius E et al.:Cardiovasc Diabetol 2021; 20: 172 32 Mandal S et al.: Thorax 2021; 76: 396-8 33 Yeoh YK et al.: Gut 2021; 70: 698-706 34 König RS et al.: Front Immunol 2022; 12: 628741 35 Proal AD, VanElzakker MB: Front Microbiol 2021; 12: 698169 36 Yong SJ: ACS Chem Neurosci 2021; 12: 573-80 37 Blitshteyn S, Whitelaw S: Immunologic Res 2021; 69: 205-11 38 Astin R et al.: Kompass Pneumologie 2023; 11: 60-7
Das könnte Sie auch interessieren:
Klimakosten im Gesundheitswesen – eine massiv unterschätzte Folge der Erderwärmung
Auch wenn sich viele Konsequenzen erst langfristig zeigen: Die klimatischen Veränderungen haben Folgen für unsere Gesundheit. Dennoch werden die Gesundheit und die Gesundheitskosten in ...
Was tun bei Medikamentenunverträglichkeit?
Wenn Patientinnen und Patienten in die Praxis kommen und über eine Medikamentenunverträglichkeit klagen, gilt es herauszufinden, ob dies tatsächlich der Fall ist. Wie man dabei vorgeht ...
Der Tiefenrausch ist eine häufige Ursache für einen Tauchunfall
Atemgase verändern sich in der Wassertiefe physikalisch, was physiologische und medizinische Folgen bei Taucher:innen haben kann. Sauerstoff beispielsweise wird beim Abtauchen in der ...