Schwangerschaft, post partum und Eisenmangel: welche Rolle für den Hausarzt?
Die Inzidenz der Anämie in der Schwangerschaft ist hoch. Infolge einer Vasodilatation und Hämodilution kommt es zu einem physiologischen Hämoglobinabfall in der Schwangerschaft. Gleichzeitig nehmen aber auch die Erythrozytenproduktion und damit verbunden der Eisenbedarf zu. Der Eisenmangel ist die häufigste Ursache für eine Anämie in der Schwangerschaft und mit einer Zunahme der maternalen und fetalen Morbidität und Mortalität assoziiert.1 Eine weitere Ursache für das Auftreten einer Anämie in der Schwangerschaft sind Hämorrhagien.2 Insbesondere das Auftreten postpartaler Hämorrhagien hat in den letzten Jahren zugenommen.
«Ein hohes Risiko für eine Anämie haben Frauen, bei denen ein Blutverlust über 500 ml zu erwarten ist, und solche mit einem niedrigen Hämoglobin. Bei einer Schwangerschaft trifft bei den meisten Frauen eines davon zu. Eine von zwei Frauen wird in der Schwangerschaft anämisch werden.»
M. Müller, Bern
Durch ein effizientes Patient Blood Management lässt sich das Risiko für eine Anämie in der Schwangerschaft reduzieren. Der Hausarzt nimmt vor allem in der Prävention, im Rahmen der präkonzeptionellen Beratung von Frauen mit Kinderwunsch und bei der postpartalen Betreuung eine wichtige Rolle ein.
Das Ziel ist, einen Eisenmangel mit oder ohne Anämie in der Schwangerschaft zu erkennen oder auszuschliessen. Zu diesem Zweck sollte bei der ersten Schwangerschaftskontrolle im ersten Trimenon bei allen Frauen eine Kontrolle von Blutbild, Ferritin und CRP durchgeführt werden. Üblicherweise erhalten die Frauen zur Prävention 30–60 mg Eisen oral in Kombination mit 400 µg Folsäure.
Bei Schwangeren mit einer Eisenmangelanämie ist die Therapie abhängig von der Höhe des Hämoglobinwerts und dem Stadium der Schwangerschaft. Im ersten und zweiten Trimenon kann bei leichter Anämie (Hb < 110 g/l) ein orales Eisenpräparat (80–100 mg) kombiniert mit einer Folsäuresubstitution eingesetzt werden. Ab dem zweiten Trimenon kann eine i.v. Eisentherapie mit Eisencarboxymaltose indiziert sein, so zum Beispiel bei fehlendem Ansprechen auf die orale Therapie oder Unverträglichkeit der oralen Präparate. Diese Empfehlung gilt auch für Schwangere mit einer ausgeprägten Anämie (Hb < 80 g/l) sowie bei fortgeschrittener Schwangerschaft.
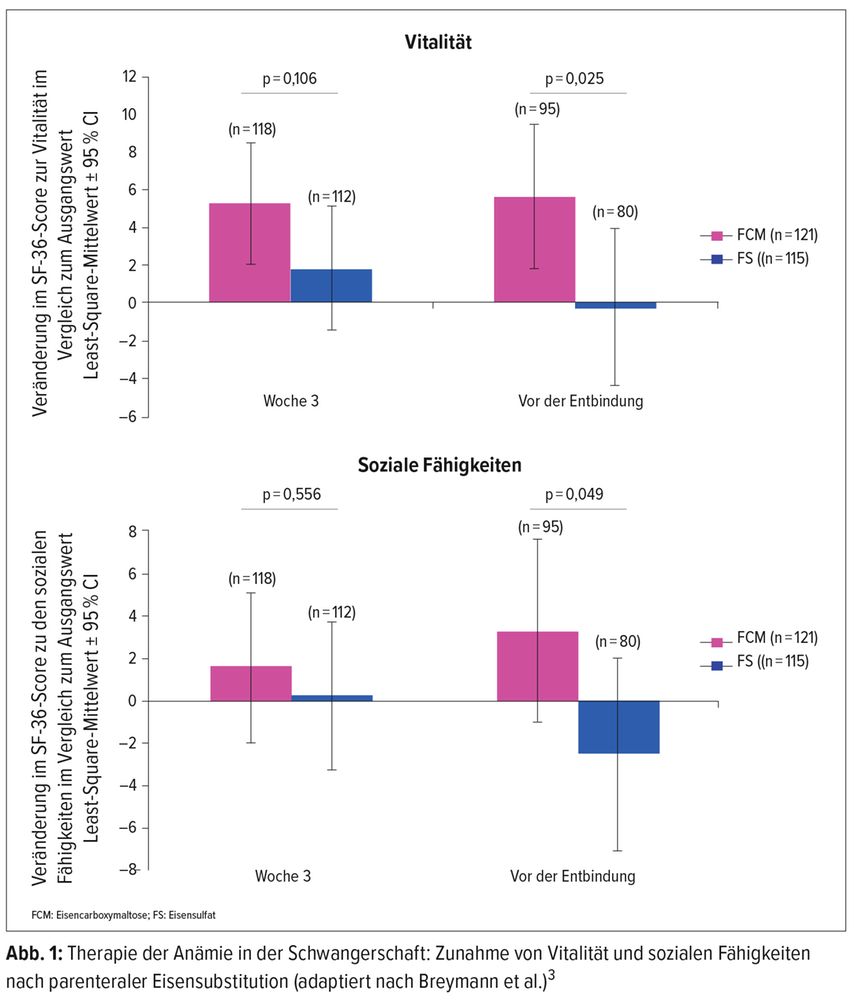
Die Evidenz für eine parenterale Eisensubstitution bei Schwangeren mit einer Eisenmangelanämie lieferte die FER-ASAP-Studie, in der bei mehr als 250 Frauen in der 16.–33. Schwangerschaftswoche und mit Eisenmangelanämie die parenterale Substitution von Eisencarboxymaltose (1000–1500 µg) mit oralem Eisensulfat (200 mg/d über 12 Wochen) verglichen wurde.3 Dabei konnte gezeigt werden, dass die parenterale Substitution in kürzerer Zeit und bei deutlich mehr Frauen zu einer Korrektur der Anämie führte. Das zeigte sich auch an der deutlichen Zunahme der Vitalität und den verbesserten sozialen Fähigkeiten (Abb. 1). Interessanterweise wiesen die Frauen, die eine parenterale Eisentherapie erhalten hatten, auch zum Zeitpunkt der Geburt höhere Ferritinwerte auf. Eine Beobachtungsstudie, die die Behandlung eines Eisenmangels mit/ohne Anämie mit i.v. Eisencarboxymaltose bei schwangeren Frauen untersuchte, zeigte, dass die parenterale Substitution unabhängig vom Schweregrad des Eisenmangels wirksam war und mit wenig unerwünschten Wirkungen einherging.4
Bericht: Regina Scharf, MPH; Redaktorin
Quelle:
Referat von Prof. Dr. Dr. med. Martin Müller, Leitender Arzt, Universitätsklinik für Frauenheilkunde, Bern, im Rahmen der Iron Academy, 19. November 2020, Zürich
Literatur
1. Means RT: Iron deficiency and iron deficiency anemia: implications and impact in pregnancy, fetal development, and early childhood parameters. Nutrients 2020; 12: 447
2. Perotto L et al.: Maternal mortality in Switzerland 2005–2014. Swiss Med Wkly 2020; 150: w20345
3. Breymann C et al.: Ferric carboxymaltose vs. oral iron in the treatment of pregnant women with iron deficiency anemia: an international, open-label, randomized controlled trial (FER-ASAP). J Perinat Med 2017; 45: 443-53
4. Froessler B et al.: Treatment of iron deficiency and iron deficiency anemia with intravenous ferric carboxymaltose in pregnancy. Arch Gynecol Obstet 2018; 298: 75-82
Kurzfachinformation
Ferinject®. Z: Eisencarboxymaltose. I: Eisenmangel, wenn orale Eisentherapie ungenügend wirksam, unwirksam oder nicht durchführbar ist. D: Die kumulative Gesamtdosis von Ferinject muss individuell berechnet werden. Ferinject kann als i.v. Infusion (verdünnt in 0,9% NaCl) oder als i.v. Injektion (unverdünnt) in wöchentlichen Einzeldosen von bis zu 20 mg/kg, maximal 1000 mg, bis zum Erreichen der berechneten kumulativen Gesamtdosis verabreicht werden. KI: Überempfindlichkeit gegenüber Wirkstoff oder Hilfsstoffen, Anämie ohne gesicherten Eisenmangel, Eisenüberladung, erstes Schwangerschaftstrimester. VM: Patienten vor jeder Verabreichung von Ferinject nach früheren UAW von i.v. Eisenpräparaten befragen. Nur anwenden, falls medizinisches Fachpersonal, das anaphylaktische Reaktionen bewerten und behandeln kann, sofort verfügbar ist, sowie nur in einer Einrichtung, in der alle Vorrichtungen zur Reanimation vorhanden sind. Patienten während mind. 30 Min. nach Verabreichung auf Anzeichen und Symptome einer Überempfindlichkeitsreaktion beobachten. Paravenöse Verabreichung kann eine braune Verfärbung und Reizung der Haut verursachen und ist deshalb zu vermeiden. Bei akuter oder chronischer Infektion, Asthma oder atopischen Allergien nur mit Vorsicht anwenden. Natriumgehalt von bis zu 5,5 mg/ml berücksichtigen. Parenterales Eisen kann zu Hypophosphatämie führen, in den meisten Fällen transient und ohne klinische Symptome. In Einzelfällen wurde bei Patienten mit bekannten Risikofaktoren und nach dauerhafter höherer Dosierung über behandlungsbedürftige Hypophosphatämie berichtet. S/S: KI im 1. Trimester, im 2. und 3. Trimester nur bei zwingender Indikation anwenden. Fetale Bradykardie kann infolge einer Überempfindlichkeitsreaktion der Mutter auftreten; Fetus sollte während der Verabreichung überwacht werden. UAW: Häufig: Hypophosphatämie, Kopfschmerzen, Gesichtsrötung (Flush), Schwindel, Hypertonie, Übelkeit, Reaktionen an der Injektions-/Infusionsstelle. Gelegentlich: Überempfindlichkeitsreaktionen vom Soforttyp, Parästhesien, Tachykardie, Hypotonie, Erröten, Dyspnoe, gastrointestinale Beschwerden, Dysgeusie, Hautausschlag, Pruritus, Urtikaria, Hautrötung, Myalgie, Rückenschmerzen, Arthralgie, Muskelkrämpfe, Gliederschmerzen, Fieber, Müdigkeit, Schmerzen im Brustkorb, peripheres Ödem, Schüttelfrost, Schmerz, Anstieg der AST, ALT, Gamma-GT, LDH und ALP. IA: Bei gleichzeitiger Verabreichung von oralen Eisenpräparaten ist deren Absorption reduziert. P: 5 Stechampullen zu 100 mg (2 ml) oder 500 mg (10 ml), 1 Stechampulle zu 500 mg (10 ml) oder zu 1000 mg (20 ml). Liste B. Detaillierte Informationen: www.swissmedicinfo.ch. Zulassungsinhaberin: Vifor (International) AG, CH-9001 St. Gallen. Vertrieb: Vifor AG, CH-1752 Villars-sur-Glâne. Stand: August 2020.