Entzündungsmarker zur Steuerung der Antibiotikatherapie auf verschiedenen Versorgungsebenen
Autoren:
José Knüsli
PD Dr. med. Noémie Boillat-Blanco
Service des maladies infectieuses
Centre hospitalier universitaire vaudois (CHUV) et
Université de Lausanne
E-Mail: jose.knusli@chuv.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Antibiotikaresistenzen drohen eine ganze Klasse von Arzneimitteln unwirksam gegenüber Krankheiten zu machen, die heute als leicht behandelbar gelten.1,2 Angesichts des Zusammenhangs zwischen dem Einsatz von Antibiotika und dem Auftreten von Resistenzen müssen dringend Mittel und Wege gefunden werden, diese Medikamente rational einzusetzen.3,4 Die meisten unnötigen Verordnungen finden bei ambulant erworbenen Atemwegsinfektionen statt.5
Keypoints
-
Die Bestimmung von Entzündungsmarkern (C-reaktives Protein und Procalcitonin) ermöglicht in Hausarztpraxen und Pflegeheimen eine sichere Reduktion der Zahl an Antibiotikaverordnungen bei Atemwegsinfektionen.
-
Bei Intensivpatienten mit schwerer Infektion ist es wichtig, die Antibiotikatherapie unabhängig von den Biomarker-Werten rasch einzuleiten.
-
Um mithilfe der Biomarker einen Effekt auf die Antibiotikaverordnung erreichen zu können, sollen sie nur bei Patienten gemessen werden, bei denen eine bakterielle Infektion durch die klinische Untersuchung allein nicht ausgeschlossen werden kann.
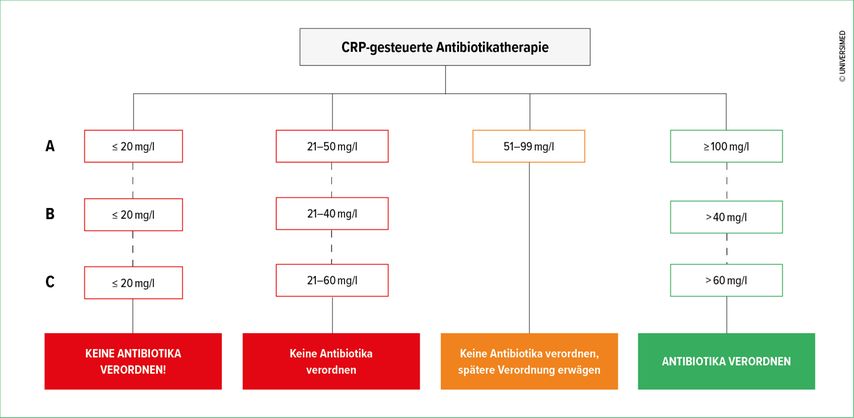
Bestimmte Entzündungsmarker lassen Rückschlüsse auf die bakterielle Ätiologie einer Infektion oder ihren Schweregrad zu und können somit bei Verordnungen als Orientierungshilfe dienen. Im Rahmen von Infektionen wurden mehr als 150 Biomarker untersucht.6 In diesem Artikel konzentrieren wir uns jedoch auf die beiden Biomarker – Procalcitonin und C-reaktives Protein (CRP) –, deren Einfluss auf die Verordnung von Antibiotika und die Sicherheit ihrer Anwendung bei ambulant erworbenen Atemwegsinfektionen in randomisiert kontrollierten Studien auf verschiedenen Versorgungsebenen untersucht wurde. Die in den verschiedenen Studien genutzten CRP- und Procalcitonin-Schwellenwerte sind in den Abbildungen 1 und 2 beschrieben.
Abb. 1: Schwellenwerte des C-reaktiven Proteins (CRP), die in verschiedenen randomisierten kontrollierten Studien zur Steuerung der Antibiotikatherapie auf 3 unterschiedlichen Versorgungsebenen angewendet wurden. A: Infektionen der unteren und oberen Atemwege in Praxen.8 B: COPD-Exazerbationen in Praxen10 C: Infektionen der unteren Atemwege in einem Pflegeheim16
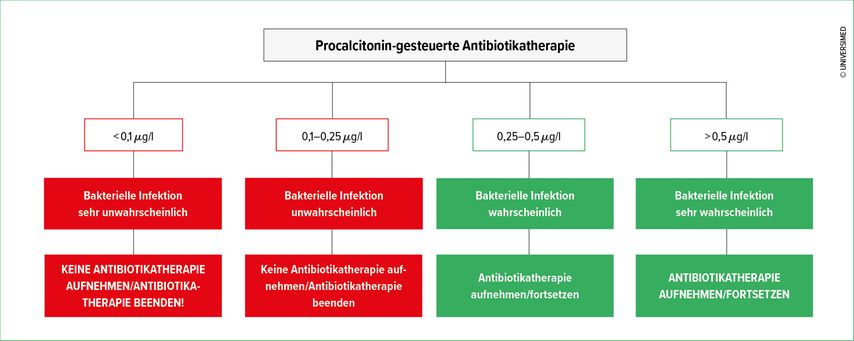
Abb. 2: Procalcitonin-Schwellenwerte, die in randomisierten kontrollierten Studien zur Steuerung der Antibiotikatherapie bei Infektionen der unteren Atemwege in Praxen (Verordnung von Antibiotika) und in Notaufnahmen (Aufnahme und Beendigung der Antibiotikatherapie) angewendet wurden7, 12
Hausarztmedizin
Eine kürzlich in 60 Schweizer Hausarztpraxen durchgeführte Studie mit 469 Patienten mit Infektionen der unteren Atemwege hat gezeigt, dass die Messung des Procalcitonins im Rahmen der POCT-Diagnostik («point-of-care test», patientennahe Sofortdiagnostik) zur Steuerung der Antibiotikatherapie zu einer deutlichen Reduktion der Antibiotikaverordnung führt: Diese sank von 70% in der Kontrollgruppe auf 40% bei den Patienten, deren Procalcitonin gemessen wurde (–26%; 95%CI: –41% bis –10%).7 Diese Reduktion war für die Patienten sicher und darüber hinaus mit dem Vorteil verbunden, dass weniger Röntgenuntersuchungen des Thorax durchgeführt wurden, die Zahl der Kontrolltermine gleichzeitig jedoch nicht zunahm: Die Nutzung von Procalcitonin war somit auch aus wirtschaftlicher Sicht effektiv.
In einer grossen multinationalen Studie zu Infektionen der unteren und oberen Atemwege bei 6771 Patienten aus 259 Hausarztpraxen wurden POCT-Messungen des CRP sowie Kommunikationsschulungen für Allgemeinmediziner untersucht. Mit beiden Interventionen, sowohl allein als auch in Kombination, war eine deutliche Reduktion der Antibiotikaverordnung zu beobachten.8 Zwölf Monate nach dieser Studie wurde in den gleichen Praxen eine Follow-up-Studie durchgeführt; diese ergab jedoch, dass die Allgemeinmediziner, die nur das CRP gemessen hatten, davon wieder abgerückt und ihre Antibiotikaverordnungen auf das Ursprungsniveau zurückgekehrt waren, während die in Kommunikation geschulten Mediziner weiterhin weniger Antibiotika verordneten.9 In einer britischen Studie mit 653 Patienten aus 86 Hausarztpraxen erwies sich das CRP bei der Behandlung von Exazerbationen einer COPD ebenfalls als nützlich und führte zu einer sicheren Reduktion der Antibiotikaverordnungen.10 Eine solche Reduktion der Verordnungen bei Infektionen der unteren Atemwege durch die POCT-Messung des CRP wurde auch in einem völlig anderen Versorgungskontext, dem der Pflegeheime, beobachtet. Eine kürzlich in 11 niederländischen Einrichtungen durchgeführte Studie mit 241 Patienten ergab eine absolute Reduktion der Verordnungsrate von 82% in der Kontrollgruppe auf 54% in der Interventionsgruppe.11 Auch dieser Rückgang war für die Patienten sicher und führte weder zu häufigerem Therapieversagen noch zu mehr Spitalaufnahmen; ferner war die Mortalität in beiden Gruppen gleich.
Notaufnahme
Der Effekt einer Procalcitonin-gesteuerten Antibiotikatherapie wurde auch in Spitälern untersucht. Eine in 6 Schweizer Notaufnahmen durchgeführte Studie, in der die Procalcitonin-Messung bei 1359 Patienten mit Infektionen der unteren Atemwege bewertet wurde, ergab zahlreiche Vorteile: eine kürzere Dauer der Antibiotikatherapie (Reduktion von 8,7 auf 5,7 Tage), eine geringere Rate an Antibiotikaverordnungen (Reduktion von 88% auf 75%; –13%; 95%CI: –16% bis –8,1%), aber auch eine Reduktion auf klinischer Ebene bei den mit Antibiosen verbundenen unerwünschten Wirkungen (Reduktion von 28 auf 20%).12 Diese Reduktion war gemessen an den unerwünschten Ereignissen und der Mortalität für die Patienten sicher. Wiederholte Procalcitonin-Messungen halfen bei der Entscheidung sowohl über den Beginn einer Antibiotikatherapie als auch über deren Beendigung.
In einer multizentrischen Studie mit 1656 Patienten in 14 Notaufnahmen in den USA bestätigten sich diese Ergebnisse jedoch nicht. Bei Anwendung des gleichen Procalcitonin-Algorithmus wie in der oben erwähnten Studie konnte weder ein Unterschied bei der Dauer der Antibiotikatherapie noch bei der Rate der Antibiotikaverordnungen beobachtet werden.13 Es ist jedoch anzumerken, dass der Procalcitonin-Algorithmus in der amerikanischen Studie lediglich in 73% der Fälle befolgt wurde, die Adhärenz in der Schweizer Studie mit 91% jedoch deutlich höher war. Zudem bestand bei einem grossen Teil der Patienten in der amerikanischen Studie eine Asthmadiagnose, bei der die Vortestwahrscheinlichkeit einer bakteriellen Infektion bereits so gering ist, dass Procalcitonin gegenüber der klinischen Untersuchung allein keinen Mehrwert bringt. Es gilt also, die Patienten, bei denen das Procalcitonin gemessen werden soll, sorgfältig auszuwählen, indem die Wahrscheinlichkeit einer bakteriellen Infektion beurteilt wird.
Intensivmedizin
Eine bei 302 Intensivpatienten in 11 französischen Spitälern durchgeführte Studie zu schweren COPD-Exazerbationen kam zu dem Ergebnis, dass die Messung des Procalcitonins keinen Effekt auf die Dauer der Antibiotikatherapie hatte.14 Die Mortalität der Patienten in der Procalcitonin-Gruppe, die bei Aufnahme ins Spital keine Antibiotika erhielten, war höher als in der Kontrollgruppe. Bei schwer erkrankten Patienten ist es somit gefährlich, Procalcitonin als Entscheidungsgrundlage für den Beginn einer Antibiotikatherapie zu nutzen: Bei dieser Gruppe von Patienten muss unverzüglich mit der Antibiotikatherapie begonnen werden, wenn der Verdacht auf eine bakterielle Infektion besteht.
Aktuell ist eine weitere Studie in 20 französischen Spitälern zur intensivmedizinischen Versorgung von Patienten mit schwerer ambulant erworbener Pneumonie im Gang; in dieser wird der Effekt einer Steuerung der Therapie anhand des Procalcitonins in Kombination mit einer molekularen mikrobiologischen Diagnostik untersucht.15
Diskussion und Fazit
In Hausarztpraxen und Pflegeheimen können die Antibiotikaverordnungen bei Patienten mit Infektionen der unteren Atemwege durch die POCT-Messung des CRP gefahrlos gesenkt werden. Procalcitonin ist für Allgemeinmediziner ein ebenso nützlicher Biomarker. Es ist jedoch zu berücksichtigen, dass die Bereitschaft zur Durchführung dieser Tests mit der Zeit oft nachlässt; ein personalisiertes Feedback zu ihrer Anwendung und zum Antibiotikaverbrauch wäre eine denkbare Lösung, um den Hausärzten dabei zu helfen, den Einfluss der Tests auf die Zahl der Verordnungen zu verstehen und diese dauerhaft zu reduzieren.
In Notaufnahmen kann die Antibiotika-Exposition durch eine POCT-Messung des Procalcitonins ebenfalls gesenkt werden, wenn diese in den richtigen Situationen eingesetzt wird: Bei Patienten mit eher geringem Risiko für eine bakterielle Infektion ist sie unnötig; hier reicht eine klinische Untersuchung aus, um die Verordnung von Antibiotika zu vermeiden.
Bei Intensivpatienten mit schwerer Infektion darf der Procalcitonin-Wert nicht als Entscheidungsgrundlage für die Aufnahme einer Antibiotikatherapie herangezogen werden, da die Patienten dadurch dem Risiko einer erhöhten Mortalität ausgesetzt sind: Die Antibiotikatherapie muss begonnen werden, sobald der Verdacht auf eine Infektion besteht.
Der Nutzen und die Sicherheit einer Biomarker-gesteuerten Antibiotikatherapie bei Atemwegsinfektionen hängen somit stark vom klinischen Schweregrad der Erkrankung ab.
Literatur:
1 Organisation Mondiale de la Santé: Résistance aux antibiotiques. Published July 31, 2020. Accessed February 16, 2022. https://www.who.int/fr/news-room/fact-sheets/detail/antibiotic-resistance 2 Murray CJ et al.: Global burden of bacterial antimicrobial resistance in 2019: a systematic analysis. Lancet 2022; 399: 629-55 3 Costelloe C et al.: Effect of antibiotic prescribing in primary care on antimicrobial resistance in individual patients: systematic review and meta-analysis. BMJ 2010; 340: c2096 4 Spellberg B: The new antibiotic mantra–“shorter is better”. JAMA Intern Med 2016; 176: 1254-5 5 Federal Office of Public Health and Federal Food Safety and Veterinary Office: Swiss Antibiotic Resistance Report 2020. Usage of antibiotics and occurrence of antibiotic resistance in Switzerland. 2020. http://www.anresis.ch/wp-content/uploads/2020/11/Swiss-Antibiotic-Resistance-Report-2020_def_WEB.pdf 6 Pierrakos C, Vincent JL: Sepsis biomarkers: a review. Crit Care 2010; 14: R15 7 Lhopitallier L et al.: Procalcitonin and lung ultrasonography point-of-care testing to determine antibiotic prescription in patients with lower respiratory tract infection in primary care: pragmatic cluster randomised trial. BMJ 2021; 374: n2132 8 Little P et al.: Effects of internet-based training on antibiotic prescribing rates for acute respiratory-tract infections: a multinational, cluster, randomised, factorial, controlled trial. Lancet 2013; 382: 1175-82 9 Little P et al.: Antibiotic prescribing for acute respiratory tract infections 12 months after communication and CRP training: a randomized trial. Ann Fam Med 2019; 17: 125-32 10 Butler CC et al.: C-reactive protein testing to guide antibiotic prescribing for COPD exacerbations. N Engl J Med 2019; 381: 111-20 11 Boere TM et al.: Effect of C reactive protein point-of-care testing on antibiotic prescribing for lower respiratory tract infections in nursing home residents: cluster randomised controlled trial. BMJ 2021; 374: n2198 12 Schuetz P et al.: Effect of procalcitonin-based guidelines vs standard guidelines on antibiotic use in lower respiratory tract infections: the ProHOSP randomized controlled trial. JAMA 2009; 302: 1059-66 13 Huang DT et al.: Procalcitonin-guided use of antibiotics for lower respiratory tract infection. N Engl J Med 2018; 379: 236-49 14 Daubin C et al.: Procalcitonin algorithm to guide initial antibiotic therapy in acute exacerbations of COPD admitted to the ICU: a randomized multicenter study. Intensive Care Med 2018; 44: 428-37 15 Voiriot G et al.: Combined use of a broad-panel respiratory multiplex PCR and procalcitonin to reduce duration of antibiotics exposure in patients with severe community-acquired pneumonia (MULTI-CAP): a multicentre, parallel-group, open-label, individual randomised trial conducted in French intensive care units. BMJ Open 2021; 11: e048187 16 Boere TM et al.: Using point-of-care C-reactive protein to guide antibiotic prescribing for lower respiratory tract infections in elderly nursing home residents (UPCARE): study design of a cluster randomized controlled trial. BMC Health Serv Res 2020; 20: 149
Das könnte Sie auch interessieren:
Was tun bei Medikamentenunverträglichkeit?
Wenn Patientinnen und Patienten in die Praxis kommen und über eine Medikamentenunverträglichkeit klagen, gilt es herauszufinden, ob dies tatsächlich der Fall ist. Wie man dabei vorgeht ...
Traumatologie der Wirbelsäule und des Beckens im Sport
Sportverletzungen an Wirbelsäule und Becken sind medizinisch bedeutsam, da sie schwere Komplikationen und neurologische Folgen haben können. Die Epidemiologie ist stark ...
Der Tiefenrausch ist eine häufige Ursache für einen Tauchunfall
Atemgase verändern sich in der Wassertiefe physikalisch, was physiologische und medizinische Folgen bei Taucher:innen haben kann. Sauerstoff beispielsweise wird beim Abtauchen in der ...