<p class="article-intro">Das bereits seit 2011 von der FDA (US Food & Drug Administration) als eigenständige Krankheit anerkannte BIA-ALCL erlangte zuletzt mehr mediale Aufmerksamkeit. In diesem Artikel erklären wir, wie man ein ALCL erkennt und was im Ernstfall zu tun ist.</p>
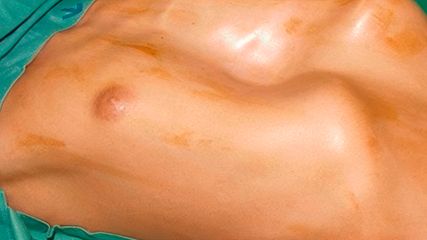
<p class="article-content"><div id="keypoints"> <h2>Keypoints</h2> <ul> <li>Die genaue Entstehung des Brustimplantat-assoziierten anaplastischen großzelligen Lymphoms (BIA-ALCL) ist bis dato ungeklärt.</li> <li>Mögliche Auslöser sind chronische Entzündungsreaktionen, weitere begünstigende Faktoren sind die bakterielle Besiedelung der Implantate und das Vorliegen von <em>JAK/ STAT</em>-Mutationen.</li> <li>Das Risiko für Frauen, an einem BIA-ALCL zu erkranken, ist sehr gering, wenngleich auch infolge fehlender Aufklärung unterschätzt.</li> <li>Bei Verwendung von Brustimplantaten sollte präoperativ über das BIA-ALCL aufgeklärt und die Patientinnen sollten über einen längeren Zeitraum nachbeobachtet werden.</li> <li>Bei bestätigtem BIA-ALCL behördliche Meldung (BASG) nach §70 des Medizinproduktegesetzes und informell an Referenzzentrum (Stichwort: BIA-ALCL, E-Mail: plastischechirurgie@ medunigraz.at)</li> </ul> </div> <p>Erstmals beschrieben wurde diese Pathologie von John Keech und Brevator Creech als lymphatopoetische Masse, welche Brustimplantaten adhärent war.<sup>1</sup> Seither gibt es eine Vielzahl an investigativen Studien, welche auf die Diagnose und Therapie des BIA-ALCL zielen. Die aktuellen NCCN Guidelines (National Comprehensive Cancer Network)<sup>2</sup> zur Diagnostik und Therapie wie auch die Entschlüsselung der Ursachen sind derzeit eine wichtige Priorität an den vielen Zentren.</p> <h2>Ätiologie noch nicht restlos geklärt</h2> <p>Das BIA-ALCL ist ein T-zelliges Non- Hodgkin-Lymphom, welches sich wie ein primär (chronisches) indolentes Lymphom verhält.<sup>3</sup> Ungefähr 85 % der Patientinnen befinden sich zum Zeitpunkt der Erstdiagnose im Stadium IA bis IIA, lediglich 15 % weisen ein höheres Stadium auf.<sup>4</sup> Die genaue Entstehung des BIA-ALCL ist bis dato nicht vollkommen entschlüsselt, analog zu anderen Lymphomen ist ein möglicher gemeinsamer Auslöser eine chronische Entzündungsreaktion, die zu einer monoklonalen T-Zell-Stimulation führt.<sup>5–7</sup> Durch eine subklinische Irritation kommt es zu einer Chemotaxis von u. a. Makrophagen, welche IL-6 und andere Mediatoren freisetzen und somit die Entstehung des BIA-ALCL begünstigen. Diese Botenstoffe sind maßgeblich an der Differenzierung von T-Zellen beteiligt.<br /> Weitere begünstigende Faktoren der Pathogenese sind die bakterielle Besiedelung texturierter Implantate (einem höheren Texturierungsgrad wird eine höhere Affinität zur Krankheitsentstehung zugeschrieben) und das Vorliegen von <em>JAK/STAT</em>-Mutationen.<sup>2, 8–11</sup> Obwohl bislang hauptsächlich gramnegative Bakterien und deren Lipopolysaccharide (LPS) als auslösender Bestandteil beschrieben wurden, konnten rezent auch grampositive Bakterien als potenzielle Trigger nachgewiesen werden.<sup>8, 12, 13</sup> Obgleich eine rezente Theorie sich auf die Anzahl der besiedelnden Bakterien fokussiert, welche als Ursache fungieren können, treten die meisten BIA-ALCL-Fälle nicht bei Rekonstruktionspatientinnen, sondern bei Patientinnen mit ästhetischen Augmentationen auf.<sup>7</sup> Selbst das Einhalten des 14-Punkte-Plans ist keine absolute Garantie, um eine potenzielle bakterielle Kontamination zur Gänze zu verhindern.<sup>10, 15</sup><br /> Eine weitere Studie befasst sich mit der Rolle von Partikeln und Kristallen, welche sowohl in der Implantathülle vorkommen (Salz-/Zuckerkristalle) als auch durch die Implantathülle diffundieren und folglich eine chronische Entzündungsreaktion auslösen können.<sup>16, 17</sup><br /> Aufgrund der multifaktoriellen Genese des BIA-ALCL ist ein exakter Krankheitsbeginn bislang nicht definierbar. Ebenso besteht derzeit keine Möglichkeit einer kompletten Prävention, auch nicht bei isolierter Verwendung von Implantaten eines geringeren Texturierungsgrades.<sup>2, 4, 13, 14</sup> Wurden beispielsweise in der Vergangenheit zuvor texturierte Implantate eingesetzt, ist eine BIA-ALCL-Entstehung auch bei weiterem Gebrauch glatter Prothesen möglich.<sup>9, 13, 18, 19</sup></p> <h2>Diagnose eines BIA-ALCL</h2> <p>In den meisten Fällen eines BIA-ALCL liegt eine periimplantäre Flüssigkeitsansammlung nach frühestens einjähriger Implantatverweildauer (mittlere Verweildauer bei Erstdiagnose 8–10 Jahre) vor. Dieses „Late onset“-Serom unterscheidet sich makroskopisch kaum von benignen Seromen, weswegen eine weiterführende Zytologie der erste Schritt einer zielführenden Diagnostik ist.<sup>2, 20</sup> Bei der Detektion periimplantärer Flüssigkeit weisen Ultraschalluntersuchungen eine Sensitivität von 84 % und eine Spezifität von 75 % auf.<sup>2, 21</sup> Bei Inkonklusivität ist eine MRT-Diagnostik zusätzlich sinnvoll. Idealerweise erfolgt bereits interventionell bei der Diagnostik eine Punktion von Flüssigkeit, welche dann mikrobiologisch sowie zytologisch mit der entsprechenden Verdachtsdiagnose weiter analysiert wird.<br /> Aber auch das Vorliegen knotiger, Implantat-assoziierter Formation wurde beobachtet. Bei Antreffen dieser sollte eine Biopsie durchgeführt werden und eine histologische Aufarbeitung erfolgen. Zeigt das angefertigte Präparat einen Verdacht auf eine lymphozytäre Pathologie, muss eine Immunhistochemie durchgeführt werden.<sup>2, 22</sup> Da es sich beim BIA-ALCL um ein T-Zell-Lymphom handelt, liegt hier eine Vermehrung monoklonaler T-Zellen mit entsprechenden CD-Markern vor. In jedem Fall ist ein BIA-ALCL immer CD30-positiv und ALK(anaplastische Lymphomkinase)-negativ.<sup>2, 8</sup> Das Vorkommen ausschließlich dieser beiden Marker ist jedoch nicht pathognomonisch. Ein weiterer Faktor zum Ausschluss anderer T-Zell-Lymphome und somit zur Verifizierung des Brustimplantat-assoziierten großzelligen Lymphoms ist das Vorliegen der Marker CD2, CD3, CD4, CD5, CD7, CD8 und CD45.<sup>2, 8, 20, 23</sup></p> <h2>Therapie</h2> <p>Konnte bereits präoperativ ein BIA-ALCL-Verdacht erhärtet werden, ist präoperativ die Durchführung eines Ganzkörper-PET-CT mit Kontrastmittel zur Detektion weiterer maligner Formationen erforderlich. Die Therapie richtet sich nach dem Stadium der Erstdiagnose (Tab. 1) und ist chirurgischerseits die En-bloc-Resektion (vollständige Kapselentfernung mit darin enthaltenem Implantat inklusive evtl. angrenzender Tumor- bzw. verdächtiger Lymphknotenformationen).<sup>2, 4, 24</sup> Sofern eine R0-Resektion erzielt werden kann, ist eine weitere Therapie in der Regel nicht nötig. Bei R1- und R2-Resektion bzw. Residuen und Brustwandinfiltrationen ist aktuell in weiterer Folge eine Strahlentherapie zu empfehlen. Befinden sich Patientinnen zur Zeit der Erstdiagnose bereits im Stadium IIB oder höher, ist zusätzlich eine Chemotherapie nach dem ALCLSchema (CHOP oder CHOEP) bzw. als Zweitlinientherapie Brentuximab vedotin indiziert.<sup>2, 25–27</sup> Weitere chemotherapeutische Kombinationsmöglichkeiten mit beispielsweise Nivolumab befinden sich derzeit noch in der Erprobungsphase.<sup>25–27</sup> Nichtsdestotrotz sollten Patientinnen mit bestätigter Diagnose in multidisziplinären Tumorboards besprochen werden, um eine optimale patientenzentrierte Therapie zu gewährleisten.<br /> In Remission befindliche Patientinnen sollten in einem Zeitraum von 2 Jahren alle 3–6 Monate routinemäßig klinisch kontrolliert werden, danach je nach Indikation. Bildgebende Diagnostiken beinhalten CT von Thorax/Abdomen/Becken bzw. PETCT.<sup>2, 21, 28</sup> Nach dem derzeitigen Wissensstand über das BIA-ALCL mit den geringen Fallzahlen konnte jedoch noch nicht dezidiert beschrieben werden, ab wann Patientinnen als genesen gelten bzw. wie hoch die Rezidivrate ist.</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2020_Jatros_Derma_2001_Weblinks_jat_derma_2001_s46_tab1_lumenta.jpg" alt="" width="550" height="430" /></p> <h2>Zusammenfassung</h2> <p>Das Risiko für Frauen, an einem Brustimplantat- assoziierten anaplastischen großzelligen Lymphom zu erkranken, ist mit jährlich 0,35–3/1 Million sehr gering. Die Behandlungsempfehlungen folgen einem primär kurativen Ansatz mit deutlich besserer Prognose als bei einem systemischen anaplastischen Lymphom. Nach derzeitigen Erkenntnissen besteht eine zusätzliche Dunkelziffer, nicht nur aufgrund der latenten Inkubationszeit und des primär chronischen Verhaltens des BIA-ALCL, sondern auch aufgrund der Informationslage der Betroffenen.<sup>3, 29</sup> Es ist daher erforderlich, dementsprechend bei Verwendung von Brustimplantaten präoperativ über das BIAALCL aufzuklären und die Patientinnen über einen längeren Zeitraum nachzubeobachten. Zusätzlich sollten alle Patientinnen entsprechend gescreent werden (Anamnese, Bildgebung, Fragebögen etc.), um eine möglichst detaillierte Aufbereitung der seltenen Fälle zu ermöglichen.<sup>2</sup> Aktuell gibt es unterschiedliche Bestrebungen, angesichts gehäufter Fallzahlen und bestehender nicht diagnostizierter Fälle medizinische Registrierungsplattformen zu erstellen und sich thematisch auf spezialisierten Konferenzen auszutauschen.<sup>29</sup><br /> BIA-ALCL-Fälle sollten an spezialisierten Zentren mit entsprechend ausgestatteter Infrastruktur abgeklärt und behandelt werden. Das LKH-Univ.-Klinikum Graz der Medizinischen Universität Graz fungiert in Österreich als Referenzzentrum und Ansprechpartner und stellt den aktuellen Behandlungspfad (SOP, Standard Operating Procedure) zur Verfügung (Abb.).<sup>1, 30–32</sup><br /> Es wird gebeten, neben der behördlichen Meldung (BASG) nach Medizinproduktegesetz (§70 ff. MPG, BGBl. 657/1996 idgF.), neue Fälle eines bestätigten BIA-ALCL in Österreich informell dem Referenzzentrum zu melden (Stichwort: BIA-ALCL, E-Mail: <a href="mailto:plastischechirurgie@medunigraz.at)">plastischechirurgie@medunigraz.at)</a>.</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2020_Jatros_Derma_2001_Weblinks_jat_derma_2001_s45_grafik_lumenta.jpg" alt="" width="800" height="1078" /></p></p>
<p class="article-footer">
<a class="literatur" data-toggle="collapse" href="#collapseLiteratur" aria-expanded="false" aria-controls="collapseLiteratur" >Literatur</a>
<div class="collapse" id="collapseLiteratur">
<p><strong>1</strong> Miranda RN et al.: Plast Reconstr Surg 2019; 143: 7S-14S <strong>2</strong> Clemens MW et al.: Aesthet Surg J 2019; 39(Suppl_1): S3-S13 <strong>3</strong> de Leval L: Hematol Oncol 2019; 37(Suppl 1): 24-9 <strong>4</strong> Collins MS et al.: Plast Reconstr Surg 2019; 143: 41S-50S <strong>5</strong> Bizjak M et al.: J Autoimmun 2015; 65: 64-73 <strong>6</strong> Mempin M et al.: Materials (Basel) 2018; 11(12). pii: E2393 <strong>7</strong> Rieger UM et al.: Br J Surg 2013; 100(6): 768-74 <strong>8</strong> Rastogi P et al.: Plast Reconstr Surg 2019; 143: 23S-29S <strong>9</strong> Adams WP Jr et al.: Plast Reconstr Surg 2017; 140(3): 427-31 <strong>10</strong> Mukthar RA et al.: Plast Reconstr Surg Glob Open 2019; 7(4): e2188 <strong>11</strong> Huang X et al.: Oncotarget 2017; 8(59): 99772-83 <strong>12</strong> Hu H et al.: Plast Reconstr Surg 2016; 137(6): 1659-69 <strong>13</strong> Walker JN et al.: Sci Rep 2019; 9(1): 10393 <strong>14</strong> Reischies FMJ et al.: PLoS ONE 2017; 12(8): e0182267 <strong>15</strong> Agarwal A et al.: Global Spine J 2019; 9(1): 62-6 <strong>16</strong> Santanelli di Pompeo F, Sorotos M: J Plast Reconstr Aesthet Surg 2018; 71(6): 785-7 <strong>17</strong> Munford RS: Infect Immun 2008; 76(2): 454-65 <strong>18</strong> James GA et al.: Aesthetic Plast Surg 2019; 43(2): 490-7 <strong>19</strong> Rastogi P et al.: Curr Hematol Malig Rep 2018; 13(6): 516-24 <strong>20</strong> Kadin ME et al.: Aesthet Surg J 2017; 37(7): 771-5 <strong>21</strong> Chacko A, Lloyd T: Insights Imaging 2018; 9(5): 683-6 <strong>22</strong> Clemens MW et al.: Plast Reconstr Surg 2018; 141(4): 586e-99e <strong>23</strong> Kadin ME et al.: Aesthet Surg J 2016; 36(7): 773-81 <strong>24</strong> Clemens MW et al.: J Clin Oncol 2016; 34(2): 160-8 <strong>25</strong> Prince HM et al.: Lancet 2017; 390(10094): 555-66 <strong>26</strong> Kim YH et al.: J Clin Oncol 2015; 33(32): 3750-8 <strong>27</strong> Duvic M et al.: J Clin Oncol 2015; 33(32): 3759-65 <strong>28</strong> Dashevsky BZ et al.: Breast J 2019; 25(1): 69-74 <strong>29</strong> McCarthy CM et al.: Plast Reconstr Surg 2019; 143: 65S-73S <strong>30</strong> Ebner PJ et al.: J Surg Oncol 2019; 120(4): 573-7 <strong>31</strong> Leberfinger AN et al.: JAMA Surg 2017; 152(12): 1161-8 <strong>32</strong> Mehta-Shah N et al.: Blood 2018; 132(18): 1889-98</p>
</div>
</p>