Was erwartet uns 2022?
Autoren:
Dr. Raimund Lunzer
Abteilung Innere Medizin
Krankenhaus der Barmherzigen Brüder, Graz
E-Mail: raimund.lunzer@gmx.at
Dr. Thomas Nothnagl
Kompetenzzentrum für Rheumatologie
Landesklinikum Stockerau
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der Versuch eines Blicks in die Zukunft ist in einem so schnelllebigen wissenschaftlichen Diskurs immer riskant. In einem nur kurzen historischen Intervall hat sich die Medizin stark weiterentwickelt. Seit dem Jahr 2000 erlebt die Rheumatologie dank der molekularen biologischen Therapie eine Revolution. Die Behandlungsoptionen nehmen seither stetig zu, was die Therapiefindung immer komplexer, aber auch individueller werden lässt.
Keypoints
-
Die therapeutischen Optionen nehmen weiter zu – eines ist sicher, einfacher wird es nicht!
-
Das Problem wird sein, die korrekte Therapie zum richtigen Zeitpunkt zu wählen (Option Biomarker).
-
Interessante Aspekte ergeben sich durch Kombinationen von DMARDs und Erweiterung der Indikationen der etablierten Substanzen.
-
Die patientenbezogenen Parameter (PROs) sollten uns interessieren!
Ausgehend von mitunter toxischen Medikamenten konnten in den vergangenen beiden Jahrzehnten zielgerichtete Therapien in der Rheumatologie etabliert werden. Bemerkenswert waren dabei vor allem die Entwicklung von Plasmazellen als Targets sowie die Eingriffe in die Autoinflammation.
Ganz so individuell, wie wir es formulieren, geht es aber doch (noch) nicht. Die Mehrzahl der Patienten benötigt im Laufe ihrer entzündlichen Erkrankung neue zielgerichtete Therapien. Die Optionen werden immer mehr, sodass die Herausforderung sein wird, die eine effektive biologische Therapie zum korrekten Zeitpunkt einzusetzen. Neben der künstlichen Intelligenz, die zweifelsohne massive Fortschritte mit sich bringt, wird die ärztliche Kunst weiter Bestand haben: „Du musst viel wissen, um wenig zu tun“, wie es die Rheumatologin Prof. Dr. Elisabeth Märker-Hermann aus Wiesbaden formuliert. Um erfolgreich zu sein – im Sinne des Erreichens von Therapiezielen und im besten Fall einer Remission – sind komplexere Behandlungsstrategien erforderlich, die ein engmaschiges Monitoring erfordern.
Was befindet sich in den Pipelines?
Die großen Pharmafirmen lebten zu Beginn gut davon, kleine Erfolgversprechende Entwicklungsfirmen zu kaufen. Mittlerweile müssen aber aufgrund der Komplexität, des organisatorischen Aufwands und der rechtlichen Auflagen klinischer Studien hohe Summen investiert werden, um Therapien auf den Markt zu bringen. Auf den großen Kongressen finden sich etwas versteckt die Medikamente mit dem größten Potenzial für weitere Studien. Neben den Patienten geht es hier aber auch darum, die Investoren und Aktionäre zu bedienen. Nicht selten kommt es vor, dass eine Phase-III-Studie abgebrochen werden muss, was zum sofortigen Absinken des Aktienskurses der jeweiligen Firma führt. Neue Therapiekonzepte von Eli Lilly, AbbVie oder BMS zeigen, was wir in Zukunft erwarten können: Therapeutika primär für eine bestimmte Indikation, allerdings stets mit der Option der Erweiterung ihrer Einsatzgebiete. In Studien sind ein IL-13-Inhibitor (Lebrikizumab) für die Behandlung der atopischen Dermatitis, ein IL-23-Inhibitor (Mirikizumab) bei chronisch-entzündlichenDarmerkrankungen, ein IL-2-AK für die Therapie des systemischen Lupus erythematodes (SLE) oder auch auch orale(!) IL-17A-Inhibitoren untersucht worden. Kombinationen von Januskinase(JAK)- mit Bruton-Tyrosinkinasehemmern (Upadacitinib und Elsubrutinib) geben uns Hinweise auf zukünftige Strategien für die Behandlung von entzündlichen Erkrankungen. Von BMS werden Deucravacitinib und Breprocitinib als Tyrosinkinase(TYK)-II-Inhibitoren für die Indikationen SLE, Psorisasis und Psoriasisarthropathie erforscht. Im Gegensatz zu den etablierten JAK-Inhibitoren zeigen sie keine Interaktionen mit Neutrophilen, NK-Zellen und Thrombozyten. Ob das dann klinisch einen Unterschied macht und tatsächlich einen Vorteil mit sich bringt, müssen die Studien klären.
„Artificial intelligence“
Keine Angst, die medizinische Kompetenz der Ärzte wird durch die Einführung künstlicher Intelligenz sicher nicht untergraben. Als Vergleich sei hier nur angeführt, dass auch die Implementierung von Excel® keine personelle Reduktion in der Verwaltung zur Folge hatte.
Die Charité Universitätsklinik Berlin stellt – einstweilen noch gratis – ein Tool zur radiologischen Beurteilung der Iliosakralgelenke für die Diagnose der axialen Spondyloarthropathie (SpA) mit einer Genauigkeit von 88% zur Verfügung. Für die Diagnose einer nichtradiografisch axialen Manifestation der SpA mittels MRT liegt dessen Genauigkeit bei 77%.
Es wird auch nach möglichen Biomarkern für die Wahl der passenden Therapie gesucht. In der SELECT-CHOICE-Studie wird, nach Versagen von bis zu drei Biologika, das Ansprechen von Patienten mit rheumatoider Arthritis (RA) auf einen JAK-Hemmer (Upadacitinib) oder auf Abatacept analysiert. Numerisch erzielen JAK-Hemmer bei diesen aufwendigen RA-Patienten ein besseres Ansprechen. Als Biomarker für das Therapieansprechen haben sich IL-6, CSF-1, CCL7 und HSD11B1 als signifikant erwiesen. Mit ähnlichen „Biomarker-Kits“ kann auch das Ansprechen einer Methotrexat(MTX)-Therapie mit 80% errechnet werden.
Frühe Remission bei RA-Patienten
Die bekannte NORD-STAR-Studie aus Skandinavien untersuchte Patienten mit früher RA, die mit MTX, TNF-α + MTX, IL-6-Inhibitor (Tocilizumab) + MTX oder Abatacept + MTX behandelt wurden. Nach 48 Wochen ging Abatacept + MTX mit einer 60%igen Responserate als signifikant wirksamer gegenüber der MTX-Monotherapie hervor. Die radiologische Progression war in allen Gruppen erwartungsgemäß sehr gering.
Was ist, wenn wir noch früher behandeln, um eine Arthritis eventuell zu verhindern? Diese Idee des „window of opportunity“ griff PD Dr. Jürgen Rech vom Universitätsklinikum Erlangen auf. Er behandelte RA-Patienten mit Abatacept, wenn Arthralgien, ein positiver MRT-Befund der Hände und ein positiver ACPA(anticitrullinierte Proteinantikörper)-Test vorlagen. 90% entwickelten keine Arthritis – nicht unerheblich für die zukünftigen therapeutischen Entwicklungen.
Was ist kurzfristig zu erwarten?
Der IL-23-Inhibitor Risankizumab steht auch für die Psoriasisarthritis kurz vor dem breiten Einsatz; Guselkumab ist bereits in den Erstattungskodex aufgenommen worden. Neben ihrer Effektivität zeigten IL-23-Inhibitoren in Studien eine geringere Rate an Nebenwirkungen. Auch hinsichtlich ihres Einsatzes bei SLE und IBD („inflammatory bowel disease“) laufen Analysen. Der etwas breiter wirksame IL-17A/F-Inhibitor Bimekizumab wird heuer für die Indikationen Psoriasis, Psoriasisarthritis und Spondyloarthropathie zugelassen werden.
Anifrolumab wird 2022 für die Behandlung des SLE auf den Markt kommen – primär als Kurzinfusionstherapie alle 4 Wochen, später auch als Pen zur Selbstapplikation. Die Daten der Zulassungsstudien waren etwas heterogen und die erste TULIP-Studie verlief nicht signifikant. Danach änderten die Autoren die Programme und verwendeten einen neuen Score (Lupus Low Disease Activity State). SLE-Studien sind immer sehr aufwendig, da die Manifestationsbreite des SLE sehr groß ist. Von Belimumab haben wir aber gelernt, dass die „Real life“-Ergebnisse dann besser als aus den Zulassungsstudien sein können. Da bei SLE-Studien die Placebogruppe, auch aus ethischen Gründen, eine effektive Standardtherapie erhält, fallen hier die Prozentsätze der Ansprechraten nicht so massiv aus.
Etablierte Biologika – neue Indikationen
Secukinumab, der wirksame IL-17-Inhibitor bei Psoriasis, Psoriasisarthritis und Spondyloarthropathie, hat in der Proof-of-Concept-Studie „TitAIN“ aus Freiburg deutliche Remissionsdaten bei der Riesenzellarteriitis gezeigt – und das sogar mit deutlich weniger Glukokortikoiden. Über diesen Erfolg waren vermutlich auch die Autoren überrascht. Die Phase-III-Studien sind folglich schon im Laufen.
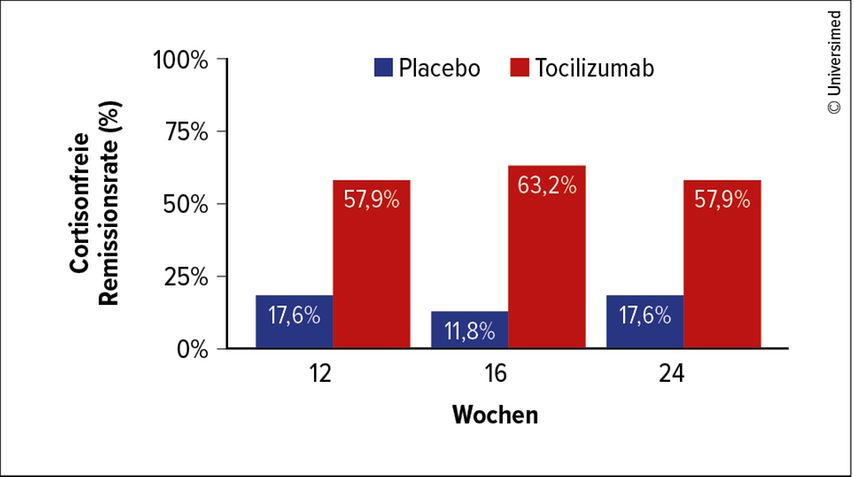
Wie weit ist die Polymyalgie von einer Riesenzellarteriitis entfernt? Bei 22% finden sich subklinische Gefäßentzündungen. PD Dr. Michael Bonelli vom Universitätsklinikum AKH Wien setzte Tocilizumab bei Polymyalgie ein und konnte zeigen, dass 60% der Patienten nach 12 Wochen in Remission waren – und das sogar ohne Glukokortikoide, was auch für die Praxis relevant ist, da diese Patienten häufig Komorbiditäten aufweisen (Abb.1).
Abb. 1: Wirksamkeit von Tocilizumab bei Polymyalgie (mod. nach Bonelli M et al.: Tocilizumab in patients with new onset polymyalgia rheumatica – a phase 2/3 randomized controlled trial. ACR Convergence 2021: Abstract 0507)
Um wen geht es?
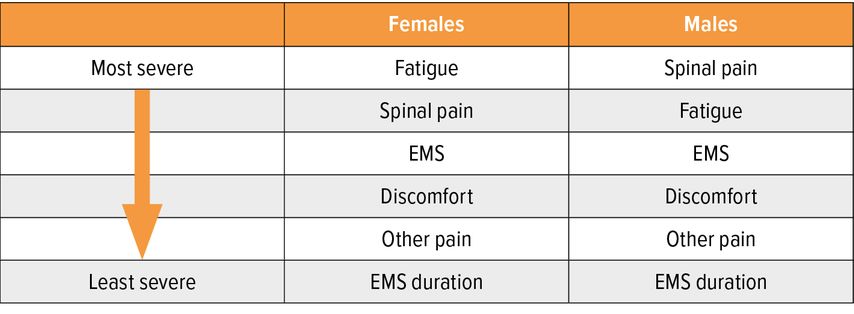
Abschließend möchten wir noch kurz die Diskussion der PROs („patient-reported outcomes“) ansprechen. Diesbezüglich wird es in Zukunft sicher neue Erkenntnisse geben, wie die Therapie neben den klinischen-laborchemischen Aspekten individuell auszuwählen ist. Hierzu vielleicht zwei Beispiele: Bei Spondyloarthropathien reihen Frauen bei der Gewichtung ihrer Symptome Fatigue ganz nach oben (Tab.1) und Ärzte ganz nach unten. Weiters zeigen Analysen, dass Frauen später und erst bei höherer Krankheitsaktivität eine Biologikatherapie erhalten. Die JAK-Inhibitoren bessern den Schmerz im Rahmen der RA sehr rasch, sogar schon innerhalb von zwei Wochen, aber die entzündliche Aktivität mit Schwellungen der Gelenke folgt erst später. Wenn es dem Patienten gut geht, heißt das also noch lange nicht, dass er in klinischer Remission ist. Wir werden weiter mit unseren Patienten reden müssen, am besten „live“.
Tab. 1: Wie gewichten Frauen und Männer mit Spondyloarthropathie ihre Symptome? (mod. nach Maguire S et al.: Looking beyond BASDAI total scores: analysis of the BASDAI on the basis of sex. EULAR 2021: OP0051)
Literatur:
bei den Verfassern
Das könnte Sie auch interessieren:
Biologikatherapien in der Schwangerschaft
„Biologika sind in der Schwangerschaft in Ordnung“ – mit dieser klaren Aussage fasste Prof.Dr. Ian Giles, University College London, im Rahmen der RheumaPreg-2025- Konferenz in Wien die ...
Riesenzellarteriitis: Ultraschall ist erste Wahl in der Diagnostik
Bei der Riesenzellarteriitis ist, insbesondere wenn sie die Arteria temporalis betrifft, rasches Handeln erforderlich. Die Diagnose kann mittels Sonografie und Labor schnell gestellt ...
ANCA-assoziierte Vaskulitiden
Als ANCA-assoziierte Vaskulitiden wird eine Gruppe von nekrotisierenden Entzündungen der kleinen Gefäße bezeichnet, die ein hohes Risiko von Organversagen mit sich bringen können. In der ...