TTV – der neue Immunmarker: Was steckt dahinter?
Autorin:
Irene Görzer, PhD
Zentrum für Virologie
Medizinische Universität Wien
E-Mail: irene.goerzer@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das Torque-Teno-Virus (TTV) wurde erstmals 1997 bei einem Patienten nachgewiesen und nach seinen Initialen als TT-Virus bezeichnet. Die TTV-Last bleibt bei gesunden Personen stabil, steigt aber durch Immunsuppression deutlich an, was das Virus als Immunmarker u.a. nach Transplantationen interessant macht.
Keypoints
-
TTV ist ein apathogenes DNA-Virus, das im frühen Kindesalter erworben wird, weltweit verbreitet ist, in Balance mit dem Immunsystem im Blut persistiert und ein fester Bestandteil des gesunden humanen Viroms ist.
-
Die TTV-Last steigt unter Immunsuppression an, kann rasch und zuverlässig gemessen werden und wird von antiviralen Medikamenten nicht beeinflusst.
-
Ziel von Studien ist es, TTV-Werte zu identifizieren, die eine optimale individuelle Immunsuppression für die entsprechenden Patient:innen-gruppen anzeigen.
TTV steht für das Torque-Teno-Virus. Unsere Neugierde für TTV wurde durch eine im Jahr 2010 veröffentlichte Arbeit einer italienischen Forschungsgruppe geweckt, in der die TTV-Last im Blut als möglicher Surrogatmarker eines funktionellen Immunsystems beschrieben wurde.1 Basierend auf dieser Arbeit etablierten wir die quantitative PCR zur Bestimmung der TTV-Last und untersuchten zur Testüberprüfung zufällig ausgewählte Blutproben von gesunden Proband:innen und Verlaufsproben eines Lungentransplantationspatienten. In 73% der Proben von gesunden Proband:innen war eine TTV-Last von durchschnittlich 103Kopien/mL im Blutplasma nachweisbar, die TTV-Werte nach Lungentransplantation betrugen 109 Kopien/mL. Diese Vorversuche lieferten zwei wesentliche Ergebnisse: Erstens ist TTV im Blut gesunder, immunkompetenter Personen vorhanden. Zweitens ist die TTV-Last unter Immunsuppression stark erhöht. Bevor wir jedoch die ersten klinischen Studien in Kooperation mit Dr. Peter Jaksch vom Lungentransplantationszentrum des AKH Wien durchführten, mussten wir Kenntnis über dieses Virus gewinnen.
Die Entdeckung und Benennung
TTV wurde erstmals 1997 bei einem Patienten mit unklarer Hepatitis nachgewiesen und nach den Initialen des Patienten (T. T.) als TT-Virus bezeichnet.2 In der Folge wurde das TT-Virus auch als „transfusion-transmitted virus“ bezeichnet, da es häufig in Blutspendeproben nachgewiesen wurde. Ab 2004 wurde das TT-Virus offiziell Torque-Teno-Virus genannt und der Familie der Anelloviren zugeordnet. Eine erneute Änderung der Nomenklatur erfolgte 2023; seither lautet die offizielle Bezeichnung Alphatorquevirus.3
Die Virusstruktur
Bereits im Jahr 2000 wurden erste elektronenmikroskopische Aufnahmen von TTV-Partikeln veröffentlicht, die aus dem Blut isoliert worden waren.4 Die ersten kryoelektronenmikroskopischen Aufnahmen erschienen 2024, stammen von sogenannten „virus-like particles“ und zeigten erstmals mit hoher Auflösung die ikosaedrische Virusstruktur.5 TTV hat eine zirkuläre Einzelstrang-DNA von etwa 3800 Nukleotiden, die im Viruskapsid mit einem Durchmesser von rund 30 Nanometern eingeschlossen ist. Das sehr kleine DNA-Genom codiert zumindest für vier virale Proteine.
TTV zählt zu den Anelloviren
Anelloviren wurden in zahlreichen Säugetierarten sowie in einigen Vogelarten gefunden. Ein typisches Kennzeichen der Anelloviren ist ihre ausgeprägte Genomdiversität. Auf Basis der Sequenzunterschiede werden sie zunächst in Gattungen und anschließend in Spezies unterteilt.3 Die drei hauptsächlichen Gattungen, die den Menschen infizieren, sind das Alphatorquevirus (TTV), das Betatorquevirus (TTV-Minivirus) und das Gammatorquevirus (TTV-Midivirus), sie werden anhand ihrer Sequenz und Genomgröße (2200 bis 3800 Nukleotide) voneinander unterschieden. Für TTV sind derzeit etwa 20 Spezies bekannt, deren Nukleotidsequenzen sich um bis zu 41% unterscheiden. Jede Spezies umfasst wiederum zahlreiche unterschiedliche TTV-Stämme.
Die Gesamtheit aller Anelloviren
Mittels Hochdurchsatzsequenzierung können die in einer Probe vorhandenen Anelloviren qualitativ und quantitativ erfasst werden. Gesunde Menschen haben ein individuelles „Anellom“.6 Untersuchungen von Plasma- und BAL-Proben von Lun-gentransplantationspatient:innen zeigten, dass sich die Zusammensetzung der Anelloviren, bestehend aus Spender- und Empfängeranellom, zwischen zwei Messzeitpunkten stark verändern kann, während die Gesamtmenge meist konstant bleibt.7 Eine Folgestudie zeigte zudem, dass bestimmte Anelloviren gemeinsam mit Nicht-Anelloviren wie Herpesviren Cluster bilden, was auf mögliche Kooperationen hinweist.8 Zusammengefasst ergaben die Metagenomanalysen, dass TTV in nahezu allen Proben von immunkompetenten und immunsupprimierten Personen vorkommt, während andere Anelloviren nur sporadisch nachweisbar sind. Da weder das Vorhandensein noch die Höhe der TTV-Last mit einer Erkrankung assoziiert ist, wird TTV als „the most friendly component“ des humanen Viroms angesehen.9,10
Die Bestimmung der TTV-Last
Da Metagenomanalysen zeit- und kostenintensiv sind, eignet sich für das regelmäßige Monitoring die quantitative TTV-PCR, mit der innerhalb von zwei Stunden die Gesamtmenge von TTV bestimmt werden kann. Als PCR-Targetstelle dient ein kurzer, hochkonservierter Sequenzbereich im nichtcodierenden Bereich des Genoms, der bei allen TTV-Spezies nahezu identisch ist.
Die TTV-Infektion erfolgt in den ersten Lebensmonaten
Studien zeigten, dass bis zum Ende des ersten Lebensjahres nahezu alle Kinder TTV-positiv sind.10 Wahrscheinlich erfolgt die Infektion über mehrere Transmissionswege, darunter Muttermilch, Speichel sowie Schmier- und Tröpfcheninfektionen. Bei mindestens 80% der gesunden Erwachsenen ist TTV im Blut nachweisbar, wobei die Viruslast über lange Zeiträume stabil bleibt.11
TTV-Persistenz und weltweite Verbreitung
Es wird angenommen, dass hämatopoetische Vorläuferzellen maßgeblich für die Persistenz von TTV verantwortlich sind. Durch Migration und Differenzierung dieser Zellen gelangt TTV in die Blutbahn, vermehrt sich, wird im Körper verteilt und kehrt schließlich wieder ins Knochenmark zurück.12 Entsprechend wurde TTV in verschiedenen Blutzelltypen nachgewiesen und eine kürzlich erschienene Studie zeigte zudem, dass TTV in nahezu allen Körpergeweben – mit Ausnahme des Gehirns – vorkommt.13
Eine 2017 veröffentlichte Studie verglich das humane Darmvirom von fünf Populationen aus Europa, den USA sowie isoliert lebenden Jäger-und-Sammler-Gruppen aus Peru und Tansania. TTV und andere Anelloviren wurden in allen Populationen in vergleichbarer Häufigkeit nachgewiesen.14 Darüber hinaus ist TTV ein sehr altes Virus. Wie kürzlich publiziert, konnte TTV-DNA in einem etwa 7000 Jahre alten menschlichen Knochenfund aus der heutigen Ukraine nachgewiesen werden.13 Der Vergleich mit heutigen Sequenzen zeigte eine Aminosäuresequenz-Identität von 97%.
Die TTV-spezifische Immunantwort
Die Immunantwort gegen TTV ist bislang nur unzureichend untersucht. Studien zur humoralen und zellulären Immunantwort zeigten, dass nur wenige TTV-spezifische Peptide eine messbare Antikörper- oderT-Zell-Antwort auslösen.16,17 Der Anteil TTV-spezifischer T-Zellen betrug etwa 0,6% der gesamten T-Zell-Population und wies einen funktionell eingeschränkten Phänotyp auf. Insgesamt besteht somit eine sehr schwache, aber eindeutig nachweisbare Immunantwort, die die TTV-Last bei gesunden Personen stabil hält, durch Immunsuppression jedoch deutlich ansteigt.
Die TTV-Last unter Immunsuppression
In unserer ersten retrospektiven Studie in Kooperation mit Dr. Peter Jaksch konnten wir zeigen, dass nach Lungentransplantation die TTV-Last kontinuierlich zunahm, nach 60–90 Tagen den Peak erreichte und anschließend auf hohem Niveau relativ stabil blieb.18 Patient:innen unter Tacrolimus zeigten signifikant höhere TTV-Werte als Patient:innen unter Cyclosporin A, was mit der erwarteten Stärke der Immunsuppression zusammenpasste. Diese Ergebnisse bildeten die Grundlage für zahlreiche weitere Studien mit dem Ziel, TTV-Werte zu identifizieren, die eine optimale individuelle Immunsuppression für die entsprechenden Patient:innengruppen anzeigen.19
Warum TTV gut als Immunmarker geeignet ist
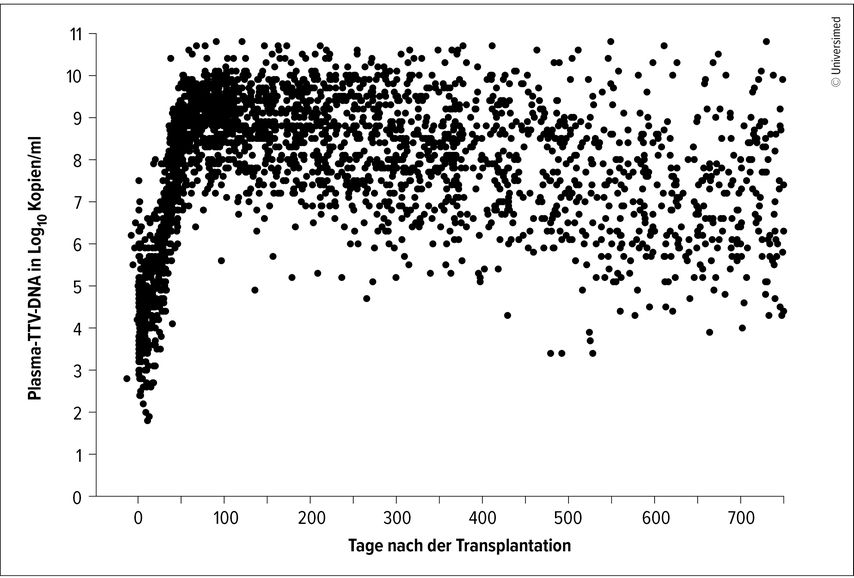
TTV ist ein kleines, apathogenes DNA-Virus, das im frühen Kindesalter erworben wird, weltweit verbreitet ist, in Balance mit dem Immunsystem im Blut persistiert, mit dem Menschen koevoluiert ist und ein fester Bestandteil des gesunden humanen Viroms ist. Die TTV-Last kann rasch und zuverlässig gemessen werden, wird von gängigen antiviralen Medikamenten nicht beeinflusst und steigt unter Immunsuppression signifikant an (Abb.1).
Abb. 1: Die Plasma-TTV-Werte nach Lungentransplantation. Es werden 2675 Messungen von 143 Lungentransplantationspatient:innen gezeigt. Die mittlere TTV-Last beträgt vor der Transplantation 4x 10³ Kopien/ml und erreicht nach ca. 90 Tagen mit 3x 10⁹ Kopien/ml den Peak (modifiziert nach Jaksch P et al. 2019)19
Ausblick und offene Fragen
Für eine gute Vergleichbarkeit der Studien müssen die TTV-Messungen standardisiert werden. Weitere Fragen betreffen mögliche Einflussfaktoren wie Koinfektionen oder unterschiedliche Medikamente sowie die Bestimmung optimaler TTV-Zielbereiche in verschiedenen klinischen Settings. Für Patient:innen nach Lungen- und Nierentransplantation wurden bereits Zielbereiche festgelegt, die in ersten randomisierten Doppelblindstudien auf ihre Effektivität überprüft werden.20,21 Das biologische Verhalten von TTV ist noch wenig erforscht, da bislang kein geeignetes Zellkulturmodell existiert. Um grundlegende Fragen der Virus-Wirt-Interaktion zu beantworten, hat dazu unter anderem Dr. Marco Hein von den Max Perutz Labs letztes Jahr ein von den Vienna Research Groups for Young Investigators (WWTF)gefördertes Forschungsprojekt in Kooperation mit der Medizinischen Universität Wien gestartet.22
Literatur:
1 Focosi D et al.: Torquetenovirus viremia kinetics after autologous stem cell transplantation are predictable and may serve as a surrogate marker of functional immune reconstitution. J Clin Virol 2010; 47(2): 189-92 2 Nishizawa T et al.: A novel DNA virus (TTV) associated with elevated transaminase levels in posttransfusion hepatitis of unknown etiology. Biochem Biophys Res Commun 1997; 241(1): 92-7 3 Varsani A et al.: Summary of taxonomy changes ratified by the International Committee on Taxonomy of Viruses (ICTV) from the Animal DNA Viruses and Retroviruses Subcommittee, 2025. J Gen Virol 2025; 106(7): 002113 4 Itoh Y et al.: Visualization of TT virus particles recovered from the sera and feces of infected humans. Biochem Biophys Res Commun 2000; 279(2): 718-24 5 Liou SH et al.: Structure of anellovirus-like particles reveal a mechanism for immune evasion. Nat Commun 2024; 15(1): 7219 6 Arze CA et al.: Global genome analysis reveals a vast and dynamic anellovirus landscape within the human virome. Cell Host Microbe 2021; 29(8): 1305-15 7 Segura-Wang M et al.: Temporal dynamics of the lung and plasma viromes in lung transplant recipients. PLoS One 2018; 13(7): 0200428 8 Widder Set al.: Metagenomic sequencing reveals time, host, and body compartment-specific viral dynamics after lung transplantation. Microbiome 2022; 10(1): 66 9 Koonin EV et al.: The healthy human virome: from virus-host symbiosis to disease. Curr Opin Virol 2021; 47: 86-94 10 Tyschik EA et al.: Torque teno virus dynamics during the first year of life. Virol J 2018; 15(1): 96 11 Focosi D et al.: Assessment of prevalence and load of torquetenovirus viraemia in a large cohort of healthy blood donors. Clin Microbiol Infect 2020; 26(10): 1406-10 12 Maggi F et al.: Role of hematopoietic cells in the maintenance of chronic human torquetenovirus plasma viremia. J Virol 2010; 84(13): 6891-3 13 Pyoria L et al.: Unmasking the tissue-resident eukaryotic DNA virome in humans. Nucleic Acids Res 2023; 51(7): 3223-39 14 Rampelli S et al.: Characterization of the human DNA gut virome across populations with different subsistence strategies and geographical origin. Environ Microbiol 2017; 19(11): 4728-35 15 Sikora M et al.: The spatiotemporal distribution of human pathogens in ancient Eurasia. Nature 2025; 643(8073): 1011-9 16 Venkataraman T et al.: Comprehensive profiling of antibody responses to the human anellome using programmable phage display. Cell Rep 2022; 41(12): 111754 17 Vietzen H et al.: Torque teno viruses exhaust and imprint the human immune system via the HLA-E/NKG2A axis. Front Immunol 2024; 15: 1447980 18 Gorzer I et al.: Plasma DNA levels of Torque teno virus and immunosuppression after lung transplantation. J Heart Lung Transplant 2014; 33(3): 320-3 19 Jaksch P et al.: Integrated immunologic monitoring in solid organ transplantation: The road toward torque teno virus-guided immunosuppression. Transplantation 2022; 106(10): 1940-51 20 Gottlieb J et al.: Viral load-guided immunosuppression after lung transplantation (VIGILung)-study protocol for a randomized controlled trial. Trials 2021; 22(1): 48 21 Haupenthal F et al.: A multicentre, patient- and assessor-blinded, non-inferiority, randomised and controlled phase II trial to compare standard and torque teno virus-guided immunosuppression in kidney transplant recipients in the first year after transplantation: TTVguideIT. Trials 2023; 24(1): 213 22 Hein M, Görzer I: Deconstructing and reconstructing Anelloviruses. https://www.wwtf.at/funding/programmes/ls/LS24-059/ ; zuletzt aufgerufen am 19.1.2026
Das könnte Sie auch interessieren:
Künstliche Intelligenz in der Medizin – eine rechtliche Einordnung
KI eröffnet neue Möglichkeiten in Diagnostik, Therapie und Patientenbetreuung. Gleichzeitig bringt ihr Einsatz auch erhebliche Risiken und Herausforderungen mit sich, insbesondere im ...
Immuntherapie: Krankheitsmodifikation bei allergischem Asthma
Allergisches Asthma ist die einzige Form von Asthma, für die mit der Immuntherapie eine kausale, krankheitsmodifizierende Therapie zur Verfügung steht, die in manchen Fällen sogar ...