Aktuelle Studien zur ILD-Therapie
Bericht:
Dr. Corina Ringsell
Redaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Interstitielle Lungenkrankheit (ILD) ist der Oberbegriff für eine grosse und heterogene Gruppe von Krankheiten, die sich vorwiegend im distalen Bronchoalveolarraum manifestieren. Einige ILD haben nachweisbare Ursachen, andere gelten als idiopathisch. So die idiopathische Lungenfibrose (IPF), die durch klinische, radiologische und histologische Kriterien definiert ist. Vor Kurzem wurde eine Subgruppe progressiv-fibrotischer ILD beschrieben und als progressive Lungenfibrose (PPF) festgehalten.1
Neue Targets für die Therapie der idiopathischen Lungenfibrose (IPF)
Die Pathogenese der IPF ist komplex und hat genetische sowie nichtgenetische Ursachen. Bridges et al. gehen davon aus, dass nicht nur die Fibroblasten, sondern verschiedene Zelltypen an der Entstehung beteiligt sind. Zudem braucht es zwei Angriffspunkte, um eine IPF zu entwickeln: Der erste ist ein vulnerables Bronchialepithel, der zweite löst eine Umprogrammierung distaler Epithelien aus, was die Fibrosierung einleitet und unterhält.
Eine gesteigerte Empfindlichkeit beruht oft auf mehr oder weniger häufigen genetischen Varianten. Die anschliessende Schädigung des Bronchialepithels kann beispielsweise durch Rauchen, Umweltfaktoren, Entzündungen oder Alterungsprozesse verursacht werden. Sie resultiert in dauerhaften Veränderungen der Zellbiologie mit Aktivierung der Fibroblasten.2 Aufgrund dieser Erkenntnisse wird an neuen Targets für Medikamente zur IPF-Behandlung geforscht.
Phosphodiesterase-4B-Inhibitoren
PDE4-Hemmer sind bereits in der klinischen Anwendung. Der erste PDE4-Inhibitor Roflumilast wurde für die Behandlung der COPD entwickelt. Später kamen weitere Wirkstoffe für andere Indikationen hinzu, etwa für Psoriasis und andere Hautkrankheiten sowie für weitere entzündliche/hochentzündliche Krankheiten.
Mittlerweile ist eine speziell für die IPF entwickelte Substanz in der klinischen Erprobung: der selektive PDE4B-Inhibitor Nerandomilast. Er wurde in der Phase-III-Studie FIBRONEER-IPF in zwei verschiedenen Dosierungen (18mg, 9mg) gegen Placebo getestet. Primärer Endpunkt war die absolute Veränderung der forcierten Vitalkapazität (FVC) über einen Zeitraum von 52 Wochen. Insgesamt nahmen knapp 1200 IPF-Patienten teil, von denen 77,7% bereits zu Studienbeginn eine antifibrotische Therapie mit Nintedanib oder Pirfenidon einnahmen. Die adjustierte Veränderung der FVC zu Woche 52 betrug unter Nerandomilast 18mg –114,7ml, unter Nerandomilast 9mg –138,6ml und –183,5ml in der Placebogruppe. Die häufigste Nebenwirkung von Nerandomilast war Durchfall.3 Aufgrund der Ergebnisse wurde der Wirkstoff im Oktober 2025 von der FDA zur Behandlung von Erwachsenen mit IPF zugelassen.4 Die europäische Zulassung soll folgen.
Entzündungshemmender Mechanismus der PDE4-Inhibition
Das Enzym PDE4 ist an der cAMP-Signalübertragung beteiligt. Es baut cAMP zu AMP ab. Wird PDE4 gehemmt, so steigt der cAMP-Spiegel in den Zellen. Mittels Durchflusszytometrie konnte gezeigt werden, dass ein erhöhter cAMP-Spiegel in Monozyten eine antientzündliche Wirkung entfaltet, da er zur Zunahme von Interleukin-10 (IL-10) führt, während die Spiegel von TNF-α und IL-12 gesenkt werden.5
Nerandomilast hemmte in vitro die Kontraktilität und Markerexpression von Myofibroblasten in zytokinstimulierten menschlichen IPF-Fibroblastenzellen und induzierte deren Entdifferenzierung. Zudem reduzierte es die vaskuläre Dysfunktion, indem es die Endothelverbindungen stärkte und die Expression von Adhäsionsproteinen unterdrückte.6
Prostacyclinanaloga
Auch diese Substanzen steigern die cAMP-Spiegel.7 Ein Wirkstoff aus dieser Gruppe, der bei pulmonaler Hypertonie eingesetzt wird, aber auch auf Fibroblasten abzielt und als antifibrotisch gilt, ist Treprostinil. Inhalierbares Treprostinil wurde bereits vor einigen Jahren bei Patienten untersucht, bei denen sich aufgrund einer interstitiellen Lungenfibrose Lungenhochdruck entwickelt hatte. Trotz einer kurzen Beobachtungszeit von 16 Wochen zeigte sich ein Anstieg der FVC im Vergleich zu Placebo.8
Derzeit wird der Wirkstoff in der Phase-III-Studie TETON bei Patienten mit IPF getestet.9
Lysophosphatidsäure (LPA)
Lysophospholipide wie LPA und Sphingosin-1-Phosphat (S1P) regulieren in vitro die Epithelzell- und Fibroblastenapoptose, die Fibroblastenmigration und die Myofibroblastendifferenzierung ebenso wie die Gefässpermeabilität und TGF-β.10
In einer Phase-II-Studie wurde der orale LPA-Rezeptor-1-Antagonist Admilparant bei Patienten mit IPF und mit progredienter pulmonaler Fibrose (PPF) gegen Placebo getestet. Erfasst wurde die prozentuale Veränderung der FVC über 26 Wochen. In der IPF-Gruppe lag sie bei –2,7% (Placebo), –2,8% (Admilparant 30mg) und –1,2% (Admilparant 60mg); in der PPF-Gruppe bei –4,3% (Placebo), –2,9% (30mg) und –1,1% (60mg).11
Wahl des geeigneten Medikaments
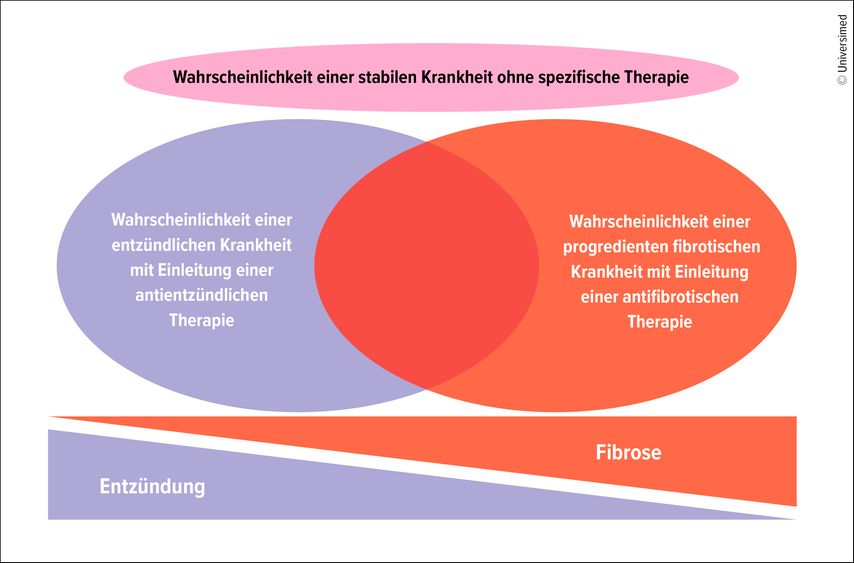
Bei der Entwicklung von ILD liegen zunächst Entzündungen gefolgt von Fibrosen vor, wobei sich beide auch überlappen können (Abb.1).1 In der klinischen Situation ist es schwierig, die Lungenentzündung zu quantifizieren und zu beurteilen, doch das ist relevant für die Therapieentscheidung. Noch schwieriger wird es, wenn Fibrose und Entzündung gemeinsam vorliegen.
Abb. 1: Kriterien für die Wahl der Erstlinientherapie bei ILD (modifiziert nach Behr J et al. 2024)1
Anwendung systemischer Steroide in der Praxis
Eine Metaanalyse des REMAP-ILD-Konsortiums zur systemischen Steroidtherapie bei fibrotisierenden ILD (fILD) hat ergeben, dass Steroide unter Umständen einen leicht positiven Einfluss auf die Verschlechterung der Lungenfunktion bei Non-IPF-fILD haben. Ansonsten konnte kein Vorteil der Steroidbehandlung festgestellt werden. Auch zur Sicherheit war die Evidenz schwach.12 In einer früheren Studie wurde jedoch gezeigt, dass bei IPF die Steroidgabe im Vergleich zu Placebo die Mortalitätsrate steigert.13
Da valide Daten fehlen, sollte eine modifizierte Delphi-Umfrage einen globalen Expertenkonsens über die Indikationen und die Rolle von Steroiden bei der Behandlung der fILD erzielen und zukünftige Forschungsschwerpunkte aufzeigen. Es bestand Einigkeit darüber, dass milchglasartige Trübungen im CT und eine Lymphozytose von >30% in der bronchoalveolären Lavage (BAL) auf eine Lungenentzündung hindeuten und auch die Steroidreaktion bei fILD vorhersagen können. Allerdings ist der Grenzwert von 30% Lymphozyten nicht durch Studien belegt. Und auch die Milchglastrübung ist nicht eindeutig. Eine Milchglastrübung kann bei fILD ebenso auftreten wie in Bereichen, in denen eine Traktionsbronchiektasie vorliegt.14
Diagnostische Kriterien für Therapieansprechen und Progression
Eine retrospektive Studie aus Kanada untersuchte den Zusammenhang zwischen der Morphologie bei ILD und ihrem Einfluss auf Krankheitsprogression, Mortalität und das Ansprechen auf immunsuppressive Therapie. Mehr als 600 Patienten mit Bindegewebserkrankung-ID wurden mit hochauflösender CT (HRCT) untersucht, wobei verschiedene morphologische Muster gefunden wurden: organisierende Pneumonie (OP), nichtspezifische interstitielle Pneumonie (NSIP), gewöhnliche interstitielle Pneumonie (UIP) und fibrosierende Hypersensitivitätspneumonitis (fHP). Dabei waren NISP und OP mit besserem Ansprechen auf Immunsuppression und einer höheren Überlebensrate verbunden als UIP und fHP.15
Eine andere kanadische Studie untersuchte, ob BAL-Befunde mit radiologischen Ergebnissen und klinischer Diagnostik korrelieren. Es zeigte sich, dass BAL-Zellanalysen nicht signifikant mit radiologischen Merkmalen korrelierten. Die oft als Zeichen einer Lungenentzündung interpretierten Milchglasopazitäten standen in dieser Kohorte nicht im Zusammenhang mit einer Lymphozytose in der BAL.16
Rheumatoide Arthritis und ILD
Bei der rheumatoiden Arthritis (RA) lassen sich bereits viele Jahre vor dem Auftreten der ersten Gelenkbeschwerden erhöhte Autoantikörper-Spiegel nachweisen. So ist etwa anticitrulliniertes Protein-Antikörper-IgG (ACPA-IgG) bereits rund 18 Jahre vor der Diagnose einer RA erhöht, Rheumafaktor-IgA (RF-IgA) 14 Jahre, RF-IgM 7 Jahre, ACPA-IgA 6 Jahre und ACPA-IgM sowie RF-IgA 5 Jahre vorher. Dabei beginnt die Produktion der Autoantikörper ausserhalb der Gelenke, unter anderem in der Lunge.17 Daher ist die RA nicht nur eine Gelenks-, sondern eine systemische Krankheit, die bei Patienten mit systemischer Beteiligung mit einer bis zu dreimal höherer Mortalität einhergeht.18 Und trotz zahlreicher Therapieoptionen sprechen bis zu 40% der Betroffenen nicht ausreichend auf die Behandlung an.19
Unterdiagnostiziert und untertherapiert: RA-assoziierte ILD
Die RA-assoziierte ILD (RA-ILD) kommt je nach Veröffentlichung bei 5 bis 60% der RA-Patienten vor, wobei sie nur in 10 bis 18% der Fälle Symptome verursacht.20,21 Dennoch ist eine frühe Diagnose wichtig, denn Patienten mit RA-ILD haben im Vergleich zu RA-Patienten ohne ILD nicht nur eine höhere 10-Jahres-Mortalitätsrate (60% vs. 35%).22 Zum Zeitpunkt der Diagnose ist auch bei den meisten Betroffenen die Lungenfunktion bereits stark eingeschränkt: 14% haben eine FVC <50%; 29% eine Kohlenmonoxid-Diffusionskapazität (DLCO) <40%. Im HRCT-Muster finden sich vor allem UIP und NSIP.21
Daten aus einer grossen deutschen Datenbank zu RA zeigen, dass vor Ausbruch der ILD schon verstärkt Entzündungsparameter wie CRP und eine erhöhte Erythrozytensedimentationsrate nachgewiesen werden können. Dabei ist die systemische Entzündung mehr noch als die RA-Krankheitsaktivität, gemessen mit dem DAS28 («Disease Activity Score in 28 joints»), ein Prädiktor für eine erhöhte Mortalität.20
Therapie bei RA-ILD
Konventionelle synthetische DMARDs («disease-modifying anti-rheumatic drugs») wie Methotrexat (MTX), die zur Basistherapie bei RA gehören, wurden immer wieder in Zusammenhang mit Schädigungen der Lunge, vor allem einer MTX-Pneumonie, gebracht. Es konnte aber nicht bewiesen werden, dass MTX auch eine RA-ILD auslöst.23 Neuere Studien haben ergeben, dass es nicht notwendig ist, die konventionellen synthetischen DMARDs abzusetzen, sondern dass ein Absetzen das PFS und die Mortalität eher negativ beeinflusst.24 Die Gabe von TNF-Inhibitoren geht im Vergleich mit anderen Substanzen ebenfalls mit einer höheren Sterblichkeit einher.20
Dagegen haben Mycophenolat Mofetil, Azathioprin und Rituximab offenbar einen positiven Effekt auf die Lungenfunktion, wie eine retrospektive Real-World-Studie zeigte.25
RA und andere Bindegewebskrankheiten
Die RA ist oft mit weiteren Bindegewebskrankheiten verbunden, zum Beispiel mit dem Sjögren-Syndrom. Diese Patienten weisen eine höhere Krankheitsaktivität auf und sprechen schlechter auf die Therapie an. Zudem zeigen Daten aus dem Schweizer Register für entzündlich-rheumatische Erkrankungen, dass bei gleichzeitigem Vorliegen von RA und Sjögren-Syndrom die Betroffenen deutlich kürzer bei einem TNF-Inhibitor verweilen als bei anderen Therapien.26 Es besteht daher eine höhere Wahrscheinlichkeit, dass in der Gruppe von RA-ILD-Patienten ein Teil eine Überschneidung mit dem Sjögren-Syndrom aufweist. Daher ist es wichtig, über die RA hinauszuschauen und zu prüfen, ob diese Patienten zusätzlich eine Bindegewebserkrankung haben könnten.
Quelle:
«New ILD treatment targets – from bench to bedside», Referat von Prof. Dr. med. Antje Prasse, Hannover; «Antifibrotic & anti-inflammatory treatment approaches – how to choose?», Referat von Prof. Dr. med. Manuela Funke-Chambour, Bern; «Rheumatoid arthritis-associated ILD», Referat von Prof. Dr. med. Florian Kollert, Basel. Jahreskongress der Schweizerischen Gesellschaft für Pneumologie, 15. bis 16. Mai 2025, Genève
Literatur:
1 Behr J et al.: Am J Respir Crit Care Med 2024; 210(4): 392-400 2 Bridges JP et al.: J Clin Invest 2025; 135(1): e183836 3 Richeldi L et al.: N Engl J Med 2025; 392(22): 2193-202 4 JASCAYD® (Nerandomilast) prescribing information. Boehringer Ingelheim Pharmaceuticals, Inc; 2025 5 Prasse A et al.: J Allergy Clin Immunol 2007; 119(2): 464-71 6 Reininger D et al.: Am J Respir Cell Mol Biol 2025; 73(5): 700-12 7 Roberts MJ et al.: Front Pharmacol 2021; 12: 669227 8 Waxman A et al.: N Engl J Med 2021; 384(4): 325-34 9 Nathan SD et al.: BMJ Open Respir Res 2022; 9(1): e001310 10 Shea BS, Tager AM: Proc Am Thorac Soc 2012; 9(3): 102-10 11 Corte TJ et al.: Am J Respir Crit Care Med 2025; 211(2): 230-8 12 Pitre T et al.: BMJ Open Respir Res 2023; 10(1): e002008 13 Raghu G et al.: N Engl J Med 2012; 366: 1968-77 14 Funke-Chambour M et al.: ERJ Open Res 2024; 10(5): 00561-2024 15 Zheng B et al.: Rheumatology (Oxford) 2024; 63(10): 2734-40 16 Grant-Orser A et al.: Chest 2025; 167(1): 172-82 17 Kelmenson LB et al.: Arthritis Rheumatol 2020; 72(2): 251-61 18 Kimbrough BA et al.: Arthritis Care Res (Hoboken) 2024; 76(4): 454-62 19 Olsen IC et al.: Rheumatology (Oxford) 2019; 58(3): 481-91 20 Rudi T et al.: RMD Open 2024; 10(2): e003789 21 Koduri G, Solomon JJ: Arthritis Rheumatol 2023; 75(12): 2067-77 22 Hyldgaard C et al.: Ann Rheum Dis 2017; 76(10): 1700-6 23 Fragoulis GE et al.: Rheumatology (Oxford) 2019; 58: 1900-6 24 Kim K et al.: Ther Adv Respir Dis 2022; 16: 17534666221135314 25 Matson SM et al.: Chest 2023; 163(4): 861-9 26 Christ L et al.: Arthritis Res Ther 2024; 26(1): 68
Das könnte Sie auch interessieren:
Umweltbelastungen der Atemwege
Atemwege sind besonders anfällig für luftgetragene Schadstoffe wie Gase, Stäube und Allergene. Eine Studie untersuchte den Einfluss der Endotoxinbelastung in Klassenräumen auf die ...
Nikotinabusus als Herausforderung für die Kinder- und Jugendmedizin
Vom fetalen Tabaksyndrom bis zu den neuen nikotinhaltigen Suchtmitteln bei Jugendlichen: Tabakkonsum hat bei Kindern und Jugendlichen negative medizinische Auswirkungen, die bis ins ...