Dreidimensionale In-vitro-Modelle für humane Haut
Autor:innen:
Julia Fink, BSc MSc1
Mag. Dr. Elisabeth Hofmann1
Univ.-Prof. Dr. Lars-Peter Kamolz, MSc1,2
Assoc. Prof. Mag. Dr. Petra Kotzbeck1
1COREMED – Zentrum für Regenerative Medizin und Präzisionsmedizin
JOANNEUM RESEARCH Forschungsgesellschaft mbH, Graz
2 Klinische Abteilung für Plastische, Ästhetische und Rekonstruktive Chirurgie
Universitätsklinik für Chirurgie
Medizinische Universität Graz
Korrespondierende Autorin:
Assoc. Prof. Mag. Dr. Petra Kotzbeck
E-Mail: petra.kotzbeck@joanneum.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Haut dient als wichtige Barriere, die den Körper vor physikalischen, chemischen und pathogenen Gefahren schützt und den bidirektionalen Transport von Wasser, Ionen und Nährstoffen reguliert. Um mehr Wissen über die Struktur und Funktion der Haut sowie über Hautkrankheiten zu generieren, werden häufig Tierversuche durchgeführt. In-vitro-Modelle, wie z.B. rekonstruierte humane Epidermis- oder Vollhautäquivalente, sind wertvolle Alternativen zu Tierversuchen. In der Vergangenheit wurden enorme Fortschritte bei der Herstellung von unterschiedlichen Hautmodellen mit zunehmender Komplexität erzielt. Zu den neuesten Errungenschaften zählen unter anderem der Einsatz von induzierbaren pluripotenten Zellen sowie neuartige 3D-Bioprinting-Verfahren.
Die Haut steht an der vordersten Front unseres Körpers und fungiert als Hülle, die den Organismus vor schädlichen Umwelteinflüssen wie Chemikalien, UV-Strahlung oder Krankheitserregern schützt. Tierversuche wurden und werden häufig verwendet, um die grundlegende Struktur der Haut, die Mechanismen der Wundheilung sowie unterschiedliche Hautkrankheiten zu erforschen. Die anatomischen Unterschiede zwischen Tier und Mensch beeinträchtigen jedoch häufig die Übertragbarkeit von Tierversuchen.1–3 Die Modellierung der menschlichen Haut in vitro würde die Übertragbarkeit der Ergebnisse gewährleisten und Tierversuche bei der präklinischen Bewertung neuartiger Therapieansätze reduzieren. Das „3R“-Prinzip (Replacement, Reduction und Refinement) der humanen Tierforschung ist weltweit anerkannt und in vielen nationalen und internationalen Gesetzen verankert.2 Ein voll funktionsfähiges, vollständig humanes In-vitro-Modell sollte eine native Hautstruktur und -funktionalität aufweisen; es sollte unterschiedliche Zelltypen enthalten, die sich sowohl vermehren als auch differenzieren können und zugleich auch Fettgewebe und Blutgefäße beinhalten. Ein solches ideales Modell würde sowohl die Infiltration von Immunzellen als auch eine langfristige Kultivierung ermöglichen. Es gibt bereits einige Modelle, die diesem Ziel nahekommen, jedoch sind noch weitere Optimierungen vonnöten.
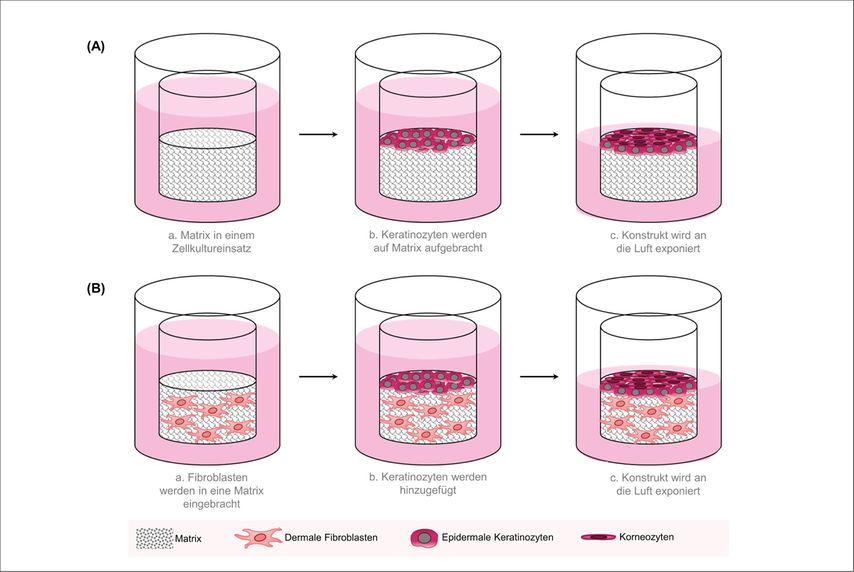
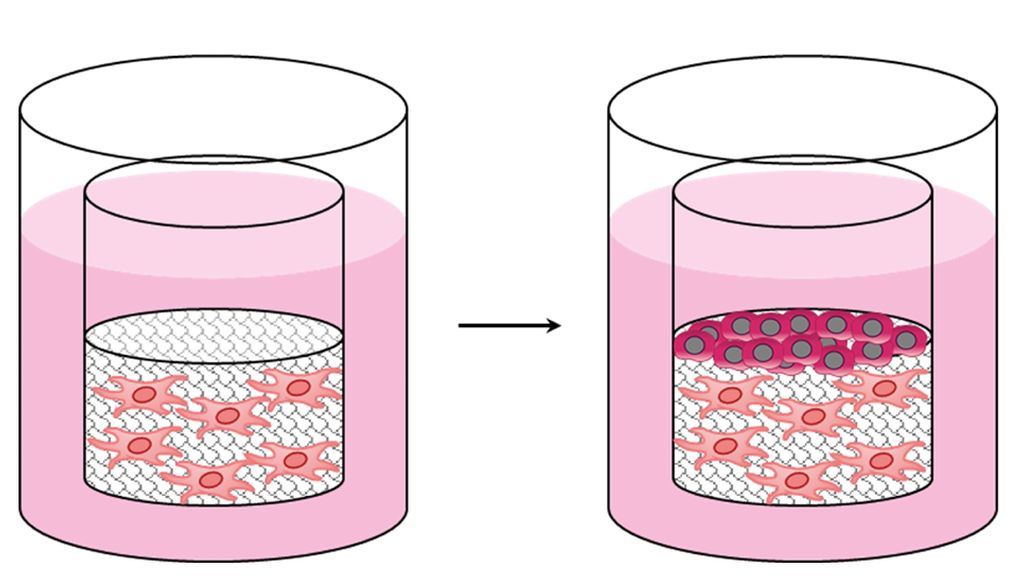
Abb. 1: Rekonstruierte humane Epidermis (RHE) und humanes Hautäquivalent (HSE). (A) Bei der Erstellung einer RHE werden Keratinozyten in eine Matrix gebracht, kultiviert und nach Exponierung an die Luft ausdifferenziert. (B) Durch eine zusätzliche Integration von dermalen Fibroblasten in die Matrix, kann ein HSE erstellt werden
Rekonstruierte humane Epidermis (RHE) und humanes Hautäquivalent (HSE)
Für die rekonstruierte menschliche Epidermis (RHE) beispielsweise werden normale menschliche Keratinozyten aus Hautbiopsien isoliert und in einem Kulturmedium expandiert. Die Zellen werden kurzzeitig unter submersen Bedingungen bzw. im Nährmedium kultiviert, bevor sie an die Luft-Flüssigkeits-Grenze gebracht (sogenannter „Air-lift“) werden, was essenziell für die Differenzierung der Keratinozyten ist.4,5 In einem kontinuierlichen Prozess, der etwa zwei Wochen dauert, bildet sich eine epidermisähnliche Struktur, die nachweislich die morphologischen, biochemischen und physiologischen Eigenschaften der nativen Epidermis zuverlässig reproduziert.6–8 Neben der rekonstruierten Epidermis wurden humane Hautäquivalente (HSE), sogenannte Vollhautmodelle, entwickelt. Diese bestehen aus einer dermalen Schicht, welche aus einer mit dermalen Fibroblasten besiedelten 3D-Matrix aufgebaut ist. Hierbei werden Keratinozyten nach ausreichender Kultivierung auf dieses Grundgerüst aufgebracht und integriert. Ähnlich wie bei der Herstellung von RHE werden die HSE für kurze Zeit unter submersen Kulturbedingungen inkubiert, bevor der „Air-lift“ durchgeführt und die Keratinozytendifferenzierung eingeleitet wird.9
Weiterentwicklung der Modelle mit zunehmender Komplexität
Künftige HSE würden von einem dreischichtigen Aufbau mit einer hypodermalen Schicht profitieren, der der physiologischen Hautanatomie entspricht und wichtige Funktionen wie die Hormonsekretion vermittelt.10–12 Die Einführung von Immunkompetenz in HSE ist ebenso ein wichtiges Thema im Tissue-Engineering, da das Fehlen von Immunzellen die physiologische Relevanz der derzeitigen HSE einschränkt. Insbesondere die Entzündung, ein wesentlicher Faktor bei der Wundheilung, hängt sowohl von gewebeeigenen Immunzellen als auch von Immunzellen ab, die aus dem Blutkreislauf rekrutiert werden.13 Eine wichtige Herausforderung besteht darin, alle notwendigen Signale für die verschiedenen Immunzellpopulationen bereitzustellen und gleichzeitig die Lebensfähigkeit und Funktionalität von Keratinozyten, Fibroblasten und möglicherweise Adipozyten zu erhalten. So hat sich beispielsweise gezeigt, dass die Zusammensetzung des Kulturmediums ein kritischer Faktor bei der Einbringung von Makrophagen in ein HSE ist.14
Die Durchblutung des Konstrukts ist ebenfalls eine weitere große Herausforderung auf dem Weg zu einem physiologischeren In-vitro-Hautmodell. Die Vaskularisierung des dermalen (und hypodermalen) Kompartiments wäre für die Erforschung der Entwicklung von Hautkrankheiten, der Wundheilung, der Metastasierung von malignen Melanomen oder auch der Pharmakodynamik von wesentlicher Bedeutung. Ein HSE, das ein Gefäßsystem auf der Grundlage einer Matrix, bei der zuvor alle Zellen entfernt wurden (sog. dezellularisiert) und konservierte Gefäßstrukturen enthält, ist ein vielversprechender Ansatz.15 Auch die Fortschritte beim 3D-Biodruck zeigen vielversprechende Ergebnisse,16 obwohl die Mikrozirkulation der Haut noch nicht vollständig nachgeahmt werden kann.
Ein weiterer wichtiger Bestandteil der Haut sind Nerven. Um innervierte Hautäquivalente zu erzeugen, wurden bereits Neuronen der Dorsalwurzelganglien entweder von Schweinen17 oder von Mäusen18 in ansonsten vollständig menschliche Hautäquivalente integriert. Ein weiterer Ansatz ist die Verwendung von induzierten humanen neuralen Stammzellen (ihNSCs), welche durch direkte Reprogrammierung von dermalen Fibroblasten erzeugt werden können.19 Diese ihNSCs differenzieren sich unabhängig von der Medienzusammensetzung in Neuronen, sind robust und behalten ihren neuronalen Phänotyp auch in komplexen Ko-Kulturen bei. Mithilfe des ihNSC-Ansatzes konnte bereits ein vollständig humanes innerviertes HSE erfolgreich hergestellt werden, was wiederum die In-vivo-Situation widerspiegelt.20
3D-Bioprinting
Eine revolutionäre Technologie in diesem Forschungsgebiet ist das sogenannte 3D-Bioprinting. Bei dieser Methode werden zur Herstellung dreidimensionaler komplexer biologischer Strukturen lebende Zellen, Biomaterialien („Bio-Tinten“) und biologische Moleküle als Ausgangsmaterial für den schichtweisen Druck verwendet. Bei diesem additiven Herstellungsverfahren können Gewebekonstrukte mit einem individuellen Design auf hochflexible und reproduzierbare Weise erzeugt werden.21,22 Die Möglichkeit, anatomisch präzise Strukturen mit verschiedenen Zelltypen herzustellen, ist ein Highlight des 3D-Bioprintings, insbesondere im Hinblick auf die Option, gefäßähnliche Strukturen in diese Konstruktion einzubeziehen.16,23,24
Fazit
Komplexe HSE sind wertvolle und vielversprechende Instrumente für die Erforschung der Struktur und Funktion der Haut. Innovative Technologien wie die Verwendung von iPSCs und 3D-Bioprinting sind natürlich anspruchsvoll, werden aber die Entwicklung menschlicher Hautmodelle nachhaltig beeinflussen. Neben der Grundlagenforschung können zukünftig noch komplexere Hautmodelle auch für die Erforschung von Hautkrankheiten und die kutane Wundheilung mit hoher translationaler Effizienz eingesetzt werden. Die standardisierte Erstellung von humanen Vollhaut-Äquivalenten wird es ermöglichen, diese in Experimenten zum Wirkstoffscreening einzusetzen und damit Tierversuche zu ersetzen oder zumindest stark zu reduzieren.
Literatur:
1 Avci P et al.: Animal models of skin disease for drug discovery. Expert Opin Drug Discov 2013; 8(3): 331-55 2 Dellambra E et al.: Non-animal models in dermatological research. ALTEX 2019; 36(2): 177-202 3 Jung EC, Maibach HI: Animal models for percutaneous absorption. J Appl Toxicol 2015; 35(1): 1-10 4 Prunieras M et al.: Methods for cultivation of keratinocytes with an air-liquid interface. J Invest Dermatol 1983; 81(1): S28-33 5 Asselineau D et al.: Human epidermis reconstructed by culture: Is it “normal”? J Invest Dermatol 1986; 86(2): 181-6 6 Rosdy M et al.: Production of basement membrane components by a reconstructed epidermis cultured in the absence of serum and dermal factors. BR J Dermatol 1993; 129(3): 227-34 7 Rosdy M, Clauss LC: Terminal epidermal differentiation of human keratinocytes grown in chemically defined medium on inert filter substrates at the air-liquid interface. J Invest Dermatol 1990; 95(4): 409-14 8 Ponec M et al.: Lipid and ultrastructural characterization of reconstructed skin models. Int J Pharm 2000; 203(1-2): 211-25 9 Sriram G et al.: Fibroblast heterogeneity and its implications for engineering organotypic skin models in vitro. Eur J Cell Biol 2015; 94(11): 483-512 10 Bellas E et al.: In vitro 3D full-thickness skin-equivalent tissue model using silk and collagen biomaterials. Macromol Biosci 2012; 12(12): 1627-36 11 Trottier V et al.: IFATS collection: Using human adipose-derived stem/stromal cells for the production of new skin substitutes. Stem Cells 2008; 26(10): 2713-23 12 Monfort A et al.: Production of human tissue-engineered skin trilayer on a plasma-based hypodermis. J Tissue Eng Regen Med 2013; 7(6): 479-90 13 Pupovac A et al.: Toward Immunocompetent 3D Skin Models. Adv Healthc Mater 2018; 7(12): 1701405 14 Griffoni C et al.: In vitro skin culture media influence the viability and inflammatory response of primary macrophages. Sci Rep 2021; 11(1): 7070 15 Groeber F et al.: A first vascularized skin equivalent as an alternative to animal experimentation. ALTEX 2016; 33(4): 415-22 16 Liu X et al.: A biofabricated vascularized skin model of atopic dermatitis for preclinical studies. Biofabrication2020; 12(3): 035002 17 Roggenkamp D et al.: Epidermal nerve fibers modulate keratinocyte growth via neuropeptide signaling in an innervated skin model. J Invest Dermatol 2013; 133(6): 1620-8 18 Blais M et al.: Sensory neurons accelerate skin reepithelialization via substance P in an innervated tissue-engineered wound healing model. Tissue Eng Part A 2014; 20(15-16): 2180-8 19 Cairns DM et al.: Expandable and Rapidly Differentiating Human Induced Neural Stem Cell Lines for Multiple Tissue Engineering Applications. Stem Cell Reports 2016; 7(3): 557-70 20 Lightfoot Vidal SE et al.: 3D biomaterial matrix to support long term, full thickness, immuno-competent human skin equivalents with nervous system components, Biomaterials 2019; 198: 194-203 21 Matai I et al.: Progress in 3D bioprinting technology for tissue/organ regenerative engineering. Biomaterials 2020; 226: 119536 22 Murphy SV, Atala A: 3D bioprinting of tissues and organs. Nat Biotechnol 2014; 32(8): 773-85 23 Kim BS et al.: 3D Cell Printing of Perfusable Vascularized Human Skin Equivalent Composed of Epidermis, Dermis, and Hypodermis for Better Structural Recapitulation of Native Skin. Adv Healthc Mater 2019; 8(7): e1801019 24 Baltazar T et al.: Three dimensional bioprinting of a vascularized and perfusable skin graft using human keratinocytes, fibroblasts, pericytes and endothelial cells. Tissue Eng Part A 2020; 26(5-6): 227-38
Das könnte Sie auch interessieren:
„Ich habe den schönsten Beruf der Welt“
Mit dem diesjährigen Jahreskongress der Österreichischen Gesellschaft für Plastische, Ästhetische und Rekonstruktive Chirurgie (ÖGPÄRC) in Salzburg hat Prim. Univ.-Doz. Dr. Rupert Koller ...
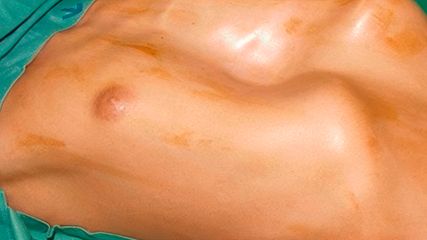
Die Trichterbrust – Diagnostik, Symptomatik und moderne Therapieansätze
Die Trichterbrust führt je nach Ausprägung zu psychischen, aber auch zu organischen Problemen, die mit einer körperlichen Leistungseinschränkung einhergehen. Die immer wieder geäußerte ...
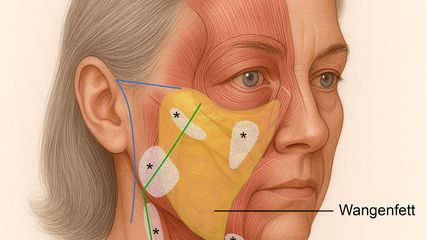
Moderne Faceliftchirurgie
Das Facelift, eine klassische Operation der plastischen Chirurgie, erfährt in den letzten Jahren ein Revival. Die gestiegene Nachfrage der Patienten ist einerseits auf bessere Ergebnisse ...