Laborkontrollen bei Epilepsien
Autor:
PD Dr. Christian Tilz
Epilepsiezentrum Bodensee
Zentrum für Psychiatrie Südwürttemberg
Standort Ravensburg-Weissenau
Ravensburg
Krankenhaus Barmherzige Brüder Regensburg
Klinik für Neurologie, Epileptologie
Regensburg
Universitätsklinik für Neurologie
MedUni Graz
Graz
E-Mail: Christian.Tilz@ZfP-Zentrum.de
Indikationen für Laborkontrollen bei Epilepsien ergeben sich aus unterschiedlichen Gründen: Sie sind erforderlich, um Nebeneffekte der anfallssupprimierenden Medikamente auf verschiedene Organsysteme zu erkennen, können aber auch nach einem Anfallsereignis für die differenzialdiagnostische Abklärung von epileptischen Anfällen gegenüber anderen Anfallsereignissen wie etwa Synkopen oder dissoziativen Anfällen wertvolle Informationen liefern. Zudem kommt der Liquordiagnostik zunehmende Bedeutung für die Diagnostik von Epilepsien im Rahmen der Abklärung einer entzündlichen Genese, insbesondere auch von Autoimmunenzephalitiden, zu.
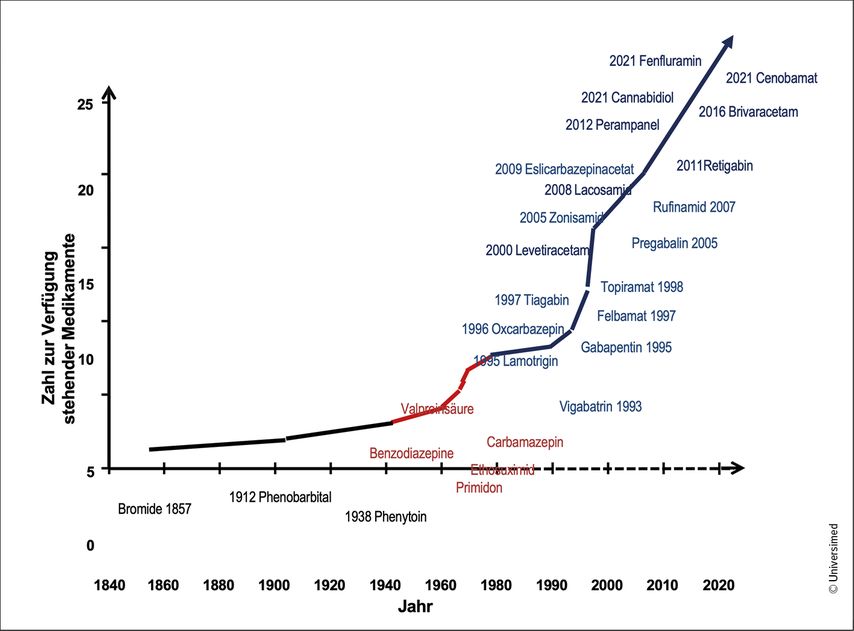
Da die medikamentöse Behandlung von Epilepsien eine symptomatische Therapie darstellt und somit in der Regel über viele Jahre erfolgt, sind die Erkennung und die Überwachung von Nebenwirkungen durch die anfallssupprimierenden Medikamente (früher Antiepileptika, Abb. 1) erforderlich, um solche therapieabhängigen Nebenwirkungen auf Organsysteme wie etwa das hämatopoetische System, die Leber- oder Nierenfunktion sowie den Elektrolythaushalt zu erkennen und rechtzeitig zu erfassen. Das Risiko für solche Nebenwirkungen ist zwischen den einzelnen Substanzen sehr unterschiedlich. Die Frage, wie häufig welche Laborkontrollen erfolgen sollten, um entsprechende Konsequenzen aus veränderten Laborwerten ziehen zu können, lässt sich somit nicht einheitlich beantworten. Die Datenlage zur Notwendigkeit von regelmäßigen Laborkontrollen ist sehr heterogen, sodass einheitliche Standards zu den Laborkontrollen unter anfallssupprimierender Therapie fehlen.
Empfohlene Laborkontrollen
Pragmatisch empfehlen somit viele Autoren als Basisprogramm die Bestimmung folgender Parameter vor Beginn der Therapie und im Verlauf:
-
„Großes“ Blutbild einschließlich Differenzialblutbild und Thrombozyten (Hämatopoese!)
Leberwerte: Bilirubin, γ-GT, GOT, GPT, alkalische Phosphatase (AP)
Nierenwerte
-
Elektrolyte: Natrium, Kalium, Kalzium, Phosphat
-
Triglyzeride, Cholesterin
-
Gesamteiweiß und Serum-Elektrophorese
-
Gerinnung
Grundsätzlich kann festgehalten werden, dass für die sogenannten „alten“ anfallssupprimierenden Medikamente, insbesondere Valproinsäure, wesentliche detaillierte Daten zu laborchemischen und hämatopoetischen Veränderungen zur Verfügung stehen, da bei Valproat bereits innerhalb kurzer Zeit hepatotoxische Reaktionen vor allem im Kindesalter möglich sind. Allerdings sind auch unter neuen anfallssupprimierenden Medikamenten Veränderungen des Blutbildes möglich, wie etwa seltene Fälle eines DRESS-Syndroms unter Cenobamat oder aplastische Anämien unter Felbamat. Als pragmatische Empfehlung sollten Verlaufskontrollen 1–3 Monate nach Behandlungsbeginn bzw. bei Dosisanpassungen erfolgen, im Verlauf nach 4–6 Monaten, bei Anfallsfreiheit und guter Verträglichkeit im Verlauf auch in größeren Intervallen (z.B. 1x/Jahr), wobei substanzspezifische Besonderheiten bedacht werden müssen, die dann ggf. häufigere Kontrollen erfordern.
Monitoring der Plasmaspiegel
Die Festlegung der Referenzwerte für die Blutspiegel der anfallssupprimierenden Therapie erfolgte für die ersten und alten Substanzen, insbesondere Phenobarbital, Phenytoin, Carbamazepin und Valproinsäure, unter Berücksichtigung ausführlicher Studien zur Dosis-Wirkungs-Relation. Dies hat angesichts der Interaktionen und teilweise komplexen Verstoffwechselungsprozesse, etwa der nichtlinearen Kinetik von Phenytoin, direkte Bedeutung für die Bestimmung der Zieldosis. Für die „neuen“ anfallssupprimierenden Medikamente fehlen entsprechende Studien für die Bestimmung der Referenzwerte jedoch weitgehend, sodass diese arbiträr festgelegt wurden.
Blutspiegelkontrollen dienen daher insbesondere bei neuen anfallssupprimierenden Medikamenten im Allgemeinen NICHT der Festsetzung der Zieldosis, da anerkannte Referenzwerte für neue anfallssupprimierende Medikamente bezüglich der Dosis-Wirkungs-Beziehung fehlen. Sie können jedoch hilfreiche Zusatzinformationen für die Frage der Compliance oder veränderter Stoffwechselbedingungen (Schwangerschaft, Interaktionen) liefern. Da jedoch die Bereiche des „therapeutischen“ Serum-Spiegels von Patient:in zu Patient:in einer großen interindividuellen Breite unterliegen, wäre der Ausdruck des „individuellen therapeutischen Bereichs“ angemessener.
Laborkontrollen für die differenzialdiagnostische Abklärung
Für die differenzialdiagnostische Abgrenzung von epileptischen Anfällen gegenüber anderen Anfallsereignissen eignet sich die Bestimmung der Kreatinkinase, von Prolaktin und Laktat. Die Bestimmung von Prolaktin unmittelbar nach dem Anfallsereignis erlaubt nach einem tonisch-klonischen Anfall mit einer Spezifität von bis zu 96% und einer Sensitivität von 46% die differenzialdiagnostische Zuordnung gegenüber einem psychogenen Anfall, unterliegt allerdings einer zirkadianen Rhythmik. Der Prolaktinwert steigt innerhalb der ersten 20 Minuten nach einem tonisch-klonischen Anfall, fällt danach aber rasch wieder ab, sodass er unmittelbar nach dem Anfall und 24 Stunden danach bestimmt werden muss. Er eignet sich zur differenzialdiagnostischen Abgrenzung eines tonisch-klonischen Anfalls gegenüber einem psychogenen Anfall, weniger gut zur Abgrenzung eines tonisch-klonischen Anfalls gegenüber einer Synkope. Die Kreatinkinase (CK) als Ausdruck der Rhabdomyolyse eignet sich ebenso vor allem für die Erfassung von tonisch-klonischen Anfällen, kann jedoch nach intensiver körperlicher Belastung erhöht sein. Der Anstieg der CK erfolgt üblicherweise innerhalb der ersten 24 Stunden und erreicht 24–72 Stunden nach dem Anfall sein Maximum, sodass eine zu frühe Bestimmung mit falsch negativen CK-Werten einhergehen kann und die Bestimmung im Bedarfsfall am Folgetag wiederholt werden sollte. Die Bestimmung von Laktat hat in jüngster Zeit zunehmend an Bedeutung gewonnen. Laktat kann aus der Blutgasanalyse sowie aus dem Serum bestimmt werden, auch im Liquor ist ein Laktatanstieg nach tonisch-klonischen Anfällen messbar. Die Bestimmung von Laktat kann mit einer Sensitivität bis zu 89% und einer Spezifität von 89% eine Unterscheidung zwischen einem tonisch-klonischen Anfall und einem nicht epileptischen Anfall ermöglichen, sodass die neuen Leitlinien zum ersten epileptischen Anfall und zu Epilepsien im Erwachsenenalter empfehlen, Laktat und die CK zeitnah nach dem Ereignis und nach 24–48 Stunden bei unklarem Ereignis zur Differenzialdiagnose zu bestimmen.
Liquorpunktion zur Abklärungvon Enzephalitiden
Die Liquorpunktion ist unerlässlich für die Diagnostik von erregerbedingten Enzephalitiden und Autoimmunenzephalitiden. Allerdings ist sie nicht in jedem Fall bei einem erstmaligen Anfall erforderlich. Da die Liquorpunktion in der überwiegenden Anzahl der Erstmanifestationen einer Epilepsie unauffällig ist, insbesondere wenn der epileptische Anfall das einzige Symptom der Erkrankung ist, wird eine generelle Lumbalpunktion nach einem ersten unprovozierten Anfall grundsätzlich nicht empfohlen. Allerdings wäre jedoch ein fehlender Liquorbefund im Falle eines ersten Anfalls bei einer akuten Enzephalitis mit fatalen Folgen verbunden, sodass eine klare Empfehlung erforderlich ist, in welchen Fällen eine Liquorpunktion nach einem ersten Anfall erforderlich ist. Hierfür eignet sich die Bestimmung des IDEAL-Scores (Süße et al., 2021), bei dem mittels der Abfrage von 9 klinischen Symptomen mit einer Sensitivität von 98% und einem negativen prädiktiven Wert von 99% die Notwendigkeit für eine Indikationsstellung zur Lumbalpunktion geprüft werden kann.
Generell ist eine Zellzahlerhöhung als Folge eines isolierten epileptischen Anfalls stets sehr gering, während das Laktat innerhalb der ersten 6 Stunden nach einem Anfall deutlich ansteigt. Daher muss eine Zellzahlerhöhung von mehr als 10 Zellen/µl im Liquor immer als Red Flag gesehen werden und darf nicht als Reizpleozytose nach einem Anfall verkannt werden. In diesen Fällen sollte eine probatorische antivirale Therapie unmittelbar begonnen werden, bis die weitere virologische, mikrobiologische bzw. gegebenenfalls auch immunologische Diagnostik erfolgt ist. Die autoimmunologische Diagnostik sollte stets aus Serum und Liquor erfolgen. Sofern der klinische Verdacht auf eine Autoimmunenzephalitis besteht, also etwa eine klinisch rasch progrediente therapieresistente Epilepsie oder neuropsychologische bzw. psychiatrische Symptome in Kombination mit der Erstdiagnose einer Epilepsie (Graus-Kriterien), so sollte auch bei unauffälligem MRT oder Liquorroutinebefund die autoimmunologische Diagnostik erfolgen. Im Unterschied zur Zellzahl steigt das Laktat sowohl im Liquor als auch im Serum nach einem tonisch-klonischen Anfall innerhalb von 6 Stunden rasch an, fällt dann aber auch im Verlauf rascher ab als die CK.
Take-Home-Message
Bei der Langzeittherapie mit anfallssupprimierenden Medikamenten sollten aufgrund von potenziellen Organveränderungen Laborkontrollen vor und unter Therapie erfolgen. Ausmaß und Häufigkeit der Kontrollen sind abhängig von der Substanz, dem Alter des Patienten und dem klinischen Behandlungsverlauf.
Die Referenzwerte für die Blutspiegel unter anfallssupprimierender Therapie sind insbesondere für die alten, anfallssupprimierenden Medikamente gut untersucht, bei den „neuen“ anfallssupprimierenden Medikamenten fehlen jedoch entsprechende Studien zur Festlegung der Referenzwerte, sodass diese willkürlich festgelegt wurden. Insofern dient die Spiegelbestimmung nicht für die Findung der Zieldosis dieser Medikamente, kann jedoch wertvoll für Fragen zur Compliance oder zur Prüfung von Interaktionen bzw. veränderten Stoffwechselbedingungen sein.
Nach einem unklaren Anfallsereignis sollten Laktat und CK zeitnah nach dem Ereignis und 24–48 Stunden danach zur differenzialdiagnostischen Klärung bestimmt werden.
Die Liquorbestimmung nach dem ersten Anfall ist nicht in jedem Fall grundsätzlich erforderlich, ist aber unerlässlich, sofern sich klinisch oder anamnestisch der Anhalt für eine Enzephalitis ergibt. Der IDEAL-Score ermöglicht, die Indikationsstellung für die Lumbalpunktion klar zu definieren.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Pharmakologische und neuromodulatorische Behandlungen des Clusterkopfschmerzes
Die Behandlung des chronischen Clusterkopfschmerzes steht noch heute vor großen Herausforderungen. Am 19. European Headache Congress (EHC) 2025 präsentierte Dr. Anja Petersen, ...
Ist die ketogene Diät eine Präzisionsmedizin?
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...