Chronische Schluckstörungen bei Motoneuronerkrankungen
Autor:
Dr. Helmut F. Novak
Universitätsklinik für Neurologie, neurologische Intensivmedizin und Neurorehabilitation
Christian-Doppler-Klinik
Paracelsus Medizinische Universität Salzburg
E-Mail: h.novak@salk.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Schluckstörungen sind bei chronischen neurologischen Erkrankungen, wie Motoneuronerkrankungen (MND), Parkinson, Myasthenia gravis, Multiple Sklerose (MS), Chorea Huntington oder Demenz, häufig. Für eine möglichst lange und weitgehende Erhaltung der Lebensqualität und Selbstständigkeit der Patient*innen ist ein früher, multidisziplinärer Therapieansatz ausschlaggebend.
Keypoints
-
Patient*innen mit Motoneuronerkrankungen sind durch Schluckstörungen gravierend und dauerhaft belastet.
-
Durch frühe aktivierende Therapien soll die Funktion möglichst lange erhalten bleiben und kann der progrediente Verlauf verzögert werden.
-
Apparative Verfahren können sowohl die klinische Verlaufsdiagnostik sinnvoll ergänzen als auch z.B. die Indikationsstellung für die PEG-Sonden-Anlage erleichtern.
-
Im Mittelpunkt müssen nach medizinethischen Gesichtspunkten jedenfalls die Autonomie und die Lebensqualität der Patient*innen stehen, durch sämtliche möglichen Maßnahmen darf niemals mehr geschadet als genützt werden.
Bei Myasthenia gravis wird die Häufigkeit mit bis zu 40%, bei Alzheimer mit bis zu 84%, bei Parkinson mit bis zu 50% (82% „end-stage disease“), bei ALS mit 10–30% bis 100% („end-stage disease“) und bei MS mit bis zu 44% (im Schub) angegeben (Boeykens et al., 2014; Dziewas et al., 2020). Bei den Motoneuronerkrankungen, wie amyotrophe Lateralsklerose (ALS), spinale Muskelatrophie (SMA) und progressive bulbäre Muskelatrophie (PBMA), sind jene Patient*innen mit bulbärem Beginn mit beinahe 34% am häufigsten davon betroffen (Donohue et al., 2022).
Ursachen, Komplikationen und Langzeitfolgen
Bezüglich der dazu beitragenden funktionellen Mechanismen bestehen gewisse Überschneidungen mit Schluckstörungen beim Schlaganfall (zu früher Bolusabfluss, pharyngeale Residuen), aber auch deutliche Unterschiede. Bei ALS kommt nämlich noch die reduzierte Kontraktilität mit konsekutiver Schwäche der Rachen- bzw. der Zungenmuskulatur hinzu (Warneke et al., 2021), während durch die weitgehend erhaltene Sensibilität die Auslösung des Schluckreflexes gegenüber dem Schlaganfall nicht beeinträchtigt wird.
Durch die Schluckstörung werden auch die häufigsten Komplikationen verursacht, nämlich Pneumonie durch stille Aspiration, an welcher bei zusätzlich mangelnder Mundhygiene die folgenden grampositiven wie auch gramnegativen Mikroorganismen am häufigsten beteiligt sind: Staphylococcus aureus, Streptococcus pneumoniae, Haemophilus influenzae, Pseudomonas aeruginosa, Escherichia coli (Ortega et al., 2017). Durch häufig erforderliche Antibiosen werden in weiterer Folge auch multiresistente Keime selektioniert, welche nicht nur die Betroffenen gefährden, sondern ein hohes infektiologisches Risiko im Gesundheitssystem darstellen.
Bei etwa einem Drittel der Patient*innen kommt es durch ein Missverhältnis von Speichelproduktion und Schluckkompetenz zur Pseudohypersalivation, was ebenfalls mit bulbärem Beginn assoziiert ist, und nur etwa 53% der untersuchten Patient*innen erhielten dagegen Medikamente (Pearson et al., 2020).
Eine völlig unberechenbare und akut lebensbedrohende Komplikation stellen Bolusevents dar, über deren Häufigkeit es keine sicheren Angaben gibt. Dabei kommt es meist während des Essens durch einen für die Schluckkompetenz zu großen Bissen zu einer plötzlichen Verlegung des Kehlkopfeingangs mit Asphyxie und raschem Eintritt von Bewusstlosigkeit.
Mit zunehmendem Fortschritt der Erkrankungen treten langfristige Auswirkungen der neurogenen Schluckstörung in den Vordergrund und beeinträchtigen in erheblichem Ausmaß die Lebensqualität. Es kann dabei zu Mangelernährung und unzureichender Medikamentenwirkung kommen (Dziewas et al., 2020). Für die Messung der Lebensqualität wurden in der Logopädie verschiedene Scoring-Instrumente etabliert, wie etwa MDADI, SWAL-QOL, Deglutition Handicap Index, Dysphagia Handicap Index oder EAT-10. Dabei werden physische, funktionelle und emotionale Domänen erfasst (Vieira & Bolles, 2017).
Bedeutsam für die Lebensqualität ist darüber hinaus das gleichzeitige Auftreten von Dysphagie und Sprechstörungen, woran nahezu 60% der untersuchten Patient*innen leiden (Donohue et al., 2022).
Dysphagiediagnostik
Zur Diagnostik der neurogenen Schluckstörung stehen auch bei MND bewährte Methoden zur Verfügung:
-
Videokinematografie = Videofluoroskopie (VFS)
-
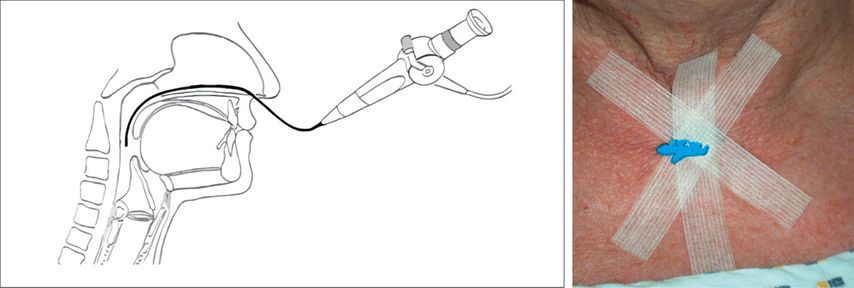
Flexible endoskopische Evaluation des Schluckakts (FEES, Abb. 1A)
-
Wasser-Schluck
-
Milch-Schluck
-
(Methylen-/Toluidin-)Blau-Schluck (Tracheostoma, Abb. 1B)
Abb. 1: Dysphagiediagnostik mittels Endoskopie (A) und Blau-Schluck (B)
Darüber hinaus versuchen neuerdings auch neue Untersuchungsmethoden, sich zu etablieren, wie Zungenkraft-Manometrie (Robison et al., 2022), sonografische Messung der Zungendicke (Potente et al., 2023) sowie die Kombination beider (Recasens et al., 2023), welche sowohl bei der Beurteilung der oralen wie auch der pharyngealen Transitphase eine deutliche Korrelation zur Aussagekraft der VFS aufweisen.
Behandlungsstrategien
Hinsichtlich der Behandlungsmöglichkeiten neurogener Schluckstörungen stehen auch bei MND – insbesondere zur Hintanhaltung der stillen Speichelaspiration – sowohl medikamentöse Maßnahmen mit anticholinerg wirksamen Substanzen (Atropin als Tropfen, Hyoscin, Methylscopolamin als transdermales System, Amitriptylin in niedriger Dosierung) oder Botulinumtoxin-Applikationen in die Speicheldrüsen (Garuti et al., 2019) als auch in gegenüber der Medikation resistenten Fällen die Radiotherapie der Speicheldrüsen oder mikrochirurgische Eingriffe auf Glottisebene zur Verfügung.
Darüber hinaus ist aber grundsätzlich ein multidisziplinäres Konzept mit interprofessioneller Zusammenarbeit gefordert, in welchem klinische Ernährungsexpert*innen bzw. Diätassistent*innen (Auswahl der Nahrung, z.B. Breikost oder hochkalorische Zusatznahrung), die Logopädie (hinsichtlich Schluckstatus, Schlucktraining und Wahl der adäquaten Nahrungskonsistenz) sowie die Ergotherapie (bezüglich Hilfsmittelstellung und Feinmotoriktraining) eine große Rolle spielen (Boeykens et al., 2014).
Eine gelungen erscheinende Kombinationsmöglichkeit von Therapie und Ernährung stellt die pharyngeale Elektrostimulationssonde dar, welche nicht nur eine ausreichende Flüssigkeits- und Kalorienzufuhr über die Sonde gewährleisten kann, sondern auch positive Effekte auf die Kräftigung der am Schluckakt beteiligten Muskeln ausüben soll. Allerdings zeigte eine Untersuchung bei ALS-Patient*innen keinen anhaltenden Besserungseffekt (Herrmann et al., 2022).
Bei einem weiteren Fortschreiten der Schluckstörung ist es besonders wichtig, die Indikation zum Beginn mit klinischer Ernährungstherapie zeitgerecht zu wählen. Dabei helfen eine Prognoseeinschätzung hinsichtlich des weiteren Krankheitsverlaufs durch regelmäßige Evaluation und klinische Kontrollen wie auch medizinethische Überlegungen einschließlich der Berücksichtigung des Patient*innenwillens. Letzterer sollte bei MND-Patient*innen im gesamten Verlauf im Sinne von Advance Care Planning begleitend erfragt und dokumentiert werden.
Für eine parenterale Ernährungstherapie gibt es bei MND keine ausreichende Indikation, zumal die Verwendung auch im intensivmedizinischen Kontext gegenüber früher deutlich in den Hintergrund gerückt ist.
Als logische Konsequenz der besonders bei akuter Verschlechterung der Schluckfunktion – z.B. im Rahmen von fieberhaften Infekten – rasch praktikablen nasogastrischen Sonde ergibt sich sohin die Indikationsstellung (unterstützt z.B. durch die VFS-Dysphagieskala nach Shijo et al., 2023) für die Anlage einer PEG-Sonde. Dabei muss jedoch immer das unmittelbare Risiko (Blutung, Infektion) gegenüber dem mittelbaren Nutzen für die Patient*innen abgewogen werden. In diesem Zusammenhang sollte auch klargestellt werden, zu welchem Zeitpunkt bzw. ab welchem Krankheitsfortschritt keine Indikation mehr für die Weiterführung der klinischen Ernährungstherapie gegeben ist, wenn Patient*innen davon nicht mehr hinsichtlich der Verbesserung oder mindestens des Erhalts ihrer Lebensqualität profitieren können.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Wichtige Laborparameter bei Epilepsie: ein aktueller Überblick
Laborkontrollen sind bei Epilepsien aus verschiedensten Gründen erforderlich. Anfallssupprimierende Medikamente können Störwirkungen auf unterschiedliche Organsysteme haben, die unter ...
Alzheimer: laufende klinische Studien, State of the Art der Biomarkerdiagnostik und gemischte Pathologien
Die Forschung an neuen Therapien für die Alzheimerkrankheit (AD) erfährt ein nie dagewesenes Momentum. Auf der internationalen Alzheimer- und Parkinsonkonferenz AD/PD in Wien gab es ...
Nahrungsergänzungsmittel bei ME/CFS: neue Hoffnung oder falsche Versprechen?
Chronische Erschöpfung, die nicht vergeht, Schmerzen, Konzentrationsprobleme, ein Leben in Zeitlupe. Myalgische Enzephalomyelitis/Chronisches Fatigue-Syndrom (ME/CFS) betrifft weltweit ...