Immunsuppression und Infektion: Durchimpfen so gut wie möglich
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Autoimmunerkrankungen sind mit erhöhtem Infektionsrisiko verbunden, das durch immunsupprimierende Therapien weiter verstärkt wird. Impfungen sind also in der betroffenen Patient:innengruppe von besonderer Bedeutung. Leider ist unter Immunsuppression jedoch auch das Ansprechen auf Impfungen eingeschränkt.
Dr. Sabine Koppelstätter von der Innsbrucker Universitätsklinik für Innere Medizin II weist darauf hin, dass die zelluläre Immunantwort mit dem Alter an Effektivität verliert. Im Alter sind T-Zellen schlechter in der Lage, sich in aktive Subpopulationen zu differenzieren (Immunoseneszenz) und entwickeln vermehrt sogenannte Checkpoints, die als Bremsen der Immunantwort fungieren. Dies sei bei Patient:innen mit Autoimmunerkrankungen nicht per se eine ungünstige Entwicklung, so Koppelstätter. Im Zusammenhang mit Infektionskrankheiten könne es jedoch zu Problemen kommen.
Eine Reihe chronischer Erkrankungen kann ebenfalls ungünstigen Einfluss auf die Immunabwehr ausüben. Hier nennt Koppelstätter neben Diabetes mellitus, Niereninsuffizienz und Lungenerkrankungen auch rheumatische Erkrankungen. Das Risiko ist bei unbehandeltem Rheuma in etwa verdoppelt. In der klinischen Praxis hat man es nicht selten mit der Kombination von Rheuma, höherem Alter, immunsupprimierender Therapie und Komorbiditäten zu tun, so Koppelstätter. Eine italienische Studie, die das Risiko für schwere Infektionen bei Patient:innen mit rheumatoider Arthritis (RA), Psoriasisarthritis (PsA) und axialer Spondyloarthritis (axSpA) über zehn Jahre untersuchte, identifizierte als wichtigen Risikofaktor ein Alter über 65. Unter den rheumatischen Erkrankungen war die RA mit einem erhöhten Infektionsrisiko assoziiert. Auch die kumulative Steroiddosis, nicht jedoch eine Biologikatherapie erhöhten das Risiko, wobei es in den ersten sechs Therapiemonaten mit einem TNF-Blocker zu vermehrten Infektionen kam, sich dieses Risiko doch bei längerer Behandlung normalisierte. Am häufigsten traten respiratorische und gastrointestinale Infekte auf. Auch opportunistische Infektionen treten in Verbindung mit rheumatischen Erkrankungen auf. Das höchste Risiko besteht bei Dermatomyositis, gefolgt vom systemischen Lupus erythematodes (SLE) und der systemischen Sklerose.1 Infektionen erhöhen das Risiko für Verschlechterungen bzw. Komplikationen entzündlich-rheumatischer Erkrankungen, so Koppelstätter, beispielsweise lösen Influenza- oder Covid-19-Erkrankungen bei einem hohen Prozentsatz von SLE-Patient:innen Flares aus.2
Bei Rheuma auch auf vollständigen Impfschutz achten
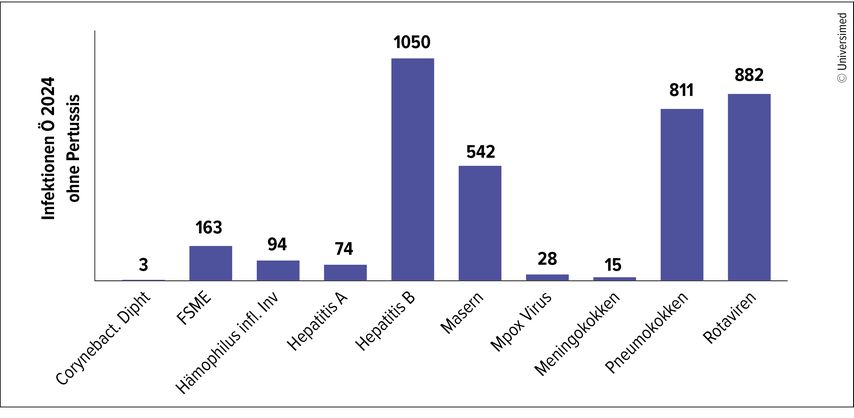
Alle diese Faktoren sprechen dafür, bei rheumatologischen Patient:innen den Impfschutz möglichst früh zu vervollständigen, um den Therapiebeginn nicht zu verzögern und um das bessere Impfansprechen vor Beginn einer immunsupprimierenden Therapie zu nutzen. Zwar ist das Impfansprechen bei Krankheitsaktivität vermindert, jedoch solle einen das nicht daran hindern, die notwendigen Impfungen auch zu verabreichen, betont Koppelstätter, die auch darauf hinweist, dass in bis zu sieben Prozent der Fälle von Vaskulitis oder SLE eine funktionelle Asplenie vorliegt, was Impfungen gegen gekapselte Bakterien nahelegt. Leider spielen impfpräventable Erkrankungen in Österreich nach wie vor eine nicht zu unterschätzende Rolle (Abb. 1). Pertussis tritt wieder auf, im Jahr 2025 wurde in Mitteleuropa ein Hepatitis-A-Ausbruch registriert und in der Inzidenz von Masern liegt Österreich mit 23,6 Fällen pro Million Einwohner im vergangenen Jahr unter den schlechteren europäischen Ländern.
Abb. 1: Jahresbericht meldepflichtiger Krankheiten 2024 Stand: 22. 04.2025 des Bundesministeriums Arbeit, Soziales, Gesundheit, Pflege und Konsumentenschutz, aus Gründen der besseren Darstellung ohne Pertussis (15470 Fälle)
Internationale Studiendaten zeigen, dass hinsichtlich der Durchimpfungsraten rheumatologischer Patient:innen Luft nach oben besteht – mit deutlichen Unterschieden zwischen den Staaten. Insgesamt am besten steht Großbritannien da, mit 50% Pneumokokken- und 80% Influenza-Geimpften unter den Rheumapatient:innen. In den meisten Ländern sind auch in dieser Risikopopulation weniger als 50% gegen Influenza geimpft. Koppelstätter betont auch die Wichtigkeit der Pneumokokken-Impfung, da es auch in Österreich immer häufiger zu invasiven Pneumokokken-Infektionen kommt. Eine Chance, hier gegenzusteuern bietet der neue 21-valente Konjugatimpfstoff (PCV 21 CAPVAXIVE®), der auch vor acht Serotypen schützt, die durch die älteren Impfstoffe nicht abgedeckt waren. Die Impfung ist in Österreich für Menschen ab 60 Jahren und für bestimmte Risikogruppen (darunter Patient:innen mit jeglicher Form der Immunsuppression) gratis. Es handelt sich um eine einmalige Impfung, zu Notwendigkeit und Sinnhaftigkeit von Auffrischungen fehlen noch die Daten. Allerdings wird bei Immunsupprimierten ein alternatives Schema empfohlen. Es wird zunächst mit dem Konjugatimpfstoff PCV 15/20 geimpft, acht Wochen später erfolgt die Impfung mit PCV 21. Bereits vorgeimpfte Patient:innen sollen nach 12 Monaten eine Impfung mit PCV 21 erhalten.
Schutz vor Herpes zoster durch rekombinanten Totimpfstoff
Ein weiteres relevantes Problem für immunsupprimierte Patient:innen stellt Herpes zoster dar. Dieser tritt auf, wenn das Immunsystem nicht in der Lage ist, die nach einer Varizellenerkrankung im Körper verbleibenden Varizella-Zoster-Viren zu kontrollieren. Die Wahrscheinlichkeit dafür steigt ab dem 50. Lebensjahr, bei Immunsuppression jedoch schon früher. Im höheren Alter kommt es auch häufiger zum Auftreten einer sehr schmerzhaften postherpetischen Neuralgie. Gegen Herpes zoster steht ein rekombinanter Totimpfstoff zur Verfügung. Geimpft wird zweimal im Abstand von zwei bis sechs Monaten. Besteht wegen eines geplanten Therapiebeginns besondere Eile, so kann dieser Abstand auf einen Monat verkürzt werden, erläutert Koppelstätter. Die derzeit vorliegenden Langzeitdaten zeigen eine Wirksamkeit von mindestens elf Jahren. Die Impfung ist ab 50 Jahren zugelassen und ab 60 Jahren kostenlos. Bei speziellen Indikationen (darunter rheumatische Erkrankungen) ist die Impfung bereits ab 18 Jahren zugelassen und kostenlos.
Das Impfansprechen ist unter Immunsuppression schlechter als bei Gesunden, Schutz vor Erkrankung und insbesondere schwerer und letaler Erkrankung besteht dennoch. So reduziert die Impfung in der immunsupprimierten Population die Covid-19-Mortalität um 61%, das Risiko für Hospitalisierung jedoch nur um 33 bis 56%. Für Influenza werden ähnliche Werte angegeben, gegen RSV ist die Schutzwirkung etwas besser. Allerdings zeigen Studiendaten, dass rund zehn Prozent der rheumatologischen Patient:innen nicht auf die Covid-Impfung ansprechen, was in der gesunden Normalbevölkerung nur zu einem Prozent der Fall ist.4 Dies liegt zum Teil, aber nicht nur an der immunsuppressiven Behandlung. Auch bei unbehandelten Rheumapatient:innen ist das Ansprechen auf die Therapie schlechter als bei Gesunden, so Koppelstätter. Die Datenlage dazu ist allerdings dünn, da Immunsupprimierte aus Impfstoffstudien ausgeschlossen werden und die Effekte der Immunsuppression auf die Impfantwort nicht generalisierbar sind. Eine Titerbestimmung ist nur begrenzt aussagekräftig, da sie lediglich Antikörper und keine gewebeständigen Immunzellen erfasst. Darüber hinaus müsse zwischen mechanistischen Antikörpern, die tatsächlich eine Schutzfunktion haben, und Surrogatantikörpern unterschieden werden. Letztere erlauben keine zuverlässigen Aussagen über die Schutzwirkung, können aber eingesetzt werden, um die Reaktion von Patient:innen auf die Impfung zu evaluieren. Dies sollte in der rheumatologischen Patient:innenpopulation auch tatsächlich gemacht werden, um die Wirkung von Impfungen überprüfen zu können.
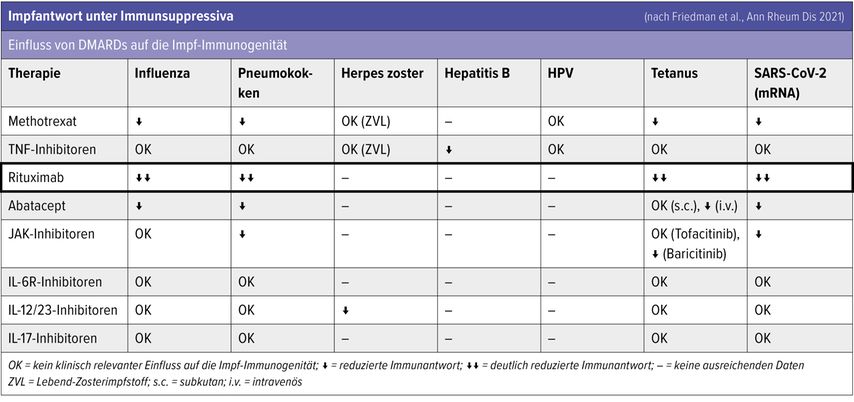
Vor diesem Hintergrund wurde bereits 2021 von Expertinnen und Experten verschiedener österreichischer Zentren die Kittelkarte „Rheuma, Immunsuppressiva, Impfungen“ erstellt, die aktuell ein Update erfährt. Die allgemeinen Empfehlungen bleiben unverändert: Der Impfstatus soll vor Beginn der Therapie evaluiert und Impfungen gemäß dem Österreichischen Impfplan umgesetzt werden. Dies darf jedoch die dringende Indikation einer Immunsuppression nicht verzögern. Totimpfstoffe sollten vorzugsweise in Phasen mit niedriger Krankheitsaktivität und geringer Immunsuppression zum Einsatz kommen. Impfungen mit Totimpfstoffen sollten zwei Wochen vor Beginn der Immunsuppression abgeschlossen sein. Auf Umgebungsprophylaxe, also die Impfung von Haushaltsmitgliedern, darf nicht verzichtet werden.
Lebendimpfstoffe sind unter Immunsuppression grundsätzlich kontraindiziert. Impfungen mit Lebendimpfstoffen sollten vier Wochen vor Beginn der Immunsuppression abgeschlossen sein. Ausnahmen erfordern sorgfältiges Management und sind von der jeweiligen Impfung und der Form der Immunsuppression abhängig. Die Kategorisierung der Immunsuppression wurde verändert. Rituximab erhält nun als Kategorie 3b einen Sonderstatus, da es B-Zell-Depletion und damit eine lang anhaltende Immunsuppression bewirkt. In Ergänzung zur Kittelkarte wird auch eine Patientenbroschüre erarbeitet.
Impfen bei Rheuma: Zeitfenster nutzen
Eine immunsuppressive Therapie erschwert das Impfen, da unter laufender Therapie ein schlechteres Ansprechen auf Totimpfstoffe zu erwarten ist und Lebendimpfstoffe kontraindiziert sein können. Dies erfordert die sorgfältige zeitliche Abstimmung von rheumatologischer Therapie und Impfplan.
Wie Impfungen rheumatologischer Patient:innen in der Praxis umgesetzt werden können und sollen, schildert Dr. Alexander Bartuschka, Rheumatologe am Institut für Spezifische Prophylaxe und Tropenmedizin an der Medizinischen Universität Wien, am Fall einer 23-jährigen Patientin mit Psoriasis, die bislang keine immunsupprimierende Therapie erhalten hat. Da seit einigen Wochen zunehmende Schmerzen an den Achillessehnen und Ellbogen angegeben wurden, bestand Verdacht auf eine beginnende Psoriasisarthritis. In dieser Situation wurde eine Therapie mit einem gegen Interleukin 23 gerichteten Biologikum geplant. Aus diesem Grund wurden die Impfungen des Impfplans überprüft, sie erwiesen sich weitgehend als dokumentiert. Mit einer wichtigen Ausnahme: Zur Masern-Mumps-Röteln-Impfung fehlt der Eintrag im Impfpass. Zwar wurde nach Angabe der Eltern MMR geimpft, ein Nachweis oder nähere Informationen waren jedoch nicht auffindbar. Daher wurde bei der Patientin eine qualitative Titerbestimmung durchgeführt, die ein negatives Resultat ergab. Daher erfolgte eine MMR-Impfung und vier Wochen später eine weitere Titerbestimmung, die allerdings nur ein grenzwertig positives Ergebnis zeigte. Daher erfolgte eine zweite MMR-Impfung, was letztlich zu einer Verzögerung der Biologikatherapie um insgesamt zwei Monate führte. In Fällen wie dem beschriebenen könne man mit einer einzelnen Impfung das Auslangen finden, wenn eine entsprechende Reaktion auf diese Impfung nachgewiesen werden kann, so Bartuschka. Die Masernimpfung rechtfertigt eine Therapieverzögerung, da es 2024 in Europa zu einem Ausbruch mit mehr als 30000 Fällen und 19 Todesopfern gekommen war. Ist eine MMR-Impfung nicht möglich, weil die Immunsuppression dringend begonnen werden muss, sollen die Patient:innen über die Möglichkeit einer Postexpositionsprophylaxe mit Immunglobulin aufgeklärt werden, die innerhalb von sechs Tagen nach einem infektiösen Masern-Erstkontakt erfolgen sollte. Bartuschka weist auch darauf hin, dass bis zu 20% der Bevölkerung im Erwachsenenalter keinen positiven Masern-Titer mehr zeigen, wenn sie als Kinder gegen Masern geimpft wurden.5 Für den Umgang mit einer derartigen Situation fehlen aktuell die Empfehlungen.
B-Zell-Depletion: Rituximab als immunologischer Sonderfall
Unter laufender Immunsuppression ist eine Lebendimpfung problematisch bis kontraindiziert. Allerdings ist gemäß den aktuellen Leitlinien des American College of Rheumatology auch bei Immunsuppression Grad III (die meisten Biologika und JAK-Inhibitoren) lediglich eine relativ kurze Therapieunterbrechung erforderlich.2 In der Regel gilt: Vor der Impfung muss ein Biologikum für ein Dosisintervall pausiert werden, JAK-Inhibitoren müssen für eine Woche abgesetzt werden. Vier Wochen nach der Impfung kann die Therapie wieder aufgenommen werden. Eine Ausnahme stellt Rituximab dar, dessen letzte Applikation mehr als sechs Monate vor einer Lebendimpfung erfolgen muss.
Wie vorzugehen ist, wenn eine immunsuppressive Therapie nicht hinausgezögert werden kann, schildert Bartuschka am Fall einer 76-jährigen Patientin mit Erstmanifestation einer Granulomatose mit Polyangiitis (GPA). Der Schub, der sich mit Hämoptysen präsentierte, wurde mit oralen Glukokortikoiden unter Kontrolle gebracht, der Beginn einer Therapie mit Rituximab stand in drei bis fünf Wochen an. Damit entstand insofern eine schwierige Situation, als eine B-Zell-depletierende Therapie nicht nur bedeutet, dass keine Lebensimpfungen verabreicht werden dürfen, sondern auch das Ansprechen auf Totimpfstoffe verhindert. Im konkreten Fall war die Patientin insgesamt zwar gut durchgeimpft, es fehlten jedoch die neuen Impfstoffe gegen Pneumokokken und Herpes zoster. Daher wurde bereits beim ersten Kontakt gegen Influenza und Covid-19 geimpft, Impfungen gegen Pneumokokken und Hepatitis B, Hämophilus influenzae, Meningokokken B und ACWY sowie Herpes zoster erfolgten innerhalb von vier Wochen, also noch vor Beginn der Therapie mit Rituximab. Lediglich die zweite Impfung gegen Herpes zoster wurde nach zwei Monaten bereits unter der immunsuppressiven Therapie verabreicht. Dies sei möglich, da die neue Zoster-Vakzine zu einer robusten T-Zell-Antwort führt. Bei den übrigen genannten Impfstoffen sei unter B-Zell-Depletion nicht mit einer adäquaten Immunantwort zu rechnen, so Bartuschka.
Quelle:
ÖGR-Jahrestagung, 27.–29.11.2025, Wien
Literatur:
1 Quartuccio L et al.: Risk of serious infection among patients receiving biologics for chronic inflammatory diseases: Usefulness of administrative data. J Adv Res 2018; 15: 87-93 2 Felten R et al.: Incidence and predictors of COVID-19 and flares in patients with rare autoimmune diseases: a systematic survey and serological study at a national reference center in France. Arthritis Res Ther 2021; 23(1): 188 3 Fragoulis GE et al.: Systematic literature review informing the 2022 EULAR recommendations for screening and prophylaxis of chronic and opportunistic infections in adults with autoimmune inflammatory rheumatic diseases. RMD Open 2022; 8(2): e002726 4 Simon D et al.: SARS-CoV-2 vaccination responses in untreated, conventionally treated and anticytokine-treated patients with immune-mediated inflammatory diseases. Ann Rheum Dis 2021; 80(10): 1312-6 5 Springer DN et al.: Seroprevalence against measles, Austria, stratified by birth years 1922 to 2024. Euro Surveill 2025; 30(16): 2400684 6 Bass AR et al.: 2022 American College of Rheumatology Guideline for Vaccinations in Patients With Rheumatic and Musculoskeletal Diseases. Arthritis Care Res (Hoboken) 2023; 75(3): 449-64
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
Osteoporose bei rheumatischen Erkrankungen
Zu den zahlreichen Komplikationen und Komorbiditäten, die mit unterschiedlichen entzündlich-rheumatischen Erkrankungen einhergehen können, zählt auch die Osteoporose. Diagnostische ...