Ungewöhnliche Erreger: was atypische Pneumonien atypisch macht
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Sogenannte atypische Pneumonien werden durch ein charakteristisches Keimspektrum verursacht und unterscheiden sich auch klinisch von „typischen“ Pneumonien. Exakte Begriffsdefinitionen fehlen allerdings. Gemeinsam ist den involvierten Keimen, dass sie nicht auf Betalaktamantibiotika reagieren. In der Therapie dieser Erkrankungen werden daher Makrolide, Tetrazykline und Chinolone eingesetzt.
Der Begriff der atypischen Pneumonie ist ebenso alt wie unscharf. Als Charakteristika einer atypischen Pneumonie werden bestimmte intrazelluläre und/oder zellwandlose Erreger ebenso diskutiert wie Erreger, die sich in der Gram-Färbung nicht anfärben lassen oder eine intrinsische β-Laktam-Resistenz aufweisen, wie Assoz. Prof. Priv.-Doz. Dr. Volker Strenger von der Klinischen Abteilung für allgemeine Pädiatrie der Medizinischen Universität Graz ausführte. Außerdem sei die Frage, was eigentlich eine „typische Pneumonie“ ausmache, ebenso ungeklärt.
In Publikationen aus dem frühen 20. Jahrhundert wurden Pneumonien als atypisch eingestuft, wenn sie nicht durch Pneumokokken oder Tuberkulosebakterien verursacht wurden. Als typische „atypische“ Erreger werden heute Mycoplasma pneumoniae, Chlamydia pneumoniae (viel seltener auch C. psittaci), Legionella pneumophila, Bordetella pertussis,Coxiella burnetii, Francisella tularensis und Pneumocystis jirovecii eingestuft. Wie in so vielen Bereichen gilt es allerdings auch im Umgang mit Pneumonien, die Verdachtsdiagnose zu hinterfragen, wenn Klinik und diagnostischer Verdacht nicht zusammenpassen, so Strenger: „Wenn es nicht ‚typisch bakteriell‘ aussieht, sind es oft Viren!“
Unklare Daten zur Häufigkeit atypischer Pneumonien
Eine Arbeit aus dem Jahr 2022 listet Charakteristika atypischer Pneumonien auf, wie zum Beispiel subakuter Beginn und protrahierter Verlauf, extrapulmonale und pulmonale Symptome, fehlender Nachweis eines Pathogens in der Sputum- und Blut-Kultur, flächige, wenig definierte Infiltrate im Lungenröntgen sowie fehlendes Ansprechen auf Betalaktamantibiotika und Aminoglykoside.1
Pneumonien mit atypischen bakteriellen Erregern sind keine Seltenheit, wobei ihre Häufigkeit in Studien sehr unterschiedlich angegeben wird.2 In manchen Arbeiten ist von mehr als 20% die Rede. Bei intensivpflichtigen Patient:innen wurden beispielsweise in einer Arbeit in 8% der Fälle Legionellen als Krankheitsursache gefunden, in einer anderen Studie waren Legionellen nur für 1% der Erkrankungen verantwortlich. Mögliche Erklärungen für die Heterogenität der Studien sind Zeitraum und Region, in denen die Studien durchgeführt wurden, lokale Epidemien, Impfstatus (weniger Pneumokokken-Erkrankungen durch Pneumokokken-Impfung), sozioökonomische Bedingungen sowie die Geografie. Auch die Covid-19-Pandemie nahm Einfluss. Nicht zuletzt wies Strenger auch auf Probleme mit dem Erregernachweis hin, wobei die PCR gegenüber der Serologie als klar verlässlicher zu werten ist.
Eine komplexe Modellierung aus dem Jahr 2021 auf Basis von 344 Millionen Infektionen des unteren Respirationstraktes weltweit („all available data“) weist für Pneumonien aufgrund von Mycoplasma spp. eine Inzidenz von 25,3 Millionen Fällen (7,35%) aus.3 Wie sehr die Nachweismethode das Ergebnis beeinflusst, zeigen auch Daten zu Chlamydia pneumoniae. Während der Anteil von Chlamydien-Infektionen an Pneumonien bei Kindern mittels Serologie mit 9% ermittelt wurde,4 lag er in späteren Untersuchungen auf PCR-Basis deutlich unter 1%.5
Die große Bandbreite der atypischen Pneumonie-Erreger
Chlamydia pneumoniae verursacht in der Mehrzahl der Fälle asymptomatische bis milde Verläufe, schwere Erkrankungen sind mit weniger als 1% der Fälle von ambulant erworbener Pneumonie (CAP) sehr selten. Für die Erregerbestimmung eignet sich ausschließlich die PCR, da die Serologie keine verlässlichen Resultate liefert.
Bei Risikopersonen wie bei Kindern mit Grunderkrankung dürfte die Inzidenz etwas höher sein. Auch Ausbrüche in beengten Settings, wie zum Beispiel Gefängnissen, wurden beschrieben. In seltenen Fällen kommt es zu extrapulmonalen Manifestationen wie Meningoenzephalitis, Guillain-Barré-Syndrom, Myokarditis oder Endokarditis.
Eine besondere Gruppe an atypischen Pneumonien stellen Zoonosen dar, die nur selten Menschen befallen. So verursacht Chlamydia psittaci die Psittakose (Ornithose), Coxiella burnetii ist der Erreger des Q-Fiebers, Francisella tularensis ruft die Tularämie (Hasenpest) hervor. Alle diese Erkrankungen können schwer verlaufen. Eine Pneumonie ist dabei nicht obligat und tritt allenfalls im Rahmen einer systemischen Erkrankung auf. Bei Verdacht auf eine dieser Erkrankungen ist die Anamnese von hoher Bedeutung, da sie die Wahrscheinlichkeit eines Erregerkontakts offenbart.
Ein atypischer Erreger, der zunehmend Probleme bereitet, ist Legionella pneumophila. Derzeit verursachen Legionellen bis zu 8% aller CAP. Der Erreger kommt in Wasserleitungen, Klimaanlagen etc. vor, die Infektion erfolgt durch Aerosole. Risikopersonen sind vor allem Männer über 65, eine Reihe von Grundkrankheiten wie Diabetes mellitus oder chronische Lungenerkrankungen erhöhen das Risiko.
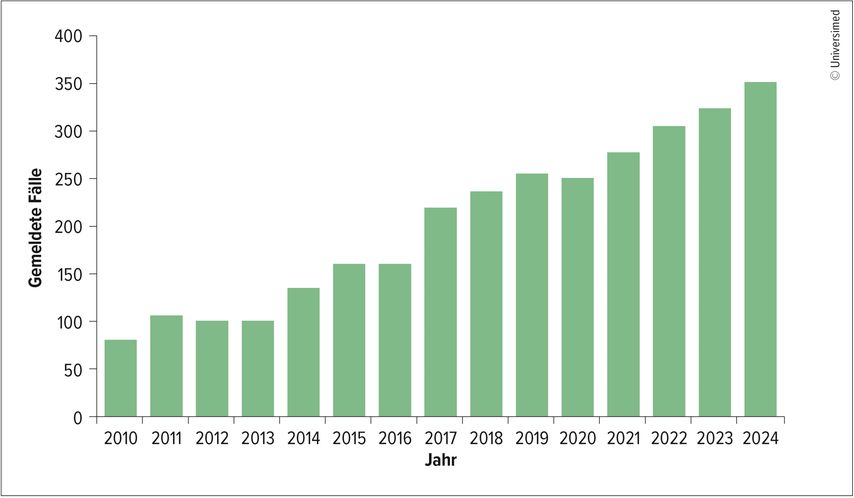
Legionellen können sehr schwere Erkrankungen verursachen.6 Sie äußern sich mit Fieber, Dyspnoe, Husten, Diarrhö und u.U. akutem Nierenversagen. Es besteht das Risiko für akutes respiratorisches Versagen und septischen Schock, eine extrakorporale Membranoxygenierung (ECMO) kann erforderlich werden. Die Zahl der gemeldeten Fälle steigt beständig (Abb.1). Dies ist vermutlich auf die zunehmend größer werdende Zahl an Personen mit relevanten Risikofaktoren zurückzuführen, so Strenger.
Mycoplasma pneumoniae: häufig und nicht immer harmlos
Der zahlenmäßig relevanteste Erreger atypischer Pneumonien ist Mycoplasma pneumoniae. Die Infektion fällt klinisch durch Husten, aber auch eine Reihe extrapulmonaler Symptome wie Abgeschlagenheit, Erbrechen, Kopfschmerzen, hohes Fieber etc. auf.
Strenger wies in seinem Vortrag auch auf eine Arbeit hin, die bei Schulkindern mit Mycoplasma-Pneumonien zu einem hohen Prozentsatz Konsolidierungen und Atelektasen im Lungenröntgen fand. Auch Hautmanifestationen kommen relativ häufig vor. Mykoplasmen-assoziierte Haut- und Schleimhautveränderungen („Mycoplasma pneumoniae-induced rash and mucositis“; MIRM) äußern sich in okulären, oralen und urogenitalen Schleimhautläsionen und können einem Stevens-Johnson-Syndrom ähnlich sehen. Auch ZNS-Manifestationen sind möglich.7 Sie können sich als Enzephalitis, Cerebellitis, Polyradikulitis, Hirnnervenlähmung, aseptische Meningitis/Meningoenzephalitis, akute disseminierte Enzephalomyelitis (ADEM), Neuritis nervi optici oder auch als Psychose äußern. Diese Komplikationen sind schwerwiegend, aber zum Glück selten, wie Strenger erläuterte.
Der Erregernachweis ist schwierig. Die Serologie ist unzuverlässig, aber auch die PCR liefert keine sichere Diagnose. Eine niederländische Studie fand bei asymptomatischen Kontrollen einen höheren Anteil positiver PCR-Befunde als bei symptomatischen Patient:innen. Die Autor:innen schließen aus diesen Daten, dass eine Besiedelung der Atemwege mit Mycoplasma pneumoniae auch bei asymptomatischen Personen häufig vorkommt und die PCR daher keine verlässliche Methode ist, um eine Mycoplasma-pneumoniae-Pneumonie zu identifizieren.8
Epidemiologische Daten zeigen, dass Kinder und Jugendliche häufiger von Mycoplasma-pneumoniae-Pneumonien betroffen sind als ältere Erwachsene.5 Die Erkrankung weist sowohl saisonale Häufungen als auch eine typische Periodizität mit Inzidenzspitzen alle drei bis fünf Jahre auf. Daten aus Großbritannien sprechen allerdings für ein Abflauen dieses Musters mit immer kleiner werdenden Spitzen seit der Jahrtausendwende. Rezente, weltweite Daten lassen jedoch mit Verzögerung einen neuerlichen Anstieg nach der Pandemie erkennen.9 Strenger hielt dazu fest, dass in den Jahren ohne relevantes Infektionsgeschehen der Anteil der Suszeptiblen in der Gesamtbevölkerung deutlich angestiegen ist. Dieser Trend wurde jedoch durch die relativ zahlreichen Erkrankungen des Jahres 2024 gebrochen, sodass man nun mit mehreren relativ ruhigen Jahren rechnen könne.
Therapieoptionen
Für die Therapie atypischer Pneumo-nien bestehen unterschiedliche Empfehlungen. Infrage kommende Substanzgruppen sind Makrolide, Tetrazykline und Chinolone, zu denen allerdings widersprüchliche Daten aus randomisierten, kontrollierten Studien vorliegen und bei denen oft kein eindeutiger Benefit nachgewiesen werden konnte. Die Empfehlungen in den Guidelines sind abhängig vom Schweregrad sowie von den Begleit- und Grunderkrankungen. Bei vergleichsweise harmlosen Infektionen wie jenen mit Mycoplasma pneumoniae verlaufen Pneumonien oft selbstlimitierend, andere, wie zum Beispiel schwere Legionellose, müssen intensiv behandelt werden. Strenger riet jedenfalls, vor Beginn der Behandlung auch eine virale Genese zu erwägen: „Makrolide sind kein Hustensaft.“
Quelle:
„Mykoplasmen, Chlamydien und andere atypische respiratorische Erreger, es gibt sie doch!“, Vortrag von Assoz.-Prof. Priv.-Doz. Dr. Volker Strenger, Graz, am 20. März 2025 im Rahmen des ÖIK 2025, Saalfelden
Literatur:
1 Garin N et al.: Microorganisms 2022; 10(12): 2326 2 Cavalazzi R, Ramirez JA: Semin Respir Crit Care Med 2024; 45: 143-57 3 GBD 2021 Lower Respiratory Infections and Antimicrobial Resistance Collaborators: Lancet Infect Dis 2024; 24(9): 974-1002 4 Michelow IC et al.: Pediatrics 2004; 113(4): 701-7 5 Jain S et al.: N Engl J Med 2015; 372(22): 2167-8 6 Rello J et al.: Ann Intensive Care 2024; 14(1): 51 7 Bae JW et al.: Case Rep Neurol 2011; 3(2): 109-12 8 Spuesens EBM et al.: PLoS Med 2013; 10(5): e1001444 9 Meyer Sauteur PM et al.: Lancet Microbe 2025; 101191
Das könnte Sie auch interessieren:
Ageismus und Wege dagegen – Frauen mit HIV in der ärztlichen Praxis
Seit 2021 ruft die WHO unter dem Hashtag #AWorld4AllAges zum Kampf gegen Ageismus weltweit auf und fordert mehr Forschung und Aufklärung zu diesem Thema.1 Gerade ältere Frauen*, die mit ...
Eradikation bei EHEC-Dauerausscheidung mit Antibiotika
Mit dem Akronym EHEC (enterohämorrhagische Escherichia coli) werden Shigatoxin (Stx) produzierende, humanpathogene E.-coli-Stämme (STEC) bezeichnet. Neben zytotoxischen, mit einem ...
Malaria: Diagnostik und Behandlung nach aktuellen Leitlinien
Gleich mehrere Leitlinien zum Thema Malaria wurden im vergangenen Jahr aktualisiert. Dies betrifft die WHO-Guidelines, die deutsche S1-Leitlinie und die Malaria Treatment Recommendations ...