Neues zur GVHD-Prophylaxe und Risikobewertung bei Myelofibrose
Bericht:
Dr. Therese Schwender
Die Prophylaxe der Graft-versus-Host-Krankheit (GVHD) bleibt eine zentrale Herausforderung nach allogener Stammzelltransplantation. Auf dem diesjährigen EBMT-Kongress wurden dazu neue Entwicklungen besprochen – von optimierten Einsatzplänen bewährter Medikamente über innovative Wirkstoffe bis hin zu komplexen Graft-Manipulationen. Ausserdem wurde ein KI-basiertes Tool vorgestellt, das die Risikoeinschätzung bei Myelofibrose-Erkrankten vor Transplantation verbessern soll.
Eine der Sitzungen am diesjährigen Kongress der European Society for Blood and Marrow Transplantation (EBMT) beschäftigte sich mit der Prophylaxe der Graft-versus-Host-Krankheit (GVHD). Dr. med. Benjamin Watkins (New Orleans/USA) wies in seiner Einleitung darauf hin, dass es aktuell sehr viele laufende Studien zu diesem Thema gibt. Allerdings sei zu beachten, dass die Untersuchungen auch sehr heterogen seien in Bezug auf Faktoren wie die zugrunde liegende Erkrankung, die Intensität des Therapieregimes oder auch das Alter der Spendenden. «Es gibt auch keinen echten Konsensus dazu, welchen Endpunkt man verwenden soll», führte er weiter an. Zudem seien zusammengesetzte Endpunkte wie GRFS («GVHD-free, relapse-free survival») nicht einheitlich definiert.
Wie Watkins weiter erklärte, hätten sich mittlerweile Substanzen wie Abatacept (Aba), Cyclophosphamid (Cy) und Antithymozytenglobulin (ATG) gegenüber dem historischen Standard Calcineurin-Inhibitoren (CNI) und Methotrexat (MTX) als überlegen erwiesen und würden vielerorts standardmässig eingesetzt. «Die zusätzliche Immunsuppression hat jedoch ihren Preis, geht sie doch mit Risiken wie einer verzögerten Immunrekonstitution, Infektionen und einer erhöhten Rezidivrate einher», sagte er. Deshalb bestehe weiterhin Bedarf an neuen Ansätzen zur GVHD-Prophylaxe.
Neue Ansätze mit bewährten Substanzen
Ein möglicher neuer Ansatz ist die Modifikation beim Einsatz bereits bewährter Substanzen. Watkins verwies in diesem Zusammenhang auf die aktuell laufende Phase-II-Studie OPTIMIZE.1 Sie untersucht niedrigere Dosierungen von Posttransplantations-Cyclophosphamid (PTCy, 25mg/kg bzw. 37,5mg/kg an Tag 3 und 4 anstelle von 50mg/kg). Dies soll zur Reduktion der Rate an Infektionen bei erhaltener GVHD-Prophylaxe bei Personen mit hämatologischen Neoplasien nach einer Blutstammzelltransplantation (PBSC) von einem MMUD («mismatched unrelated donor») beitragen. Weitere laufende Studien wie ABA3 testen verlängerte Dosierungsschemata von Aba/Tacrolimus/MTX (bis Tag 150) bei pädiatrischen und erwachsenen Personen, besonders in Bezug auf die Prophylaxe einer chronischen GVHD (cGVHD).2
Ebenfalls getestet werden CNI-freie Optionen. So untersuchte eine Studie bei Erwachsenen mit hämatologischen Neoplasien und einem HLA-gematchten Spender eine CD34-selektionierte PBSC sowie eine PTCy-Prophylaxe nach Knochenmarktransplantat im Vergleich zu Tacrolimus (Tac) und MTX nach Knochenmarktransplantat (Kontrolle).3 Die CD34-Selektion führte zu signifikant geringeren Raten von akuten GVHD (aGVHD) und cGVHD, jedoch gleichzeitig zu einer höheren Mortalität im Vergleich zu PTCy und Tac/MTX. Grund dafür war eine höhere Rate an Infektionen und Rezidiven. «Dieser Ansatz scheint also insgesamt zu einer zu starken Immunsuppression geführt zu haben», kommentierte Watkins die Resultate.
Eine weitere Verbesserungsmöglichkeit der GVHD-Prophylaxe ist der kombinierte Einsatz bewährter Medikamente. Der Referent erwähnte in diesem Zusammenhang die Phase Ib/II-Studie CAST, die eine Kombination aus PTCy, Aba und einer zeitlich befristeten Tac-Gabe im Setting einer haploidentischen PBSC untersuchte.4 «Mit 6% einer aGVHD von Grad 3–4 und 16% einer moderaten bis schweren cGVHD sowie einem 1-Jahres-GRFS von 66% zeigte die Studie wirklich ermutigende Resultate», fand Watkins.
Studie zu neuen Wirkstoffen
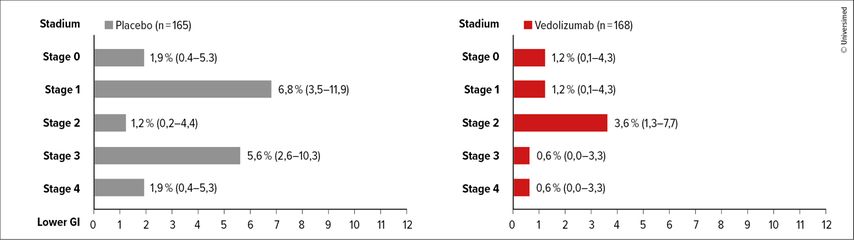
Im Anschluss präsentierte er einige Studien, in denen neue Substanzen untersucht wurden. Den Anfang machte dabei Vedolizumab, ein immunmodulatorischer humanisierter monoklonaler Antikörper, der an das α4β7-Integrin auf pathogenen Homing-Lymphozyten im Darm bindet und selektiv die Adhäsion dieser Zellen an das mukosale Addressin-Zelladhäsionsmolekül-1 (MAdCAM-1) hemmt. «Vedolizumab verhindert, dass α4β7-Integrin-exprimierende T-Zellen ins Darmgewebe einwandern und eine GVHD auslösen», erläuterte Watkins. In einer randomisierten Phase-III-Studie wurde Vedolizumab bzw. Placebo (Tage –1,+13,+41,+69,+97,+125 und+153) in Kombination mit einer Standardprophylaxe (CNI plus MTX/Mycophenolat-Mofetil) untersucht.5 «Wichtig ist zu betonen, dass es hier aufgrund des Wirkmechanismus der Substanz lediglich um die Reduktion der gastrointestinalen GVHD ging», sagte er. In der Gruppe mit Vedolizumab im Vergleich zu Placebo konnten denn auch eine geringere Rate einer aGVHD des unteren Gastrointestinaltrakts («lower GI») sowie ein signifikant längeres «lower-GI aGVHD»-freies Überleben gezeigt werden (Abb.1).
Abb. 1: Raten einer akuten GVHD im unteren Gastrointestinaltrakt im Placebo- sowie im Vedolizumab-haltigen Studienarm nach maximalem klinischem Stadium5
Neben Vedolizumab liegen auch zu Januskinase-Inhibitoren ermutigende Studienergebnisse auf. Insbesondere Ruxolitinib zeigte in Kombination mit Tac/MTX bei älteren Erwachsenen mit gematchten PBSC-Spendern gute Resultate (aGVHD: Grad 3–4 5%; 2-Jahres-cGVHD moderat bis schwer: 16%; 2-Jahres-GRFS 62%).6 «Dies hat zum Start der Phase-III-Studie PROGRESS geführt, in welcher nun Ruxolitinib, Tacrolimus und Methotrexat im Vergleich zu Postransplantations-Cyclophophamid, Tacrolimus und Mycophenolat-Mofetil untersucht werden», so der Referent.
Zusätzlich wird intensiv an Methoden zur Graft-Manipulation wie der αβ-T-Zell-Depletion geforscht. Dieses Verfahren soll gezielt die GVHD-verursachenden T-Zellen eliminieren, gleichzeitig aber die immunologischen Schutzfunktionen erhalten.7 In pädiatrischen Studien führte eine αβ-T-Zell/CD19-Depletion zu bemerkenswert niedrigen GVHD-Raten bei einer hohen Rate des langfristigen Überlebens, jedoch mit verzögerter Immunrekonstitution.8
Wie Watkins abschliessend betonte, gibt es derzeit keinen allgemein anerkannten Standard für die GVHD-Prävention, mit Ausnahme von PTCy bei der haploidentischen Transplantation. PTCy, ATG und Abatacept hätten sich in Studien gegenüber CNI/MTX als überlegen erwiesen, weshalb Letzteres nicht mehr als Kontrollarm bei Studien eingesetzt werden sollte. «Von den neuen Ansätzen haben sich alle in einem gewissen Mass als vielversprechend erwiesen, aber keiner als klar überlegen. Jedes Regime hat seine Risiken und seinen Nutzen. Zu wissen, welches die beste Option ist, wird in Zukunft für uns immer schwieriger werden, ausser wir beginnen damit, direkte Vergleichsstudien durchzuführen», sagte er.
Transplantationsrisiko bei Myelofibrose berechnen
Um die Ermittlung des Transplantationsrisikos bei Personen mit Myelofibrose (MF) ging es im Vortrag des Hämatologen und Experten für maschinelles Lernen (ML) Dr. med. Adrián Mosquera Orgueira (Santiago de Compostela/Spanien). «Die Entscheidung, bei einer Person mit Myelofibrose eine Transplantation durchzuführen, ist häufig sehr komplex und nur etwa 10% werden tatsächlich transplantiert», sagte er. «Da es keine Instrumente zur Risikobewertung gibt, können wir uns bei dieser schwierigen Entscheidung in der Regel nur auf unsere persönliche Erfahrung und nicht auf genau definierte Kriterien verlassen.»
Zusammen mit Dr. med. Juan Carlos Hernández-Boluda (Valencia/Spanien), Erstautor der praktisch zeitgleich erschienenen Publikation in der Zeitschrift Blood, und einem Team an Forschenden versuchte Mosquera Orgueira daher, die Risikobewertung für MF-Betroffene mithilfe eines ML-Tools zu verbessern.9 Dazu identifizierten sie 5183 erwachsene MF-Betroffene aus 288 EBMT-registrierten Zentren, die sich zwischen 2005 und 2020 einer ersten allogenen Stammzelltransplantation unterzogen hatten. Von diesen Datensätzen wurden 3887 zum Trainieren des Algorithmus verwendet, während 1296 zur Bewertung und Validierung des neuen Modells herangezogen wurden. Das auf «random survival forests» (RSF) basierende Modell des Forscherteams lieferte schliesslich bessere Resultate als verschiedene Vergleichsmethoden (u.a. das CIBMTR-Modell). So ergab es einerseits besser reproduzierbare Ergebnisse, andererseits übertraf es die Standardmodelle in Bezug auf die Genauigkeit. Es identifizierte 25% der MF-Betroffenen als Hochrisikopatienten (vs. 10,1% bei einem Cox-basierten Modell und 8,2% mit dem CIBMTR-Modell), die eine 40%ige Wahrscheinlichkeit aufwiesen, innerhalb eines Jahres nach der Transplantation zu sterben.
Frei zugänglicher Risikorechner
Das Forschungsteam übersetzte sein RSF-Modell mittlerweile in einen frei zugänglichen webbasierten Rechner ( https://gemfin.click/ebmt/ ). Das Tool prognostiziert das Gesamtüberleben von MF-Erkrankten nach der Transplantation auf der Grundlage von 10 Parametern (Alter, Leistungsstatus, Komorbiditätsindex, hämatologische Parameter, Spendertyp, Konditionierungsintensität und Art der GVHD-Prophylaxe).
Der Referent wies aber darauf hin, dass die Studie einige Einschränkungen aufweist, vor allem die Tatsache, dass sie sich auf ein Patientenregister stützt, in dem Daten für einige Variablen fehlten, darunter der Grad der Knochenmarkfibrose und das Vorhandensein zusätzlicher somatischer Mutationen zum Zeitpunkt der Transplantation. Die Forschenden hoffen, in Zukunft die in die Anwendung eingegebenen realen Daten sammeln und weitere spezifische Krankheitsfaktoren einbeziehen zu können, um die Anwendbarkeit des Modells zu verbessern. «Zusammenfassend lässt sich sagen, dass unser Tool über drei wichtige Voraussetzungen für die effektive Integration künstlicher Intelligenz in die Medizin verfügt», so Mosquera Orgueira. «Erstens ist es breit anwendbar, d.h., die Variablen, aus denen das Modell besteht, sind unabhängig vom Gesundheitssystem leicht zu ermitteln. Zweitens ist es im Internet frei verfügbar und damit leicht zugänglich. Und drittens ist es klinisch verwertbar. Es unterstützt multidisziplinäre Teams bei der Entscheidung, ob eine Transplantation durchgeführt oder andere medizinische Optionen geprüft werden sollen, und hilft sowohl Behandelnden als auch Betroffenen, fundiertere Entscheidungen zu treffen.»
Quelle:
51st Annual Meeting of the EBMT, 30. März bis 2. April 2025, Florenz/Italien und online
Literatur:
1 HLA-mismatched unrelated donor peripheral blood stem cell transplantation with reduced dose post transplantation cyclophosphamide GvHD prophylaxis (OPTIMIZE). https://clinicaltrials.gov/study/NCT06001385 2 Extended vs short-term abatacept dosing for graft versus host disease prophylaxis (ABA3). https://clinicaltrials.gov/study/NCT04380740 3 Luznik L et al.: Randomized phase III BMT CTN trial of calcineurin inhibitor-free chronic graft-versus-host disease interventions in myeloablative hematopoietic cell transplantation for hematologic malignancies. J Clin Oncol 2022; 40(4): 356-68 4 Al-Homsi AS et al.: PTCy, abatacept, and a short course of tacrolimus for GVHD prevention after haploidentical transplantation. Blood Adv 2023; 7(14): 3604-11 5 Chen YB et al.: Vedolizumab for the prevention of intestinal acute GVHD after allogeneic hematopoietic stem cell transplantation: a randomized phase 3 trial. Nat Med 2024; 30(8): 2277-87 6 DeFilipp Z et al.: Low rates of chronic graft-versus-host disease with ruxolitinib maintenance following allogeneic HCT. Blood 2025; doi: 10.1182/blood.2024028005. Epub ahead of print 7 Pistoia V et al.: Human γδ t-cells: from surface receptors to the therapy of high-risk leukemias. Front Immunol 2018; 9: 984 8 Merli P et al.: TCRαβ/CD19 cell-depleted HLA-haploidentical transplantation to treat pediatric acute leukemia: updated final analysis. Blood 2024; 143(3): 279-89 9 Hernandez-Boluda JC et al.: Use of machine learning techniques to predict poor survival after hematopoietic cell transplantation for myelofibrosis. Blood 2025; doi: 10.1182/blood.2024027287
Das könnte Sie auch interessieren:
Die Rolle der Endothelzellen
Tim Dreier schloss sein Studium der Humanmedizin 2023 in Wien ab. Im Doktoratsstudium bei Ap.Prof. Priv.-Doz. Dr. Johanna Gebhart, PhD, forscht er an Endothelschäden bei leichten bis ...
Single-Port da Vinci – der nächste Entwicklungsschritt?
In den letzten zwei Jahrzehnten ist das Interesse an minimalinvasiven Techniken in der Urologie stark gestiegen und in vielen Bereichen „State of the Art“ geworden. Die neueste ...
Chancen und Grenzen der Immuntherapie bei Krebs
Immuntherapien eröffnen neue Wege in der Behandlung von hämatologischen sowie soliden Tumoren und geben Hoffnung auf ein längeres Überleben bis hin zur möglichen Heilung der Betroffenen ...