Was ist aus reproduktionsmedizinischer Sicht zu beachten?
Autorin:
Priv.-Doz. Dr. Monika Wölfler
Leitung Universitäre Kompetenzeinheit Endometriose
Universitätsklinik für Frauenheilkunde und Geburtshilfe
Universitätsklinikum Graz
E-Mail: monika.woelfler@medunigraz.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Kinderwunsch bei Uterus myomatosus stellt mitunter eine besondere Herausforderung dar. Die strukturierte sonografische Diagnostik des Uterus und der Ovarien und die standardisierte Sterilitätsdiagnostik bilden die Basis für zielgerichtete Beratung und Behandlungsplanung.
Bis zu 70% aller Frauen entwickeln zwischen Menarche und Menopause mit altersabhängig steigender Wahrscheinlichkeit einen Uterus myomatosus. Myome sind die häufigste Ursache für Hypermenorrhö und damit auch einer der häufigsten Gründe für eine Hysterektomie nach abgeschlossener Familienplanung.1 Myome können die pelvine Anatomie stark verändern und beeinträchtigen. Fertilitätsstörungen durch submuköse und auch intramurale Myome können durch Veränderung der physiologischen myometrialen Kontraktilität, Störung des endometrialen Milieus mit proinflammatorischen Veränderungen und nachteiligen Effekten auf die Implantation begründet werden. In einer rezenten Übersichtsarbeit konnte gezeigt werden, dass bei Uterus myomatosus und Kinderwunsch die Wahrscheinlichkeit für Subfertilität 3,5-fach erhöht ist und das Intervall bis zum Eintreten der gewünschten Schwangerschaft sich fast verdoppelt („odds ratio uterine fibroids and subfertility“: 3,54 [95% CI: 1,55–8,11], „odds ratio time to pregnancy in presence of fibroids“ 1,93 [95% CI: 0,89–4,18]).2 Vor diesem Hintergrund ist eine gründliche Evaluation der Symptomatik und reproduktiven Gesamtsituation bei Uterus myomatosus zur Beratung hilfesuchender Paare unbedingt erforderlich.
Diagnostik
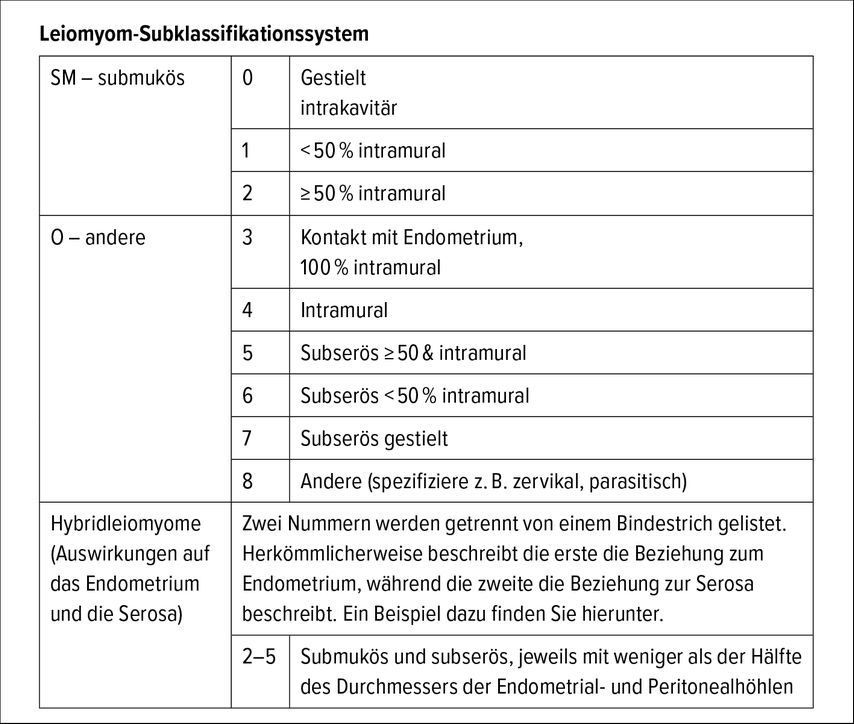
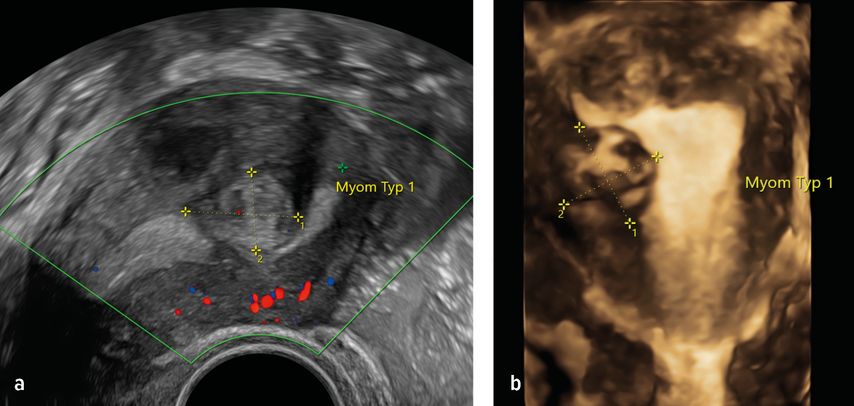
Mittels transvaginaler Sonografie können Myome lokalisiert und beurteilt werden und entsprechend der FIGO-Klassifikation die exakte Lage, die Größe und der Bezug zum Cavum uteri genau beschrieben werden (siehe Abb. 1).3 Eine besondere Bedeutung für Störungen der Implantation und Plazentation im weiteren Verlauf und damit gegebenenfalls auch für erhöhtes Abortrisiko oder Plazentationsstörungen kommt den submukösen Myomen (FIGO Typ 0, 1, 2) zu. Mittels 2D-Sonografie und unter Hinzunahme des Color-Dopplers können die Myome präzise dargestellt werden, die ergänzende 3D-Sonografie kann die Lage der Myome oft besonders gut verdeutlichen und ist für die Planung des Eingriffes hilfreich (Abb. 2).
Abb. 2: Submuköse Myome in der Sonografie – Typ-1-Myome in der 2D-Sonografie (a) und in der 3D-Darstellung (b). Die Einschätzung der Lage des submukösen Myoms und die Zuordnung nach der FIGO-Klassifikation sind mithilfe der 3D-Sonografie präzise möglich
An das Cavum uteri heranreichende intramurale Myome (FIGO Typ 3, Typ 3–4 oder 3–5) können aufgrund ihres Bezuges zum Cavum uteri ebenfalls für die Plazentation und das Einsprossen von Gefäßen im Laufe der Schwangerschaft von Nachteil sein.
Ergänzend zur Evaluation der Myome sind eine vollständige Sterilitätsdiagnostik mit Hormonstatus, Evaluation der ovariellen Reserve und möglicher anderer uteriner, tubarer oder ovarieller Pathologien sowie die Abklärung des Partners erforderlich.
Behandlungsplanung und Therapieoptionen
In Zusammenschau aller erhobenen Befunde wird der Behandlungsplan erstellt. Je nachdem, ob die Lage der Myome fertilitätseinschränkend einzuschätzen ist und/oder klinische Symptome wie Hypermenorrhö, Dysmenorrhö, Dyspareunie, Eisenmangel oder eine Eisenmangelanämie vorliegen, müssen alle therapeutischen Optionen überlegt werden. Medikamentöse Therapieoptionen zur symptomatischen Behandlung (z.B. therapeutische Amenorrhö durch Gestagene oder Kombinationspräparate) sind bei Kinderwunsch nicht zielführend. Sofern weitere Ursachen für die Subfertilität („male factor“, Tubenfaktor) festgestellt werden und/oder sich die Frau bereits im fortgeschrittenen reproduktiven Alter befindet oder eine reduzierte ovarielle Reserve festgestellt wurde, kann eine ovarielle Stimulation zur Gewinnung von Eizellen (oder Embryonen) vor der Durchführung der operativen Behandlung sinnvoll sein. Nach einer Myomenukleation ist eine sichere Kontrazeption für mehrere Monate erforderlich und die Realisierung des Kinderwunsches ist erst zeitverzögert möglich.
Submuköse Myome
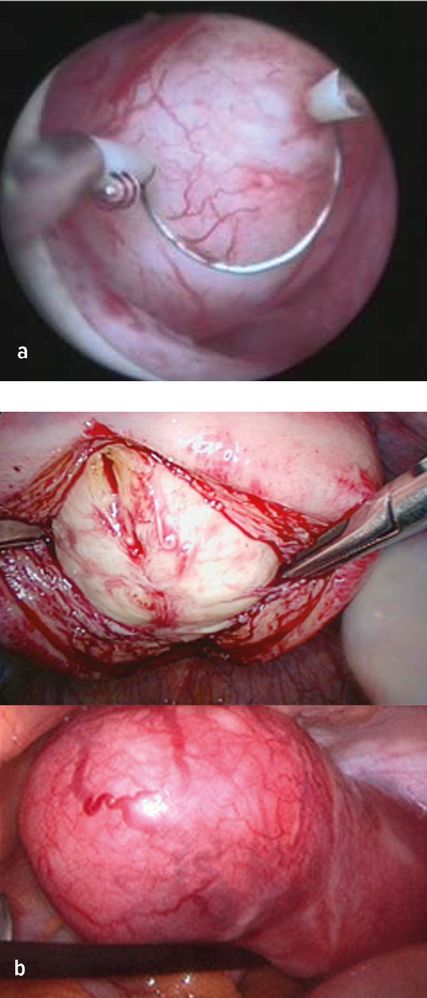
Abb. 3: Operativer Situs – hysteroskopisches Bild eines FIGO-Typ-1-Myoms vor der Abtragung (a) und laparoskopische Bilder von intramuralen und subserösen Myomen (b)
Bei submukösen Myomen ist eine hysteroskopische Myomabtragung (Abb. 3) empfohlen, insbesondere Typ-0- und Typ-1-Myome sind für diese Eingriffe gut zugänglich. Bei Typ-2-Myomen mit mehr als 50% intramuralem Myomanteil kann es je nach Größe und Lokalisation in Einzelfällen erforderlich sein, das Myom in zwei Sitzungen abzutragen: Im Rahmen der ersten Hysteroskopie wird das Myom bis knapp unter das Niveau des Cavum uteri abgetragen. Durch die Kontraktilität des Myometriums kommt der verbliebene Teil des Myoms im Verlauf an die Oberfläche des Cavum uteri und kann im Rahmen einer neuerlichen hysteroskopischen Myomresektion dann vollständig abgetragen werden. Alternativ stehen auch transzervikale Radiofrequenzablationstechniken zur Verfügung, die zur Nekrose und Vernarbung des Myoms führen.
Intramurale und Hybridmyome
Entsprechend der FIGO-Klassifikation werden Myome mit Bezug sowohl zum Endometrium als auch zur Serosa als Hybridmyome bezeichnet (z.B. Typ-2–5-Myom, wenn der submuköse Anteil und auch der subseröse Anteil jeweils weniger als 50% betragen). Je nach Lokalisation, Größe und Symptomatik stehen sie einer Schwangerschaft im Wege und sollen präkonzeptionell behandelt werden. Folgende Techniken stehen zur Verfügung
-
Myomenukleation per Laparoskopie, in seltenen Fällen per Laparotomie
-
Myomembolisation
-
Radiofrequenzablation per Laparoskopie (sofern verfügbar)
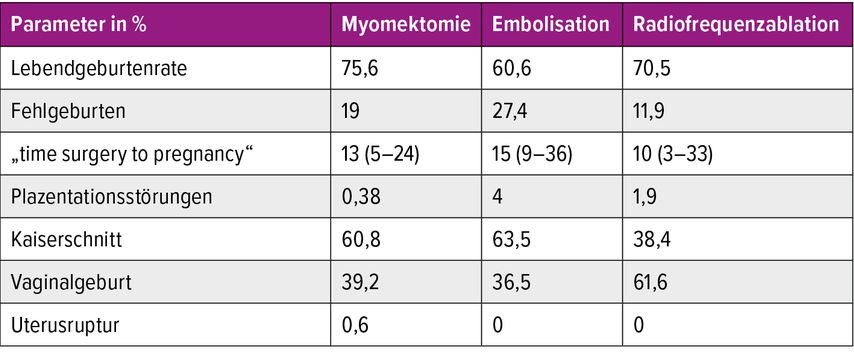
Subseröse und gestielte Myome spielen aufgrund des fehlenden Bezugs zum Cavum uteri für die Implantation und Plazentation kaum eine Rolle, eine Entfernung kann aber aufgrund von Verdrängungssymptomatik der Nachbarorgane oder möglichem Geburtshindernis sinnvoll sein. In einer rezenten Übersichtsarbeit wurden die einzelnen Behandlungsoptionen verglichen und es zeigte sich, dass die Myomenukleation per Laparoskopie weiterhin die Standard-Behandlungsoption sein sollte: Die höchste Lebendgeburtenrate, die geringste Fehlgeburtenrate und die geringste Rate an Plazentationsstörungen waren in der Gruppe der Myomenukleationen festgestellt worden – siehe auch Tabelle 1.4
Tab. 1: Übersicht über fertilitätserhaltende Therapien bei Uterus myomatosus im Vergleich. Adaptiert nach Khaw SC et al.4
Bezüglich geburtshilflicher Risiken während einer Schwangerschaft nach Myomenukleation hat eine weitere Arbeit aufschlussreiche Informationen geliefert: Das Risiko für eine Uterusruptur ist dann am geringsten, wenn der Verschluss des Myometriums und der Serosa mehrschichtig erfolgte und ein Intervall bis zur Schwangerschaft von mindestens 6 Monaten eingehalten wurde. Im Falle von Cavumeröffnung, Hämatomen oder Abszessen im Myometrium nach der Myomenukleation war das Risiko erhöht.5 Die Autoren schlussfolgern und empfehlen, dass im Operationsbericht diesbezüglich detailliert Auskunft gegeben und zumindest ein Hinweis für den Geburtsmodus festgehalten werden soll.
Fazit
Eine frühzeitige und genaue sonografische Evaluation bei Uterus myomatosus und (prospektivem) Kinderwunsch lässt für die Beratung und Therapieplanung Spielraum und ist die Basis für ein gutes reproduktives Outcome. Obwohl mittlerweile mehrere Therapieoptionen zur Verfügung stehen, ist die laparoskopische Myomenukleation weiterhin die Standard-Behandlung mit den besten Ergebnissen, für submuköse Myome stehen hysteroskopische Operationstechniken zur Verfügung.
Literatur:
1 American College of Obstetricians and Gynecologists’ Committee on Practice Bulletins: Management of Symptomatic Uterine Leiomyomas: ACOG Practice Bulletin, Number 228. Obstet Gynecol 2021; 137(6): e100-15 2 Somigliana E et al.: Fibroids and natural fertility: a systematic review and meta-analysis. Reprod Biomed Online 2021; 43(1): 100-10 3 Munro G et al.: The FIGO classification of causes of abnormal uterine bleeding in the reproductive years. Fertil Steril 2011; 95(7): 2204-8, 2208 4 Khaw SC et al.: Systematic review of pregnancy outcomes after fertility-preserving treatment of uterine fibroids. Reprod Biomed Online 2020; 40(3): 429-44 5 Cezar C et al.: Laparoscopy or laparotomy as the way of entrance in myoma enucleation. Arch Gynecol Obstet 2017; 296(4): 709-20
Das könnte Sie auch interessieren:
Die FARBEN-Studie
Die Vereinbarkeit von Familie und Beruf sowie flexible Arbeitszeiten sind für junge Menschen zentrale Faktoren der Karrierewahl. Auch in der Medizin gewinnen Fragen wie die Möglichkeit ...
Schilddrüsenhormondefizienz und assistierte Reproduktion
In der Behandlung von Kinderwunschpatientinnen wird ein besonderes Augenmerk auf die Schilddrüsenfunktion gelegt. Hierbei stellt sich die Frage, welche Kriterien herangezogen werden ...
Alternative Therapieoptionen bei rezidivierenden Harnwegsinfekten
Brennende Schmerzen, häufiger Harndrang und immer wiederkehrende Infektionen – für viele Frauen gehören rezidivierende Harnwegsinfektionen (rUTI) zum Alltag. Da die wiederholte Anwendung ...