Überaktives Komplementsystem verursacht bei Long Covid Zellschäden
Eine Forschungsgruppe der Universität Zürich und des Universitätsspitals Zürich hat herausgefunden, dass das Komplementsystem bei Menschen mit Long Covid dauerhaft überaktiviert ist.1 Diese Erkenntnisse könnten zu einer besseren Diagnostik und Behandlung von Long Covid beitragen.
Etwa 5% aller mit dem SARS-CoV-2-Virus infizierten Personen entwickeln langfristige Komplikationen, die als Long Covid bezeichnet werden. Zu den derzeitigen Hypothesen über die Faktoren, die zu Long Covid beitragen, gehören Gewebeschäden, virale Reservoirs, Autoimmunität und anhaltende Entzündungen.
Zürcher Studie1
Um mehr über die Ursachen von Long Covid zu erfahren, beobachtete das Forschungsteam unter Leitung von Prof. Dr. med. Onur Boyman 113 Covid-19-Patienten bis zu einem Jahr nach der ersten Bestätigung einer akuten SARS-CoV-2-Infektion, um Biomarker zu identifizieren, die mit Long Covid in Verbindung stehen. Bei der Untersuchung nach 6 Monaten wiesen 40 Patienten Long-Covid-Symptome auf. Als Kontrolle dienten 39 gesunde Personen. Es wurden wiederholte klinische Untersuchungen und Blutentnahmen durchgeführt. Daraus resultierten insgesamt 268 Blutproben. Mittels Proteomik wurden im Serum >6500 Proteine gemessen und die wichtigsten Biomarker-Kandidaten wurden mithilfe von Berechnungsprogrammen identifiziert und experimentell weiter untersucht.
Resultate
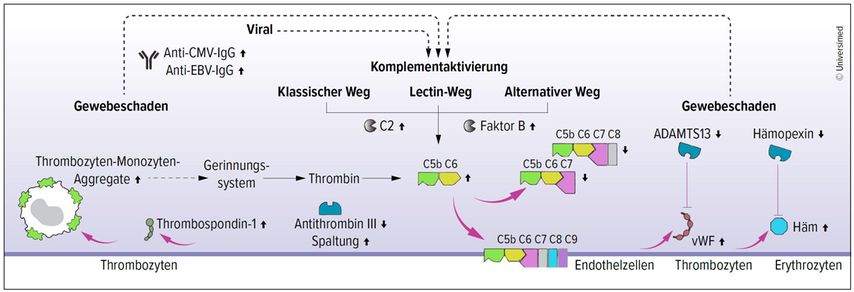
Dabei fand sich bei Long-Covid-Patienten während der akuten Erkrankung eine erhöhte Komplementaktivierung, die auch bei der Nachuntersuchung nach 6 Monaten noch anhielt. Interessanterweise normalisierte sich die Komplementaktivtät bei Patienten, die sich vor der Nachuntersuchung nach 6 Monaten von Long Covid erholten. Die Aktivierung des Komplementsystems führt zur Bildung des terminalen Komplementkomplexes (TCC), der aus den Komponenten C5b–C9 besteht. Diese Komplexe können in Zellmembrane eindringen und eine Zellaktivierung oder -lyse auslösen. Im Serum von Long-Covid-Betroffenen fanden die Forscher eine unausgewogene Bildung von TCC, die durch höhere Mengen an löslichen C5bC6- und geringere Mengen an C7-Komplexen, die in Zellmembranen eindringen können, gekennzeichnet war. Dies deutet gemäss den Autoren darauf hin, dass bei Long Covid vermehrt TCC in Membranen eingebaut werden, was zur Schädigung des Gewebes beiträgt. Dazu passen weitere Befunde, wie erhöhte Marker für Gewebeschäden im Blut und eine thromboinflammatorische Signatur, die sich durch Marker für die Endothelaktivierung (z.B. Von-Willebrand-Faktor) und die Lyse von Erythrozyten auszeichnete. Niedrige Antithrombin-III-Spiegel bei Long-Covid-Betroffenen waren mit Hinweisen auf eine verstärkte Spaltung durch Thrombin, einen Treiber der TCC-Bildung, assoziiert. Zudem konnten, insbesondere bei einer Long-Covid-Dauer von ≥12 Monaten, erhöhte Thrombozyten-Aktivierungsmarker und Thrombozyten-Monozyten-Aggregate nachgewiesen werden. In diesen Fällen gab es auch Anzeichen einer Antikörper-vermittelten Aktivierung des klassischen Komplementwegs, die mit erhöhten Anti-CMV- und Anti-EBV-IgG-Antikörperspiegeln assoziiert war.
Schlussfolgerungen
Die Resultate der Studie deuten darauf hin, dass aktives Long Covid von einer Blutproteinsignatur begleitet wird, die durch eine vermehrte Komplementaktivierung und eine Thromboinflammation gekennzeichnet ist. Gewebeschäden können Komplement-vermittelt sein und ihrerseits das Komplementsystem aktivieren. Zusätzlich kann die Komplementaktivierung auch durch Antigen-Antikörper-Komplexe mit Beteiligung von Autoantikörpern und Antikörpern gegen Herpesviren sowie durch eine Wechselwirkung mit einem fehlregulierten Gerinnungssystem ausgelöst werden. (red)
Literatur:
1 Cervia-Hasler C et al.: Persistent complement dysregulation with signs of thromboinflammation in active Long Covid. Science 2024; 383: eadg7942
Das könnte Sie auch interessieren:
Was tun bei Medikamentenunverträglichkeit?
Wenn Patientinnen und Patienten in die Praxis kommen und über eine Medikamentenunverträglichkeit klagen, gilt es herauszufinden, ob dies tatsächlich der Fall ist. Wie man dabei vorgeht ...
Physiotherapie bei akuten muskuloskelettalen Schmerzen
Akute muskuloskelettale Schmerzen zählen zu den häufigsten Beratungsanlässen in der Hausarztmedizin und im Notfallsetting. Eine frühzeitige physiotherapeutische Mitbeurteilung kann die ...
Der Tiefenrausch ist eine häufige Ursache für einen Tauchunfall
Atemgase verändern sich in der Wassertiefe physikalisch, was physiologische und medizinische Folgen bei Taucher:innen haben kann. Sauerstoff beispielsweise wird beim Abtauchen in der ...