Urothelkarzinom – was ändert sich?
Redaktion:
Mag. Dr. Anita Schreiberhuber
Geprüft von: OA Dr. Kilian Gust
Universitätsklinik für Urologie
Medizinische Universität Wien
E-Mail: kilian.gust@meduniwien.ac.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Highlights zum Urothelkarzinom vom EAU wurden von OA Dr. Kilian Gust, Medizinische Universität Wien, im Rahmen des 1. Post-EAU-Symposiums präsentiert und sorgen für angeregte Diskussionen über die Umsetzung in die Praxis.
Keypoints
-
In der Therapie des nichtmuskelinvasiven Harnblasenkarzinoms (NMIBC) hat BCG (Bacillus Calmette-Guérin) nach wie vor einen fixen Platz.
-
Die Behandlung von Patienten mit Very-High-Risk-NMIBC stellt aufgrund ihrer schlechten Prognose eine große Herausforderung dar.
-
Beim metastasierten Urothelkarzinom kann im Optimalfall mit der Erstlinien- und Erhaltungstherapie ein Gesamtüberleben von 31 Monaten erzielt werden.
Blaulicht-Fluoreszenz-Zystoskopie: Outcome-Verbesserung?
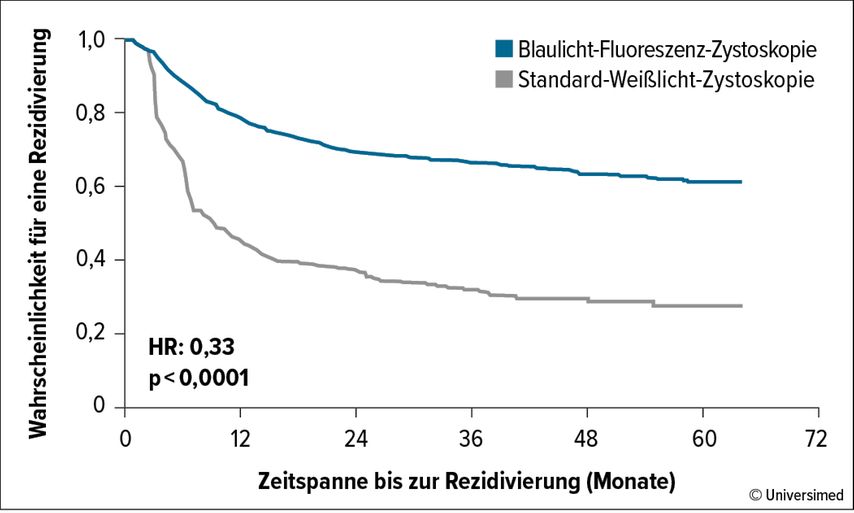
Gust griff mit dem „enhanced imaging“ und in diesem Zusammenhang mit der Frage, ob mittels photodynamischer Diagnostik (PDD) die Outcomes verbessert werden können, ein in der Folge stark diskutiertes Thema auf. Mit der PDD in Form der Blaulicht-Fluoreszenz-Zystoskopie (BL) vs. Standard-Weißlicht-Zystoskopie (WL) können mehr Tumoren, insbesondere Carcinomata in situ (CIS), detektiert undumfänglichere Resektionen erzielt werden. Ahmadi et al. haben gezeigt, dass das rezidivfreie Überleben (RFS) durch die Verwendung der BL signifikant verlängert werden kann (HR: 0,33; p>0,0001; Abb. 1).1
Abb. 1: Verlängerung der Rezidivfreiheit durch Einsatz der Blaulicht-Fluoreszenz-Zystoskopie (modifiziert nach Ahmadi H et al.: 2022)1
In der Diskussion wurden die positiven BL-assoziierten Effekte auf den weiteren Krankheitsverlauf skeptisch gesehen. Dabei wurde auf eine rezent publizierte Studie verwiesen, in der eine PDD-gelenkte im Vergleich mit einerWL-gelenkten transurethralen Blasentumorresektion (TURBT) zu keiner Reduktion der Rezidivraten geführt hat.2 Zudem wurde auf die hohen Kosten hingewiesen. Gust erklärte, dass grundsätzlich die Frage zu stellen sei, was eine potenziell vollständige Resektion verhindern kann. Insbesondere bei High-Risk(HR)-Patienten sei davon auszugehen, dass durch eine verbesserte Detektion ein präziseres Staging erzielt werden kann und durch die vollständigere Resektion ein Effekt auf die Rezidivhäufigkeit erzielbar ist.
Mittels PDD sind CIS, die einen wichtigen prognostischen Parameter darstellen, besser detektierbar. Ebenso sinkt die Morbidität der Patienten im Fall von Low-Grade-Rezidiven. An der Universitätsklinik für Urologie in Wien werde, so Gust, BL-PDD nicht unselektioniert, jedoch bei den meisten TURBT angewendet. Insbesondere bei multilokulären Befunden sowie bei High-Grade-Tumoren und einer etwaigen Nachresektion wird die PDD eingesetzt.
Nichtmuskelinvasives Harnblasenkarzinom (NMIBC)
Mit der Einführung der Risikofaktoren Alter >70 Jahre, multiple papilläre Tumoren und Tumordurchmesser >3cm wurde die Einteilung der NMIBC gemäß den EAU-Guidelines komplizierter. Zudem wurden Low(LR)-, Intermediate(IR)- und High-Risk(HR)-Tumoren um die Gruppe der Very-HR-Tumoren erweitert.3 In der Praxis bedeutet das, dass z.B. ein pTa-NMIBC bei Vorliegen von 3 zusätzlichen Risikofaktoren als HR-Befund upgegradet wird. Einen Spezialfall stellt das Very-HR-NMIBC mit histologischem Subtyp dar. „Wir diskutieren seit Jahren, ob in dieser Situation die intravesikale Therapie eine gute Option ist, verfügen aber über fast keine Outcome-Daten dazu“, so Gust. Very-HR-Tumoren gehen mit einem hohen Risiko für eine Progression einher. Der Anteil an Progressionen bzw. Übergängen zu einem muskelinvasiven Karzinom nach 10 Jahren beträgt >50%.3
Therapie des NMIBC
Als SOC („standard of care“) für die Therapie des NMIBC hat sich die intravesikale Therapie mit dem Bacillus Calmette-Guérin (BCG) etabliert. „Alternativ kann bei IR-Tumoren auch eine intravesikale Chemotherapie (CTx) verabreicht werden. HR-Patienten sollten BCG mindestens 1 Jahr lang erhalten, noch besser über einen Zeitraum von 3 Jahren“, erläuterte Gust.
Es stellt sich die Frage, was bei HR-Patienten, die ein Rezidiv nach BCG-Therapie zeigen, zu tun ist. Für dieses Kollektiv ist von der Food and Drug Administration (FDA), nicht aber von der Europäischen Arzneimittel Behörde (EMA) der Immuncheckpoint-Inhibitor (CPI) Pembrolizumab als Rescue-Medikation zugelassen, wenn die Patienten ein CIS mit oder ohne weiteren papillären Tumor aufweisen und keiner Zystektomie zugeführt werden wollen/können.4 In der einarmigen Phase-II-Studie KEYNOTE-057 (n=101) wurde so bei 40% der Patienten eine komplette Response (CR) erzielt, die bei 48% dieser Patienten bis zu 12 Monate anhielt.5
Die Frage nach seiner persönlichen Erfahrung mit Pembrolizumab beantwortete Gust dahingehend, dass er diese Substanz zur Behandlung des NMIBC bislang nur im Rahmen von klinischen Studien, aber mit guten Erfahrungen eingesetzt habe. In Europa ist die Gabe im klinischen Alltag „off-label“ und auch in Bezug auf die Kostenübernahme als kritisch zu erachten. „Wir wissen, dass BCG effektiv ist, aber bei Patienten mit Rezidiv nach HR-NMIBC oder Very-HR-r-Patienten sollten wir das „window of opportunity“ für eine radikale Zystektomie nicht verpassen“, so Gust.
In einer retrospektiven Studie zu HR-Patienten wurde BCG mit der sequenziellen Gabe von Gemcitabin (Gem) und Docetaxel verglichen. Dabei wurde im primären Endpunkt, dem rezidivfreien Überleben (RFS), eine signifikante Überlegenheit der CTx gegenüber BCG nachgewiesen (HR: 0,57; p=0,04).6
Zurzeit laufen viele Studien mit verschiedenen Substanzklassen wie zielgerichteten Therapien, Gentherapien, aber auch Device-assistierten Therapien (z.B. Hyperthermie) und Kombinationsstrategien (Immun- und CTx, Immun- und Radiotherapie).7 So wird in der drei-armigen Phase-III-Studie POTOMAC (NCT03528694) BCG + das CPI Durvalumab vs. eine BCG-Monotherapie untersucht, wobei BCG entweder nur als Induktion oder auch als Erhaltungstherapie appliziert wird.
Muskelinvasives Blasenkarzinom (MIBC)
„Im metastasierten Setting hat sich viel getan, wobei die perioperative (neoadjuvante oder adjuvante) Cisplatin(Cis)-haltige CTx den Standard beim muskelinvasiven oder lokal fortgeschrittenen Blasenkarzinom darstellt“, fasste Gust den Status in der Therapie des MIBC zusammen. Das heißt konkret: Cis-fitte Patienten sollten neoadjuvant eine Kombination aus Cis + Gem (oder dosisdichtes MVAC [Methotrexat, Vinblastin, Doxorubicin, Cis]) erhalten. In diesem Kontext stellte sich auch die Frage, ob tatsächlichbei allenPatienten, die bereits auf die neoadjuvante CTx eine CR entwickelt haben, eine radikale Zystektomie durchgeführt werden muss.
Prim. Univ.-Prof. Dr. Stephan Madersbacher, Klinik Wien-Favoriten, Moderator und Vorsitzender der Veranstaltung, äußerte sich dazu so: „Ich gehe davon aus, dass die Zystektomieraten sinken und die hohen CR-Raten dazu führen werden, dass sich viele Patienten nicht mehr operieren lassen werden, was zu neuen Überlegungen in Bezug auf dieNachsorgeschemata führen wird.“ Blasenerhaltende Therapiekonzepte werden zurzeit in mehreren klinischen Studien untersucht.7
In der adjuvanten Situation wurde zuletzt Nivolumab (Nivo) durch die EMA bei Patienten mit PD-L1 positiven Tumoren zugelassen.8,9 In der Phase-III-Studie CheckMate 274 konnte unter Nivo vs. Placebo in der ITT(„Intenttotreat“)-Population eine signifikante Verlängerung des krankheitsfreien Überlebens um 10 Monate (20,8 vs. 10,8 Monate) nachgewiesen werden.10
Im metastasierten Stadium bestätigte die platinhaltige Chemotherapie zuletzt ihren Stellenwert, wobei Cisplatin-ungeeignete Patienten Gem + Carboplatin erhalten. Patienten, die nicht für eine platinbasierte CTx infrage kommen, können sich einer CPI-Therapie mit Pembrolizumab oder Atezolizumab unterziehen.
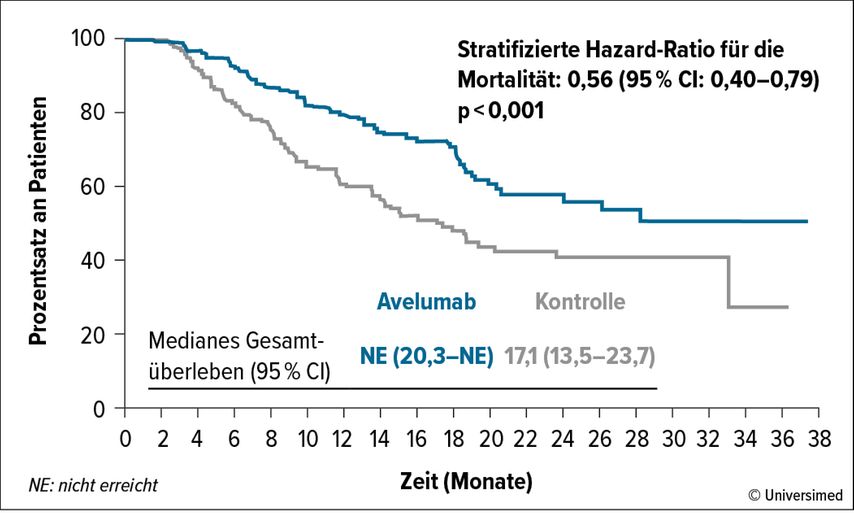
Als Erhaltungstherapie nach Erstlinien-Chemotherapie konnte sich Avelumab etablieren: In der Phase-III-Studie JAVELIN Bladder 100 wurde bei Patienten, die unter 4–6 Zyklen einer vorangegangenen platinhaltigen CTx keine Progression entwickelt hatten, unter dem CPI gegenüber alleiniger„best supportive care“ (BSC) eine signifikante Überlegenheit im Gesamtüberleben (OS) erzielt: Die 1-Jahres-OS-Rate betrug in der Gesamtpopulation 71,3% vs. 58,4% (medianes OS: 21,4 vs. 14,3 Monate; HR: 0,69; p=0,001) und in der PD-L1-positiven Population 79,1% vs. 60,4% (nicht erreicht vs. 17,1 Monate; HR: 0,56; p<0,001; Abb. 2).11 Avelumab ist unabhängig vom PD-L1-Status zugelassen.12 „Wir können bei Patienten mit lokal fortgeschrittenem/metastasiertem MIBC mit der platinbasierten CTx und einer Avelumab-Erhaltungstherapie in der Erstlinie ein OS von 31 Monaten erzielen. Damit haben wir das mediane OS von 15 Monaten, welches wir einmal erreicht haben, verdoppelt – das ist beim Urothelkarzinom der bislang größte Erfolg der vergangenen Jahre“, so das Fazit von Gust, welcher in diesem Zusammenhang auch die Frage aufwarf, ob bei Patienten, welche eine CR nach Erstlinienchemotherapie erreicht haben, überhaupt einer Erhaltungstherapie mit Avelumab notwendig ist. „Die OS-Kurven bei Patienten mit CR nach initialer Chemotherapie trennen sich bereits deutlich, wahrscheinlich wird dies auch statistisch signifikant werden“, ist sich Gust sicher.
Abb. 2: Medianes Gesamtüberleben in der PD-L1-positiven Population (modifiziert nach Powles T et al.: 2020)11
In der Zweitlinientherapie ist Pembrolizumab zugelassen,8 sofern noch keine Erhaltungstherapie mit Avelumab durchgeführt worden ist– also bei allen Patienten mit Progress unter Erstlinien-Chemotherapie.
In der Drittlinie ist für Patienten, die bereits mit einer CTx und einem CPI behandelt wurden, das Antikörper-Wirkstoff-Konjugat Enfortumab vedotin (EV) zugelassen, das sich in einer offen randomisierten Phase-III-Studie als signifikant effektiver erwiesen hat als eine Zweitlinien-CTx. Das mediane OS unter EV vs. CTx nach Wahl des Prüfarztes belief sich auf 12,88 vs. 8,97 Monate (HR: 0,79; p=0,001).13,14

Quelle:
1. Post-EAU: Was bleibt für Klinik und Praxis? 22. März 2023, Wien
Literatur:
1 Ahmadi H et al.: Role of blue-light cystoscopy in detecting invasive bladder tumours: data from a multi-institutional registry. BJU Int 2022; 130(1): 62-7 2 Rakesh H et al.: A randomized trial of PHOTOdynamic surgery in non-muscle-invasive bladder cancer. NEJM Evid 2022; 1(10) 3 https://d56bochluxqnz.cloudfront.net/documents/full-guideline/EAU-Guidelines-on-Non-muscle-Invasive-Blad-der-Cancer-2023_2023-03-10-101110_jued.pdf (Zugriff: 2. April 2023) 4 https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pembrolizumab-bcg-unresponsive-high-risk-non-muscle-invasive-bladder-cancer (Zugriff: 2. April 2023) 5 Balar AV et al.: Pembrolizumab monotherapy for the treatment of high-risk non-muscle-invasive bladder cancer unresponsive to BCG (KEYNOTE-057): an open-label, single-arm, multicentre, phase 2 study. Lancet Oncol 2021; 22(7): 919-30 6 McElree IM et al.: Comparison of sequential intravesical gemcitabine and docetaxel vs bacillus Calmette-Guérin for the treatment of patients with high-risk non-muscle-invasive bladder cancer. JAMA Netw Open 2023; 6(2): e230849 7 https://clinicaltrials.gov/ 8 https://d56bochluxqnz.cloudfront.net/documents/full-guideline/EAU-Guidelines-on-Muscle-Invasive-Bladder-Cancer-2023_2023-03-14-145913_jsen.pdf (Zugriff: 2. April 2023) 9 Fachinformation Opdivo®, Stand: März 2023 10 Bajorin FL et al.: Adjuvant nivolumab versus placebo in muscle-invasive urothelial carcinoma. N Engl J Med 2021; 384: 2102-14 11 Powles T et al.: Avelumab maintenance therapy for advanced or metastatic urothelial carcinoma. N Engl J Med 2020; 383: 1218-30 12 Fachinformation Bavencio®, Stand: März 2023 13 Fachinformation Padcev®, Stand: Dezember 2022 14Powles T et al.: Enfortumab vedotin in previously treated advanced urothelial carcinoma. N Engl J Med 2021; 384: 1125-35
Das könnte Sie auch interessieren:
Aktuelle Entwicklungen und Erkenntnisse beim Urothelkarzinom
Auf dem diesjährigen Genitourinary Cancers Symposium der American Society of Clinical Oncology (ASCO-GU-Kongress) wurden bedeutende Fortschritte in der Diagnose und Behandlung des ...
Aktuelles aus der 7. Version der S3-Leitlinie: wesentliche Leitlinienänderungen
Im Mai 2024 wurde die Prostatakarzinom-S3-Leitlinie unter der Federführung der Deutschen Gesellschaft für Urologie e.V. (DGU) im Rahmen des Leitlinienprogramms Onkologie in ihrer 7. ...
Neues vom ASCO GU zum Prostatakarzinom
Im Rahmen des ASCO GU 2025 in San Francisco wurden eine Vielfalt von neuen praxisrelevanten Studien zum Prostatakarzinom präsentiert. Mit Spannung wurde unter andem auch auf die finalen ...