Systemtherapie beim oligometastasierten Prostatakarzinom
Das oligometastasierte Prostatakarzinom stellt mit lokalen und systemischen Therapieoptionen eine wachsende Herausforderung dar. Mit der Zulassung von Apalutamid Ende Jänner 2020 und Enzalutamid in Kürze steht eine erfreuliche Anzahl von Therapieoptionen zur Verfügung, die neben der jeweiligen Effektivität individuell für den Patienten anhand der Ausdehnung der Metastasierung, des Allgemeinzustandes des Patienten und der Nebenwirkungen ausgewählt werden kann.
Keypoints
-
Die Therapieoptionen beim HNPCa und HSPCa haben sich deutlich erweitert.
-
Auch Patienten mit einer Oligometastasierung profitieren hinsichtlich des Gesamtüberlebens.
-
Bei der Therapie sind Metastasenlast, Risikostatus und die Zulassung zu berücksichtigen.
-
Bei der Therapiewahl sollte daran gedacht werden, welche Optionen bei einem Progress zur Verfügung stehen.
Oligometastasierung beim Prostatakarzinom
Die Oligometastasierung ist im Allgemeinen als das Vorhandensein von ≤5 Metastasen definiert.1 Prinzipiell kann eine Oligometastasierung in jedem Stadium des Prostatakarzinoms auftreten, namentlich dem hormonnaiven (HNPCa), hormonsensitiven (HSPCa) und kastrationsresistenten Stadium (CRPCa).
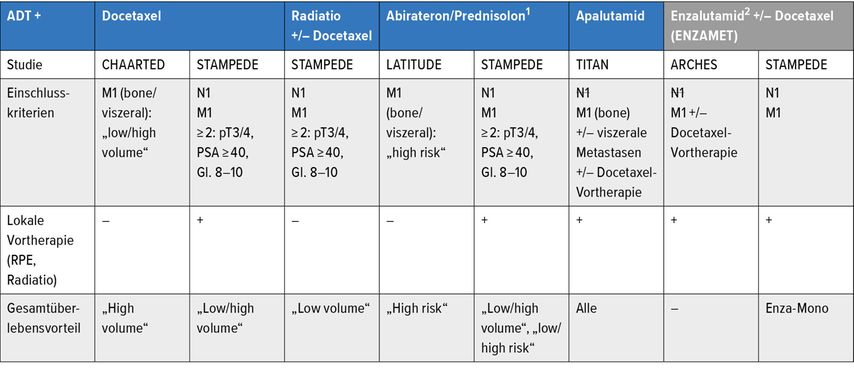
Mit Verbesserung der Diagnostik vor allem unter Verwendung des PSMA-PET hat die Oligometastasierung an klinischer Bedeutung gewonnen, bei der sowohl lokale als auch systemische Therapieoptionen zur Verfügung stehen. Diese multimodalen Therapiekonzepte können bei selektierten Patienten zu einer deutlichen Prolongierung des Verlaufs der Erkrankung führen. Neben operativen und strahlentherapeutischen Verfahren für die lokale Primärtumor- und Metastasentherapie ist inzwischen eine Reihe medikamentöser systemischer Therapien zugelassen (Tab. 1). Der Einsatz der verschiedenen Therapien wird neben der vorhandenen Evidenz auch vom Zulassungsstatus bestimmt, was nicht immer deckungsgleich und daher im klinischen Alltag zu beachten ist.
Tab. 1: Übersicht über die Therapieoptionen beim hormonnaiven/-sensitiven Prostatakarzinom (1nur beim primär metastasierten PCa zugelassen; 2Zulassung wird in der 2. Jahreshälfte des Jahres 2020 erwartet.)
CHAARTED-Studie
Die CHAARTED-Studie zeigte erstmalig eine Verbesserung des Gesamtüberlebens beim metastasierten, hormonnaiven Prostatakarzinom (HNPCa) durch die Kombination der Androgendeprivation (ADT) mit Docetaxel.2 Dabei wurde zwischen einem „Low“- und einem „High volume“-HNPCa unterschieden (Tab. 2). Allerdings profitierten in der Studie Patienten mit einem „Low volume“-HNPCa, entsprechend einem oligometastasierten Prostatakarzinom, nicht von der zusätzlichen Therapie mit Docetaxel.3 Erst mit den Daten aus der STAMPEDE-Studie wurde deutlich, dass auch Patienten mit einem lokal fortgeschrittenen und oligometastasierten HNPCa von der Kombination mit Docetaxel profitieren.4 Die europäische Zulassung von Docetaxel erlaubt den Einsatz sowohl beim HNPCa/HSPCa als auch beim CRPCa.

Tab. 2: Definition des Tumorvolumens aus der CHAARTED-Studie2
Neben der Kombination mit Docetaxel zeigen weitere Daten aus der STAMPEDE-Studie, dass auch die Lokaltherapie des Primärtumors mit einer Radiatio bei Patienten mit einem oligometastasierten („low volume“) Prostatakarzinom zu einer Lebensverlängerung führt.5 Allerdings ist unklar, inwieweit hier die Kombination mit Docetaxel für den Effekt auf das Gesamtüberleben notwendig ist, da ca. 80% der Patienten in der Studie lediglich die Kombination von ADT + Radiatio und ca. 20% die Kombination von ADT + Docetaxel + Radiatio erhalten haben.
LATITUDE-Studie
Die LATITUDE-Studie mit der Kombination von ADT + Abirateron/Prednison führte zur Zulassungserweiterung von Abirateron beim HNPCa.6 Allerdings wurden in die Studie nur Patienten mit einem „High risk“-Status und einem primär metastasierten Prostatakarzinom aufgenommen (Tab. 3). Darunter fallen jedoch durchaus auch Patienten mit einem oligometastasierten PCa, wenn z.B. 3–5 Metastasen vorliegen. Die Zulassung der EMA bezieht die Kriterien des „High risk“-Status und des primär metastasierten PCa ein, sodass bei der Anwendung im klinischen Alltag darauf geachtet werden sollte, um nicht im Off-Label-Bereich zu therapieren. Die Evidenzlage ließe auch den Einsatz außerhalb dieser strengen Indikation zu, da abgesehen von der LATITUDE-Studie auch aus der STAMPEDE-Studie Phase-III-Daten zum Einsatz von Abirateron beim HNPCa vorhanden sind.7 Diese belegen, dass Abirateron auch bei Patienten mit einem „Low risk“-Status sowie bei Patienten mit einem „Low“- oder „High volume“-Prostatakarzinom einen Gesamtüberlebensvorteil erbringt. Zudem waren in die STAMPEDE-Studie auch Patienten inkludiert, die nicht primär metastasiert waren.

Tab. 3: Definition des Hochrisiko-Status aus der LATITUDE-Studie6
TITAN-Studie
Ende Jänner 2020 erfolgte die Zulassung von Apalutamid, einem Androgen-Rezeptor-Antagonisten, vergleichbar mit Enzalutamid. Die Zulassung beruht auf den Daten der TITAN-Studie.8 Hierbei wurden Patienten mit einem ossär metastasierten HNPCa bzw. hormonsensitiven Prostatakarzinom (HSPCa) eingeschlossen, da die Patienten im Sinne der CHAARTED-Studie mit der Kombination von ADT + Docetaxel behandelt sein durften, sofern sie keinen Progress zum CRPCa gezeigt hatten. Für den Einschluss in die Studie war dabei der Nachweis einer solitären Knochenmetastase ausreichend. Der Zulassungstext erlaubt den Einsatz von Apalutamid beim metastasierten Prostatakarzinom – ob hier entsprechend der TITAN-Studie eine ossäre Metastase vorliegen muss, geht aus dem Zulassungstext nicht eindeutig hervor und ist noch Gegenstand von Diskussionen.
Ausblick
Bisher noch nicht zugelassen ist der Einsatz von Enzalutamid beim HNPCa bzw. HSPCa.Die Zulassung von Enzalutamid ist noch nicht erfolgt und wird in der 2. Jahreshälfte des Jahres 2020 erwartet. Die Evidenz für den Einsatz von Enzalutamid beruht auf der ARCHES-9 und der ENZAMET-Studie.10 Vergleichbar mit der TITAN-Studie war auch in der ARCHES-Studie eine Vortherapie mit Docetaxel erlaubt. Im Gegensatz zur TITAN-Studie war allerdings das Vorhandensein einer Knochenmetastase keine Voraussetzung der Studie, es reichte der bildgebende Nachweis von Metastasen außerhalb des Beckens. Der primäre Endpunkt der Studie, das radiografisch progressionsfreie Überleben, war positiv – es fehlt jedoch noch der Nachweis eines Überlebensvorteils. Einen Überlebensvorteil hat jedoch die ENZAMET-Studie gezeigt, in der Patienten mit jeglicher Metastasierung einschließlich Lymphknoten-Metastasen im Becken eingeschlossen wurden. Zudem war eine Vortherapie mit bis zu 2 Zyklen Docetaxel erlaubt, die dann begleitend zur Therapie mit Enzalutamid fortgeführt werden konnte. Allerdings zeigte sich, dass der Überlebensvorteil auf die Patientengruppe beschränkt war, die keine zusätzliche Docetaxel-Therapie erhalten hat. Bei beiden Studien gibt es keine Subgruppen-Auswertungen im Hinblick auf den Einfluss der Metastasenlast auf die Effektivität der Therapie, sodass davon ausgegangen werden kann, dass auch Patienten mit einer Oligometastasierung von der Kombination aus ADT + Enzalutamid profitieren.
Fazit
Zusammenfassend haben sich die Therapieoptionen von Patienten mit einem HNPCa und einem HSPCa in den letzten 12 Monaten nochmals deutlich erweitert und die Studienergebnisse zeigen, dass auch Patienten mit einer Oligometastasierung im Hinblick auf das Gesamtüberleben profitieren. Die Auswahl der Therapie ist dabei neben den dargestellten Aspekten der Metastasenlast, des Risikostatus und der Zulassung auch von der Sequenz der Therapie abhängig. Dabei sollte bereits frühzeitig daran gedacht werden, welche weiteren Therapien der jeweilige Patient nach einem Progress zum CRPCa noch erhalten könnte.
Autor:
Prof. Dr. Carsten-H. Ohlmann
Klinik für Urologie
Malteser Krankenhaus
Bonn/Rhein-Sieg
E-Mail: carsten.ohlmann@malteser.org
Literatur:
1 Rao A et al.: Oligometastatic prostate cancer: ashrinking subset or an opportunity for cure? Am Soc Clin Oncol Educ Book 2019; 39: 309-20 2 Sweeney CJ et al.: Chemohormonal therapy in metastatic hormone-sensitive prostate cancer. N Engl J Med 2015; 373: 737-46 3 Kyriakopoulos CE et al.: Chemohormonal therapy in metastatic hormone-sensitive prostate cancer: long-term survival analysis of the randomized phase III E3805 CHAARTED Trial. JClin Oncol2018; 36: 1080-7 4 Clarke NW et al.: Addition of docetaxel to hormonal therapy in low- and high-burden metastatic hormone sensitive prostate cancer: long-term survival results from the STAMPEDE trial. Ann Oncol 2019; 30: 1992-2003 5 Parker CC et al.: Radiotherapy to the primary tumour for newly diagnosed, metastatic prostate cancer (STAMPEDE): a randomised controlled phase 3 trial. Lancet 2018; 392: 2353-66 6 Fizazi K et al.: Abiraterone plus prednisone in metastatic, castration-sensitive prostate cancer. N Engl J Med 2017; 377: 352-60 7 Hoyle AP et al.: Abiraterone in ‘high-’ and ‘low-risk’ metastatic hormone-sensitive prostate cancer. Eur Urol 2019; 76: 719-28 8 Chi KN et al.: Apalutamide for metastatic, castration-sensitive prostate cancer. N Engl J Med 2019; 381: 13-24 9 Armstrong AJ et al.: ARCHES: arandomized, phase III study of androgen deprivation therapy with enzalutamide or placebo in men with metastatic hormone-sensitive prostate cancer. J Clin Oncol 2019; 37: 2974-86 10 Davis ID et al.: Enzalutamide with standard first-line therapy in metastatic prostate cancer. N Engl J Med 2019; 381: 121-31
Das könnte Sie auch interessieren:
Vom Siegeszug der ADC und von neuen Active-Surveillance-Therapieansätzen
Auf dem 11. Michael J. Marberger Meeting der Universitätsklinik für Urologie, Medizinische Universität Wien, wurden aktuelle Daten zu Antikörper-Wirkstoff-Konjugaten, neue Ansätze zum ...
Heutiger Stellenwert der ESWL: Renaissance in Sicht?
Die ESWL (extrakorporale Stoßwellenlithotrypsie) ist eine Technik zur urologischen Steintherapie, die in den 80er-Jahren des vorigen Jahrhunderts in den klinischen Alltag Einzug gehalten ...
PCNL-Indikationen in Zeiten von flexibler Ureterorenoskopie mit Absaugung?
In der Behandlung von Nierensteinen, die größer als 2cm sind, spielt die perkutane Nephrolithotomie (PCNL) weiterhin eine wichtige Rolle. Die flexible Ureterorenoskopie (URS) mit ...