Rekonstruktionsmöglichkeiten bei Nervenläsionen
Autor:innen:
Dr. Magdalena Köhl
Dr. Marit Zwierzina
Dr. Turkhan Mehdiyev
Verena Müller, BSc.
Dr. Eva-Maria Baur
Universitätsklinik für Plastische, Ästhetische und Rekonstruktive Chirurgie, Innsbruck
Korrespondierende Autorin:
E-Mail: eva-maria.baur@tirol-kliniken.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Rekonstruktion peripherer Nervenläsionen bleibt eine Herausforderung – besonders bei langen Defektstrecken, verzögerter Diagnostik oder ausgeprägter Denervierung. Der Artikel beleuchtet moderne Verfahren wie Nerventransfers und funktionelle Muskeltransfers, stellt neue Techniken wie Venen-Muskel-Interponate vor und gibt praxisrelevante Entscheidungshilfen für schwierige Fälle
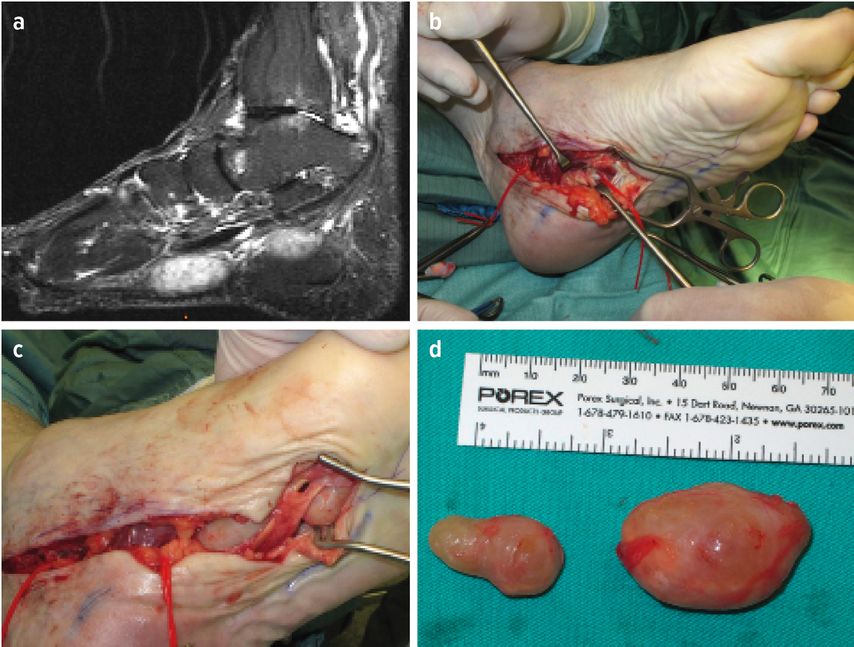
Nervenläsionen können unterschiedlichste Ursachen haben. Der Erfolg der Behandlung ist auch maßgeblich durch das richtige und zeitnahe Erkennen und Festlegen des weiteren Prozedere bestimmt. Dies können sowohl ein direkter operativer Eingriff bei nachgewiesener Durchtrennung eines Nervs oder auch die zeitlich korrekte erneute elektrophysiologische Messung und ggf. Bildgebung sein. Ursachen von Nervenläsionen können offene Verletzungen, beispielsweise durch einen Messerschnitt in den Finger sein, oder auch im Rahmen von Frakturen/Luxationen sowie in deren Behandlung liegen. Iatrogene Verletzungen sind ebenfalls möglich. Dazu kommt das große Gebiet der Nervenkompressionen. Entweder primär an entsprechenden anatomischen Engstellen eines Nervs, wie beispielsweise das häufigste und allen bekannte Karpaltunnelsyndrom oder sekundäre Kompressionen durch Ganglien, Fehlstellungen im Bereich der Knochen, Synovialitiden oder andere Tumoren wie Lipome. Auch Nerventumoren können zu einer Funktionsstörung führen, hier ist das häufigste sicher das Neurinom/Schwannom (Abb. 1), welches in seltenen Fällen bösartig sein kann, insbesondere wenn es eine bestimmte Größe überschritten hat.
Abb. 1: Neurinome Fußsohle, MRT und klinische Fotos intraoperativ. a) MRT, b) Situs intraop, c) Tumoren in situ, d) Präparat
Zur Rekonstruktion gibt es verschiedene Möglichkeiten je nach Läsion, Substanzverlust und zeitlicher Abfolge. Je früher, desto besser, da dann das Zielorgan – die motorische Endplatte am Muskel – noch funktioniert.
Naht und Transplantation
Periphere Nerven sind von einer äußeren Bindegewebsschicht (Epineurium) umgeben. Darin verlaufen die gebündelten Nervenfasern (Axone), welche vom Perineurium umhüllt sind und in Summe als Faszikel zusammengefasst werden. Diese beiden stabilen Schichten werden für epineurale bzw. perineurale Nähte verwendet.
Bei vollständiger Nervendurchtrennung (Neurotmesis, Sunderland Grad 5) ist eine operative Therapie im Sinne einer Koaptation nötig. Unter Axonotmesis versteht man eine Verletzung des Perineuriums mit Unterbrechung der Axone bei erhaltenem Epineurium. Auch hier ist eine zeitnahe OP erforderlich.
Regeneration erfolgt durch Waller’sche Degeneration im distalen Stumpf, wobei Axone im distalen Stumpf zugrunde gehen, aber die Nervenscheiden erhalten bleiben. Axone wachsen von proximal pro Tag ca. 1mm nach. Ein positives Hoffmann-Tinel-Zeichen gibt Auskunft über Verletzung, zeigt aber auch Fortschritt oder Stillstand der Heilung.
Bei Verdacht auf Läsion wird eine Exploration unter Allgemeinanästhesie, optischer Vergrößerung (Lupenbrille/Mikroskop) und ohne Muskelrelaxanzien empfohlen, um eine intraoperative Nervenstimulation zu ermöglichen. Kurze Eingriffe an distalen Extremitäten können fallweise auch in Lokalanästhesie durchgeführt werden. Entscheidend für eine optimale Heilung ist die Ausrichtung der Faszikel, um ein adäquates Aussprossen der Axone zu ermöglichen. Die „Traumazone“ sollte reseziert und der Nerv unbedingt spannungsfrei koaptiert werden.
End-zu-End-Naht (Neurorhaphie) erfolgt spannungsfrei mit wenigen epineuralen Einzelknopfnähten (8–0 bis 10–0, nicht resorbierbar, monofil). Fibrinkleber kann ergänzend oder alternativ verwendet werden – sparsam, um Gewebsbarrieren zu vermeiden.
Ruhigstellung: 7–14 Tage postoperativ.
Primäre vs. sekundäre Nervennaht
Ziel ist eine zeitnahe primäre Rekonstruktion (idealerweise innerhalb von 5 Tagen bis max. 3 Wochen), um Fibrose, Retraktion und Denervierung zu verhindern („time is muscle“). Bei Infektionen, schlechter Gewebequalität oder komplexen Verletzungen mit Quetschtraumata oder Zerrung kann eine sekundäre Rekonstruktion notwendig werden. In solchen Fällen sind häufig das Rückkürzen bis zum Erscheinen gesunder Nervenstrukturen und Transplantate/Interponate erforderlich. Ist keine primäre Rekonstruktion möglich, sollten die Nervenenden mit feinen, nicht resorbierbaren Fäden markiert werden, um das Auffinden im Rahmen einer späteren Versorgung zu erleichtern. Sind motorische Nerven betroffen, wird eine konsequente Elektrotherapie zum Erhalt des Muskels bis zur definitiven Nervenversorgung empfohlen.
Transplantation
Wenn keine direkte, spannungsfreie Nervenkoaptation möglich ist, erfolgt eine Überbrückung durch Transplantate. Dafür stehen unterschiedliche Möglichkeiten zur Verfügung.
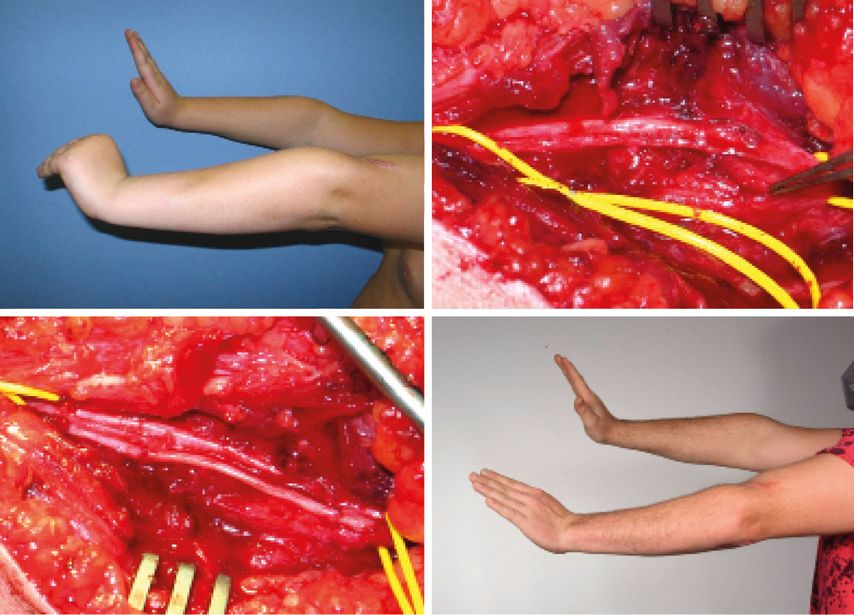
Autologe Transplantate bieten strukturelle und zelluläre Unterstützung für die Regeneration. Wichtig ist die spannungsfreie Naht, mit ca. 10% Längenzugabe zur Defektstrecke. Faszikel müssen adäquat ausgerichtet werden, ggf. mithilfe von perineuralen Nähten. (Abb.2a Patient prä- und postoperativ, Abb.2b Suralis-Interponat). Die Faszikel sollten in keinem Fall überlappen. Defektstrecken von 3–6cm gelten als optimal. Der Regenerationserfolg nimmt mit zunehmender Defektlänge ab.
Abb. 2a: Nervenrekonstruktion mit Suralis-Interponaten. Oben: prae OP klinisch Z.n. distaler Humerusfraktur, mit Bohrdrähten versorgt. Initial Ulnaris- und Radialisläsion. N. ulnaris hat sich verbessert (li.). Nerven-OP mit Neurolyse N. ulnaris und radialis und partieller Rekonstruktion N. radialis bei Teilläsion (re.). Unten: post OP (Zusammenarbeit Unfallchirurgie und Plastische Chirurgie Innsbruck)
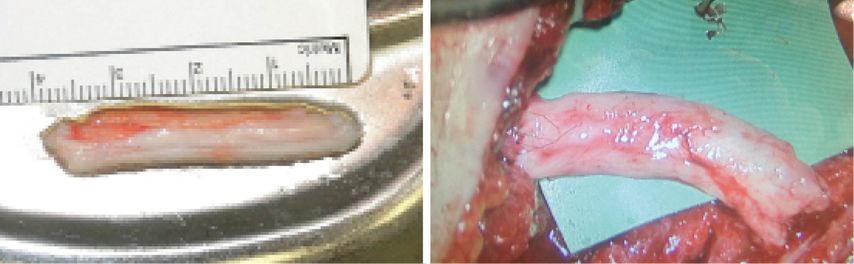
Abb. 2b: Vorbereitung Suralis-Interponate mit Fibrinkleber (links), mikroskop. Bild mit eingenähtem Nerventransplantat (rechts)
Allogene Transplantate werden von menschlichen Spendernerven gewonnen. Sie sind meist azellulär, weshalb in der Regel ein immunologischer Abstoßungsprozess ausbleibt. Als Limit für die Defektstrecke gelten ca. 7cm. Da sie keine lebenden Schwann-Zellen aufweisen, wird eine längere Regeneration diskutiert.
Nerven-Conduits (Tubes) können biologischen oder synthetischen Ursprungs sein (z.B. Kollagen, Polyglykolsäure). Sie dienen sozusagen als „Führungsrohr“ für Nervenenden, haben sich aber bisher eher nur für kleine Defektstrecken sensibler Nerven etabliert.
Venen-Muskel-Interponate sind ein kosteneffizientes und biologisch autologes Verfahren zur Überbrückung kurzer Nervendefekte, insbesondere bei sensorischen Nerven. Dabei dient ein Veneninterponat als Tube, durch welchen ein Muskelstreifen hindurchgezogen wird, um das Lumen offen zu halten. Ähnlich den Nerven-Conduits ist der Hintergedanke ein Aussprossen der Axone entlang dieser Leitstruktur. Die klinische Anwendung ist bislang aufgrund seltener Indikationsstellung beschränkt, da autologe Transplantate wegen des besseren Outcomes nach wie vor der Goldstandard sind.
Nerventransfer
Nervenverletzungen können zu erheblichen Funktionseinschränkungen im Alltag führen. Diverse Rekonstruktionsmöglichkeiten wie z.B. Transplantate können nicht immer angewandt werden – abhängig von Trauma, Lokalisation, Zeitpunkt, Defektstrecke und Alter. Nerventransfers bieten durch Rekonstruktion nahe dem Zielmuskel und außerhalb der Verletzungszone eine Chance auf schnellere Reinnervation und bessere funktionelle Ergebnisse. Für ihren Erfolg sind Timing, adäquate Patientenselektion, präoperative Planung und OP-Technik entscheidend.
Es gibt drei Hauptarten von Nerventransfers:
-
End-zu-End-Verbindung: Stümpfe des Empfänger- und Spendernervs werden direkt koaptiert.
-
End-zu-Seit-Verbindung: Das proximale Ende des Empfängernervens wird durch ein kleines, epineurales Fenster mit der Seite des Spendernervens verbunden. Indikation: sensorische Nerven.
-
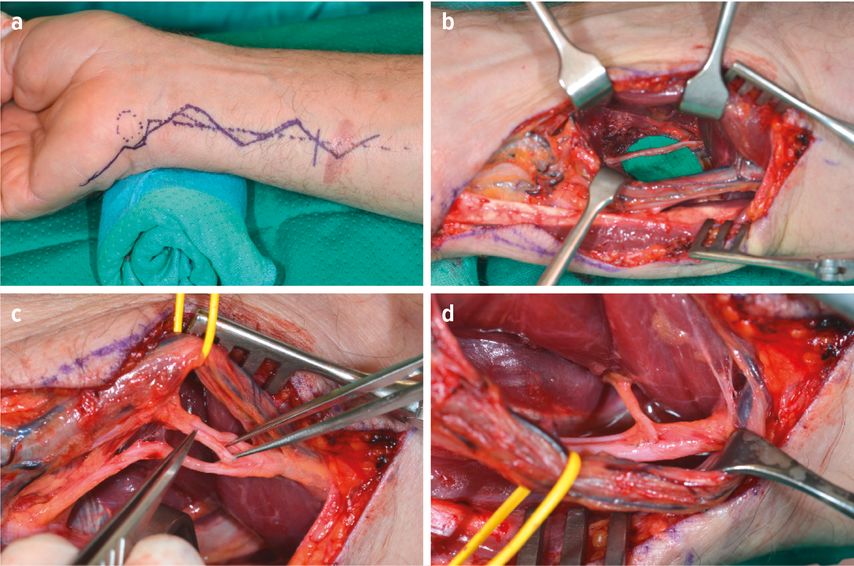
Umgekehrte End-zu-Seit-Verbindung („supercharge“): Das Ende des Spendernervs wird über o.g. Technik mit der Seite des Empfängernervs verbunden. Indikation: schnelle, aber nur teilweise Reinnervation der motorischen Endplatten. Ziel ist es, der Muskelatrophie entgegenzuwirken, bis die ursprünglichen Nervenfasern zu ihren Zielmuskeln aussprossen. Beispiel: Oberlin-Transfer (von N. medianus zu N. ulnaris), AIN-Transfer (von N. interosseus anterior zu N. ulnaris), siehe Abb.3.
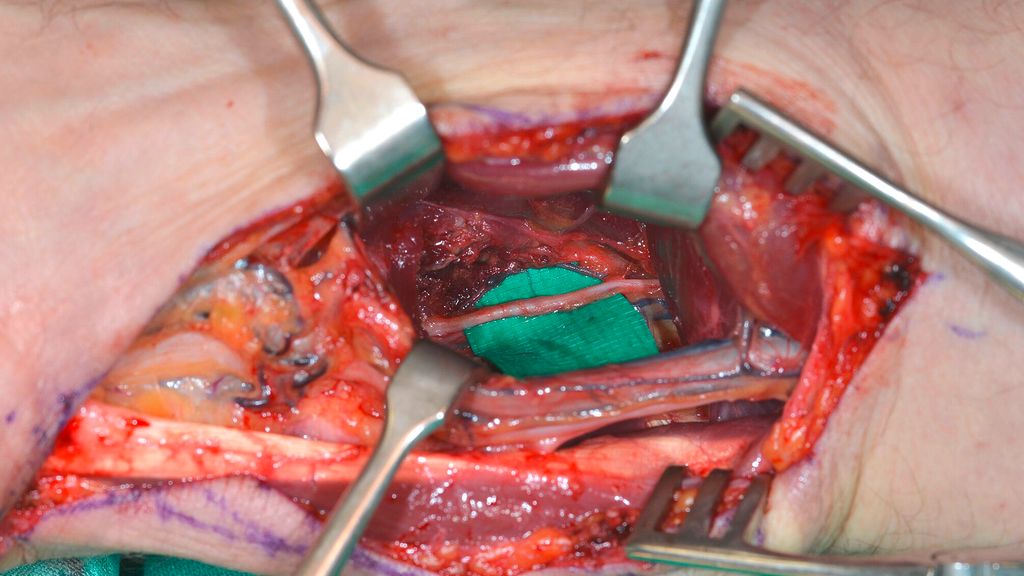
Abb. 3: AIN-Transfer. a) Operativer Zugang für Dekompression der Loge-de-Guyon inklusive AIN-Transfer (N. interosseus anterior → N. ulnaris) am rechten distalen Untarm. b) Darstellen des N. interosseus anterior am M. pronator quadratus. c) Topographie des N. ulnaris (R. superficialis – oben, R. profundus – mittig, R. dorsalis – unten). d) Mikrochirurgische End-zu-Seit-Verbindung („supercharging“) des N. interosseus anterior an den R. profundus n. ulnaris
Ein idealer Spendernerv weist folgende Eigenschaften auf:
-
rein motorisch oder sensorisch
-
enthält ausreichend Axone, um Empfängernerv zu reinnervieren
-
ähnliches Kaliber
-
keine/minimale Hebemorbidität
-
synergistische Wirkung zum Empfängernerv
-
keine Pathologien bei elektrophysiologischen Untersuchungen
Nerventransfers sind indiziert bei:
-
sehr proximalen Nervenverletzungen
-
wenn primäre Nervennaht nicht möglich
-
Defektstrecke >7cm (schlechte Ergebnisse mit Nerventransplantation)
-
großer Distanz zwischen Höhe der Verletzung und motorischen Endplatten
Nerventransfers sind kontraindiziert bei:
-
Dauer seit Trauma >18Monate (keine effektive motorische Funktion mehr zu erwarten)
-
motorischer Funktion des Spenders MRC <4 (Medical Research Council)
-
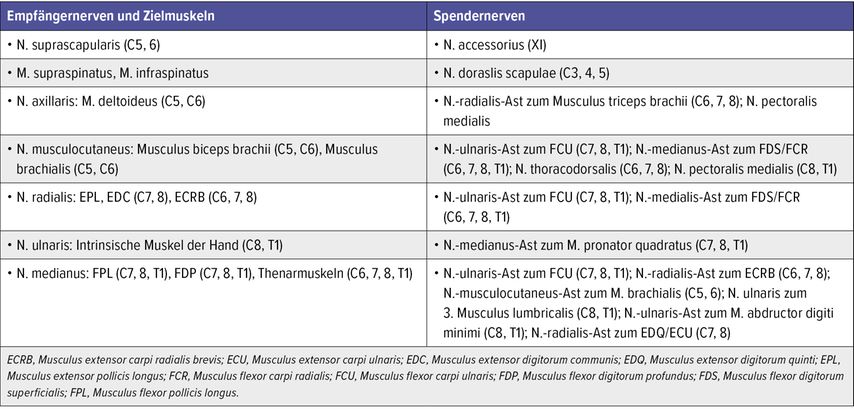
Die häufigsten Nerventransfers an der oberen Extremität sind in Tabelle 1 aufgelistet.
Aufgrund der größeren Regenerationsstrecken an der unteren Extremität und der exzellenten Ergebnisse mit Prothesen, sind Nerventransfers an der unteren Extremität noch nicht so etabliert wie an der oberen Extremität. Aber auch hier gibt es jedoch Möglichkeiten, wie beispielsweise einen Ast für den M.soleus auf den N.peroneus umzusetzen. Die Rehabilitation nach einem Nerventransfer ist entscheidend für den Erfolg. Bereits präoperativ sollte idealerweise mit einem auf motorisches Retraining spezialisierten Therapeuten die Rehabilitation beginnen. Dieser unterstützt beim frühzeitigen Üben der Muskelkontraktionen des Spendernervs. Bei sensiblen Nerventransfers ist der sensorische Input in das neu innervierte Gebiet für den Heilungsprozess wichtig. Sowohl bei motorischen als auch sensiblen Nerventransfers ist ein kortikales Mapping für den Erfolg unerlässlich.
Funktioneller Muskeltransfer
Wenn durch eine Verletzung auch ein Muskeldefekt entstanden ist, dann kommt auch ein freier mikrochirurgischer Muskeltransfer infrage. Als Spendermuskel hierfür ist, je nach Größe und Hub, der M.gracilis (erste Wahl) oder auch der M.latissimus dorsi möglich.
Motorische Ersatzplastik
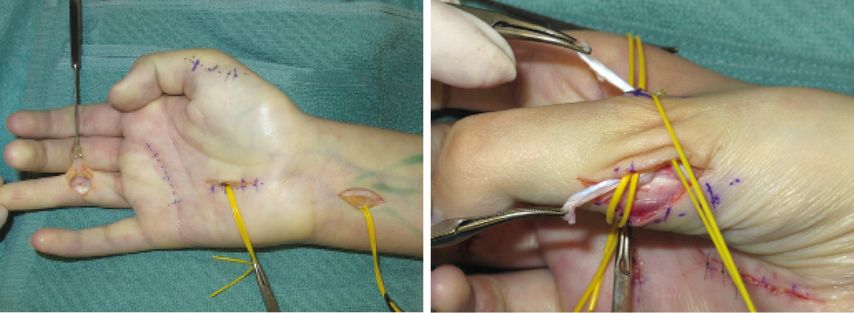
Wenn weder Nervenrekonstruktion noch -transfer aufgrund der Dauer der Verletzung oder Defektstrecke möglich ist, kann zu jedem Zeitpunkt auch ein Sehnen-/Muskeltransfer erfolgen. Hierzu wird ein funktionierender Muskel (idealerweise ein Antagonist) „geopfert“ und zur Wiederherstellung der fehlenden Funktion umgeleitet. Hierbei ist sowohl der Verlauf der umgesetzten Sehne/Muskel als auch die Spannung von Bedeutung, damit ein guter Hub und damit Funktion entsteht. Gerade diese Einstellung der Spannung ist nicht immer ganz einfach. Intraoperativ kann einem hier der Tenodeseeffekt helfen. Das häufigste hier ist sicher die Radialis-Ersatz-Plastik für die Streckung der Finger, Daumen und ggf. auch Handgelenk oder der Opponensersatz (Abb.4). An der unteren Extremität kommt hier v.a. der Tibialis-posterior-Transfer auf den M.tib. anterior zur Wiederherstellung des Fußhebers zum Einsatz.
Abb. 4: Opponens-Ersatzplastik
Nachbehandlung
Neben der etablierten Elektrotherapie vor und nach der operativen Versorgung von Nervenverletzungen ist eine intensive ergotherapeutische Nachbehandlung von entscheidender Bedeutung. Aufgrund der langwierigen Regenerationsprozesse peripherer Nerven erfordert die Therapie eine konsequente und oftmals lang anhaltende Durchführung über mehrere Monate.
Ein wesentlicher Schwerpunkt der ergotherapeutischen Intervention liegt in der individuellen Schienenversorgung. Diese schützt die rekonstruierten Nerven, Sehnen und Muskulatur und fördert gleichzeitig eine optimale Heilungsumgebung. So werden beispielsweise bei einer Radialisläsion statische Nachtschienen eingesetzt, um Fehlstellungen zu vermeiden und die betroffene Extremität während der Ruhephase zu stabilisieren. Im Alltag kommen dynamische Funktionsschienen zum Einsatz, welche die Handfunktion unterstützen und die Beweglichkeit fördern. Durch diese Maßnahmen wird einerseits die Alltagsfunktionalität bestmöglich erhalten und andererseits einem Ausleiern der Sehnen und damit verbundenen Komplikationen effektiv entgegengewirkt.
Darüber hinaus umfasst die ergotherapeutische Nachbehandlung ein ganzheitliches Konzept, das passive und aktive Mobilisation, sensomotorisches Training sowie funktionelle Übungen beinhaltet. Ziel ist es, die neuroplastischen Potenziale der Nervenregeneration optimal zu nutzen und die Wiedererlangung der Handfunktion nachhaltig zu fördern.
Zusammenfassung
Die Funktionswiederherstellung bei Nervenläsion hat vielfältige Möglichkeiten. Grundsätzlich gilt „je eher, desto besser“. Natürlich erwartet oder erhofft man teilweise eine spontane Erholung nach Verletzung oder Operation. Diese trifft auch häufig ein. Allerdings sollten engmaschige klinische und technische Untersuchungen geplant sein, um das Zeitfernster der Nervenwiederherstellung nicht zu verpassen. Wenn der Schaden schon sehr ausgeprägt und/oder lange zurückliegt, dann kommen noch Ersatzverfahren wie Sehnen- und/oder Muskelumlagerungen bzw. ein freier mikrochirurgischer Muskeltransfer infrage.
Literatur:
1 Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF). S3-Leitlinie 005/010: Versorgung peripherer Nervenverletzungen 2023 2 Ballance CA et al.: Remarks on the operative treatment of chronic facial palsy of peripheral origin. BMJ 1903; 1(2209): 1009-13 3 Boyd KU et al.: Nerve reconstruction in the hand and upper extremity. Clin Plast Surg 2011; 38(4): 643-60 4 Carlsen BT et al.: Comparison of single versus double nerve transfers for elbow flexion after brachial plexus injury. Plast Reconstr Surg 2011; 127(1): 269-76 5 Cheng J, Ellison RW: Selected readings in plastic surgery. Hand: peripheral nerves and tendon transfers. 2010; 10(27) 6 Ferris S, Maciburko SJ: Partial tibial nerve transfer to tibialis anterior for traumatic peroneal nerve palsy. Microsurgery 2017; 37(6): 596-602 7 Flores LP: Comparative study of nerve grafting versus distal nerve transfer for treatment of proximal injuries of the ulnar nerve. J Reconstr Microsurg 2015; 31(9): 647-653 8 García-López A et al.: Nerve transfers from branches to the flexor carpi radialis and pronator teres to reconstruct the radial nerve. J Hand Surg Am 2014; 39(1): 50-56 9 Giuffre JL, Bishop AT, Spinner RJ et al.: Partial tibial nerve transfer to the tibialis anterior motor branch to treat peroneal nerve injury after knee trauma. Clin Orthop Relat Res 2012; 470(3): 779-90 10 Goubier JN, Teboul F: Rhomboid nerve transfer to the suprascapular nerve for shoulder reanimation in brachial plexus palsy: a clinical report. Hand Surg Rehabil 2016; 35(5): 363-366 11 Koshima I et al.: Deep peroneal nerve transfer for established plantar sensory loss. J Reconstr Microsurg 2003; 19(7): 451-54 12 Koshy JC, Agrawal NA, Seruya M: Nerve transfer versus interpositional nerve graft reconstruction for posttraumatic, isolated axillary nerve injuries: a systematic review. Plast Reconstr Surg 2017; 140(5): 953-60 13 Koopman J et al.: A systematic review and meta-analysis on the use of fibrin. J Plast Reconstr Aesthet Surg 2022; 75(3): 1018-33 14 Kovachevich R, Kircher MF, Wood CM et al.: Complications of intercostal nerve transfer for brachial plexus reconstruction. J Hand Surg Am 2010; 35(12): 1995-2000 15Kretschmer T, Antoniadis G, Assmus H: Nervenchirurgie. S 95 ff. Berlin: Springer, 201316 Lee SK, Wolfe SW: Nerve transfers for the upper extremity: new horizons in nerve reconstruction. J Am Acad Orthop Surg 2012; 20(8): 506-17 17 Mackinnon SE, Colbert SH: Nerve transfers in the hand and upper extremity surgery. Tech Hand Up Extrem Surg 2008; 12(1): 20-33 18 Mackinnon SE et al.: Results of reinnervation of the biceps and brachialis muscles with a double fascicular transfer for elbow flexion. J Hand Surg Am 2005; 30(5): 978-85 19 Moore AM et al.: Femoral nerve transfers for restoring tibial nerve function: an anatomical study and clinical correlation: a report of 2 cases. J Neurosurg 2018; 129(4): 1024-33 20 Oberlin C et al.: Nerve transfer to biceps muscle using a part of ulnar nerve for C5–C6 avulsion of the brachial plexus: anatomical study and report of four cases. J Hand Surg Am 1994; 19(2): 232-37 21 Ruijs AC et al.: Median and ulnar nerve injuries: A meta-analysis of predictors of motor and sensory recovery after modern microsurgical nerve repair. Plast Reconstr Surg 2005; 116: 484-94 22 Schünke M et al.: Anatomie: Duale Reihe. 1. Aufl. Stuttgart: Thieme, 2010: 66 23 Sunderland S: A classification of peripheral nerve injuries producing loss of function. Brain 1951; 74(4): 491-516 24 Tung TH et al.: Obturator nerve transfer for femoral nerve reconstruction: anatomic study and clinical application. Plast Reconstr Surg 2012; 130(5): 1066-74 25 Tung TH, Mackinnon SE: Nerve transfers: indications, techniques, and outcomes. J Hand Surg Am 2010; 35(2): 332-41 26 Wolfe SW et al.: Green’s Operative Hand Surgery. 6th ed Philadelphia: Elsevier, 2011 27 Waller A: Experiments on the section of the glossopharyngeal and hypoglossal nerves of the frog, and observations of the alterations produced thereby in the structure of the primitive fibres. Philos Trans R Soc Lond 1850; 140: 423-29 28 Zheng MX et al.: Phrenic nerve transfer for elbow flexion and intercostal nerve transfer for elbow extension. J Hand Surg Am 2010; 35(8): 1304-9
Das könnte Sie auch interessieren:
Orthopädisches Management des erworbenen Fallfußes
Als komplexes Problem erfordert das Management des Fallfußes einen interdisziplinären Zugang mit individuellen Therapieansätzen, abhängig von der Ursache, Schwere, Lokalisation, von ...
Behandlung von periprothetischen Gelenkinfektionen einer Hüft- oder Knie-Totalendoprothese
Der Wechsel der mobilen Teile, im Englischen als DAIR (Debridement, Antimicrobial Therapy, and Implant Retention) bezeichnet, stellt eine etablierte Option zur Behandlung ...
Behandlungspfad bei azetabulären Defekten in der Revisionsendoprothetik
Revisionseingriffe aufgrund azetabulärer Knochendefekte nach Hüfttotalendoprothesen stellen eine große Herausforderung dar. Einestrukturierte Diagnostik und Einteilung sowie ein ...