BRCA-Mutationen: Screening und Management bei PCa
Bericht:
Mag. Dr. Anita Schreiberhuber
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Neben anderen Tumorentitäten können BRCA1/2-Mutationen auch mit der Entwicklung eines Prostatakarzinoms assoziiert sein.Internationale Leitlinien geben unterschiedliche Empfehlungen für das Screening und Management von Risikopersonen. Zudem besteht auch ein dringlicher Bedarf an einem personalisierten Ansatz, für den auch in den nächsten Jahren keine umfassenden Daten vorliegen werden.
Keypoints
-
BRCA2-Mutationsträgerhabenim Vergleich zu BRCA1-Mutationsträgernein erhöhtes Risiko für aggressivere PCa und eine erhöhte PCa-spezifische Mortalität.
-
Während NCCN wie auch EAU BRCA2-Mutationsträgern eine frühe PSA-Messung (ab 40) empfehlen, wird sie BRCA1-Mutationsträgern nur vom NCCN empfohlen.
-
PARP-Inhibitoren stellen nach wie vor einen Meilenstein in der Therapie von Patienten mit BRCAm dar.
-
Den BRCA-Status vor Brustkrebsdiagnose zu kennen ist mit einem signifikant verlängerten OS assoziiert.
Assoziation BRCA1/2-Mutationen – Prostatakarzinom
Mutationen in den Tumorsuppressorgenen BRCA1 und 2 (BRCA1/2m) sind mit einem 2- bis 4-fach erhöhten Prostatakarzinom(PCa)-Risiko im Vergleich zur allgemeinen männlichen Population assoziiert. Dabei habenBRCA2-Mutationsträgerim Vergleich zu BRCA1-Mutationsträgern ein höheresRisiko für die Entwicklung von aggressiveren Prostatakarzinomen mit höhergradigen Krankheitsstadien bei Diagnose, die mit einem aggressiveren Krankheitsverhalten und einer höheren PCa-spezifischen Mortalität einhergehen.1
Screening bei Risikopersonen
Wer sollte demnach auf das Vorliegen einer BRCAm gescreent werden? Die Leitlinien des NCCN (National Comprehensive Cancer Network) empfehlen eine Testung bei relevanten Hochrisikopopulationen zu erwägen, wenn das Outcome wahrscheinlich einen Einfluss auf das Risikomanagement oder die Therapie der Betroffenen haben wird. Die Hochrisikopopulation umfasst u.a. jene Personen, bei denen in persönlicher bzw. Familienanamnese ein PCa oder Karzinom (Ca) der Brust, der Ovarien oder des Pankreas diagnostiziert worden ist, insbesondere, wenn die Diagnose in jungem Alter gestellt worden ist und/oder eine aggressive Tumorvariante vorgelegen ist.2
Bislang sind >50 Studien zur Prävalenz von BRCA1/2m bei PCa-Patienten publiziert worden. Demnach weisen PCa-Patienten im Allgemeinen eine BRCA1/2m-Prävalenz von von 1–2% auf, bei jenen mit aggressivem oder metastasiertem PCa liegt die Prävalenz bei 4–13%.3,4
Während sowohl die NCCN- als auch die EAU(European Association of Urology)-Leitlinien bei BRCA2-Mutationsträgern ab 40 Jahren ein Screening in Form einer PSA(Prostata-spezifisches Antigen)-Messung empfehlen, sollte diese gemäß NCCN bei BRCA1-Mutationsträgern in Erwägung gezogen werden. Gemäß der EAU wird bei bei BRCA1-Mutationsträgern keine frühe PSA-Bestimmung empfohlen.5,6
In der IMPACT-Studie wurden die Effekte eines konsekutiven PSA-Screenings bei Männern zwischen 40 und 69 Jahren mit BRCA1/2m in der Keimbahn (gBRCAm) und Kontrollen untersucht. Ab einem PSA-Spiegel >3ng/ml wurde den Männern eine Biopsie angeboten. Im Zeitraum von 3 Jahren wurde bei 31 von 919 Männern mit gBRCA1m und bei 47 von 902 Männern mit gBRCA2m ein PCa diagnostiziert. Demgegenüber lagen PCa-Diagnosen bei Nicht-gBRCA1-bzw.Nicht-gBRCA2-Trägern in 19 von 709 bzw. 15 von 497 Fällen vor. Die PCa-Inzidenzrate pro 1000 Personen war bei gBRCAm-Trägern signifikant höher als bei Nicht-Trägern (19,4% vs. 12,0%; p=0,03).7
In einer weiteren Studie wurde bei gBRCA1/2m-Trägern (n=188; Alter: 40–70 Jahre) zusätzlich zur PSA-Testung ein multiparametrisches MRI (mpMRI) der Prostata durchgeführt. 110 Männer hatten entweder erhöhte PSA-Werte (40%), eine verdächtige Läsion im MRI (36%) oder beides (17%). Von diesen stimmten 92 (85%) einer Prostatabiopsie zu. Bei 16 Männern (8,5%) wurde ein PCa diagnostiziert und davon wurde der Tumor bei 44% als intermediär oder Hochrisiko eingestuft. Die Entscheidungskurvenanalyse zeigte, dass die Durchführung eines mpMRI unabhängig von der PSA-Bestimmung mit dem höchsten Nettobenefit einer PCa-Diagnose einherging, insbesondere bei Männern <55 Jahre. Die Autoren zogen den Schluss, dass junge gBRCAm1/2-Träger vom MRI-Screening profitieren könnten, und raten an, dass Träger >55 Jahre im Fall eines erhöhten PSA-Werts einer mpMRI-Untersuchung zugewiesen werden sollen.8
Management von BRCA1/2m-Trägern und Patienten mit Niedrigrisiko-PCa
Während die NCCN-Leitlinien im Fall von BRCA2meine radikale Therapie empfehlen, raten die EAU-Leitlinien bei BRCA1mund 2m zu einer aktiven Überwachung („active surveillance“; AS).5,6 Nicht nur Mutationen in BRCA1/2, auch solche in ATM – ebenfalls ein Gen, das zu den DNA-Reparaturgenen zählt – sind mit aggressiveren PCa assoziiert. Dies wurde auch in einer Untersuchung zur AS bei diesem Kollektiv bestätigt: Bei 289 von 1211 Patienten musste eine Reklassifikation des Gleason-Scores im Sinne eines Upgrades vorgenommen werden.9 Mit Einführung der PARP(Polyadenosin-Diphosphat-Ribose-Polymerase)-Inhibitoren (PARP-I) war ein Meilenstein in der Therapie von Patienten mit BRCAm erzielt worden. Olaparib wurde 2014 als erster PARP-I für Patientinnen mit BRCAm-Ovarialkarzinom zugelassen.10 Im Rahmen der Phase-III-Studie PROfound wurde die Substanz an Patienten mit metastasiertem kastrationsresistentem PCa (mCRPC) vs. Therapie nach Wahl des Prüfarztes (TPC; Enzalutamid oder Abirateron) untersucht. Unter einer neuen hormonellen Therapie hat sich eine Progression entwickelt. Dabei konnte eine signifikante Überlegenheit vs. TPC im progressionsfreien Überleben (PFS; 7,4 vs. 3,6 Monate; HR: 0,34; p <0,001) und im Gesamtüberleben im Ausmaß von 19,1 gegenüber 14,7 Monaten erzielt werden (HR: 0,69; p=0,02).11 In der Phase-III-Studie Propel wurde Olaparib in Kombination mit Abirateron vs. Abirateron + Placebo bei Patienten mit mCRPC als Erstlinientherapie untersucht. Auch hier wurde eine signifikante Überlegenheit im primären Endpunkt, dem PFS basierend auf der Bildgebung (ibPFS), verzeichnet: Das mediane ibPFS lag bei 24,8 vs. 16,6 Monate (HR: 0,66; p <0,001).12 In beiden Settings ist Olaparib inzwischen von der EMA (European Medicines Agency) zugelassen.10 Auch für Niraparib13 und Rucaparib14 wurde eine Antitumoraktivität nachgewiesen, beide Substanzen haben jedoch bislang keine EMA-Zulassung erhalten. Weitere Studien zu PARP-Inhibitoren bei PCa (z.B. AMPLITUDE [NCT04497844] zu Niraparib + Abiraterone) sind im Gange.
Weitere BRCAm-assoziierte Karzinome
Bei anderen bekannten mit BRCAm assoziierten Karzinomen – dem Ovarial-, Mamma- und Pankreaskarzinom – ist die genetische Testung weitgehend implementiert. Momozawa et al. haben untersucht, ob eine Assoziation von pathogenen BRCA1- und 2-Varianten in weiteren häufigen 14 Tumorentitäten besteht. Dafür haben sie 63828 Patienten untersucht und dabei ein erhöhtes Risiko auch für die Entwicklung von Gallengangs-, Ösophagus- und Magenkarzinomen identifiziert.15 Zu ähnlichen Ergebnissen sind auch Li et al. gekommen.16
Oftmals werden Personen mit BRCAm erst im Zuge einer Krebsdiagnose identifiziert. Gesunde Mutationsträger, die ihren BRCA-Status nicht kennen, können demnach auch nicht die empfohlenen Screeninguntersuchungen und prophylaktischen Operationen (bilaterale Ovarektomie bzw. risikoreduzierende bilaterale Mastektomie [RRBM]) wahrnehmen. Basierend auf der Hypothese, dass die Kenntnis des BRCA-Status bei Trägern vor der Krebsdiagnose zu einem Downstaging bei Diagnose führen würde, wurde eine entsprechende retrospektive Untersuchung an 105 BRCAm-Frauen durchgeführt.17 Davon wussten 42 vor der Diagnose (BRCA-präDX-Trägerinnen) und der Rest erst nach Brustkrebsdiagnose (BC; BRCA-postDx-Trägerinnen) über ihre BRCA-Mutation Bescheid.17 40 der 42 BRCA-präDX-Trägerinnen nahmen an einem Hochrisikoscreeningprogramm teil.17 Tatsächlich wurden sie in signifikantem Ausmaß häufiger mittels MRI diagnostiziert und wiesen dabei ein duktales Carcinoma in situ oder ein invasives BC niedrigeren Grades auf.17 Trotz Diagnose in einem früheren Stadium entschieden sich mehr BRCA-präDX-Trägerinnen als primäre Operation für eine RRBM, als dies bei BRCA-postDX-Trägerinnen der Fall war.17
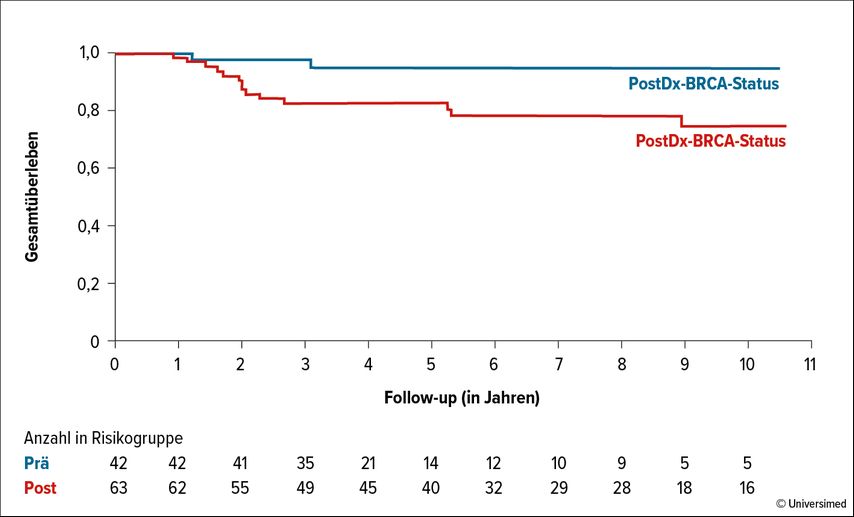
Insgesamt war die Gewissheit über den Genotyp vor der BC-Diagnose mit einem signifikant längeren Gesamtüberleben (OS) assoziiert.17 Zu den Faktoren, die bei BRCA-präDx- vs. BRCA-post-Dx-Trägerinnen mir einem längeren OS assoziiert waren,zählten ein höherer sozioökonomischer Status, die genetische Variante (BRCA2 vs. BRCA1) und das Alter bei Diagnose (Abb. 1).17
Abb. 1: Gewissheit über den BRCA-Status vor der BC-Diagnose ist mit einem signifikant besseren Gesamtüberleben assoziiert (nach Hadar T et al. 2020)17
Wie sieht es nun analog dazu beim PCa bei BRCA2-Mutationsträgern bezüglich einer präventiven Prostatektomie aus? Bestrebungen dazu, dies im Rahmen von klinischen Untersuchungen zu prüfen, sind im Gange.18 „Obwohl in einigen Studien für dieses Kollektiv ein aggressiverer Krankheitsverlauf und eine hohe PCa-assoziierte Mortalität nachgewiesen worden ist, konnte bis jetzt nicht gezeigt werden, dass ein Screening mit anschließender früher Therapie zur OS-Verlängerung oder Verbesserung der Lebensqualität geführt hat. Bislang wissen wir also nicht, ob eine prophylaktische Prostatektomie ein vernünftiger Ansatz ist“, fasste DDr. Pawel Rajwa, Medizinische Universität von Silesia, Zabrze, Polen, zusammen. Als bedauerlich erwähnte er, dass zwar der Bedarf an einem rationalen personalisierten Ansatz für BRCA1/2-Mutationsträger besteht, jedoch innerhalb der nächsten Jahre nicht mit Langzeitdaten zum optimalen Management und OS bei Vorliegen von BRCA1/2m zu rechnen ist.
Quelle:
„Prostate cancer risk, screening and management in patients with BRCA1/2 mutations“; Vortrag von DDr. Pawel Rajwa im Rahmen des CUO (Controversies in Urologic Oncology) Scientific Meeting am 14. und 15. April 2023 in Wien
Literatur:
1 Rajwa P et al.: Prostate cancer risk, screening and management in patients with germline BRCA1/2 mutations. Nat Rev Urol 2023; 20(4): 205-16 2 Daly MB et al.: NCCN Guidelines for genetic/familial high-risk assessment: Breast, ovarian, and pancreatic.J Natl Compr Canc Netw 2021; 19(1): 77-102 3 Pritchard CC et al.: Inherited DNA-repair gene mutations in men with metastatic prostate cancer. N Engl J Med 2016; 375(5): 443-53 4 Oh M et al.: The association of BRCA1 and BRCA2 mutations with prostate cancer risk, frequency, and mortality: A meta-analysis. Prostate 2019; 79(8): 880-95 5 Schaeffer EM et al.: NCCN Guidelines Prostate Cancer V. 1.2023. https://jnccn.org/configurable/content/journals$002fjnccn$002f20$002f12$002farticle-p1288.xml?t:ac=journals%24002fjnccn%24002f20%24002f12%24002farticle-p1288.xml ; zuletzt aufgerufen am 11.5.2023 6 Mottet N et al.: EAU Guidelines Prostate Cancer 2023. https://d56bochluxqnz.cloudfront.net/documents/full-guideline/EAU-EANM-ESTRO-ESUR-ISUP-SIOG-Guidelines-on-Prostate-Cancer-2023_2023-03-27-131655_pdvy.pdf ; zuletzt aufgerufen am 5.5.2023 7 Page EC et al.: Interim results from the IMPACT study: Evidence for prostate-specific antigen screening in BRCA2 mutation carriers. Eur Urol 2019; 76: 831-42 8 Segal N et al.: Imaging-based prostate cancer screening among BRCA mutation carriers-results from the first round of screening. Ann Oncol 2020; 31(11): 1545-52 9 Carter HB et al.: Germline mutations in ATM and BRCA1/2 are associated with grade reclassification in men on active surveillance for prostate cancer. Eur Urol 2019; 75(5): 743-49 10 European Medicines Agency: Lynparza. https://www.ema.europa.eu/en/medicines/human/EPAR/lynparza . zuletzt aufgerufen am 11.5.2023 11 De Bono J et al.: Olaparib for metastatic castration-resistant prostate cancer. N Engl J Med 2020; 382(22): 2091-102 12 Clarke NW et al.: Abiraterone and Olaparib for metastatic castration-resistant prostate cancer. N Engl J Med Evid 2022; 1(9): doi:10.1056/EVIDoa2200043 13 Smith MR et al.: Niraparib in patients with metastatic castration-resistant prostate cancer and DNA repair gene defects (GALAHAD): A multicentre, open-label, phase 2 trial. Lancet Oncol 2022; 23(3): 362-73 14 Abida W et al.: Rucaparib in men with metastatic castration-resistant prostate cancer harboring a BRCA1 or BRCA2 gene alteration. J Clin Oncol 2020; 38(32): 3763-72 15 Momozawa Y et al.: Expansion of cancer risk profile for BRCA1 and BRCA2 pathogenic variants. JAMA Oncol 2022; 8(6): 871-78 16 Li S et al.: Cancer risks associated with BRCA1 and BRCA2 pathogenic variants. J Clin Oncol 2022; 40(14): 1529-41 17 Hadar T et al.: Presymptomatic awareness of germline pathogenic BRCA variants and associated outcomes in women with breast cancer. JAMA Oncol 2020; 6(9): 1460-63 18Clark Ret al.: A Clinical trial of prophylactic prostatectomy for BRCA2 mutation carriers: Ist now the time? Eur Urol Focus 2021; 7(3): 506-7
Das könnte Sie auch interessieren:
Der Weg von neoadjuvanter Therapie und radikaler Zystektomie hin zum Blasenerhalt
Beim diesjährigen Post EAU 2025 Meeting in Wien präsentierte Dr. Kilian Gust, FEBU (Medizinische Universität Wien), ein aktuelles Update zur systemischen Therapie des muskelinvasiven ...
Highlights zum Prostatakarzinom vom EAU in Madrid
Zahlreiche im Rahmen des EAU-Kongresses 2025 in Madrid vorgestellte Arbeiten beschäftigten sich mit Diagnostik und Management des Prostatakarzinoms in allen Stadien der Erkrankung. So ...
Neues zur Li-ESWT in der Therapie der ED
Zwei Arbeiten zeigen den praktischen Einsatz der extrakorporalen Stoßwellentherapie mit niedriger Intensität (Li-ESWT; „low-intensity extracorporal shockwave therapy“) in der Therapie ...