Klinische Faktoren und respiratorische Medikation bei COPD
Autoren:
Prof.Dr. Peter Alter
Klinik für Innere Medizin, Pneumologie und Intensivmedizin
Philipps-Universität Marburg
E-Mail: palter@med.uni-marburg.de
PD Dr.rer.nat. Rudolf A. Jörres
Institut und Poliklinik für Arbeits-, Sozial- und Umweltmedizin
Klinikum der Universität München
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In der nicht-interventionellen COPD-Kohorte COSYCONET wurde der Gebrauch der COPD-Dauermedikation untersucht. Es zeigte sich, dass die respiratorische Therapie in dieser realitätsnahen Kohorte im Wesentlichen konsistent mit gängigen nationalen und internationalen Empfehlungen war.
Keypoints
-
Die Auswahl der respiratorischen Medikation wird wesentlich vom spirometrischen GOLD-Grad und von der GOLD-Gruppe bestimmt.
-
Die LAMA-haltige Medikation hat in den letzten Jahren deutlich zugenommen.
-
Die Studie zeigt, dass Geschlecht, aktives Rauchen und Komorbiditäten wie Asthma und Diabetes mellitus eine Rolle spielen.
Hintergrund
Die COPD ist aufgrund ihrer hohen weltweiten Prävalenz und einer oft gravierenden individuellen Erkrankungsschwere mit einem erheblichen sozioökonomischen Ressourceneinsatz verbunden.1 Neben den Basismaßnahmen wie einer Karenz vom Zigarettenrauchen – als mit Abstand häufigster und am schwersten wiegender Ursache der COPD – besteht die medikamentöse Therapie im Wesentlichen aus inhalativen Bronchodilatatoren und Kortikosteroiden.2
Es gibt eine Reihe von Therapieempfehlungen unter Berücksichtigung individueller klinischer und funktioneller Charakteristika der Patienten, welche in der Regel auf randomisierte kontrollierte Therapiestudien („randomized controlled trials“, RCT) mit genau definierten und selektierten Patientengruppen zurückgehen. Viele Studien haben allerdings gezeigt, dass diese Studienbedingungen nur bedingt auf die Lebenswirklichkeit, d.h. Real-Life-Bedingungen, übertragbar sind.3 Gerade unter diesen – letztlich relevanten – Umständen dürften beispielsweise Komorbiditäten für Verlauf, Prognose und Schwere der Erkrankung eine nicht unerhebliche Rolle spielen.4 Von RCT sind solche Patienten häufig ausgeschlossen, oder es wird nur eine gezielte Fragestellung behandelt, welche nicht das breite Spektrum an Patienten, wie es realiter zu finden ist, widerspiegelt.
Daher schien es uns interessant, Daten der Beobachtungsstudie COSYCONET, die ein sehr breites Spektrum an Patienten umfasst, dahingehend zu untersuchen, welche Assoziationen zwischen deren klinischen Charakteristika und ihrer respiratorischen Medikation bestehen. Hierbei lag der Fokus darauf, möglichst nur einfach zugängliche Parameter zu verwenden, die den behandelnden Ärzten auch außerhalb einer Studie in der Regel zur Verfügung stehen oder leicht stehen könnten.
Ergebnisse der COSYCONET-Kohorte
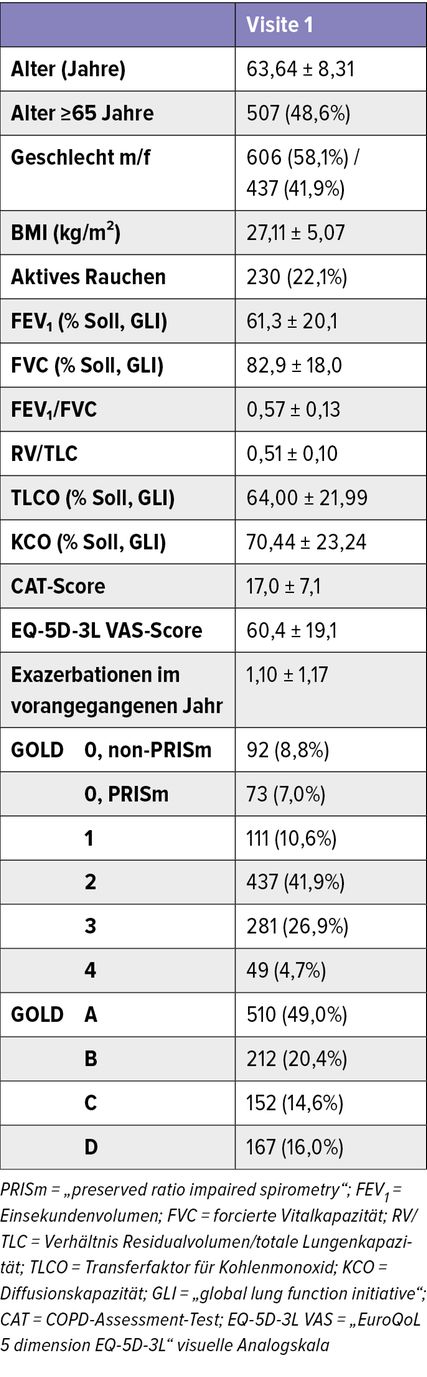
COSYCONET (COPD and Systemic Consequences-Comorbidities Network) ist eine Langzeitkohorte von Patienten mit COPD.5 Es handelt sich um eine reine Beobachtungsstudie, d.h., es gibt keine studienbedingten Interventionen. COSYCONET begann die Rekrutierung im Jahre 2010, und es wurden bis Ende 2013 insgesamt 2741 Patienten in Visite 1 eingeschlossen. Die erste Nachfolgevisite erfolgte nach 6 Monaten, die nächste 12 Monate später, sodann weitere in Abständen von jeweils 18 Monaten, von denen die ersten beiden in die Analyse eingeschlossen wurden (Visiten 1–5, Beobachtungszeitraum 4,5 Jahre). Die Patienten wurden u.a. anhand anthropometrischer Daten und anamnestischer Angaben, spirometrischer und ganzkörperplethysmografischer Messungen sowie der Diffusionskapazität der Lunge, Komorbiditäten, der Symptome sowie einer Vielzahl weiterer Erhebungen charakterisiert, und die Medikation wurde im Detail erfasst. Diese Erhebungen erfolgten bei jeder Visite, sodass der Langzeitverlauf beurteilt werden konnte.
In die nachfolgenden Analysen6 wurden Patienten der spirometrischen Schweregrade 1 bis 4 nach GOLD1 eingeschlossen, ferner auch Patienten der früheren Gruppe GOLD 07, welche nicht das Obstruktionskriterium eines reduzierten Tiffeneau-Quotienten <0,7 erfüllten. Diese wurden weiter unterteilt in Patienten mit einer eingeschränkten Einsekundenkapazität (FEV1 <80% Soll), bezeichnet als PRISm („preserved ratio impaired spirometry“), und solche ohne diese funktionelle Einschränkung, bezeichnet als „non-PRISm“.8 Dies resultierte in Daten von 1043 Patienten, welche an den Visiten 1 bis 5 teilnahmen (Tab. 1).6 Untersucht wurden statistische Prädiktoren der respiratorischen Medikation, welche inhalative Kortikosteroide (ICS), lang wirksame Beta-2-Agonisten (LABA), lang wirksame Muskarinantagonisten (LAMA) sowie gängige Kombinationen hieraus, insgesamt 6 Kategorien, umfasste. Die Häufigkeit dieser respiratorischen Medikation im Verlauf über die Visiten ist in Abbildung 1 dargestellt.6
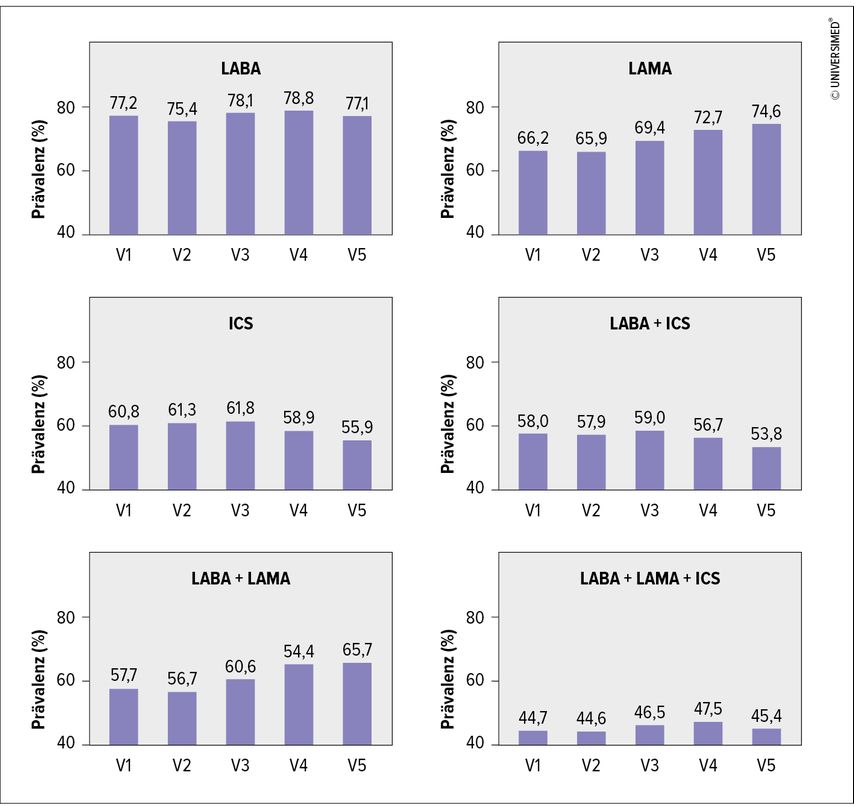
Abb. 1: Prävalenz der respiratorischen Dauermedikation bei den COSYCONET-Visiten (V) 1 bis 5 (modifiziert nach Alter P et al. 2023)6
Im Mittel hatten ca. 77% der Patienten ein LABA-Präparat, und es zeigte sich kein wesentlicher Trend über die Visiten hinweg. Ein ICS fand sich bei ca. 60% der Patienten, mit einer leichten Abnahme von Visite 3 zu Visite 5. Im Gegensatz dazu fand sich im Beobachtungszeitraum eine deutliche Zunahme der LAMA-Medikation, im Mittel war diese bei ca. 70% der Patienten zu finden. Ein ähnliches Bild ergab sich für Kombinationstherapien. Die duale Bronchodilatation mit LABA und LAMA nahm während des Beobachtungszeitraums deutlich zu.
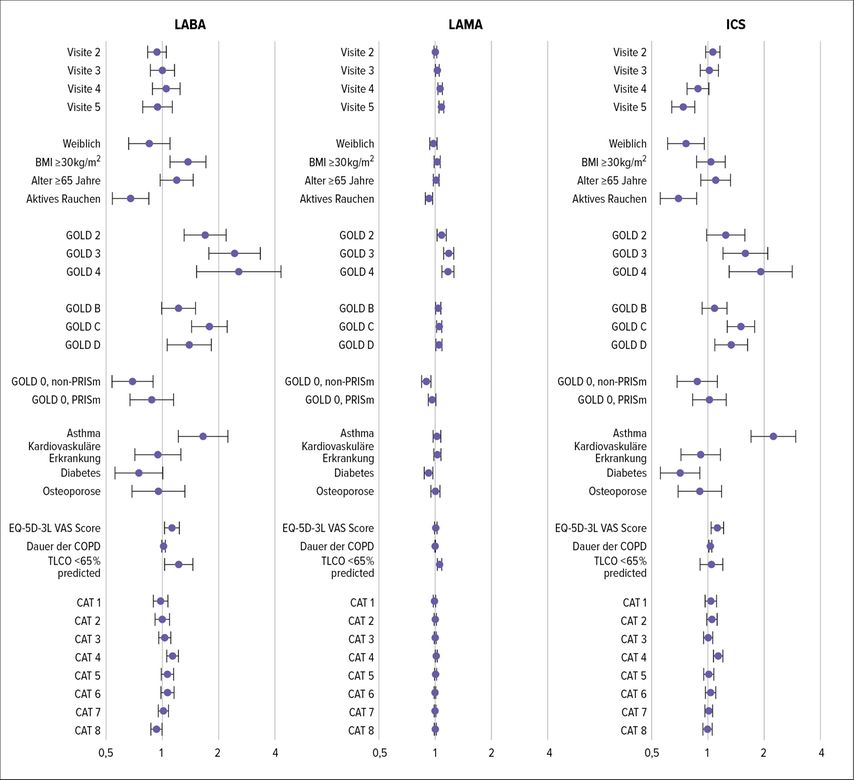
Multivariable Analysen („generalized linear models“, „repeated measures design“ mit Logit-Link), welche äquivalent zu longitudinalen logistischen Regressionsanalysen sind, wurden eingesetzt, um Beziehungen zwischen Prädiktoren und der Medikation im Querschnitt und Verlauf zu analysieren (Abb. 2).6
Abb. 2a: Odds Ratios (und 95%-Konfidenzintervalle) für Prädiktoren der Medikation (modifiziert nach Alter P et al. 2023)6
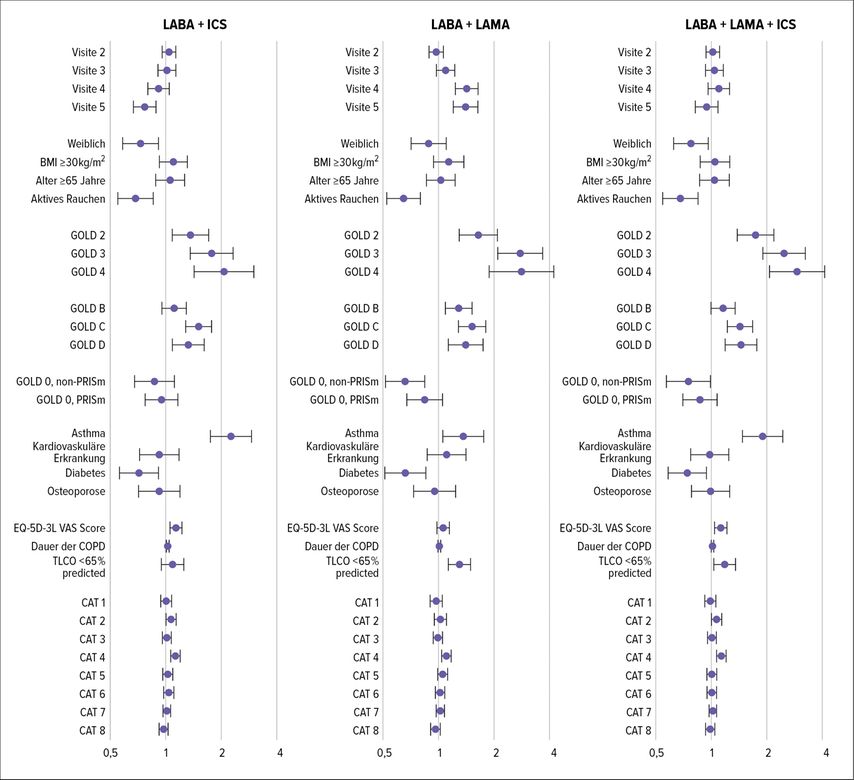
Abb. 2b: Odds Ratios (und 95%-Konfidenzintervalle) für Prädiktoren der Medikation (modifiziert nach Alter P et al. 2023)6
Hierbei zeigt sich, dass die Therapie mit LABA, LAMA oder ICS sowie deren Kombinationen vom spirometrischen Schweregrad der COPD abhängig waren. Patienten der PRISm-Subgruppe aus GOLD 0 hatten eine ähnliche Medikation wie GOLD-1-Patienten, wohingegen Non-PRISm-Patienten weniger respiratorische Therapie hatten. Ferner hatten Patienten der GOLD-Gruppen C und D (inzwischen zu Gruppe E vereint), d.h. solche mit höherem Exazerbationsrisiko, mehr Medikation.
Weitere Ergebnisse und deren Interpretation
-
Das weibliche Geschlecht war mit einer geringeren Rate ICS-haltiger Therapien assoziiert, was vermutlich der Annahme eines erhöhten Osteoporoserisikos geschuldet sein dürfte.
-
Ein erhöhter Body-Mass-Index war mit einem vermehrten LABA-Einsatz verbunden, was am ehesten auf vermehrte Symptome dieser Patienten aufgrund einer zusätzlichen Komponente der Atemwegsobstruktion durch Adipositas zurückzuführen sein dürfte.
-
Aktives Rauchen war durchgängig mit einer geringeren Rate an respiratorischer Medikation verbunden. Da Effekte der respiratorischen Medikation bei Rauchern bekanntermaßen geringer sind, hätte man auch das Gegenteil erwarten können, um dies zu kompensieren. Eine mögliche Erklärung könnte sein, dass die Aktivraucher geringere COPD-Schweregrade hatten; da allerdings für den Schweregrad adjustiert wurde, ist dies eher unwahrscheinlich. Ferner ist auch nicht anzunehmen, dass Raucher die Medikation von sich aus vermehrt ablehnten. Die wahrscheinlichste – und mit klinischer Erfahrung konkordante – Erklärung könnte darin liegen, dass das Verschreibungsverhalten der behandelnden Ärzte bei aktiven Rauchern zurückhaltender war.
-
Patienten mit einer reduzierten Diffusionskapazität als Ausdruck eines Lungenemphysems hatten vermehrt Bronchodilatatoren, vor allem LAMA. Hier scheinen die Diagnose oder Symptomatik des Emphysems ein Trigger zu sein.
-
Lag ein Asthma als Komorbidität vor, so bestand eine Assoziation mit einer vermehrten ICS-Therapie, was klinisch gut begründet und daher nicht überraschend war.
-
Das Vorliegen eines Diabetes mellitus war mit einer geringeren Medikation vergesellschaftet. Dies lässt sich, vor allem in Anbetracht der multiplen Adjustierungen, mit den vorliegenden Daten nicht hinreichend erklären und bedarf weiterer Analysen.
-
Es wurde eine Reihe von etablierten Fragebögen zu Erkrankungssymptomen und Lebensqualität in die Analyse eingeschlossen. Die meisten Medikationskategorien waren mit einer besseren Lebensqualität vergesellschaftet. Von den acht Einzelfragen des etablierten COPD-Assessment-Tests (CAT) war lediglich Frage #4 nach belastungsabhängiger Dyspnoe beim Treppensteigen oder Bergangehen stabil mit allen Medikationskategorien vergesellschaftet. Dies verweist darauf, dass dieser Fragebogen nicht in allen Fragen gleich relevant war und für klinische Zwecke womöglich kondensiert werden könnte.
Zusammenfassung und Schlussfolgerung
Die Untersuchungen zeigten einen zunehmenden LAMA-Einsatz über die Jahre von 2010 bis 2018. Wie erwartet waren höhere GOLD-Grade und -Gruppen mit mehr Medikation verbunden. Aktives Rauchen und das Vorhandensein eines Diabetes mellitus waren mit weniger Medikation assoziiert und das weibliche Geschlecht mit weniger ICS. Obwohl die GOLD-Kategorien wesentliche Determinanten der Medikationsauswahl zu sein scheinen, spielen offenbar weitere Patientencharakteristika, spezifische Symptome und belastungsabhängige Beschwerden eine weitere therapierelevante Rolle.
Ob künftige Empfehlungen in dieser Hinsicht verfeinert werden können, bleibt zu untersuchen.
Literatur:
1 Vogelmeier CF et al: Global Strategy for the diagnosis, management and prevention of chronic obstructive lung disease 2017 Report. GOLD Executive Summary. Am J Respir Crit Care Med 2017; 195: 557-82 2 Singh D et al.: Global Strategy for the diagnosis, management and prevention of chronic obstructive lung disease: the GOLD science committee report 2019. Eur Respir J 2019; 53 3 Graf J et al.: Medical treatment of COPD. Dtsch Arztebl Int 2018; 155: 599-605 4 Glaab T et al.: National survey of guideline-compliant COPD management among pneumologists and primary care physicians. COPD 2006; 3:141-8 5 Karch A et al: The German COPD cohort COSYCONET: Aims, methods and descriptive analysis of the study population at baseline. Respir Med 2016; 114: 27-37 6 Alter P et al: Clinical factors linked to the type of respiratory medication in COPD: Results from the COSYCONET cohort. Ther Adv Respir Dis 2023; 17: 1-12 7 Pauwels RA et al.: Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: National Heart, Lung, and Blood Institute and World Health Organization Global Initiative for Chronic Obstructive Lung Disease (GOLD): executive summary. Respir Care 2001; 46: 798-825 8 Wan ES et al.: Longitudinal phenotypes and mortality in preserved ratio impaired spirometry in the COPDGene study. Am J Respir Crit Care Med 2018; 198: 1397-405
Das könnte Sie auch interessieren:
COPD: neue Leitlinie für eine bessere Patientenversorgung
Die aktualisierte S2k-Leitlinie „Fachärztliche Diagnostik und Therapie der chronisch obstruktiven Lungenerkrankung (COPD) 2026“ wurde im Februar publiziert und beim DGP-Kongress im März ...
Mit welchen Pollen man nun rechnen muss
Kälteeinbruch und Regen hatten die Pollenbelastung stark gebremst. Mit Ostern stiegen nun die Temperaturen stark und damit steigen nun die Pollenbelastungen durch Esche, Forsythie und Birke.