Dyspnoe und respiratorische Insuffizienz in der Notaufnahme
Autor:
Dr. Bernhard Benda
Gemeinsame Einrichtung für internistische Intensiv- und Notfallmedizin
Universitätsklinik für Innere Medizin I
Medizinische Universität Innsbruck
E-Mail: bernhard.benda@tirol-kliniken.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Subjektive Dyspnoe ist ein häufiges Beschwerdebild in einer internistischen Notaufnahme, bei dem Patienten ohne schwerwiegende Diagnose oft ambulant geführt werden können. Objektivierbare Dyspnoe ist ebenfalls häufig und immer ernst zu nehmen. Eine Ersteinschätzung durch erfahrenes medizinisches Personal erlaubt eine rasche Triage, bei der kritisch kranke Patienten korrekt erkannt und umgehend einer Behandlung zugeführt werden.
Keypoints
-
Die Dyspnoe ist eines der häufigsten Beschwerdebilder in der Notaufnahme.
-
Ein Patient mit respiratorischer Insuffizienz ist kritisch krank und muss sofort behandelt werden.
-
Die Behandlung muss oft auf der Grundlage einer Verdachtsdiagnose anhand klinischer Anzeichen erfolgen.
-
Die NIV-Therapie ist eine Behandlungsoption in der Notaufnahme.
-
Wenn möglich sollte die Situation mit dem Patienten besprochen und seine Wünsche erfragt werden.
Das Symptom der Atemnot (Dyspnoe) ist mit bis zu 25% eines der häufigsten Beschwerdebilder in der Notaufnahme. Dyspnoe ist primär definiert als das subjektive Gefühl einer erhöhten Atemanstrengung. Da es sich um ein subjektives Symptom handelt, werden Patienten mit dem Leitsymptom subjektive Dyspnoe (ebenso wie Patienten mit subjektiv empfundenen Brustschmerzen) häufig ohne klare Klärung der Ätiologie nach Hause entlassen.
Diagnosestellung
Wesentlich ist die Unterscheidung von einer objektivierbaren Dyspnoe, anhand von sichtbaren (Einsatz der Atemhilfsmuskulatur, Atmung mit offenem Mund, weite, aufgerissene, verängstigte Augen), hörbaren (Stridor, Giemen, Pfeifen oder Brummen) oder messbaren Parametern (Atemfrequenz, SpO2,PaO2).
Bei Patienten mit objektivierbarer Dyspnoe kann zumeist eine Diagnose gestellt werden. Diese Patienten können einen potenziell lebensbedrohlichen Verlauf entwickeln, häufig sind Vitalparameter auffällig. Ein Patient mit respiratorischer Insuffizienz ist kritisch krank, kann sich schnell verschlechtern und muss sofort behandelt werden. Oft bleibt keine Zeit für eine apparative Diagnostik und es muss auf den klinischen Verdacht hin gehandelt werden. Die Differenzialdiagnosen der Dyspnoe sind zahlreich und betreffen beinahe alle Fachgebiete. Als Arzt in der Notaufnahme sollte man die Differenzialdiagnosen, insbesondere die der akuten und objektivierbaren Dyspnoe, kennen.
Klinische Zeichen wie eine Lippenbremse bei der chronisch obstruktiven Lungenerkrankung (COPD), kalte Extremitäten bei Zentralisierung, verlängerte Rekapillarisierungszeit, hohe Atemfrequenz, gestaute Halsvenen bei Herzinsuffizienz oder auffällige Auskultationsbefunde können helfen, eine klinische Verdachtsdiagnose zu stellen. Eine auffällige Schonatmung kann auf eine Pleuritis oder Rippenfrakturen hinweisen, bei einem schlanken Phänotyp sollte an einen Pneumothorax gedacht werden.
Pulmonale Ursachen
Weltweit gesehen ist die Pneumonie die häufigste Ursache für Dyspnoe. Im deutschsprachigen Raum ist der häufigste Grund für akute Dyspnoe der „obstruktive Notfall“ – wie die akut exazerbierte COPD oder der Asthmaanfall.1,2
Die akute exazerbierte COPD wird in der Regel durch eine Infektion oder exogene Noxen ausgelöst. Je nach dem klinischen Bild des Patienten kann eine Inhalationstherapie oder eine sofortige nichtinvasive Beatmung (NIV) erforderlich sein. Die aktuellen Leitlinien empfehlen eine NIV-Therapie ab einem pH-Wert von < 7,35 und einem pCO2-Wert von > 45mmHg.3 In der Praxis trifft dies auf die Mehrzahl der COPD-Patienten zu.
Wie so oft ist die Klinik entscheidend. Ein stabiler Patient kann auch bei einem pH-Wert von <7,3 einen Inhalationsversuch mit einer Kombination aus einem kurzwirksamen Beta-2-Sympathomimetikum (SABA) und einem kurz wirksamen Muskarinrezeptor-Antagonisten (SAMA) sowie die Gabe eines systemischen Glukokortikoids erhalten. Des Weiteren zeigte eine rezente Metaanalyse, dass die adjuvante Gabe von 2g Magnesiumsulfat i.v. einen Benefit bringt.4Sollte aber keine rasche klinische Besserung eintreten, sollte frühzeitig eskaliert werden, da eine Verzögerung der NIV-Therapie eine erhöhte Rate an NIV-Versagern und eine erhöhte Mortalität nach sich zieht.5,6 Bei Angst und Stress, die häufig mit starker Dyspnoe einhergehen, kann die Gabe von intravenösem Morphium hilfreich sein.
Im Falle eines Asthmaanfalls ist auch eineInhalationstherapie mit einer SABA/SAMA-Kombination plus systemische Steroidverabreichung angezeigt. Weitere therapeutische Möglichkeiten sind eine Inhalation mit unverdünntem Adrenalin 4mg sowie die Gabe von Magnesiumsulfat 2g i.v.7
Die Pneumonie stellt die häufigste Diagnose in der Notaufnahme bei dem Beschwerdebild Dyspnoe dar.1,2 Klinisch imponieren hier Rasselgeräusche sowie eine Tachypnoe. Zur Schweregradabschätzung wird häufig der CRB-65-Score benutzt, jeweils ein Punkt pro vorliegendem Item:
-
C=„confusion“, neu aufgetretene Verwirrung
-
R=„respiratory rate“, Atemfrequenz ≥30/min
-
B=Blutdruck, systolisch <90mmHg, diastolisch ≤60mmHg
-
65=Alter ≥65
Ab einem CRB-65 von 2 sollte stationär therapiert werden.8,9
Kardiovaskuläre Ursachen
Erkrankungen des Herzens werden häufig von Dyspnoe begleitet. Die koronare Herzkrankheit (KHK) kann das Symptom der Dyspnoe in akuten Fällen als akutes Koronarsyndrom (ACS) oder in chronischen Fällen als Teil des chronischen Koronarsyndroms verursachen. Der Zusammenhang zwischen koronarer Herzkrankheit und Dyspnoe wurde von der ESC berücksichtigt und in die Berechnung der Vortestwahrscheinlichkeit für KHK einbezogen.10
Es ist die Aufgabe des Arztes in der Notaufnahme, die Diagnose schnell zu stellen und weitere Schritte wie eine Koronarangiografie einzuleiten. Das chronische Koronarsyndrom kann mit den üblichen diagnostischen Mitteln der Notaufnahme (EKG, Echokardiografie, Labor einschließlich Troponin, NT-proBNP) nicht diagnostiziert werden, aber der Patient sollte über die Möglichkeit einer KHK aufgeklärt werden, und es sollte eine weitere Abklärung über den niedergelassenen Bereich erfolgen.
Das kardiale Lungenödem ist eine Diagnose an der Schnittstelle zwischen Herz und Lunge. In diesem Fall kommt es zu einem Anstieg des hydrostatischen Drucks im Lungenkreislauf, sodass vermehrt Flüssigkeit ins Interstitium und weiter in die Alveolen gelangt. Es steht folglich weniger Austauschfläche zur Verfügung. Da der Diffusionswiderstand für O2 ca. 23-mal höher ist als für CO2, kommt es somit vorrangig zu einem Abfall von paO2. Die häufigsten Ursachen sind Linksherzinsuffizienz, Herzklappenfehlfunktion sowie die Folgen einer hypertensiven Krise. Diese Patienten präsentieren sich auskultatorisch mit feuchten, feinblasigen Rasselgeräuschen sowie Tachypnoe und können auch spastische Atemgeräusche aufweisen. Meistens sind die Patienten zentralisiert mit auffallend kühlen Extremitäten.
Ein solcher Patient ist kritisch krank und muss umgehend behandelt werden. Er benötigt Sauerstoff, Schleifendiuretika intravenös und Vasodilatatoren bei hypertensiven Werten. Wenn durch die medikamentösen Therapiemaßnahmen und die Sauerstoffgabe keine Besserung der Oxygenierung und der Klinik erreicht werden kann, sollte bei einer Atemfrequenz >25/min und einer peripheren Sauerstoffsättigung von <90% eine NIV-Therapie durchgeführt werden.11
Diese therapeutischen Schritte sollten bei dem kritisch kranken Patienten sofort eingeleitet werden, anschließend sollte die Ursache schnell ermittelt werden. Zu diesem Zweck sollten eine Blutgasanalyse, ein EKG und, wenn möglich, eine Echokardiografie durchgeführt werden. Ein Lungenschall bzw. Thoraxröntgen können die Diagnose eines Lungenödems bestätigen.
Als weitere häufige Differenzialdiagnose ist die Lungenarterienembolie zu nennen, die sich sehr heterogen präsentieren kann – von einem leicht symptomatischen Patienten mit geringer Belastungsdyspnoe bis hin zum Patienten, der unter Reanimation in die Notaufnahme gebracht wird.
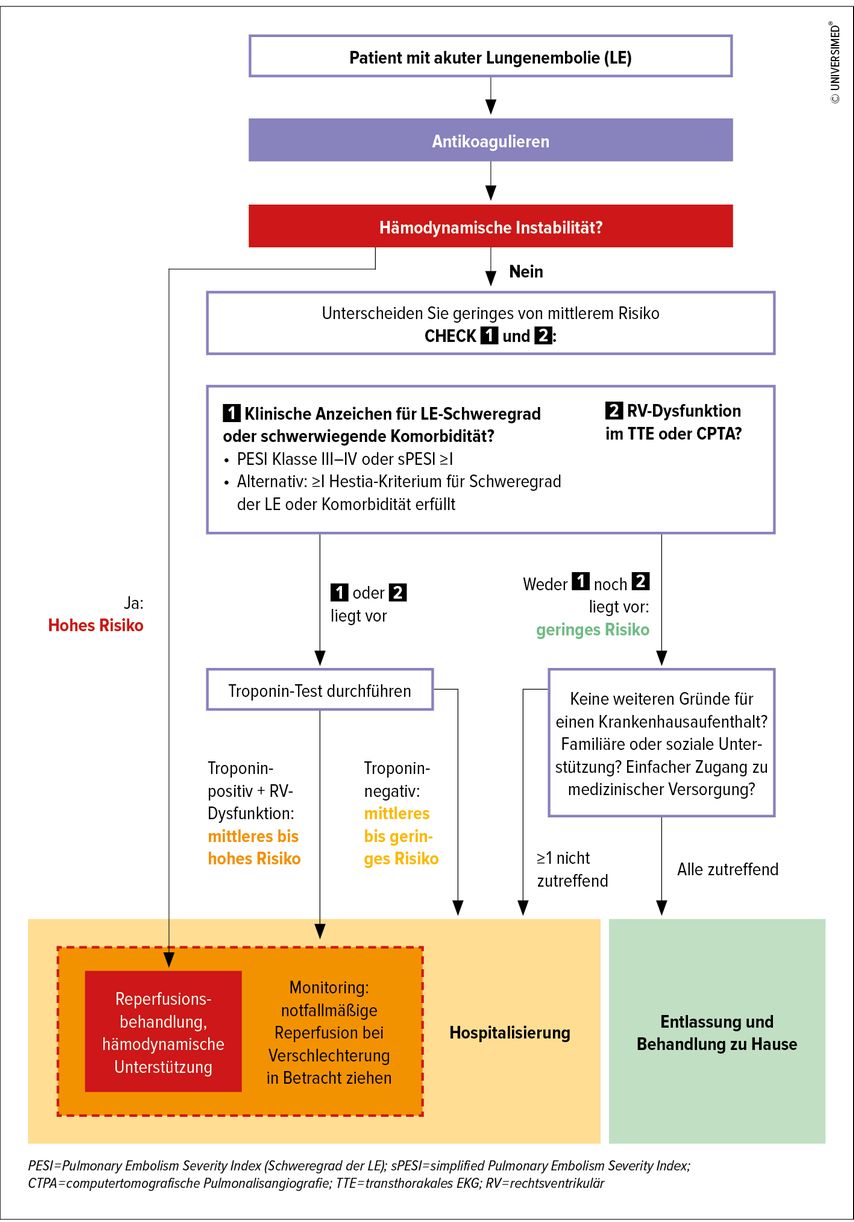
Die Lungenembolie wird anhand der Kreislaufstabilität, der Troponin/NT-proBNP, der Rechtsherzbelastungszeichen in der Bildgebung und des PESI/sPESI („simplified Pulmonary Embolism Severity Index“) in drei Risikogruppen eingeteilt, nach denen sich auch die weitere Behandlungsstrategie richtet (Abb. 1).12
Abb. 1: Risikoadjustierte Behandlungsstrategie bei akuter Lungenembolie (modifiziert nach Konstantinides SV et al. 2019)12
Respiratorisches Versagen
Bei der respiratorischen Insuffizienz unterscheidet man zwischen dem Versagen in der Atemmechanik und dem Perfusionsversagen. Eine Störung der Atmungsmechanik führt zu einer Retention von CO2, eine Störung der Perfusion führt zu einer Abnahme von paO2 durch eine reduzierte Gasaustauschfläche. Aufgrund der unterschiedlichen Pathomechanismen variiert auch die Therapie.
Die NIV-Therapie ist eine Behandlungsoption im Falle einer respiratorischen Insuffizienz. Bei hyperkapnischem Lungenversagen ist auf ein ausreichendes Atemminutenvolumen zu achten, um das erhöhte CO2 abatmen zu können. Liegt ein hypoxämisches Atemversagen vor, müssen der positive endexspiratorische Druck (PEEP) sowie die inspiratorische Sauerstoffkonzentration (FiO2) ausreichend hoch eingestellt werden.
Neben der NIV-Therapie steht uns bei der respiratorischen Insuffizienz auch die High-Flow-Sauerstofftherapie (HFOT) zur Verfügung. Hierbei wird mittels Nasenkanüle Sauerstoff mit hohem Fluss (30–70l/min) appliziert. Hierdurch entsteht ein Staudruck mit einem PEEP von 3–5mmHg. Aufgrund des hohen Gasflusses können ein „Wash-out-Effekt“ von CO2 erreicht werden sowie eine Verkleinerung des funktionellen Totraums und konsekutiv eine Reduktion der Atemarbeit.13,14 Der große Vorteil der HFOT ist der erhöhte Patientenkomfort und die damit einhergehende bessere Compliance.
Aufgrund der aktuellen Datenlage ist die HFOT im Vergleich zur NIV beim hypoxämischen Atemversagen und einem Horovitz-Index (paO2/FiO2) >150mmHg als gleichwertige Therapieoption anzusehen. Jedoch sollte beim hyperkapnischen Atemversagen die HFOT nicht zur primären Therapie herangezogen werden. Sie stellt jedoch eine gute Behandlungsoption, insbesondere bei Complianceproblemen, dar.3
Um die bestmögliche Patientencompliance unter der NIV zu erreichen, sind einige Maßnahmen hilfreich. Wie bereits erwähnt kann die Verabreichung von Morphin eine Besserung der Atemeffizienz und auch der Compliance bewirken. Des Weiteren ist es wichtig, den Patienten über jeden Schritt zu informieren. Der Patient sollte in einer sitzenden Position belassen werden, die Arme auf dem Bettgitter/der Armlehne abgestützt. Dies ermöglicht dem Patienten, die Atemhilfsmuskulatur besser einzusetzen. Weiters sollte die Maske langsam vom Arzt oder der Pflegekraft aufgesetzt werden. Man sollte nicht mit den angestrebten Zielwerten der Beatmungsdrücke beginnen, sondern niedrig anfangen und je nach Verträglichkeit steigern.
Die ersten 30 bis 60 Minuten gelten als sogenannte Adaptionsphase, in welcher die Effektivität der Behandlung anhand der BGA und der Klinik beurteilt wird.3
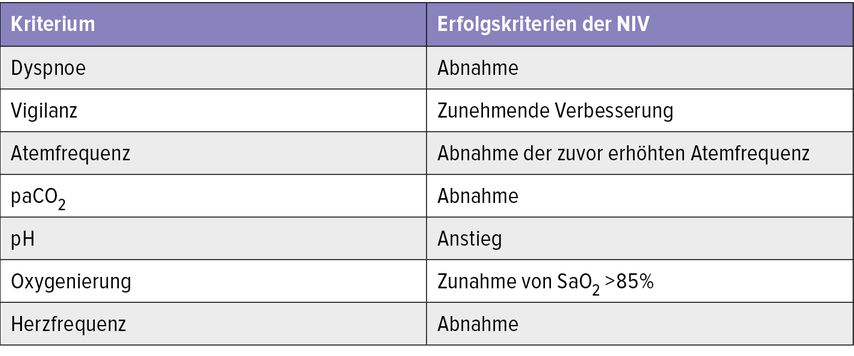
Stabile pH-Werte auf niedrigem Niveau und ein stabil erhöhter paO2 können während der NIV-Adaptation auch länger als 1 bis 2 Stunden toleriert werden, wenn sich der klinische Zustand des Patienten und andere in der Tabelle 1 angeführte Erfolgskriterien bessern.3 Bei fehlender Besserung ist von einem NIV-Versagen auszugehen und umgehend eine Intubation nötig. In diesem Fall sollte auf eine bestehende Patientenverfügung geachtet werden und, wenn möglich, die Situation mit dem Patienten besprochen und der Patientenwunsch erfragt werden.
Literatur:
1 Laribi S et al.: Epidemiology of patients presenting with dyspnea to emergency departments in Europe and the Asia-Pacific region. Eur J Emerg Med 2019; 26: 345-9 2 Berliner D et al.: The differential diagnosis of dyspnea. Dtsch Arztebl Int 2016; 113: 834-45 3 Westhoff M et al.: S2k-Leitlinie Nichtinvasive Beatmung als Therapie der akuten respiratorischen Insuffizienz. https://register.awmf.org/de/leitlinien/detail/020-004 ; zuletzt aufgerufen am 17.1. 2024 4 Jahangir A et al.: Efficacy of magnesium sulfate in the chronic obstructive pulmonary disease population: a systematic review and meta-analysis. Adv Respir Med 2022. doi: 10.5603/ARM.a2022.0012 5 Plant PK et al.: Early use of non-invasive ventilation for acute exacerbations of chronic obstructive pulmonary disease on general respiratory wards: a multicentre randomised controlled trial. Lancet 2000; 355: 1931-5 6 Trethewey SP et al.: Late presentation of acute hypercapnic respiratory failure carries a high mortality risk in COPD patients treated with ward-based NIV. Respir Med 2019; 151: 128-32 7 Global Initiative for Asthma (GINA): Global Initiative for Asthma Managment and Prevention, 2022. www.ginasthma.org ; zuletzt aufgerufen am 17.1.2024 8 Kolditz M et al.: Assessment of oxygenation and comorbidities improves outcome prediction in patients with community-acquired pneumonia with a low CRB-65 score. J Intern Med 2015; 278: 193-202 9 Ewig S et al.: Behandlung von erwachsenen Patienten mit ambulant erworbener Pneumonie und Prävention – Update 2016. Pneumologie 2016; 70: 151-200 10 Knuuti J et al.: 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 2020; 41: 407-77 11 McDonagh TA et al.: 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021; 42: 3599-726 12 Konstantinides SV et al.: 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J 2020; 41: 543-603 13 Grensemann J et al.: High-Flow-Sauerstofftherapie – Chancen und Risiken. Pneumologe 2022; 19: 21-6 14 Bräunlich J, Nilius G: Nasaler Highflow (NHF): eine neue Therapiealternative zur Behandlung der respiratorischen Insuffizienz. Pneumologie 2016; 70: 49-54
Das könnte Sie auch interessieren:
Hochfluss-Sauerstofftherapie: wann und wie lange?
Die Hochfluss-Sauerstofftherapie (HFOT) kann die inspiratorische Sauerstofffraktion (FiO2) verbessern. Sie hat einen dynamischen Effekt auf den positiven endexspiratorischen ...
Kontroversen in der Diagnostik
Interstitielle Lungenkrankheiten (ILD) sind eine heterogene Gruppe verschiedener Erkrankungen. Daher ist die Diagnostik komplex und umfasst klinische, radiologische und ...