Best of DGP 2023
Bericht:
Reno Barth
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Von 29. März bis 1. April fand im Congress Center Düsseldorf der 63. Kongress der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin (DGP) statt. Nach Ende des Kongresses gaben namhafte Expertinnen und Experten im Rahmen der Online-Veranstaltung „Best of DGP2023“ einen Überblick über ihre persönlichen Kongress-Highlights und damit über aktuelle Entwicklungen in den verschiedenen Teilgebieten der Pneumologie.
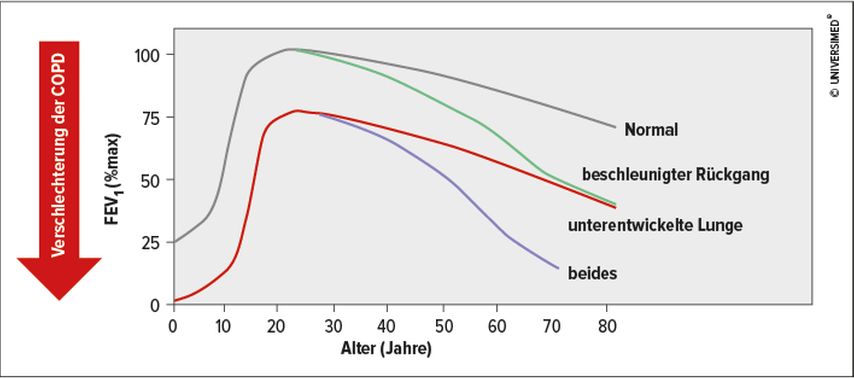
Rauchen stellt in Europa nach wie vor den wichtigsten Risikofaktor für die COPD dar. Doch die Sichtweise in Bezug auf die chronisch-obstruktive Lungenerkrankung wird komplexer. So rückt auch die Möglichkeit einer nicht vollständig abgeschlossenen Lungenentwicklung als Ursache für eine eingeschränkte Lungenfunktion zunehmend in den Mittelpunkt des Interesses. Mögliche Ursachen sind vor allem Frühgeburtlichkeit oder Schädigungen in utero. Prognostisch besonders ungünstig ist die Kombination von wenig entwickelter Lunge und frühem Verlust an Lungenfunktion (Abb. 1).1
Klassifikation der COPD nach Ätiologie gefordert
Angesichts dieser Befunde schlägt eine Lancet Commission nun eine Klassifikation der COPD nach der Ätiologie vor, aus der sich auch ein neuer Diagnose-Algorithmus ergibt. „Eine chronische Lungenerkrankung des Frühgeborenen ist nicht das Gleiche wie ein Schaden durch 40 Jahre Rauchen. Ein Zugang von der Ätiologie her wird es leichter machen, phänotypspezifische Konzepte der Therapie zu entwickeln“, sagte OÄ PD Dr. Katrin Milger-Kneidinger von der Medizinischen Klinik und Poliklinik 5, LMU München, die auch auf den zunehmenden Stellenwert der Bildgebung hinweist. Die Lancet Commission hat das CT jedenfalls in ihren Diagnose-Algorithmus als Alternative zur Spirometrieaufgenommen. Dies habe allerdings auch den Hintergrund, so Milger-Kneidinger, dass in manchen Ländern ein CT leichter verfügbar ist als eine Spirometrie. Man kann allerdings auch wertvolle Zusatzinformationen durch die Bildgebung gewinnen, wenn bereits eine COPD-Diagnose auf Basis der Spirometrie vorliegt. Ein Beispiel dafür ist die Bestimmung der Dicke der Atemwege. Diese hat sich einerseits als mit der Mortalität assoziiert erwiesen, nimmt andererseits aber bei Patienten der GOLD-Gruppen C und D unter Triple-Therapie ab.2
Ebenfalls im Rahmen der Tagung besprochen wurden die von GOLD vorgeschlagenen nichtmedikamentösen Maßnahmen bei COPD wie zum Beispiel Impfungen, Ernährung, Behandlung der Tabakabhängigkeit und palliative Maßnahmen am Ende des Lebens. Zu den nichtmedikamentösen Maßnahmen zählt nicht zuletzt auch der ventilatorische Support, wobei je nach Situation nichtinvasive Beatmung über Maske oder nasaler High-Flow zum Einsatz kommen können. Daten aus der COSYCONET-Kohorte zeigen allerdings, dass beim Einsatz dieser Methoden nach wie vor Luft nach oben besteht.3
Zahl der Asthmapatienten rückläufig
Hinsichtlich Asthma bronchiale zeigen aktuelle epidemiologische Daten, dass der Trend der zunehmenden Inzidenz und Prävalenz gebrochen sein dürfte und aktuell sogar ein leichter Rückgang zu verzeichnen ist. Die Hintergründe dieser Entwicklung sind unklar. Geringere Exposition von Kindern und Schwangeren gegenüber Tabakrauch dürfte ebenso eine Rolle spielen wie der Rückgang von Antibiotika-Verschreibungen bei Kindern. Diskutiert wird auch die reduzierte Zahl von Infektionen der unteren Atemwege aufgrund der Kontaktbeschränkungen während der Covid-Pandemie. Die Sterblichkeit durch Asthma nimmt massiv ab, was der flächendeckend besseren Behandlung mit inhalativen Kortikosteroiden geschuldet ist.
Mittlerweile wird im Zusammenhang mit Asthma auch zunehmend von Remission gesprochen. Remission wird definiert durch Symptomfreiheit über mindestens zwölf Monate, dauerhafte Abwesenheit von Exazerbationen, stabile Lungenfunktion und fehlenden Bedarf an systemischen Glukokortikoiden. Milger-Kneidinger betont, dass es dabei nicht um Heilung oder Spontanremission geht, sondern um eine Remission unter Therapie, analog zum Remissionsbegriff, wie man ihn beispielsweise in der Rheumatologie benützt. Spontanremissionen sind beim kindlichen Asthma möglich. Derzeit werde in Kohorten untersucht, ob Personen, die in der Kindheit eine Asthmaremission erlebt haben, im höheren Alter ein erhöhtes Risiko aufweisen, beispielsweise ein Adult-onset-Asthma zu entwickeln.
Erstes großes, internationales Bronchiektasen-Register
PD Dr. Jessica Rademacher von der Medizinischen Hochschule Hannover berichtete von ersten Daten aus dem europäischen Bronchiektasen-Register EMBARC, einer multizentrischen, prospektiven, beobachtenden Kohortenstudie, an der 27 europäische Länder und Israel teilnehmen.4 Zwischen 2015 und 2022 wurden 16963 Patienten eingeschlossen. Die erste Auswertung ergab eine mediane Exazerbationsrate von 2 (IQR 1–4), 26,4% hatten eine Hospitalisierung aufgrund der Exazerbation im letzten Jahr. Angesichts der Tatsache, dass man dazu bislang sehr wenige Daten hatte, stellt dieses Register einen wesentlichen Fortschritt dar, so Rademacher. Eine Auswertung hinsichtlich Ätiologie zeigt sehr unterschiedliche Ergebnisse in den verschiedenen europäischen Ländern, wobei Österreich einen ungewöhnlich hohen Anteil an primärer ziliärer Dyskinesie (PCD) aufweist. Diese Daten werden in den kommenden Jahren noch zu hinterfragen sein, so Rademacher.
Auch hinsichtlich der im Zusammenhang mit Bronchiektasen relevanten Keime bestehen Unterschiede zwischen den europäischen Ländern: Insgesamt dominiert in Europa Pseudomonas aeruginosa, gefolgt von Haemophilus influenzae, der besonders in Südeuropa dominiert.4 Rademacher wies auch auf das deutsche Bronchiektasen-Register hin, das ebenfalls Pseudomonas aeruginosa als wichtigsten Keim ausweist, wobei in Deutschland an zweiter Stelle Staphylococcus aureus steht.
Eine gute Nachricht betrifft die Resistenzsituation zumindest in Deutschland, wo multiresistenter P. aeruginosa – im Gegensatz beispielsweise zu Spanien – sehr selten ist. Dennoch besteht Bedarf an alternativen antibiotischen Strategien. In Studien untersucht werden beispielsweise Inhibitoren des Quorum Sensing, die die Bildung von Biofilm unterbinden sollen.5 Eine noch bessere Lösung wäre die Eradikation von Pseudomonas aeruginosa, für die vor wenigen Jahren ein Algorithmus vorgeschlagen wurde.6 Diese Strategie soll nun in einer Studie untersucht werden, für die derzeit Patienten rekrutiert werden.
Bei Obstruktion infolge von Bronchiektasen erwies sich Tiotropium als wirksam.7 In der Behandlung der neutrophilen Inflammation bei Bronchiektasen wird Brensocatib (INS1007), ein oraler reversibler Inhibitor der Dipeptidyl-Peptidase 1 (DPP-1), untersucht. DPP-1 ist ein Enzym für die Aktivierung der neutrophilen Serin-Protease. In einer randomisierten, doppelblinden, placebokontrollierten Phase-II-Studie über 24 Wochen verlängerte Brensocatib die Zeit bis zur nächsten Exazerbation.8 Die Phase-III-Studie ASPEN-1 läuft derzeit.
Insgesamt habe sich das Management von Bronchiektasen in den letzten Jahren verbessert, so Rademacher. Dies liege an früherer Diagnostik, effektiven Mukolytika, der besseren Charakterisierung des Entzündungstyps und fallweise auch der Behandlung mit Biologika. In Zukunft werde es wichtig sein, auch ein besseres Verständnis polymikrobieller Communitys zu entwickeln.
Rasante Entwicklung in der Therapie des Lungenkarzinoms
Dr. Matthias Raspe von der Charité Universitätsmedizin Berlin gab einen Überblick über die in den letzten Jahren deutlich verbesserten therapeutischen Optionen beim Lungenkarzinom. Dennoch ist die Prognose dieses Tumors nach wie vor schlecht. Bei rund der Hälfte der Patienten ist zum Zeitpunkt der Diagnosestellung nur noch eine palliative Therapie indiziert. Aufgrund der hohen Patientenzahlen können auch nicht alle Betroffenen in spezialisierten Zentren behandelt werden. Zu der seit vielen Jahren in dieser Indikation eingesetzten Chemotherapie sind mittlerweile mit den Immuntherapien und den bei behandelbaren onkogenen Mutationen angezeigten Tyrosinkinase-Inhibitoren zwei weitere Säulen der Therapie hinzugekommen. Damit ergeben sich in Abhängigkeit vom Stadium und von der Biologie des Tumors komplexe Therapiealgorithmen.
In den frühen Stadien, bei lokal begrenztem oder auch lokal fortgeschrittenem Tumor,steht am Beginn der Behandlung die Operation, meist in Kombination mit adjuvanter Chemotherapie. Mit weiter fortgeschrittener Erkrankung tritt zunehmend die Radio-Chemotherapie in den Vordergrund und in der metastasierten Situation sind schließlich palliative Systemtherapien indiziert. Im vergangenen Jahr sind, so Raspe, zwei neue therapeutische Optionen hinzugekommen. Zum einen Osimertinib, das bei der häufigenEGFR-Mutation eingesetzt werden kann, und zum anderen der Checkpoint-Inhibitor Atezolizumab, der nun auch adjuvant in den Stadien IIb bis IIIb eingesetzt werden kann, wenn eine PD-L1-Expression von mindestens 50% und keine EGFR- oder ALK-Mutation vorhanden sind.
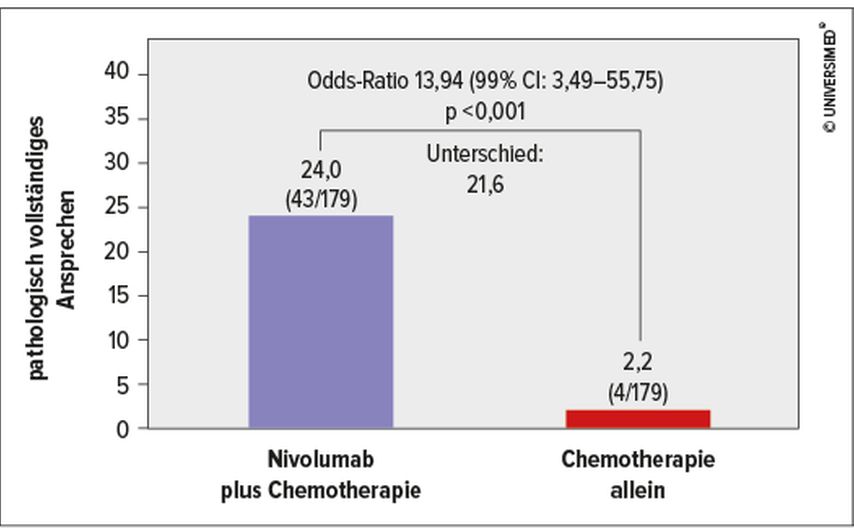
Intensiv beforscht und zum Teil auch bereits klinisch eingesetzt werden neoadjuvante Strategien. So wurde in der Studie CheckMate 816, die eine neoadjuvante Chemo-Immuntherapie mit Chemotherapie alleine verglich, bei fast einem Viertel der Patienten mit der Kombination von Nivolumab und Chemotherapie komplettes pathologisches Ansprechen erreicht. Mit Chemotherapie alleine gelang dies nur in 2,2% (Abb. 2).9 Das komplette pathologische Ansprechen hat sich als prognostisch sehr günstig erwiesen. Damit stellen sich nun neue Fragen, so Raspe. Beispielsweise sei noch nicht geklärt, ob nach einer erfolgreichen neoadjuvanten noch eine adjuvante Therapie erforderlich ist bzw. ob bei komplettem pathologischem Ansprechen überhaupt operiert werden muss.
Abb. 2: Ergebnisse der Studie CheckMate 816: Chemo-Immuntherapie vs. Chemotherapie allein (modifiziert nach Forde PM et al. 2022)9
In der palliativen Situation sind mittlerweile sechs Targets definiert, für die es die Option einer zielgerichteten Therapie mit einem Tyrosinkinase-Inhibitor gibt. Hinzugekommen ist auch eine Vielzahl von Therapien für die Zweitlinie. Allerdings sind die entsprechenden Mutationen relativ selten. In Deutschland sind insgesamt rund 14% der Patienten mit NSCLC von onkogenen Treibermutationen betroffen. Dennoch muss eine Testung vor Beginn einer palliativen Therapie zwingend durchgeführt werden, da Patienten mit onkogenen Treibermutationen bei adäquater Behandlung eine deutlich bessere Prognose aufweisen. So wird bei manchen Mutationen mittlerweile ein mittleres Gesamtüberleben von fünf Jahren erreicht. Raspe: „Diese Diagnostik ist für die Patienten also sehr relevant.“
Patienten ohne onkogene Treibermutationen sind in der palliativen Situation Kandidaten für eine Immuntherapie oder eine Immun-Chemotherapie. Eine Immun-Monotherapie ist bei einer PD-L1-Expression über 50% indiziert. In dieser Indikation stehen Atezolizumab, Pembrolizumab und Cemiplimab zur Verfügung. Für die Immun-Chemotherapien, die bei PD-L1-Expression unter 50% zum Einsatz kommen, sind mittlerweile sechs Antikörper zugelassen, die in einer Vielzahl von Studien mit jeweils geringen Unterschieden untersucht wurden, was die Wahl der idealen Kombination im klinischen Alltag schwierig machen kann, so Raspe.
In der Studie POSEIDON wurde kürzlich die Kombination zweier Checkpoint-Inhibitoren (Durvalumab und Tremelimumab) mit einer platinhaltigen Chemotherapie untersucht, wobei die Kombination im Vergleich zu Chemotherapie zu einer signifikanten Überlebensverlängerung führte.10
Auch beim Plattenepithelkarzinom sind Kombinationen von Chemo- und Immuntherapien indiziert bzw. kommen bei hoher PD-L1 Expression Immun-Monotherapien zum Einsatz.
Frühformen der interstitiellen Lungenerkrankungen: Screenen?
Bei den interstitiellen Lungenerkrankungen geht der Trend zunehmend in Richtung früher Erkennung und damit einer Erweiterung des Krankheitsbegriffs hin zu ILA („interstitial lung abnormalities“) und Early ILD. Studiendaten zeigen, dass eine ILA bereits mit einem signifikant erhöhten Risiko zu sterben assoziiert ist,11 so Dr. Julia Wälscher vom Universitätskrankenhaus Essen. Für den Fall zufällig gefundener Auffälligkeiten im Lungen-CT wurde ein Algorithmus für die Abklärung von ILA publiziert.12 Bei welchen Personengruppen ein Screening indiziert sein könnte, wird aktuell diskutiert. Kandidaten sind unter anderem Personen mit Atemwegssymptomen und Tabakanamnese oder Exposition gegenüber fibrogenen Stäuben, Patienten mit Bindegewebserkrankungen oder Verwandte von IPF-Patienten. Bei systemischer Sklerose wird bereits zum Zeitpunkt der Diagnose auch ein hochauflösendes CT empfohlen. Bei anderen rheumatischen Erkrankungen sollte nach Symptomen gefragt und mittels Auskultation nach verdächtigem Knisterrasseln gesucht werden. Alle Patienten beispielsweise mit rheumatoider Arthritis mittels HR-CT zu screenen sei angesichts der vorhandenen Kapazitäten nicht realistisch, so Wälscher.
Im Hinblick auf die Therapie der interstitiellen Lungenerkrankungen gewinnt der Begriff der PPF („progressive pulmonary fibrosis“) zunehmend an Bedeutung. Wälscher betont, dass es sich dabei um keine eigenständige Erkrankung handelt, sondern um einen Phänotyp, mit dem sich unterschiedliche Erkrankungen äußern können. Eine PPF liegt vor, wenn eine ILD, die nicht die Kriterien für eine idiopathische Lungenfibrose (IPF) erfüllt, ähnlich progredient verläuft wie eine IPF. In solchen Fällen ist eine antifibrotische Therapie indiziert.
Literatur:
1 Lange P et al.: N Engl J Med 2015; 373(2): 111-22 2 Kahnert K et al.: Ther Adv Respir Dis 2023; 17: 17534666221148663 3 Lutter JI et al.: Respir Med 2020; 171: 106087 4 ChalmersJD et al.: Lancet Respir Med 2023; S2213-2600(23)00093-0 5 Hamed MM et al.: Adv Sci (Weinh) 2023; 10(5): e2204443 6 Polverino E et al.: Eur Respir J 2017; 50(3): 1700629 7 Jayaram L et al.: Eur Respir J 2022; 59(6): 2102184 8 Chalmers JD et al.: N Engl J Med 2020; 383(22): 2127-37 9 Forde PM et al.: N Engl J Med 2022; 386(21): 1973-85 10 Johnson ML et al.: J Clin Oncol 2023; 41(6): 1213-27 11 Patel AS et al.: Respir Res 2023; 24(1): 49 12 Tomassetti S et al.: Eur Respir Rev 2022; 31(164): 210206
Das könnte Sie auch interessieren:
Mukoviszidose – eine Erkrankung mit Prädisposition für Pilzinfektionen
Pilzinfektionen stellen eine zunehmende Herausforderung in der Behandlung von Menschen mit Mukoviszidose (zystische Fibrose) dar. Spezifische diagnostische Schritte und therapeutische ...
Sarkoidose – Update 2025
Die Sarkoidose ist eine komplexe Multiorganerkrankung mit teils unzureichender wissenschaftlicher Evidenz. Der interdisziplinäre Austausch ist angesichts der vielen möglichen ...