Der Stellenwert transkutaner osseointegrierter Prothesensysteme in der Patientenversorgung
Autor:
PD Dr. Gerhard M. Hobusch, MSc
Spezialambulanz für moderne Amputationschirurgie und Rehabilitation
Universitätsklinik für Orthopädie und Unfallchirurgie (Klinikleitung: Univ.-Prof. Dr. Reinhard Windhager), Medizinische Universität Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Dem Verlust von Gliedmaßen folgt oft nicht die vom Patienten gewünschte und vom Arzt erwartete Wiederaufnahme wichtiger täglicher Aktivitäten. Gelegentlich können Amputierte nicht oder nur sehr ungenügend mit konventionellen Prothesenschäften versorgt werden. Synergien aus innovativen chirurgischen und technischen Entwicklungen werden in den letzten Jahren zur Verbesserung von Funktionalität und Lebensqualität bei Amputierten genützt.
Keypoints
-
Patienten, die nur ungenügend konventionell versorgt werden können, profitieren deutlich durch die Verwendung von TOPS hinsichtlich ihrer Funktionalität und Lebensqualität.
-
Indikationen zu TOPS müssen streng gestellt werden. Die Versorgung soll Patienten mit dauerhaft unlösbaren Versorgungsproblemen mit konventionellen Prothesenschäften vorbehalten sein.
-
TOPS sind ein wichtiger Teil in chirurgisch-technischen Gesamtversorgungskonzepten von Amputierten sowohl der oberen als auch der unteren Extremität.
-
Moderne Amputationsmedizin sollte in einem multidisziplinären Setting mit guter Vernetzung zwischen Orthopäden, Chirurgen, Orthopädietechnikern, Ergo-, Physio- und Schmerztherapeuten sowie Psychologen ausgeübt werden.
Gegenwart der Amputationsversorgung …
Aufgrund anhaltender militärischer Konflikte weltweit, des gelegentlichen Scheiterns gliedmaßenerhaltender Rekonstruktionen und der Zunahme von Gefäß- und Stoffwechselerkrankungen gehören Amputationen zu den weltweit häufigsten chirurgischen Eingriffen. Die altersbereinigten Raten von Amputationen der unteren Extremitäten liegen in verschiedenen Ländern zwischen 16,9 und 22,9 Amputierten/100000 Einwohner/Jahr.20 Dabei sind 90% der Amputationen auf die periphere arterielle Verschlusskrankheit und das diabetische Fußsyndrom zurückzuführen. Obwohl nur 10% der Amputationen aufgrund von Traumata, Muskel-Skelett-Erkrankungen (z.B. Tumoren) und Hauterkrankungen erfolgen, ist die Prävalenz dieser Amputierten jüngeren Alters deutlich höher.
Dem Bedürfnis von Amputierten, ihre täglichen Aktivitäten nach dem Verlust von Gliedmaßen wiederaufzunehmen, kann häufig nicht wie gewünscht Rechnung getragen werden. Amputationsoperationen werden oft als einfach dargestellt und daher von chirurgisch Lernenden durchgeführt, obwohl sekundäre Amputationen, z.B. nach fehlgeschlagenem Extremitätenerhalt, gelegentlich sehr komplex sein können. In der Realität leiden 51% der traumatisch Amputierten an anatomisch bedingten Problemen, sodass zumindest bei 14,5% der Patienten Revisionsoperationen erforderlich werden.16,27 63% der Amputierten leiden an Hautproblemen, die bei einem Drittel zu Einschränkungen im Alltag führen.24 Außerdem entwickeln rund 70% der Amputierten Phantom- (PLP) oder Stumpfschmerzen (RLP).8 Verständlicherweise können sich daher bei 25–56% der Amputierten soziale Probleme entwickeln.
… und Zukunft
Amputationsmedizin sollte aus diesen Gründen in einem multidisziplinären Setting ausgeübt werden, in dem eine zeitnahe und reibungslose Vernetzung von Orthopäden, Chirurgen, Orthopädietechnikern, Ergo-, Physio- und Schmerztherapeuten sowie Psychologen gewährleistet ist. Eine derartige Infrastruktur ist auch notwendig, um Synergien aus innovativen chirurgischen und technischen Entwicklungen für eine verbesserte Funktionalität und Akzeptanz von Prothesen zu nützen. Dazu gehören auf chirurgischer Seite Techniken wie z.B. gezielte Muskel- oder sensorische Reinnervation (TMR, TSR), die Schaffung vonAgonist-Antagonist myoneuralenInterfaces (AMI)28 und auch transkutane osseointegrierte Prothesensysteme (TOPS). Auf technischer Seite sind hochwertige (mikroprozessorgesteuerte) Knie- und Sprunggelenkssysteme sowie bionische Armprothesen verfügbar.17
Das Prinzip der Osseointegration
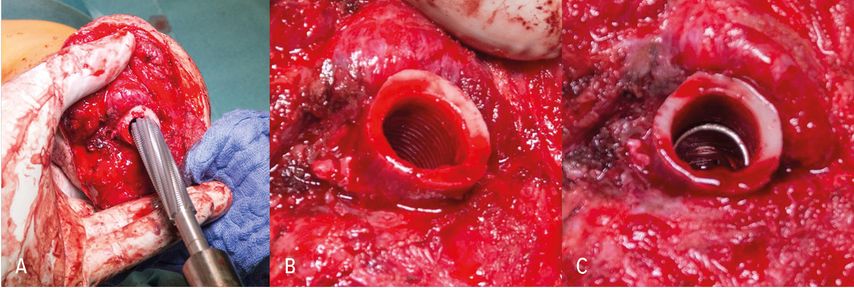
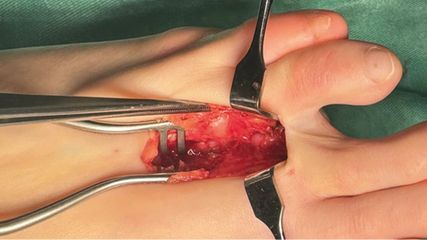
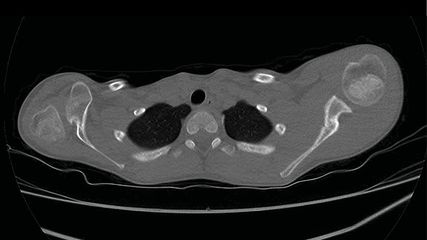
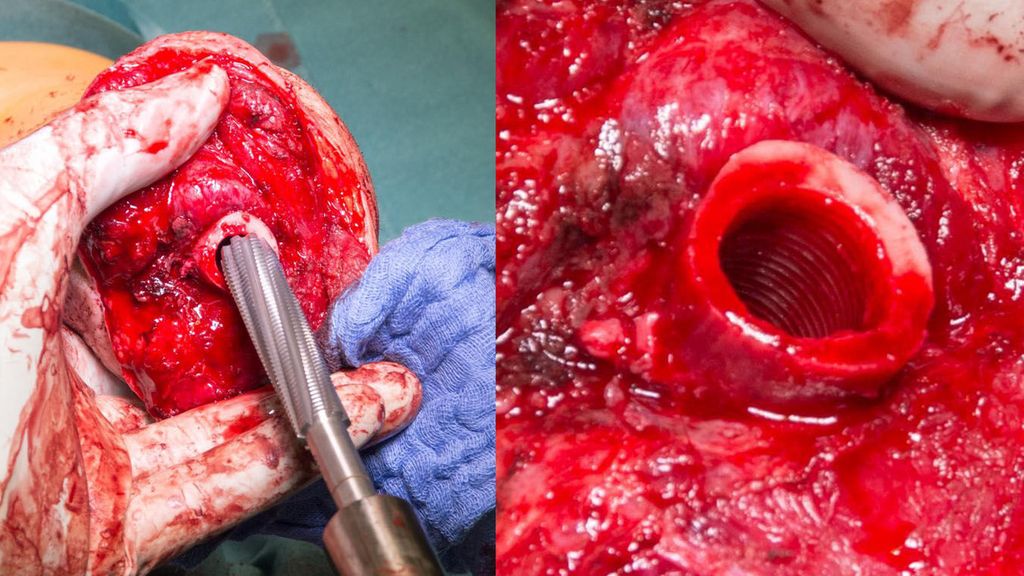
Seit jeher bildet die Verbindung zwischen Stumpf und Prothesenschaft die Versorgungsschwachstelle. Daher hat sich gerade bei Patienten, die unter Komplikationen wie Hitzegefühl, bakteriellen Infektionen und Schwitzen, aber auch Druckstellen oder einer unzureichenden Weichteildeckung leiden, die direkte Verankerung einer Prothese im Knochen durch ein Implantat als hervorragende Alternative zum Schaft erwiesen. Die Stabilität endoossärer Implantate hängt vom Implantatdesign ab, die Variablen dazu sind die Implantatlänge und der Implantatdurchmesser, die Schaft- oder Gewindeform, die poröse Oberfläche und schließlich auch der Knochen, in dem die Verankerung erfolgt.26 Dabei zeigen Implantate mit einem größeren Durchmesser eine bessere Verankerung und unterstützen eher den kortikalen Knochen bei der Reduktion von Stressspitzenbelastungen, längere Implantate reduzieren Stressspitzen im Bereich des trabekulären Interfaces.3 Bei Schraubimplantaten besteht ein Zusammenhang zwischen der Gewindesteilheit und der Osseointegration: Eine geringere Steilheit führt zu mehr Oberflächenkontakt und damit zu einem verbesserten Einwachsverhalten (Abb. 1).7 Auch Pressfit- oder Compress-Implantate können durch Implantatporosität die Osseointegration fördern, indem die Neovaskularisation und das Knocheneinwachsen in Abhängigkeit von der Geometrie der Poren gefördert werden.4 Auch die Hautdurchtrittsstelle ist streng genommen ein Interface, das der Beachtung würdig ist, weil auch hier die Möglichkeit einer aufsteigenden Entzündung besteht, die durch Oberflächenbeschichtungen verhindert werden soll. Als Beispiel sei hier eine Beschichtung mit Fibronektin-angereichertem Hydroxylapatit erwähnt, die die Anfälligkeit für Infektionen verringern, die Weichgewebsintegration aber erhöhen kann.6
Abb. 1: Implantation der OPRATM-Fixture (1. Operationsschritt) einer transhumeralen Osseointegration A) zum Zeitpunkt der Entfernung der Gewinderaspel, B) Demonstration des endoossealen Gewindeschnitts und schließlich C) die Fixture in situ
Transkutane osseointegrierte Prothesensysteme (TOPS)
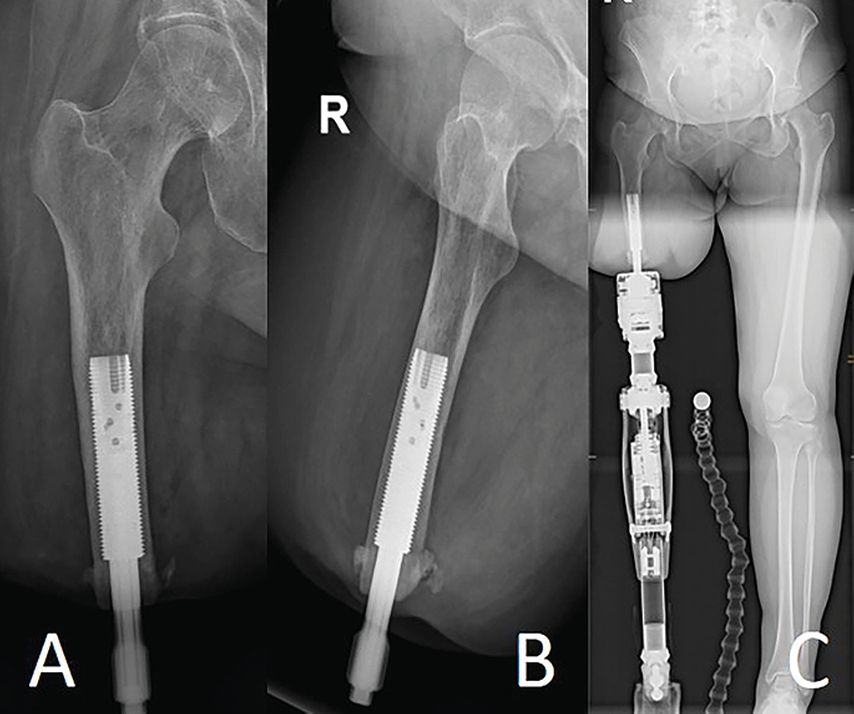
Zum heutigen Zeitpunkt – 32 Jahre nach der Einführung der Osseointegration in der Extremitätenchirurgie (1990) – umfasst das Feld eine größere Auswahl an Implantaten. Fünf humanmedizinisch relevante knochenverankerte Implantate stehen zur Verfügung. Dabei ist das schwedische OPRATM (Osseointegrated Prostheses for the Rehabilitation of Amputees, Integrum, Mölndal, Schweden) mit einer gewindeverankerten Fixture aus Titan und einer BioHelixTM-Beschichtung das am längsten verwendete Modell (Abb. 2).29 Sein direkter Vorfahre war das erste Dentalimplantat der Welt, geschaffen vom schwedischen Erfinder Per-Ingvar Brånemark. Einige Jahre jünger ist die deutsche ILP (Integral Leg Prosthesis, ESKA Orthopaedic, Lübeck, Deutschland) aus Chrom-Kobalt-Molybdän mit einem Pressfit-Verankerungsschaft und einer rauen Tripoden-Oberflächenbeschichtung, die das Einwachsen des Knochens fördert.29 Jünger und vom Implantatdesign mit diesem Implantat nahe verwandt, allerdings aus Volltitan mit einer rauen, plasmagespritzten Titanbeschichtung, ist das BADAL XTM (The Bone Anchoring Device for Artificial Limbs, OTN Implants, Arnhem, Niederlande), das neben dem OPRA das in Europa mittlerweile am häufigsten verwendete Implantat ist. Dieses Modell ähnelt wiederum dem knapp davor (2013) entstandenen australischen OGAP-OPL (The Osseointegration Group of Australia – Osseointegrated Prosthetic Limb), das insbesondere in Australien verwendet wird. Zuletzt steht als Custom Design ein drittes Verankerungsprinzip aus der Compress®-Implantattechnologie (Zimmer Biomet, Warsaw, USA) zur Verfügung, das auf dem Prinzip einer verbesserten Einheilung des Implantats durch Verdichtung des Knochenlagers basiert.23
Abb. 2: Röntgenbilder einer OPRATM-Versorgung transfemoral rechts. A) Oberschenkelröntgen einer osseointegrierten Fixture und des die Haut durchdringenden Abutment rechts a.p., B)Oberschenkelröntgen rechts axial, C) Ganzbeinaufnahme a.p. mit prothetischem Aufbau 9 Monate postoperativ
Versorgungen in der unteren und oberen Extremität
Die Osseointegration kommt besonders transfemoral zur Anwendung. Es bestehen aber auch Möglichkeiten für die transhumerale Versorgung. Diese findet naturgemäß viel seltener statt (Inzidenzen in Österreich im 10-Jahres-Durchschnitt: 15transhumeral/Jahr bzw. 950 transfemoral/Jahr), dann aber zumeist im Rahmen sehr komplexer Versorgungen. Das Osseointegrationsimplantat übernimmt hierbei die „tragende Rolle“ des bionischen Hochleistungsarms. Zusätzlich wird durch „targeted muscle reinnervation“ (TMR) eine Verstärkung von Nervensignalen und durch implantierte Muskelsensoren eine verbesserte Prothesenkontrolle erreicht.10 TMR und auch TSR konnten in den letzten Jahren aber auch als „chirurgische Schmerztherapie“ oder „Prophylaxe“ in der unteren Extremität an Bedeutung gewinnen9 und führen zu komplexeren Versorgungen, in denen die Osseointegration eine Teilaufgabe bei der Schaffung des „perfekten Stumpfes“ erfüllt. Auch transtibiale Osseointegrationsversorgungen finden statt, wenngleich auch viel seltener. Daten hierfür zeigen ein ähnliches Implantatüberleben wie für transfemorale Implantate. Hierbei gilt die gleiche Überlegung zur Osseointegration: Bei schlechter konventioneller Versorgbarkeit des Stumpfes ist eine deutlich bessere Lebensqualität für die Patient*innen zu lukrieren. Sehr limitierte Daten bestehen auch für die Osseointegration im Bereich des Daumens sowie transradial.18
Chirurgische Versorgung und Rehabilitation
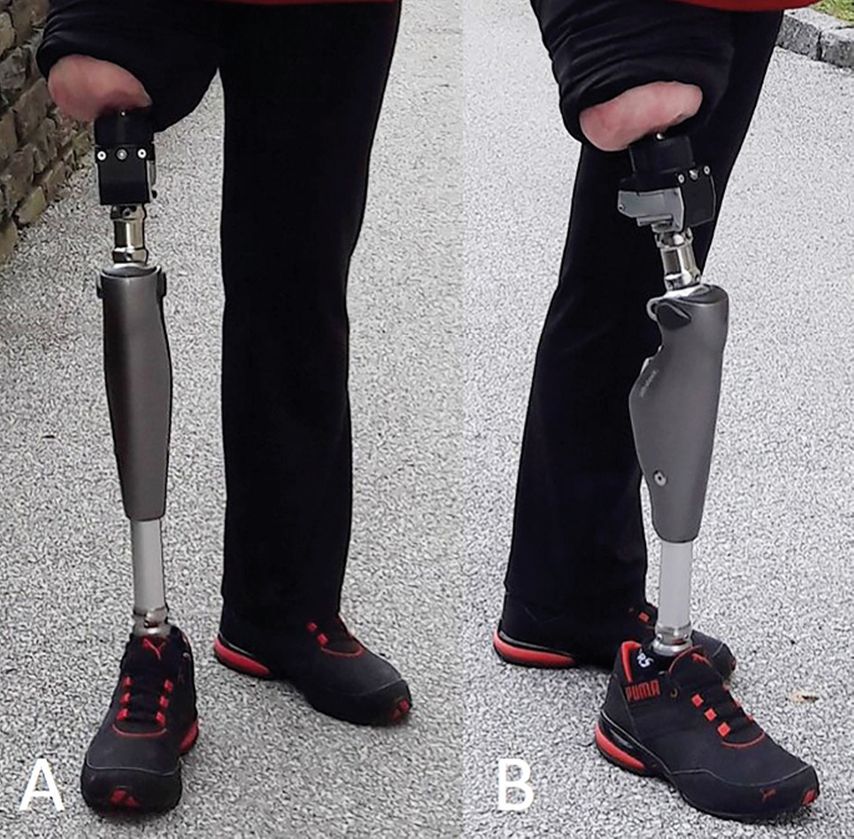
Hinsichtlich des chirurgischen Vorgehens im Bereich der unteren Extremität empfiehlt die verfügbare Literatur ein standardisiertes zweizeitiges Vorgehen. Zuerst wird die Fixierschraube oder der Pressfitschaft in den Markraum implantiert, darauf folgt eine nicht- bzw. teilbelastende Mobilisierung während der Einheilungsphase von 3–6 Monaten (OPRA) bzw. 1,5–2 Monaten (ILP, BADAL X). Danach folgt schließlich der 2.operative Schritt zur Herstellung der Hautdurchtrittsstelle. Auch diesbezüglich unterscheiden sich die Empfehlungen der Implantathersteller hinsichtlich Weichteiltechniken, die eine direkte Haut-Knochen-Verbindung anstreben, und solchen, die eine Unterhaut-Knochen-Grenzfläche gestalten. Es besteht Einigkeit darin, dass Scherkräfte am Stumpfende vermieden werden sollen, um Reizungen zu vermeiden, was durch die Fixation von Muskulatur am Knochen erreicht wird. Auf den 2. Schritt folgt wiederum eine Rehabilitationsphase mit zunehmender Gewichtsbelastung. Insgesamt ist somit mit einer Gesamtwiederherstellungszeit von 3–18 Monaten (OPRA, Abb. 3) und 2,5–4,5 Monaten (ILP, BADALX) zu rechnen. Einzeitige Implantationsverfahren sind in Erprobung.
Abb. 3: Transfemoral mittels OPRATM osseointegrierte Patientin, 9 Monate nach erstem Operationsschritt vollbelastend mobil; A) in der Frontal- und B) in der Seitenansicht
Über Lebensqualität mit transkutanen Prothesensystemen …
Alle Studien zeigten signifikante Verbesserungen in der Gesamtmobilität. Hagberg et al. konnten in einer prospektiven Fallkontrollstudie Verbesserungen der prothetischen Funktion und Lebensqualität bei transfemoral Amputierten mit OPRA-Implantat im Vergleich zu Schaftbenutzern zeigen.13 Muderis et al. beschreiben im Protokoll der Osseointegration Group of Australia (OGAAP-1) für eine zweistufige osseointegrierte Rekonstruktion bei 50 transfemoral Amputierten Verbesserungen in einfachen Gehtests, wie dem „six-minute walk test“ (6-MWT) und dem „timed up and go test“ (TUG), aber auch Verbesserungen in komplexeren Questionnaires für transfemoral Amputierte (Q-TFA), dem SF36 und den Amputation Mobility Predictor Scores.25 Leijendekkers et al. berichteten von 40 konsekutiven Patienten, deren Kraft, Gehstrecke und Lebensqualität ein Jahr nach dem Implantat im Vergleich zur Schaftprothese deutlich besser waren.21Als Grund für die klinische Verbesserung der Patienten wird die sogenannte Osseoperzeption genannt. Darunter versteht man die Fähigkeit des Amputierten, Druck, Position und Gleichgewicht des Beins direkt wahrzunehmen.15 Dieser Umstand und auch die Fähigkeit zu annähernd normalen Muskelaktivitätsmustern bei der Ambulation nach 24 Monaten scheinen für die im Vergleich zu Schaftprothesen geringeren Energiekosten beim Gehen verantwortlich zu sein.12 Außerdem beschreiben Patienten nach TOPS auch weniger Beschwerden beim Sitzen im Vergleich zu Schaftprothesen.
Auch hinsichtlich der Belastung der implantierten Extremität zeigen neuere Röntgen- und Röntgenabsorptiometriedaten, dass entgegen früheren Beobachtungen eine Zunahme des kortikalen Knochens um durchschnittlich 0,54mm nach 24 Monaten in allen periprothetischen Zonen erfolgt ist.14
… und Implantatüberleben (Komplikationen)
Einige Fallserien berichteten in Langzeituntersuchungen über ein erhöhtes Infektionsrisiko nach knochenverankerten Amputationsprothesen. Während tiefe Implantatinfekte gelegentlich vorkommen, sind oberflächliche Infekte recht häufig. Eine prospektiv untersuchte Patientenkohorte mit dem OPRA-Implantat zeigte eine Implantatüberlebensrate von 92% nach 5 Jahren postoperativ bei einem Risiko für tiefe Infektionen von 25% und für partiell rezidivierende oberflächliche Weichteilinfektionen von 66%, die konservativ oder antibiotisch zu kontrollieren waren.5 Die australische Gruppe berichtete über eine Rate von 43% an oberflächlichen Infektionen bei 2-Jahres-Kontrollen bei traumatischen einseitigen Oberschenkelamputierten ohne jegliche Implantatentfernung. Eine gemeinsame Studie aus Australien und den Niederlanden berichtet über eine Gesamtinfektrate von 34% nach 34 Monaten ohne den Nachweis einer Osteomyelitis.1 Das kumulative 10-Jahres-Risiko für Explantation der Implantate aufgrund von Osteomyelitis kann mit maximal 9% beziffert werden.30 Bei allen Implantaten zeigen sich Verbesserungen der Implantatüberlebensraten nach Implantatdesignänderungen und Umstellungen bei der Operationstechnik.19,22 Eine jüngere Arbeit aus den Niederlanden zeigt, dass bei optimierter Weichteiltechnik und einer empfohlenen Reinigung des Implantats zweimal täglich nur 6% oberflächliche Infekte aufkommen.2
Kosteneffektivität
Die Kosten für chirurgische und Rehabilitationsprozesse in Zusammenhang mit knochenverankerten Prothesen beginnen eine wichtige Rolle zu spielen. Aus Sicht der prothetischen Versorgung haben Frossard et al. im australischen Kontext berechnet, dass diese Prothesen für 19% der Patienten kostensparend und für 88% der Teilnehmer kosteneffektiv sind.11 In einem schwedischen Modell von Hansson et al. sind knochenverankerte Prothesen mit hohen Kosten verbunden, die sich aber bei größerem QALY-Gewinn langfristig rechnen.
Literatur:
1 Al Muderis M et al.: Safety of osseointegrated implants for transfemoral amputees: a two-center prospective cohort study. J Bone Joint Surg Am 2016; 98: 900-9 2 Atallah R et al.: Safety, prosthesis wearing time and health-related quality of life of lower extremity bone-anchored prostheses using a press-fit titanium osseointegration implant: a prospective one-year follow-up cohort study. PLoS One 2020; 15: e0230027 3 Baggi L et al.: The influence of implant diameter and length on stress distribution of osseointegrated implants related to crestal bone geometry: a three-dimensional finite element analysis. J Prosthet Dent 2008; 100: 422-31 4 Bauer et al.: Engineering biocompatible implant surfaces. Online unter: https://fdocuments.net/document/engineering-biocompatible-implant-surfaces.html 5 Brånemark RP et al.: Osseointegrated percutaneous prosthetic system for the treatment of patients with transfemoral amputation: a prospective five-year follow-up of patient-reported outcomes and complications. J Am Acad Orthop Surg 2019; 27: e743-51 6 Chimutengwende-Gordon M et al.: The in vivo effect of a porous titanium alloy flange with hydroxyapatite, silver and fibronectin coatings on soft-tissue integration of intraosseous transcutaneous amputation prostheses. Bone Joint J 2017; 99-B: 393-400 7 Chung SH et al.: Effects of implant geometry and surface treatment on osseointegration after functional loading: a dog study. J Oral Rehabil 2008; 35: 229-36 8 Döring K et al.: How common are chronic residual limb pain, phantom pain, and back pain more than 20 years after lower limb amputation for malignant tumors? Clin Orthop Relat Res 2021; 479: 2036-44 9 Dumanian GA et al.: Targeted muscle reinnervation treats neuroma and phantom pain in major limb amputees: a randomized clinical trial. Ann Surg 2019; 270: 238-46 10 Farina D et al.: Toward higher-performance bionic limbs for wider clinical use. Nat Biomed Eng 2021; doi: 10.1038/s41551-021-00732-x 11 Frossard LA et al.: Cost-effectiveness of bone-anchored prostheses using osseointegrated fixation: Myth or reality? Prosthet Orthot Int 2018; 42: 318-27 12 Hagberg K et al.: Socket versus bone-anchored trans-femoral prostheses: hip range of motion and sitting comfort. Prosthet Orthot Int 2005; 29: 153-63 13 Hagberg K et al.: Outcome of percutaneous osseointegrated prostheses for patients with unilateral transfemoral amputation at two-year follow-up. Arch Phys Med Rehabil 2014; 95: 2120-7 14 Haket LM et al.: Periprosthetic cortical bone remodeling in patients with an osseointegrated leg prosthesis. J Orthop Res 2017; 35: 1237-41 15 Hansen CH et al.: The process of becoming a user of an osseointegrated prosthesis following transfemoral amputation: a qualitative study. Disabil Rehabil 2019; 41: 276-83 16 Harris AM et al.: Lower Extremity Assessment Project (LEAP) study group. Complications following limb-threatening lower extremity trauma. J Orthop Trauma 2009; 23: 1-6 17 Hobusch GM et al.: Advanced techniques in amputation surgery and prosthetic technology in the lower extremity. EFORT Open Rev 2020; 5: 724-41 18 Jönsson S et al.: Osseointegration amputation prostheses on the upper limbs: methods, prosthetics and rehabilitation. Prosthet Orthot Int 2011; 35: 190-200 19 Juhnke D-L et al.: Fifteen years of experience with integral-leg-prosthesis: cohort study of artificial limb attachment system. J Rehabil Res Dev 2015; 52: 407-20 20 Kröger K et al.: Lower limb amputation in Germany. Dtsch Arztebl Int 2017; 114: 130-6 21 Leijendekkers RA et al.: Functional performance and safety of bone-anchored prostheses in persons with a transfemoral or transtibial amputation: a prospective one-year follow-up cohort study. Clin Rehabil 2019; 33: 450-64 22 Matthews DJ et al.: UK trial of the osseointegrated prosthesis for the rehabilitation for amputees: 1995-2018. Prosthet Orthot Int 2019; 43: 112-22 23 McGough RL et al.: The Compress® transcutaneous implant for rehabilitation following limb amputation. Unfallchirurg 2017; 120: 300-5 24 Meulenbelt HE et al.: Determinants of skin problems of the stump in lower-limb amputees. Arch Phys Med Rehabil 2009; 90: 74-81 25 Muderis MA et al.: The Osseointegration Group of Australia Accelerated Protocol (OGAAP-1) for two-stage osseointegrated reconstruction of amputated limbs. Bone Joint J 2016; 98-B: 952-60 26 Ogle OE: Implant surface material, design, and osseointegration. Dent Clin North Am 2015; 59: 505-20 27 Pierce RO et al.: The plight of the traumatic amputee. Orthopedics 1993; 16: 793-7 28 Srinivasan SS et al.: On prosthetic control: a regenerative agonist-antagonist myoneural interface. Sci Robot 2017; 2: eaan2971 29 Thesleff A et al.: Biomechanical characterisation of bone-anchored implant systems for amputation limb prostheses: a systematic review. Ann Biomed Eng 2018; 46: 377-91 30Tillander J et al.: Osteomyelitis risk in patients with transfemoral amputations treated with osseointegration prostheses. Clin Orthop Relat Res 2017; 475: 3100-8
Das könnte Sie auch interessieren:
Rekonstruktionsmöglichkeiten bei Nervenläsionen
Die Rekonstruktion peripherer Nervenläsionen bleibt eine Herausforderung – besonders bei langen Defektstrecken, verzögerter Diagnostik oder ausgeprägter Denervierung. Der Artikel ...
Nervenkompressionssyndrome an Sprunggelenk und Fuß
Nervenkompressionssyndrome im Bereich des Sprunggelenks sowie des Fußes stellen eine komplexe Herausforderung dar. Nicht selten sind sie schwer zu diagnostizieren und können bei ...
Die geburtstraumatische Plexusläsion
Sowohl bei einer Spontangeburt als auch bei einer Sectio caesarea kann es zu einem Dehnungsschaden des Armnervengeflechts kommen. Die entstehende Läsion kann unter Umständen ...