Anwendungsspektrum der therapeutischen Kernspinresonanz
Autorinnen:
Mag. Dr. Bettina Thauerer1
PD Mag. Dr. Bibiane Steinecker-Frohnwieser1
Anda Corina Rad, BSc2
Univ.-Doz. Dr. Werner Kullich1
1 Ludwig Boltzmann Institut für Arthritis und Rehabilitation, Saalfelden
2 Abteilung für Plastische, Rekonstruktive und Ästhetische Chirurgie, Medizinische Universität Wien
Korrespondierende Autorin:
PD Mag. Dr. Bibiane Steinecker-Frohnwieser
Degenerative Erkrankungen der großen und kleinen Gelenke sowie der Wirbelsäule wie auch Verschlechterungen der Knochendichte können das tägliche Leben und auch die berufliche Tätigkeit stark beeinflussen. Auch in Anbetracht der fortschreitenden Alterung der Bevölkerung stellen sie ein immer größer werdendes Problem dar. In Bezug auf Behandlungsaspekte der unterschiedlichen Erkrankungen steht die Anforderung in Richtung einer nicht invasiven Behandlungsmethode sehr häufig im Vordergrund. Die Kernspinresonanztherapie (KSRT) mit speziellen Behandlungsgeräten hat sich mittlerweile seit mehr als 15 Jahren bei Gelenkerkrankungen, Osteoporose oder Sportverletzungen unter anderem auch als ergänzende, nicht invasive Therapieform bewährt.
Keypoints
-
Kernspinresonanztherapie (MBST®, MedTec) hat sich seit über 15 Jahren als ergänzende nicht invasive Therapieform bewährt.
-
Ihre (additive) therapeutische Anwendung bei muskuloskelettalen Erkrankungen führt nachweislich zu einer Schmerzreduktion und Funktionsverbesserung.
-
In Chondrozyten wirkt KSRT IL-1β-induzierten zellschädigenden Prozessen entgegen.
-
Die Anwendung von KSRT auf Nervenzellen in Zellkultur verbesserte deren Regenerationsprozesse.
Prinzip der KSRT
Im Zuge einer KSRT-Behandlung werden entsprechend dem Prinzip der Magnetresonanztomografie reale, dem jeweiligen Gewebe angepasste Kernspinresonanzfelder erzeugt. Durch die Rotation der Protonen des Wasserstoffs um ein minimales Magnetfeld werden jene selbst magnetisch und können in weiterer Folge von einem stärkeren Magneten beeinflusst werden. Unter dem Einfluss des stärkeren Magnetfelds rotieren Protonen nicht nur um die eigene Achse, sondern vollziehen auch eine Kreiselbewegung entlang der magnetischen Feldlinien. Diese Bewegung definiert man als Präzession, die Frequenz wird als Larmorfrequenz bezeichnet. Da Gewebe unterschiedliche Larmorfrequenzen aufweisen, kann die KSRT diese gewebespezifischen Larmorfrequenzen für die aktive Beeinflussung des Zielgewebes nutzen. Eingestrahlte Radiowellenimpulse übertragen dabei die Energie verlustfrei auf Protonen. Während der darauffolgenden Relaxation, also der Zeit, in der die Protonen in ihre ursprüngliche Position zurückkehren, wird die zuvor absorbierte Energie wieder abgegeben. Die den Geweben eigenen unterschiedlichen Relaxationszeiten werden durch die KSRT erkannt und für die aktive Beeinflussung des Zielgewebes genutzt.
Die bei der Therapie verwendete Feldstärke ist 10000-mal schwächer als bei einer Magnetresonanztomografie-Untersuchung und hat nachweislich keine negativen Auswirkungen auf die Zelle bzw. die Gesundheit. Dabei wird Energie mit dem Ziel, Stoffwechselprozesse im Körper zu aktivieren und regenerative Prozesse auszulösen, auf die Zellen übertragen.
Arthrose
In der Anwendung der KSRT macht man sich Kernspinresonanzfrequenzen zunutze, um nachweislich einen reparativen Einfluss auf Knochen- und Knorpelgewebe auszuüben, der sich positiv auf Arthrose auswirken kann. Arthrose ist eine multifaktorielle Erkrankung, bei der das gesamte Gelenk inklusive der Gelenkskapsel betroffen ist. Durch ein Ungleichgewicht zwischen den knorpelabbauenden und knorpelaufbauenden Prozessen kommt es letztlich zur Zerstörung und Reduktion des Knorpelgewebes. Die arthrotischen Veränderungen des Gelenkknorpels sind häufig die Ursache für Schmerzen und Verschlechterungen der Gelenkfunktion. Zusätzlich stellt die daraus resultierende Inaktivität ein zusätzliches Gesundheitsrisiko dar, das zu Folgeerkrankungen (Muskelatrophie, Übergewicht, kardiovaskulären Erkrankungen, Stoffwechselerkrankungen) führen kann. Viele Jahre lang erfolgte die Behandlung von Arthrose rein symptomatisch und die Prävention wurde ignoriert. Die symptomatische Behandlung zeigt nur vorübergehende Wirkung.
Im Rahmen einer Anwendungsbeobachtung mit Folgeuntersuchung nach 6 Monaten wurde der therapeutische Einsatz der KSRT bei 32 Patient*innen mit Gonarthrose geprüft.1 Eine einstündige KSRT-Behandlung an 5 Tagen hintereinander (1h x 5) führte zur Verbesserung des Lequesne-Index, speziell in den Items „Schmerz und Unbehagen“ und „physische Funktionseinschränkung“, die die Aktivitäten des täglichen Lebens umfassen.
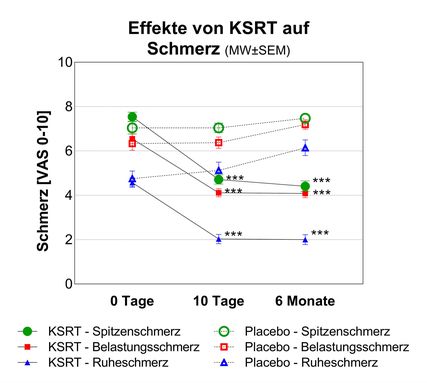
Abb. 1: Signifikante Reduktion der Schmerzintensität bei Vergleich von KSRT und Placebo 10 Tage und 6 Monate nach KSRT (***p < 0,001)
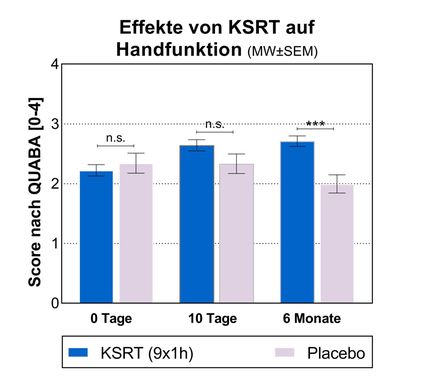
Abb. 2: Signifikante Verbesserung der Handfunktion (Gesamtscore nach QUABA) unter KSRT im Vergleich zu Placebo 6 Monate nach Therapie (***p < 0,001)
In einer weiteren Studie zur KSRT-Gonarthrosetherapie wurde der Erfolg der Therapie auch in Abhängigkeit von Alter, Geschlecht und sportlicher Aktivität bei einem weiteren Patienten*innen-Kollektiv (n=32) analysiert. Es zeigte sich eine nachhaltige Verbesserung des Gesundheitszustands mit zum Teil deutlicher Schmerzlinderung auch nach 4 Jahren, wobei gegen Ende des 4-jährigen Studienzeitraums eine leichte Rückkehr der Schmerzen zu verzeichnen war.2 Auffällig dabei war auch, dass es gerade bei älteren Patient*innen mit häufig fortgeschrittener Arthrose zu einer deutlichen Zustandsverbesserung kam. Ein totalendoprothetischer Gelenkersatz könnte damit in vielen Fällen auf Jahre hinausgezögert oder gar vermieden werden.
KSRT wurde auch zur Behandlung von Hand- und Fingergelenksarthosen eingesetzt. Eine doppelblinde, randomisierte und placebokontrollierte Studie verifizierte die therapeutische Wirkung der KSRT bereits 10 Tage nach Therapie, die Wirkung hielt bis zu 6 Monate an.3 Die Patient*innen erhielten eine Behandlungsserie mit je einer Therapiestunde täglich an 9 aufeinanderfolgenden Tagen (1h x 9). Dabei konnten eine signifikante Reduktion der Schmerzintensität bei Spitzen-, Ruhe- und Belastungsschmerz (Abb. 1) sowie eine Verbesserung der Handfunktion (Abb.2) festgestellt werden.
Um die nachhaltige Wirkung der KSRT zu überprüfen, wurden über einen Zeitraum von 10 Jahren Daten von 4518 Patient*innen, welche an Kniearthrose, Hüftarthrose, Sprunggelenksarthrose oder Spondylarthrosen der Wirbelsäule litten, zu verschiedenen Zeitpunkten (0 Tage, 6–8 Wochen, 6 Monate, 12 Monate nach Therapie) erhoben.4 Diese multizentrische Studie belegt klar, dass KSRT zu signifikanter Schmerzreduktion und Verbesserung der Gelenkfunktion in allen untersuchten Indikationen führte und dass diese Effekte bis zu 12 Monate nach Therapie nachweisbar waren.
„Low back pain“ (LBP): der chronische unspezifische Kreuzschmerz
Kreuzschmerzen („low back pain“, LBP) sind eine häufige Erkrankung der Muskeln, Nerven und Knochen des Rückens zwischen dem unteren Rand der Rippen und der unteren Falte des Gesäßes. Der Schmerz kann von einem ständigen dumpfen Schmerz bis zu einem plötzlichen scharfen Gefühl variieren. Je nach Dauer können Kreuzschmerzen als akut (Schmerzen dauern weniger als 6 Wochen), subchronisch (6–12 Wochen) oder chronisch (mehr als 12 Wochen) klassifiziert werden. Typischerweise treten die ersten akuten Schmerzen zwischen dem 20. und 40. Lebensjahr auf. Chronische Kreuzschmerzen können in weiterer Folge zu Schlafstörungen, depressiver Symptomatik oder Angstzuständen führen.
Als Behandlungsmethoden stehen Physiotherapie, Medikamente oder letztlich ein chirurgisch-orthopädischer Eingriff zur Wahl. Die Wirkung der MBST®-KSRT mit ihrem komplexen dreidimensionalen elektromagnetischen Kernresonanzfeld wurde bei 62 Patient*innen mit chronischem unspezifischem Kreuzschmerz, die eine stationäre 3-wöchige Rehabilitation durchliefen, über eine doppelblinde, randomisierte, placebokontrollierte Studie untersucht.5 Die Patient*innen bekamen zusätzlich zu der standardisierten Therapie eine KSRT-Behandlungsserie zu 1h x 5. Eine auch über 3 Monate nach der Behandlungsserie anhaltende Verbesserung von Körperfunktionen und Aktivitäten, ermittelt mit dem Roland Morris Total Score, wurde beobachtet. Diese zeigte sich auch im Schmerzbild nach 3 Monaten, bei dem eine Reduktion des Ruheschmerzes und des Schmerzes unter Stress zu sehen war.
Osteoporose
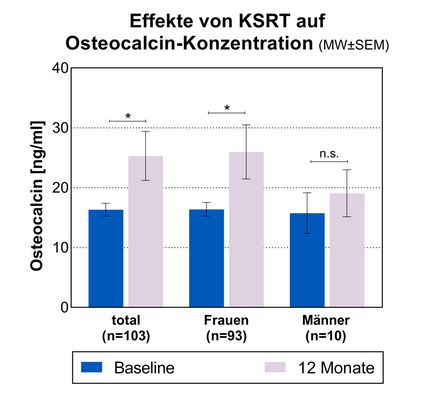
Abb. 3: Signifikante Erhöhung der Osteocalcin-Konzentration im Vergleich vor und 12 Monate nach einer KSR-Therapie (*p < 0,05)
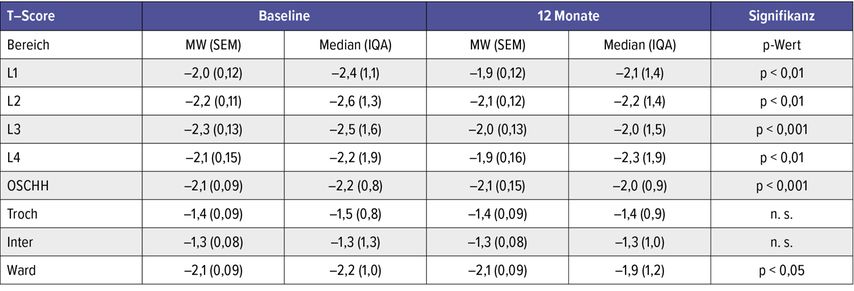
Osteoporose ist eine Skeletterkrankung, die durch verminderte Knochenmasse, Störung des Knochengewebes und reduzierte Knochenmineraldichte charakterisiert werden kann. Damit einhergehend besteht ein erhöhtes Frakturrisiko. Die Basistherapie gibt Kalzium und Vitamin D vor und wird mit knochenspezifischen Medikamenten erweitert. Der große Nachteil von solchen medikamentösen Behandlungen sind die Nebenwirkungen bei Langzeittherapien. Eine alternative oder zusätzliche Therapie stellt die risikofreie nicht invasive KSRT mit ihren positiven Effekten auf Knochenzellen dar. Langzeiteffekte auf Knochendichte und Knochenumsatz wurden bei 103 Patient*innen mit Osteoporose unter Anwendung einer Behandlungsserie von 10 aufeinanderfolgenden KSRT-Behandlungen (1h x 10) untersucht.6 Vor und ein Jahr nach der Behandlung wurden als Parameter die Knochendichte mittels DEXA-Messungen und der Knochenumsatzmarker Osteocalcin bestimmt. Der T-Score verbesserte sich in den Bereichen der Lendenwirbel (L1–L4), des Oberschenkelhalses und des Ward’schen Dreiecks (Tab. 1). Die Untersuchungen ergaben auch eine signifikante Erhöhung der Osteocalcin-Konzentration, die auf eine eventuelle Knochenneubildung hinweist (Abb. 3).
Im Fallbericht von Krpan und Kullich 2017 wurden 5 Jahre retrospektiv Daten von 450 Osteoporosepatient*innen gesammelt. Dabei wurde eine Verminderung des Frakturrisikos als Effekt einer KSRT-Behandlung zu 1h x 10 nachgewiesen.7
Einfluss der KSRT auf zellulärer Ebene, molekulare Aspekte
Obwohl die biologische Auswirkung elektromagnetischer Felder verstärkt erforscht wurde, besteht immer noch keine Einigkeit über die Bedeutung ihrer Wirkungen. Im Zusammenhang mit KSRT ließen sich jedoch durch intensive Forschung auf zellulärer Ebene in den letzten Jahren KSRT-induzierte Effekte beschreiben. So zeigte sich bei einer KSRT-Behandlung humaner Chondrozyten- und Osteoblastenzellkulturen (1h x 9) innerhalb einer kontrollierten, doppelblinden, randomisierten Studie, dass KSRT bei Zellen weder einen Zelltod verursacht noch die Lebensfähigkeit der Zellen hemmt. Eine tendenzielle Zunahme der unter anderem auch bei Arthrose erwünschten Zellproliferation von Chondrozyten konnte gezeigt werden.8
Zusätzlich wiesen Chondrozyten von Arthrosepatient*innen durch KSRT ein verändertes miRNA-Profil, eine Inhibierung der Aktivität von Histon-Deacetylasen und eine Modulation der NAD(+)/NADH-Signalübertragung auf.9 Unter hypoxischen Bedingungen konnte die KSRT in Chondrozyten den durch das proinflammatorische Interleukin IL-1β-induzierten Zellprozessen entgegenwirken. Die Anwendung von Kernspinresonanz wirkte sich nachweislich auch auf die intrazelluläre Kalziumkonzentration [Ca2+]i unter entzündlichen Bedingungen in Chondrozyten aus und modulierte den Kalziumeinstrom und/oder die Kalziumfreisetzung in der Zelle, was zu einer erhöhten MAPK-Aktivität führte: beides Faktoren, die eine Rolle bei der beobachteten Schmerzlinderung spielen könnten.10 Zellschädigende Prozesse, wie eine über IL-1β induzierte Reduktion der ATP-Produktion und eine Zunahme der NF-kB-Aktivität, konnten durch die KSRT-Behandlung in Chondrozyten reduziert werden.
Diese Ergebnisse zeigen einmal mehr, dass die Behandlung mit KSRT die IL-1β-induzierten Veränderungen aufheben kann, indem sie den katabolen Effekten entgegenwirkt und dadurch die Entzündungsmechanismen durch die Veränderung der NF-kB-Signalisierung reduziert.
Untersuchungen zum Einfluss der KSRT auf die zirkadiane Uhr und ihre Verknüpfung mit hypoxischen Signalen zeigten, dass KSRT nicht nur die zirkadiane Uhr, sondern auch den Hypoxie-induzierbaren Faktor-1α (HIF-1α) beeinflusst. Abgesehen von den Auswirkungen auf den zirkadianen Rhytmus von Säugetierzellen könnte diese Technologie der erste nichtpharmakologische Ansatz zur Veränderung des HIF-1α-Proteins in Zellen und Geweben sein. HIF-1α und die damit verbundene zirkadiane Uhr spielen eine Schlüsselrolle bei Krankheiten mit ischämischem Hintergrund, wie z.B. Infarkt, Schlaganfall und Krebs.11
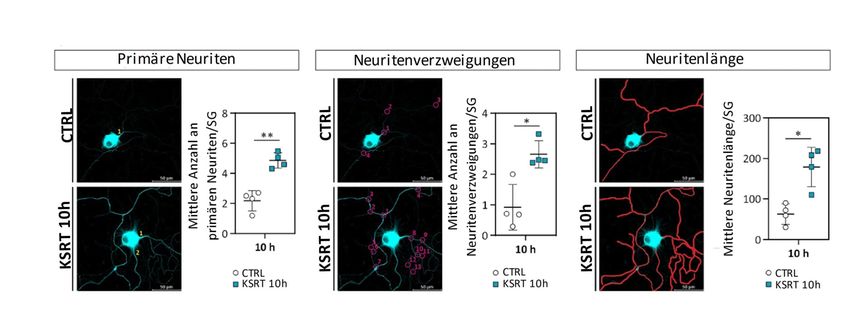
Bei KSRT-Anwendungen auf neuronaler Ebene konnte eine deutliche Reaktion der Nervenzellen beobachtet werden. Dabei kam es zur Erhöhung des Regenerationspotenzials der Spinalganglien (Neuronen). Dies zeigte sich sowohl in einem gesteigerten Zellüberleben als auch in einer vermehrten Ausbildung von neuronalen Verzweigungspunkten. Ein fortgeschrittener neuronaler Differenzierungszustand konnte aufgrund der enormen Zunahme der mittleren Neuritenlänge festgestellt werden (Abb. 4). Diese positiven Auswirkungen der KSRT sind in erster Linie durch die Stimulation von Schwann-Zellen vermittelt.12 Die aus dieser Studie eindeutig hervorgehende neuroregenerierende Eigenschaft der KSRT eröffnet dieser nicht invasiven Therapieform eine zusätzliche Behandlungsoption bei peripheren Nervenverletzungen. Weiters ermutigen diese Ergebnisse zu zukünftigen Studien, die die Wirkung der KSRT in einem physiologischen Kontext untersuchen.
Abb. 4: Vergleich von Spinalganglien(SG)-Kulturen und Neuritenmerkmalen als Antwort auf KSRT. Repräsentative Aufnahmen von TBB3-gefärbten Neuronen in der Kontrolle (CTRL) und nach Kernspinresonanzbehandlung (KSRT) plus korrespondierende Quantifizierung: primäre Neuriten (li.), Neuritenverzweigungen (Mitte), Neuritenlänge (re.) pro SG-Neuron
Abgeleitet von den Erkenntnissen aus den Untersuchungen auf zellulärer Ebene und in Verbindung zu den beobachteten positiven klinischen Effekten, stellt sich die KRST als breitenwirksame Behandlungsmethode dar. Speziell in Bereichen, wo gute bzw. nebenwirkungsarme Therapiemaßnahmen Mangelware sind, und in Ergänzung zu Behandlungs- oder Nachbehandlungsstrategien könnte die KSRT ein gutes wirksames Therapeutikum darstellen.
Literatur:
1 Fagerer N, Kullich W: . Arzt & Praxis 2007; 61(927): 180-2 2 Levers A et al.: Orthopädische Praxis 2011; 47(11): 536-43 3 Kullich W, Außerwinkler M: Orthopädische Praxis 2008; 44: 287-90 4 Kullich W et al.: J Back Musculoskelet Rehabil 2013; 26(1): 93-104 5 Kullich W et al.: J Back Musculoskelet Rehabil 2006; 19(2): 79-87 6 Krpan D et al.: Periodicum Biologorum 2015; 117(1): 161-5 7 Krpan D, Kullich W: Clin Cases Miner Bone Metab 2017; 14(2): 235-8 8 Temiz-Artmann A et al.: Methods Find Exp Clin Pharmacol 2005; 27(6): 391-4 9 Steinecker B et al.: Int J Mol Sci 2021; 31, 22(11): 5959 10 Steinecker B et al.: Clin Exp Rheumatol 2018; 36(2):294-301 11 Thöni V et al.: Chronobiol Int 2021; 38(8): 1120-34 12 Mann A et al.: Front Cell Neurosci 2022; 28(16): 859545
Das könnte Sie auch interessieren:
Präventive Strategie: extrakorporale Stoßwellentherapie
Die extrakorporale Stoßwellentherapie (ESWT) hat sich von einer ursprünglich lithotriptischen Methode zu einem vielseitigen biologischen Stimulationsverfahren entwickelt. ...
Gangpathologien nach hüftgelenksnahen Frakturen
Der routinemäßige Einsatz biomechanischer Motion-Capture-Systeme (MoCap) in einem Ganglabor liefert durch eine präzise Diagnostik wertvolle Informationen über Gangpathologien und stellt ...
Die PRS-Rekonstruktionspfanne mit zentraler Ileumschraube
Neben komplexen Frakturmorphologien erschweren osteoporotische Knochenqualität, vorbestehende Degeneration des Hüftgelenks sowie der Anspruch an eine rasche postoperative Mobilisation ...