Wichtige Laborparameter bei Epilepsie: ein aktueller Überblick
Autor:
PD Dr. med. Christian Tilz
Klinik für Neurologie und Epileptologie
Epilepsiezentrum Bodensee
Zentrum für Psychiatrie Südwürttemberg
Ravensburg-Weissenau
Universitätsklinik für Neurologie, Medizinische Universität Graz
E-Mail: Christian.Tilz@ZfP-Zentrum.de
Laborkontrollen sind bei Epilepsien aus verschiedensten Gründen erforderlich. Anfallssupprimierende Medikamente können Störwirkungen auf unterschiedliche Organsysteme haben, die unter der Therapie kontrolliert werden müssen. Andererseits helfen sie bei der differenzialdiagnostischen Bestimmung der Anfallsart. Zuletzt werden auch Indikation und Bedeutung von Blutspiegelkontrollen bewertet.
Keypoints
-
Anfallssupprimierende Medikamente (ASMs) können das Blutbild verändern. Bei den alten ASMs wurde das detailliert beschrieben, aber auch bei neuen ASMs ist Vorsicht geboten.
-
Für die «alten» ASM sind ausreichend Studien zur Dosis-Wirkungs-Relation vorhanden. Der Blutspiegel kann daher helfen, die richtige Zieldosis zu finden.
-
Blutspiegelkontrollen dürfen und können bei neuen ASM nicht zur Festsetzung der Zieldosis verwendet werden.
-
Die Messung von Laktat und Kreatinkinase (CK) erlaubt die Unterscheidung zwischen einem tonisch-klonischen Anfall und einem nichtepileptischen Anfall.
-
Der IDEAL-Score hilft zu bestimmen, ob eine Liquorpunktion indiziert ist.
Epilepsien stellen die häufigste neurologische Langzeiterkrankung dar. Sie erfordern daher in den meisten Fällen eine langjährige anfallssupprimierende Therapie. Die Behandlung von Epilepsien erfolgt zunächst im Sinne einer symptomatischen medikamentösen Therapie, die zu einer Unterdrückung der Übererregbarkeit von Nervenzellverbänden führt. Sie stellt keine kausale Therapiemöglichkeit dar. Daher ist es essenziell, potenziell akute oder auch Langzeitnebenwirkungen frühzeitig zu erkennen und zu verhindern, um Organschäden oder schädliche Interaktionen abzuwenden.
Nebenwirkungen der anfallssupprimierenden Medikamente (ASMs) können entweder dosisabhängig oder dosisunabhängig (idiosynkratisch) in Erscheinung treten und zahlreiche Organsysteme wie das hämatopoetische System, die Leber- oder Nierenfunktion sowie den Elektrolythaushalt betreffen. Die Möglichkeit solcher Nebenwirkungen ist sowohl bei den alten als auch bei den «neuen» ASMs in unterschiedlicher Häufigkeit gegeben. Auch wenn neue ASMs grundsätzlich weniger zu Interaktionen durch Enzyminduktion neigen, können diese insbesondere bei ASMs der Dibenzazepinfamilie (Oxcarbazepin und Eslicarbazepin), jedoch auch bei dem 2021 eingeführten Cenobamat vorkommen. Die Frage, wie häufig welche Laborkontrollen erfolgen sollten, lässt sich aufgrund des unterschiedlichen Einflusses auf verschiedene Organsysteme daher nur schwer für alle Substanzen in gleicher Weise einheitlich beantworten.
Empfohlene Labordiagnostik vor Behandlungsbeginn
Vor Beginn einer anfallssupprimierenden Behandlung sollten folgende Parameter erfasst werden, um Einflüsse der Therapie auf das hämatopoetische System sowie für die jeweiligen Substanzklassen charakteristische Nebenwirkungen, wie etwa Hyponatriämien, zu erfassen:
-
«grosses» Blutbild einschliesslich Differenzialblutbild und Thrombozyten
-
Leberwerte: Bilirubin, γ-GT, GOT, GPT, alkalische Phosphatase (AP)
-
Nierenwerte
-
Elektrolyte: Natrium, Kalium, Kalzium, Phosphat
-
Triglyzeride, Cholesterin
-
Gesamteiweiss, Serumelektrophorese
-
Gerinnung
-
HbA1C und Glukose vor Therapiebeginn mit Valproinsäure
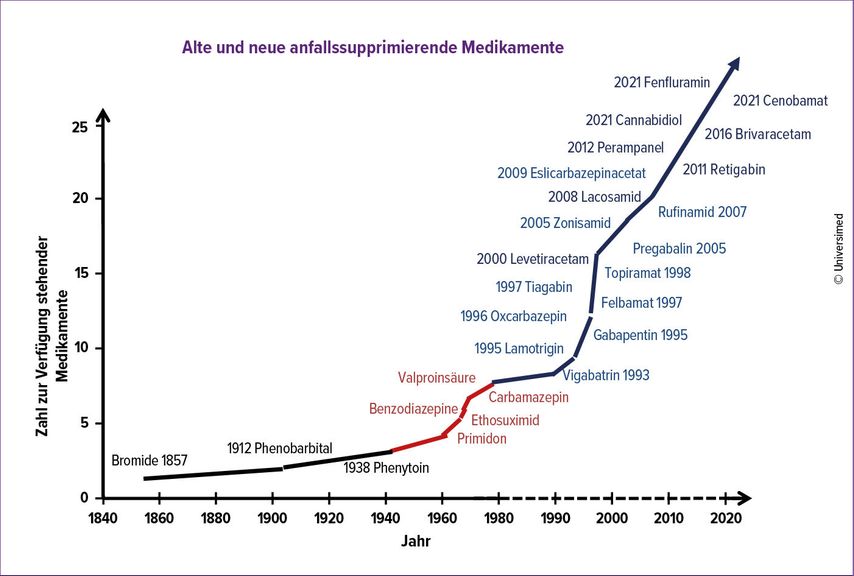
Abb. 1: In den letzten Jahren sind zahlreiche anfallssupprimierende Medikamente dazugekommen. Je nach Medikament sind spezifische Monitoringmassnahmen erforderlich
Im weiteren Verlauf empfehlen zahlreiche Autoren weitere Kontrollen 1–3 Monate nach Behandlungsbeginn oder bei Dosisanpassungen. Später reicht ein Intervall von 4 bis 6 Monaten, bei Anfallsfreiheit und guter Verträglichkeit sind auch grössere Intervalle (z.B. 1x/Jahr) möglich. Dabei sollten substanzspezifische Besonderheiten mitbedacht werden, die gegebenenfalls häufigere Kontrollen erfordern.
Bekannte Wechselwirkungen
Für die sogenannten «alten» anfallssupprimierenden Medikamente, insbesondere die Valproinsäure, ist die Datenlage zu laborchemischen und hämatopoetischen Veränderungen sehr umfangreich. Unter Therapie mit Valproinsäure ist insbesondere im Kindesalter darauf zu achten, dass bereits innerhalb kurzer Zeit hepatotoxische Reaktionen möglich sind. Aber auch unter neuen anfallssupprimierenden Medikamenten können Veränderungen des Blutbildes in Erscheinung treten. Diese sind für zahlreiche neue ASMs, insbesondere Brivaracetam, Cenobamat, Eslicarbazepinacetat, Felbamat, Gabapentin, Lacosamid, Lamotrigin, Levetiracetam, Oxcarbazepin, Pregabalin, Stiripentol, Sultiam, Topiramat und Zonisamid, beschrieben.
Besonders hervorzuheben ist, dass auch unter dem erst kürzlich zugelassenen Cenobamat in den Zulassungsstudien selten Fälle einer potenziell lebensbedrohlichen Überempfindlichkeitsreaktion auftraten, ein sogenanntes Drug-Rash-with-Eosinophilia-and-Systemic-Symptoms-Syndrom (DRESS). Vonseiten der Zulassungsbehörden wird daher eine langsamere Auftitrationsgeschwindigkeit in 14-tägigen Schritten empfohlen, unter der diese nicht mehr vorkamen. Auf diese verlangsamte Auftitrationsgeschwindigkeit unter Cenobamat ist daher unbedingt zu achten. Unter der Therapie mit Felbamat traten schwerwiegende aplastische Anämien auf, sodass Felbamat heute kaum mehr zum Einsatz kommt.
Wann hilft der Blutspiegel zur Bestimmung der Zieldosis?
Die Festlegung der Referenzwerte für die Blutspiegel der anfallssupprimierenden Therapie erfolgte für die ersten und alten Substanzen, insbesondere Phenobarbital, Phenytoin, Carbamazepin und Valproinsäure, unter Berücksichtigung ausführlicher Studien zur Dosis-Wirkungs-Relation. Dies hat angesichts der Interaktionen und teilweise komplexen Verstoffwechselungsprozesse, etwa der nichtlinearen Kinetik von Phenytoin, direkte Bedeutung für die Bestimmung der Zieldosis. Für die neuen anfallssupprimierenden Medikamente fehlen vergleichbare Studien für die Bestimmung der Referenzwerte jedoch, sodass diese weitgehend arbiträr festgelegt wurden.
Blutspiegelkontrollen dienen daher insbesondere bei neuen anfallssupprimierenden Medikamenten im Allgemeinen nicht der Festsetzung der Zieldosis, da anerkannte Referenzwerte für neue anfallssupprimierende Medikamente bezüglich der Dosis-Wirkungs-Beziehung fehlen. Sie können jedoch hilfreiche Zusatzinformationen für die Frage der Compliance oder der veränderten Stoffwechselbedingungen (Schwangerschaft, Interaktionen) liefern. Da jedoch die Bereiche des «therapeutischen» Serumspiegels von Patient:in zu Patient:in einer grossen interindividuellen Breite unterliegen, sollte daher besser der Ausdruck des «individuellen therapeutischen Bereichs» verwendet werden.
Blutwerte zur Unterstützung der Differenzialdiagnostik
Für die differenzialdiagnostische Abgrenzung von epileptischen Anfällen gegenüber anderen Anfallsereignissen eignet sich die Bestimmung der Kreatinkinase (CK) sowie von Laktat. Die CK als Ausdruck der Rhabdomyolyse eignet sich vor allem für die Erfassung von tonisch-klonischen Anfällen, kann jedoch auch etwa nach intensiver körperlicher Belastung erhöht sein. Der Anstieg der CK erfolgt üblicherweise innerhalb der ersten 24 Stunden und erreicht 24–72 Stunden nach dem Anfall sein Maximum, sodass eine zu frühe Bestimmung mit falsch negativen CK-Werten einhergehen kann und die Bestimmung im Bedarfsfall am Folgetag wiederholt werden sollte. Die Bestimmung von Laktat hat in jüngster Zeit zunehmend an Bedeutung gewonnen. Laktat kann aus der Blutgasanalyse ebenso wie aus dem Serum bestimmt werden. Im Liquor ist ein signifikanter Laktatanstieg ebenso nach tonisch-klonischen Anfällen messbar. Die Bestimmung von Laktat kann mit einer sehr hohen Sensitivität von bis zu 89% und einer Spezifität von 89% eine Unterscheidung zwischen einem tonisch-klonischen Anfall und einem nichtepileptischen Anfall ermöglichen, sodass die neuen Leitlinien zum ersten epileptischen Anfall und zu Epilepsien im Erwachsenenalter empfehlen, Laktat und die CK zeitnah nach dem Ereignis und nach 24–48 Stunden bei unklarem Ereignis zur Differenzialdiagnose zu bestimmen.
Wann ist eine Liquorpunktion indiziert?
Die Liquorpunktion ist ein wichtiger Bestandteil für die Diagnostik von Enzephalitiden als Ursache von Epilepsien. Da die Liquorpunktion in der Mehrzahl nach dem ersten Anfall jedoch unauffällig bleibt, insbesondere wenn der epileptische Anfall als einziges Symptom auftritt, wird eine generelle Lumbalpunktion nach einem ersten unprovozierten Anfall nicht empfohlen. Allerdings wäre jedoch ein fehlender Liquorbefund im Falle eines ersten Anfalls bei einer akuten Enzephalitis mit fatalen Folgen verbunden, sodass in solchen Fällen das Unterlassen einer Liquorpunktion fatale Konsequenzen hätte. Die Bestimmung des IDEAL-Scores (Süße et al. 2021) mit der Abfrage von 9 klinischen Symptomen ermöglicht mit einer Sensitivität von 98% und einem negativen prädiktiven Wert von 99% die Feststellung der Notwendigkeit einer Indikationsstellung zur Lumbalpunktion.
Warnzeichen: Zellzahlerhöhung von mehr als 10 Zellen/µl
Generell ist eine Zellzahlerhöhung als Folge eines isolierten epileptischen Anfalls stets sehr gering, während das Laktat innerhalb der ersten 6 Stunden nach einem Anfall deutlich ansteigt. Daher muss eine Zellzahlerhöhung von mehr als 10 Zellen/µl im Liquor immer als Red Flag gesehen werden und darf nicht als Reizpleozytose nach einem Anfall verkannt werden. In diesen Fällen sollte eine probatorische antivirale und antibiotische Therapie unmittelbar begonnen werden, bis die weitere virologische, mikrobiologische bzw. gegebenenfalls auch immunologische Diagnostik erfolgt ist. Bei klinischem Verdacht auf eine Autoimmunenzephalitis sollte die autoimmunologische Diagnostik stets aus Serum und Liquor erfolgen. Dieser ist gegeben bei rasch progredienter therapieresistenter Epilepsie oder neuropsychologischen bzw. psychiatrischen Symptomen. Im Unterschied zur Zellzahl steigt das Laktat sowohl im Liquor als auch im Serum nach einem tonisch-klonischen Anfall innerhalb von 6 Stunden rasch an, fällt dann aber auch im Verlauf rascher ab als die CK.
Fazit
Blutbestimmungen unter anfallssupprimierender Therapie sollten aufgrund von potenziellen Nebenwirkungen auf zahlreiche Organsysteme vor und unter der Therapie im klinischen Kontext erfolgen. Ausmass und Häufigkeit der Kontrollen sind abhängig von der Substanz, dem Alter des Patienten/der Patientin und dem Auftreten von etwaigen klinischen Nebenwirkungen. Die Referenzwerte für Serumspiegelkonzentrationen unter anfallssupprimierender Medikation sind zwar für die alten anfallssupprimierenden Medikamente gut untersucht, bei den neuen anfallssupprimierenden Medikamenten fehlen jedoch ausreichende klinische Daten zur Festlegung der Referenzwerte, sodass diese in vielen Fällen willkürlich festgelegt wurden und sich eine direkte Dosis-Wirkungs-Beziehung anhand der Werte nicht ableiten lässt. Insofern dient die Serumkonzentrationsbestimmung nicht der Findung der Zieldosis dieser Medikamente, kann jedoch wertvoll für Fragen zur Compliance oder zur Prüfung von Interaktionen bzw. veränderter Stoffwechselbedingungen sein. Nach einem unklaren Anfallsereignis sollten Laktat und CK zeitnah nach dem Ereignis und 24–48 Stunden danach zur differenzialdiagnostischen Klärung bestimmt werden.
Die Liquorbestimmung nach dem ersten Anfall ist nicht in jedem Fall erforderlich, ist aber unerlässlich, sofern sich klinisch oder anamnestisch der Anhalt für eine Enzephalitis (also etwa weitere neurologische Symptome wie Kopfschmerzen, fokal neurologische Defizite oder eine anhaltende Vigilanzstörung) ergibt. Der IDEAL-Score ermöglicht, die Indikationsstellung für die Lumbalpunktion klar zu definieren.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Welchen Beitrag kann therapeutisches Drug-Monitoring leisten?
Bariatrische Operationen sind eine wirksame Strategie zur Gewichts-reduktion bei Adipositas. Die damit veränderte Anatomie kann die Bioverfügbarkeit von Arzneimitteln massgeblich ...
Alzheimer: laufende klinische Studien, State of the Art der Biomarkerdiagnostik und gemischte Pathologien
Die Forschung an neuen Therapien für die Alzheimerkrankheit (AD) erfährt ein nie dagewesenes Momentum. Auf der internationalen Alzheimer- und Parkinsonkonferenz AD/PD in Wien gab es ...
Nahrungsergänzungsmittel bei ME/CFS: neue Hoffnung oder falsche Versprechen?
Chronische Erschöpfung, die nicht vergeht, Schmerzen, Konzentrationsprobleme, ein Leben in Zeitlupe. Myalgische Enzephalomyelitis/Chronisches Fatigue-Syndrom (ME/CFS) betrifft weltweit ...