Therapie nicht motorischer Symptome beim Morbus Parkinson
Autorin:
PD Dr. Petra Katschnig-Winter
Universitätsklinik für Neurologie
Medizinische Universität Graz
E-Mail: petra.katschnig@medunigraz.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Nicht motorische Symptome (NMS) der Parkinsonerkrankung tragen wie motorische Symptome stark zur Gesamtbelastung von Patienten und ihrer Lebensqualität bei, vor allem im fortgeschrittenen Stadium der Erkrankung. Sie können wie motorische Symptome fluktuieren und isoliert oder in Kombination auftreten.
Die zugrunde liegende Neurobiologie ist komplex und nicht vollständig geklärt, mit der größten Evidenz für neuropathologische Veränderungen im Rahmen der Parkinsonerkrankung, Mechanismen in Zusammenhang mit der dopaminergen Therapie und Effekten, die nicht spezifisch für die Parkinsonerkrankung sind. Obwohl es viele pharmakologische und nicht pharmakologische Therapieansätze gibt, stehen nur relativ wenige effektive Therapieoptionen zur Verfügung. Dieser Artikel wird sich auf die Therapie von neuropsychiatrischen NMS und Störungen von Schlaf und Wachheit beschränken.
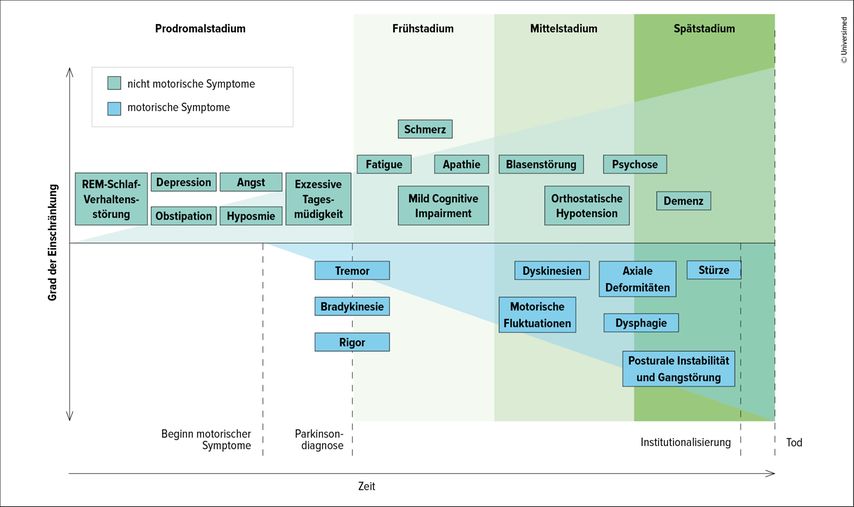
NMS können in allen Stadien der Erkrankung auftreten, oft schon im Prodromalstadium, bevor die ersten motorischen Symptome auffallen. Über die Zeit werden NMS häufiger, das fortgeschrittene Stadium ist vor allem durch neuropsychiatrische und autonome NMS gekennzeichnet.
Die Therapie basiert auf Expertenempfehlungen, wie den evidenzbasierten Empfehlungen zur Therapie von NMS der Internationalen Parkinson und Movement Disorder Society, und unserer eigenen klinischen Erfahrung. Wachsendes Interesse besteht auch an nicht pharmakologischen Therapien.
Neuropsychiatrische Symptome
Neuropsychiatrische NMS gehören zu den häufigsten NMS und können Affekt, Wahrnehmung, Denken und Motivation betreffen.
Depression
Depression ist mit Angst vor allem in frühen Krankheitsstadien ein häufiges NMS und betrifft im fortgeschrittenen Stadium bis zu 60% der Patienten. Pragmatisch werden Depressionen beim Morbus Parkinson mit Antidepressiva behandelt, ca. 25% der Parkinsonerkrankten nehmen Antidepressiva, meist SSRI, ein. Aufgrund der wenigen randomisiert-kontrollierten Studien mit SSRI, SNRI und Trizyklika ist die Evidenz dafür aber nicht sehr groß. In diesen Studien scheinen sie aber sicher und effektiv mit vergleichbaren Effektgrößen zu sein, was auch in einer rezenten Metaanalyse bestätigt wurde. Die beste Evidenz besteht neben Venlafaxin interessanterweise für die Dopaminagonisten Rotigotin und Pramipexol, insbesondere bei Depression im Rahmen von nicht motorischen Fluktuationen. Vorsicht ist geboten bei der Kombination von irreversiblen selektiven Monoaminooxidase-B-Hemmern und SSRI aufgrund der potenziellen Gefahr eines Serotonin-Syndroms.
Angst
Angst (generalisierte Angst, Panikattacken, spezifische Phobien) ist oft mit Depression assoziiert, wobei die Prävalenz im Verlauf stabiler als bei der Depression bleibt. Aufgrund ihrer Zulassung für Angsterkrankungen werden SSRI auch beim Morbus Parkinson häufig eingesetzt, zeitweise kombiniert mit niedrig dosierten Benzodiazepinen. Auch kognitive Verhaltenstherapie und bestimmte Yogaformen haben sich als wirksam erwiesen.
Apathie
Die Prävalenz für Apathie beträgt ca. 35–40%. Oft kommt Apathie gemeinsam mit Depression vor. Aufgrund der zugrunde liegenden dopaminergen und cholinergen Denervation hat sich der Dopaminagonist Rotigotin als wirksam und der Cholinesterasehemmer Rivastigmin als wahrscheinlich wirksam erwiesen. Für Stimulanzien gibt es keine Evidenz.
Psychose
Psychotische Symptome können in Form von Illusionen, Halluzinationen oder als wahnhafte Störungen auftreten und nehmen mit der Krankheitsprogression zu. Sie sind verbunden mit einem hohen Risiko für Hospitalisierung und Pflegeheimunterbringung sowie mit erhöhter Mortalität. Bei akut auftretenden psychotischen Symptomen steht die Abklärung metabolisch-toxischer Ursachen, von Infekten oder Exsikkose bzw. von Überdosierung oder Polypharmazie, insbesondere auch der Parkinsonmedikation, im Vordergrund. Nicht pharmakologische Maßnahmen umfassen die Schaffung einer hellen Umgebung und die Entfernung möglicher Trugquellen, Realitätstests und kognitive Verhaltenstherapie. Bei der pharmakologischen Therapie steht die Reduktion der Parkinsonmedikation an erster Stelle. Medikamente mit dem höchsten Risiko für psychotische Nebenwirkungen wie Amantadin, Anticholinergika und MAO-B-Hemmer müssen zuerst reduziert werden, gefolgt von Dopaminagonisten. Oft ist die Reduktion der Parkinsonmedikation allerdings nicht ausreichend, sodass der Einsatz von Neuroleptika unumgänglich ist. Clozapin hat sich als effektiv erwiesen, allerdings ist hier aufgrund des Agranulozytoserisikos ein engmaschiges Monitoring nötig. Für Quetiapin gibt es keine großen, hochwertigen Studien, allerdings hat es sich in einer Clozapin-kontrollierten Studie als ähnlich effektiv erwiesen. Aufgrund des Sicherheitsvorteils gegenüber Clozapin wird Quetiapin bei uns pragmatisch oft als Mittel der ersten Wahl verwendet. Rivastigmin ist möglicherweise effektiv bei Betroffenen mit Parkinsondemenz.
Abb. 1: Symptome der Parkinsonerkrankung (adaptiert von Poewe W et al.: Parkinson disease. Nat Rev Dis Primers 2017; 3: 17013)
Impulskontrollstörungen (ICD)
Hier besteht ein klarer Zusammenhang mit der dopaminergen Therapie, ein Auftreten ist auch Jahre nach Therapiebeginn möglich. Während Männer am häufigsten von Hypersexualität betroffen sind, stellen Kaufsucht und Binge Eating die häufigsten Impulskontrollstörungen bei Frauen dar. Aufgrund der großen persönlichen und sozialen Auswirkungen sind ein frühzeitiges Erkennen und promptes Management essenziell. Dieses besteht in der Reduktion der auslösenden dopaminergen Medikation, wobei auf ein mögliches Dopamin-Entzugssyndrom, das sich mit verschiedenen neuropsychiatrischen Symptomen manifestieren kann, geachtet werden muss. Ein Teil der Patienten kann aus diesem Grund nicht völlig von Dopaminagonisten entwöhnt werden. Im Zuge der Reduktion ist oft eine Neueinleitung oder Therapieanpassung von L-Dopa nötig. Eine kontinuierliche Zufuhr von L-Dopa über Pumpensysteme kann sich positiv auswirken. Kontroverse Daten liegen zu ICD und tiefer Hirnstimulation vor. Während es durch die postoperative Medikamentenreduktion oft zu einer Abnahme von ICD kommt, kann es auch zu einer Erstmanifestation nach der Operation kommen. Widersprüchliche Daten liegen auch für Amantadin und Naltrexon vor. Keine Evidenz gibt es für die Wirksamkeit von Clozapin oder Quetiapin. Auch nicht pharmakologische Maßnahmen wie kognitive Verhaltenstherapie oder die Beschränkung des Kreditrahmens/Internetzugangs ergänzen das Management.
Parkinsondemenz
Kognitive Einschränkungen können in allen Stadien der Erkrankung auftreten und zeigen eine große Variabilität in Bezug auf Schweregrad, Domänen und Progression. Betroffen sind v.a. Exekutivfunktionen, Gedächtnis, Aufmerksamkeit, Sprache und visuell-räumliche Fähigkeiten. Die Parkinsonerkrankung ist mit einem 2,6- bis 6-fach erhöhten Risiko für die Entwicklung kognitiver Einschränkungen assoziiert. Für das „mild cognitive impairment“ (MCI) gibt es keine zugelassene Therapie. Rivastigmin hat sich als effektiv in der Behandlung der Parkinsondemenz erwiesen und kann transdermal oder peroral angewandt werden. Für Donepezil verlief eine große Studie negativ, aufgrund der etablierten Wirkung außerhalb der Parkinsondemenz kann ein Einsatz aber erwogen werden. Widersprüchliche Daten liegen für Memantin vor. Kognitives und körperliches Training kann die Therapie abrunden.
Störungen von Schlaf und Wachheit
Störungen von Schlaf und Wachheit betreffen 60–90% der Parkinsonerkrankten und können motorische und kognitive Fähigkeiten, Stimmung und Fahrtauglichkeit beeinflussen. Neben der Neurodegeneration von schlafregulierenden Regelkreisen spielen motorische und nicht motorische Symptome, primäre Schlaferkrankungen und Nebenwirkungen der Therapie eine entscheidende Rolle.
Insomnie
Insbesondere Durchschlafstörungen mit fragmentiertem Schlaf führen zu einer eingeschränkten Leistung tagsüber. Als Ursache kommen motorische Parkinsonsymptome einschließlich motorischer Komplikationen, NMS wie Schmerzen, primäre Schlafstörungen wie die obstruktive Schlafapnoe und Nebenwirkungen der Parkinsontherapie infrage. Da gute klinische Studien fehlen, erfolgt die Behandlung oft aus Erfahrung.
Die Optimierung motorischer Symptome kann durch lang wirksame Dopaminagonisten oder eine kontinuierliche L-Dopa-Zufuhr über Pumpensysteme erfolgen. Retardiertes L-Dopa konnte in Studien zwar die nächtliche Beweglichkeit verbessern, hatte aber keine Auswirkungen auf die Schlafqualität und schlafbezogene Parameter in der Polysomnografie. Rasagilin konnte die Schlafarchitektur und -effizienz unabhängig von der Verbesserung der Motorik positiv beeinflussen. Kontinuierliche nächtliche Therapie mit Pumpen (L-Dopa, Apomorphin) scheint ebenso wirksam zu sein. Nicht medikamentöse Maßnahmen wie Schlafhygiene (regelmäßige Schlafenszeiten, Tageslichtexposition, regelmäßige Aktivitäten, v.a. im Freien), Entspannungstechniken, kognitive Verhaltenstherapie und Lichttherapie können unterstützen. Manchmal ist die kurzzeitige Einnahme von Zolpidem oder Eszopiclon indiziert. Bei Patienten mit begleitender Depression kann eine Therapie mit Trazodon, Venlafaxin, Nortriptylin oder Mirtazapin erwogen werden. Die Effekte von Melatonin sind gering, sodass dafür keine generelle Empfehlung besteht.
Exzessive Tagesmüdigkeit (ETM)
Eine erhöhte Einschlafneigung trotz ausreichender Schlafzeit betrifft ca. 20–60% der Parkinsonerkrankten. Als Ursachen kommen primäre Schlafstörungen, aber auch nächtliche motorische und nicht motorische Komplikationen sowie die dopaminerge Therapie infrage. 18–25% der Erkrankten berichten von ETM nach Therapiebeginn. Neben der Behandlung primärer Schlafstörungen steht die Therapie motorischer und nicht motorischer Komplikationen, üblicherweise durch lang wirksame oder kontinuierliche dopaminerge Therapie, im Vordergrund. Für Stimulanzien wie Koffein, Modafinil oder Methylphenidat gibt es wenig Evidenz.
REM-Schlaf-Verhaltensstörung (RBD)
Die RBD ist durch eine reduzierte REM-Schlaf-Atonie mit exzessiven Bewegungen gekennzeichnet und eng mit Alpha-Synucleinopathien assoziiert. Hier gilt es, eine sichere Schlafumgebung zu schaffen und medikamentös trotz fehlender großer Multicenterstudien Clonazepam oder Melatonin einzusetzen. Clonazepam zeigt höhere Ansprechraten, während Melatonin ein besseres Nebenwirkungsprofil aufweist.
Mit erhöhter Aufmerksamkeit für die Problematik, neuen Forschungsprojekten, spezialisiertem Training und innovativen Pflegemodellen wird es in Zukunft hoffentlich zu einer Verbesserung der Therapiemöglichkeiten von nicht motorischen Symptomen beim Morbus Parkinson kommen.
Literatur:
bei der Verfasserin
Das könnte Sie auch interessieren:
Menschen mit Demenz: Was beeinflusst deren Überleben nach Diagnosestellung?
Verschiedenste Faktoren beeinflussen die Überlebenszeit nach einer Demenzdiagnose. Das Wissen um Risikofaktoren zum Zeitpunkt der Diagnose einer Demenzerkrankung oder in deren Verlauf ...
Alzheimer: Was gibt es Neues in der Biomarker-Entwicklung?
Schätzungen zufolge leben in Österreich 115000 bis 130000 Menschen mit einer Form der Demenz. Eine Zahl, die sich bis zum Jahr 2050 verdoppeln wird.1 Antikörper-Wirkstoffe könnten in der ...
Kappa-FLC zur Prognoseabschätzung
Der Kappa-freie-Leichtketten-Index korreliert nicht nur mit der kurzfristigen Krankheitsaktivität bei Multipler Sklerose, sodass er auch als Marker zur Langzeitprognose der ...