Sequenz als Schlüssel zu guten Langzeitergebnissen
Bericht: Dr. Judith Moser
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Patient:innen mit Östrogenrezeptor-positivem/HER2-negativem metastasiertem Mammakarzinom, die nach Erstlinienbehandlung eine Progression erleiden, profitieren von Zweitlinienregimes auf Basis endokrin wirksamer Substanzen, sofern die endokrine Sensitivität erhalten ist. Elacestrant (Orserdu®) bietet hierbei als erster und bisher einziger zugelassener oraler selektiver Östrogenrezeptor-Degrader eine hochwirksame und gut verträgliche orale Therapieoption.
Keypoints
-
Neue ESMO-Guidelines bestätigen die biomarkergestützte Behandlung in der Zweitlinientherapie des metastasierten HR+/HER2– Mammakarzinoms nach CDK4/6-Inhibition plus ET.1
-
Die Monotherapie mit Elacestrant zeigte in einer explorativen Post-hoc-Analyse nach längerer CDK4/6-Inhibition + ET ≥12 Monate ein medianes PFS von 8,6 Monaten (vs. 1,9 Monate im SOC-Arm).6,**
-
Eine weitere explorative Post-hoc-Analyse der EMERALD-Studie lieferte gute Ergebnisse bei Patient:innen nach CDK4/6-Inhibition + ET ≥12 Monate mit Komutationen (ESR1 und PIK3CA).6,7
-
Real-World-Daten untermauern die Ergebnisse der Zulassungsstudie.8
-
Elacestrant zeigt ein günstiges Nebenwirkungsprofil mit einer niedrigen Rate an nebenwirkungsbedingten Therapieabbrüchen (3,4%).6
-
Elacestrant bietet den Vorteil einer einfachen oralen Einnahme einmal täglich (Standarddosis 345mg/Tag).18
Eine endokrine Therapie (ET) in Kombination mit CDK4/6-Inhibitoren ist im Management des metastasierten Östrogenrezeptor-positiven/HER2-negativen Mammakarzinoms als Erstlinienstrategie etabliert.1 Prof. Dr. Sherko Kümmel, PhD, Interdisziplinäres Brustkrebszentrum der Kliniken Essen-Mitte, Essen, diskutierte im Rahmen des ESMO Breast Cancer 2025 die Optionen ab der zweiten Behandlungslinie. „Bei Eintreten der Progression sollte eine Testung auf eine Reihe genomischer Alterationen erfolgen.“1 Als zweiter entscheidender Faktor gilt die endokrine Sensitivität. Ist sie erhalten, empfiehlt sich eine möglichst lange Fortführung der ET-basierten Strategie mit oder ohne zielgerichtete Therapie. Dagegen kommen bei Patient:innen mit primärer endokriner Resistenz oder viszeraler Krise Chemotherapie oder Antikörper-Wirkstoff-Konjugate infrage.
ET-basierte Behandlungsmöglichkeiten
Nach einer Erstlinientherapie mit einem CDK4/6-Inhibitor in Kombination mit einem Aromataseinhibitor sind heute in Abhängigkeit von der Tumorbiologie zahlreiche zielgerichtete Optionen verfügbar. Wenn Driver-Alterationen fehlen, stehen eine Fulvestrant-Monotherapie oder Everolimus plus ET oder ein Switch der ET ± CDK4/6-Inhibition zur Diskussion.
Bei Tumoren mit PIK3CA-Mutationen empfehlen die Guidelines Alpelisib/Fulvestrant, bei PIK3CA/AKT/PTEN-Alterationen Capivasertib/Fulvestrant.1 Während Aberrationen des PI3K/AKT/mTOR-Pathway eine intrinsische endokrine Resistenz auslösen können, geht eine erworbene Resistenz hauptsächlich auf die Entwicklung von ESR1-Mutationen unter ET zurück.2,3 Für Capivasertib/Fulvestrant liegen derzeit aus der CAPItello-291-Studie keine Daten für Patient:innen mit ESR1-Mutationen vor.4
EMERALD: Outcomes nach langer Erstlinien-Response
Hat die Testung eine isolierte ESR1-Mutation erbracht, legen die ESMO-Richtlinien als einzige Option den oral verabreichten selektiven Östrogenrezeptor-Degrader (SERD) Elacestrant nahe.1 In der Phase-III-Studie EMERALD wurde Elacestrant nach Progression unter oder nach ein bis zwei ET-Linien plus CDK4/6-Inhibition im metastasierten Setting geprüft.5 Der SERD bewirkte verglichen mit einer Therapie nach Wahl (Fulvestrant, Anastrozol, Letrozol, Exemestan) bei Patient:innen mit ESR1-Mutation ein medianes PFS von 3,8 Monaten vs. 1,9 Monate (primärer Endpunkt; HR: 0,55 [95% CI 0,39–0,77]; p<0,0005).
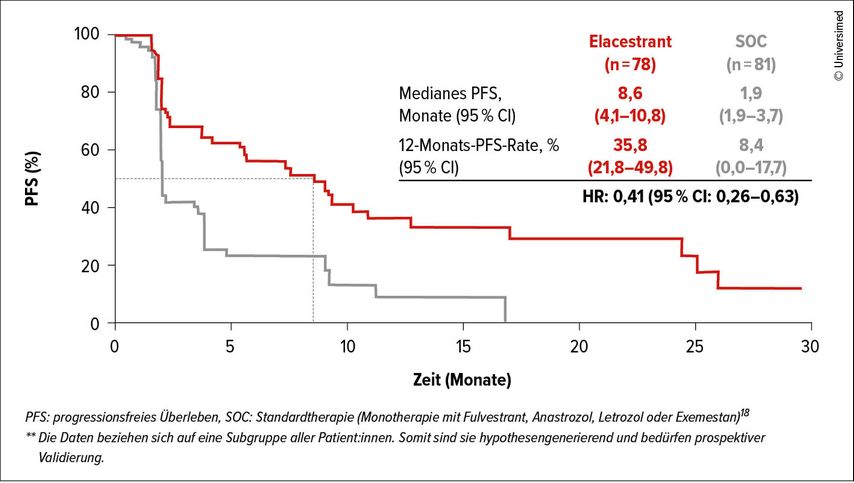
Kümmel nahm Bezug auf eine explorative Post-hoc-Analyse der EMERALD-Studie, in der Personen analysiert wurden, deren Erstlinientherapie mit ET plus CDK4/6-Inhibition mindestens zwölf Monate aufrechterhalten werden konnte (n=159).6 „In dieser ET-sensitiven Gruppe betrug das mediane PFS unter Elacestrant 8,6 Monate“, so Kümmel. Verglichen mit der Kontrolltherapie (1,9 Monate) resultierte eine relative Reduktion von Krankheitsprogression oder Tod um 59% (HR: 0,41; Abb.). Eine längere Exposition gegenüber CDK4/6-Inhibitoren ist bei ESR1-mutierten Tumoren mit endokriner Sensitivität gegenüber Elacestrant assoziiert.6,7
Abb.: Post-hoc-Analyse: PFS unter Elacestrant vs. SOC nach mindestens zwölfmonatigem Ansprechen auf die Erstlinientherapie aus ET+CDK4/6-Inhibition (modifiziert nach Bardia A et al.)6,19,**
Bemerkenswerte Ergebnisse erbrachte eine Post-hoc-Analyse, der zufolge die Effektivität von Elacestrant nicht von der „variant allele frequency“ (VAF) abhing. Dies zeigte sich eindrucksvoll im Kollektiv mit ESR1/PIK3CA-Komutationen nach vorheriger ET + CDK4/6-Inhibition ≥12 Monate (n=62): Hier verlängerte Elacestrant das mediane PFS (5,5 vs. 1,9 Monate; HR: 0,42), obwohl 89% der ESR1-Mutationen eine geringere VAF als die PIK3CA-Mutationen aufwiesen.7 Kümmel: „Wenn der Tumor eine ESR1-Mutation aufweist, funktioniert die Therapie unabhängig von der VAF.“
Verlängerung des PFS in der gelebten Praxis
In den USA gesammelte Real-World-Daten untermauern die Effektivität von Elacestrant unter klinischen Routinebedingungen.8 Bei 166 Patient:innen nach einer oder zwei ET-Linien fand sich ein medianes rwPFS* von acht Monaten in der Zweit- und Drittlinie. Dies ähnelt dem Ergebnis in der EMERALD-Subgruppe mit einem besonders langen Ansprechen auf die Erstlinien-ET, auch wenn retrospektive Beobachtungsanalysen nicht für direkte Vergleiche mit klinischen Studien gedacht sind.6 Zudem verlief die PFS-Kurve gleichmäßiger als die PFS-Kurven in EMERALD, die zu Beginn einen steilen Abfall gezeigt hatten.5,6 Laut Kümmel lässt sich dies auf die verbesserte Selektion mit einem Fokus auf der endokrin sensitiven Population zurückführen. „Man hat gelernt, welche Patient:innen besonders profitieren.“
Ein weiterer Vorteil der Behandlung mit Elacestrant ergibt sich aus der guten Verträglichkeit. In der EMERALD-Studie wurden keine Grad-4-Nebenwirkungen verzeichnet, und es fielen keine hämatologischen Signale auf.6 Am häufigsten kam es im Prüfarm zu Schmerzen des Bewegungsapparats (41%, Gruppierung von ähnlichen Begriffen) und Übelkeit (35%). Mit 3,4% war die Rate an Therapiebeendigungen aufgrund von Nebenwirkungen niedrig.
Survey bestätigt Präferenz für orale Therapie
Orale Einnahme und geringe Toxizität kommen den Bedürfnissen der Patient:innen mit metastasiertem Mammakarzinom entgegen. In einer 2024 in Deutschland, Italien und dem UK durchgeführten Umfrage gaben 90% von 191 Befragten an, eine orale Verabreichung ihrer Krebstherapie zu präferieren.9 64% sprachen sich dafür aus, Chemotherapien möglichst lang hinauszuzögern.
ESR1-Mutations-Testung aus dem Blut
„Die kumulative Inzidenz von ESR1-Mutationen steigt im Verlauf der Erstlinientherapie an und erreicht nach etwa zwei Jahren ein Plateau“, erläuterte Prof. Dr. Michail Ignatiadis, Institut Jules Bordet, Hôpital Universitaire de Bruxelles, Brüssel.10 Typischerweise zeigen ESR1-Mutationen eine subklonale Entwicklung und weisen eine unregelmäßige Verteilung innerhalb des Tumors und verschiedener Tumorherde auf, wodurch Gewebsbiopsien mit einer niedrigeren Trefferquote einhergehen als die blutbasierte Erfassung aus zirkulierender Tumor-DNA (ctDNA).11 Gemessen an der ctDNA beträgt die Mutationsprävalenz bis zu 40% (bei einer Tumorfraktion ≥1 bis zu 60%) in der zweiten und dritten Linie; dagegen liegt die ESR1-Prävalenz gemessen im Gewebe bei rund 30%.11 „Die Diagnostik soll daher vorzugsweise mittels Liquid Biopsy erfolgen“, betonte Ignatiadis.12–14
Testungen im Hinblick auf ESR1-Mutationen werden nach jedem Progressionsereignis unter ET empfohlen, da die Wahrscheinlichkeit einer Detektion mit der Zeit ansteigt.12,15–17 Da sich die Mutation in erster Linie im metastasierten Setting entwickelt, soll kein primär archiviertes Gewebe verwendet werden, sondern die Testung soll generell anhand einer aktuellen Probe erfolgen.14 Eine Detektion ist mittels Next-Generation-Sequencing oder digitaler PCR möglich.
* Zeit ab dem Indexdatum bis zum frühesten Ergebnis (Beginn der nächsten Therapielinie bei mBC bis zum Fortschreiten der Krankheit oder Tod), bewertet anhand der Time-to-Event- und Kaplan-Meier-Methode
Entgeltliche Einschaltung
Mit freundlicher Unterstützung durch die Firma Stemline
Fachkurzinformation siehe unten | 2025-08 - MAT-AT-ELA-00143
Quelle:
Symposium der Firma Menarini Stemline, 14. Mai 2025 & Poster 375P, ESMO Breast Cancer 2025, München
Literatur:
1 Gennari A et al.: Ann Oncol 2021; 32(12): 1475-95 2 Xu P et al.: Acta Pharmacol Sin 2021; 42(2): 171-8 3 Brett JO et al.: Breast Cancer Res 2021; 23(1): 85 4 Turner NC et al.: NEngl J Med 2023; 388(22): 2058-70 5 Bidard FC et al.: JClin Oncol 2022; 40(28): 3246-566 6 Bardia A et al.: Clin Cancer Res 2024; 30(19): 4299-309 7 Bardia A et al.: SABCS 2024, Abstr. #P1-01-25 8 Swallow E et al.: SABCS 2024, Abstr. #P3-10-08 9 Schumacher-Wulf E et al.: ESMO Breast Cancer 2025, Abstr. #375P 10 Bidard FC et al.: ESMO 2019, Abstr. #307PD 11 Bhave MA et al.: Breast Cancer Res Treat 2024; 207(3): 599-609 12 Burstein HJ et al.: ASCO guideline rapid recommendation update. J Clin Oncol 2023; 41(18): 3423-5 13 Turner NC et al.: Lancet Oncol 2020; 21(10): 1296-308 14 NCCN Guidelines® for Breast Cancer V.3.2025 15 Jeselsohn R et al.: Clin Cancer Res 2014; 20(7): 1757-67 16 Jeselsohn R et al.: Cancer Cell 2018; 33(2): 173-86 17 Allouchery V et al.: Breast Cancer Res 2018; 20(1): 40 18 Fachinformation Orserdu®, aktueller Stand 19 Kaklamani et al.: ASCO Annual Meeting 2023, Abstr. #1070 (Pst_ Bd_291)
Fachkurzinformation
ORSERDU® 86 mg Filmtabletten, ORSERDU® 345 mg Filmtabletten. Wirkstoff: Elacestrant. Zusammensetzung: 1 Filmtabl. enthält Elacestrant-Dihydrochlorid entsprechend 86,3 mg bzw. 345 mg Elacestrant. Sonst. Bestandt.: Tablettenkern: Mikrokristalline Cellulose (E460), Mikrokristalline Cellulose, Siliciumdioxid-beschichtet, Crospovidon (E1202), Magnesiumstearat (E470b), Kolloidales Siliciumdioxid (E551). Filmüberzug: Opadry II blau 85F105080 mit Poly(vinylalkohol) (E1203), Titandioxid (E171), Macrogol (E1521), Talkum (E553b), Brillantblau FCF Aluminiumsalz (E133). Anwendungsgebiet: Monotherapie zur Behandlung von postmenopausalen Frauen sowie von Männern mit Estrogenrezeptor (ER)-positivem, HER2-negativem, lokal fortgeschrittenem oder metastasiertem Brustkrebs mit einer aktivierenden ESR1-Mutation, deren Erkrankung nach mind. einer endokrinen Therapielinie, einschließlich eines CDK 4/6-Inhibitors, fortgeschritten ist. Gegenanzeigen: Überempfindlichk. gegen d. Wirkstoff od. einen d. sonst. Bestandt. Nebenwirkungen: Sehr häufig: Anämie, vermind. Appetit, Kopfschmerzen, Hitzewallungen, Übelkeit, Erbrechen, Diarrhö, Obstipation, abdomineller Schmerz, Dyspepsie, Arthralgie, Rückenschmerzen, Fatigue, Aspartat-Aminotransferase erhöht, Triglyceride erhöht, Cholesterin erhöht, Alanin-Aminotransferase erhöht, Kalzium erniedrigt, Kreatinin erhöht, Natrium erniedrigt, Kalium erniedrigt. Häufig: Harnwegsinfektion, Lymphozytenzahl erniedrigt, Insomnie, Schwindelgefühl, Synkope, Dyspnoe, Husten, Stomatitis, Ausschlag, Schmerzen in den Extremitäten, die Skelettmuskulatur betreffende Brustschmerzen, Knochenschmerzen, Asthenie, alkalische Phosphatase im Blut erhöht. Gelegentlich: Thromboembolie (venös), akutes Leberversagen. Warnhinweis: Arzneimittel für Kinder unzugängl. aufbewahren. Pharmakotherapeutische Gruppe: Endokrine Therapie, Antiestrogene, ATC-Code: L02BA04. Verkaufsabgrenzung: Deutschland: Verschreibungspflichtig. Österreich: Rezept- und apothekenpflichtig, wiederholte Abgabe verboten. Weitere Informationen zu Warnhinweisen und Vorsichtsmaßnahmen für die Anwendung, Wechselwirkungen mit anderen Arzneimitteln oder sonstige Wechselwirkungen, Schwangerschaft und Stillzeit sowie Nebenwirkungen sind der veröffentlichten Fachinformation zu entnehmen, deren aufmerksame Durchsicht empfohlen wird. Pharmazeutischer Unternehmer: Stemline Therapeutics B.V., Basisweg 10, 1043 AP Amsterdam, Niederlande. Örtl. Vertreter DE: Menarini Stemline Deutschland GmbH, Tel: +49 (0)800 000 8974, EUmedinfo@menarinistemline.com . Örtl. Vertreter AT: Stemline Therapeutics B.V., Tel: +43 (0)800 297 649, EUmedinfo@menarinistemline.com . (Stand 01.2025)