Strategien zur Deeskalation der Therapie bei schubförmiger Multipler Sklerose
Autor:
Prim. Priv.-Doz. Dr. Michael Guger, MBA
Abteilung für Neurologie
Pyhrn-Eisenwurzen Klinikum Steyr
E-Mail: info@drguger.com
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Prospektiv gesammelte Daten aus Österreich haben die Wirksamkeit der Deeskalation der Therapie von Kategorie 3 auf Kategorie 1 und 2 bei Patient:innen mit schubförmig remittierender Multipler Sklerose evaluiert. Eine Zusammenfassung der Ergebnisse.
Hintergrund und Ziel
Das Ziel unserer Analyse war es, die Wirksamkeit der Deeskalation von Natalizumab, Ocrelizumab und Ofatumumab (Kategorie 3) auf Cladribin, Dimethylfumarat, Fingolimod, Ozanimod, Ponesimod, Siponimod und Teriflunomid (Kategorie 1 und 2) bei Patient:innen mit schubförmiger Multipler Sklerose zu evaluieren. Dies erfolgte einerseits im Vergleich der jeweiligen sequenziellen Behandlung und andererseits in Abhängigkeit von der Dauer der Therapiepause zwischen Kategorie-3- und Kategorie-1- und -2-Medikation mittels prospektiv gesammelter Daten.
Methoden
Wir schlossen hierfür 389 Patient:innen aus dem ÖMSTR (Österreichisches Multiple-Sklerose-Therapie-Register) mit einer schubförmigen Multiplen Sklerose (RMS) ein, welche ab 2006 mit einer Behandlung mit Natalizumab, Ocrelizumab und Ofatumumab im Register begonnen haben und zumindest 3 Monate die Medikation beibehalten haben. Danach musste eine Deeskalation innerhalb eines Jahres auf Cladribin, Dimethylfumarat, Fingolimod, Ozanimod, Ponesimod, Siponimod und Teriflunomid erfolgen und ebenso für zumindest 3 Monate beibehalten werden. Die Transitionsdauer wurde in 3 Intervallgruppen unterteilt: <3 Monaten, 3–6 Monate und 6–12 Monate.
Zur Analyse der Schubrate wurden ein generalisiert lineares Modell (GLM), zur Berechnung der EDSS(Expanded Disability Status Scale)-Progression und -Regression und der Zeit bis zum ersten Schub eine Cox-Regressionsanalyse herangezogen.
Ergebnisse
Der überwiegende Anteil der Patient:innen startete eine Kategorie-3-Behandlung mit Natalizumab für durchschnittlich 42 Monate und wechselte zumeist auf Fingolimod, gefolgt von Dimethylfumarat, Cladribin und Teriflunomid für durchschnittlich 61 Monate. Innerhalb von 3 Monaten Therapiepause erfolgte bei 267 Patient:innen, zwischen 3 und 6 Monaten bei 89 Patient:innen und zwischen 6 und 12 Monaten bei 33 Patient:innen die Deeskalation. Die jährliche Schubrate (ARR) betrug 0,22 unter der Kategorie-3-Behandlung und 0,36 unter der Kategorie-1- und -2-Behandlung (p=0,009).
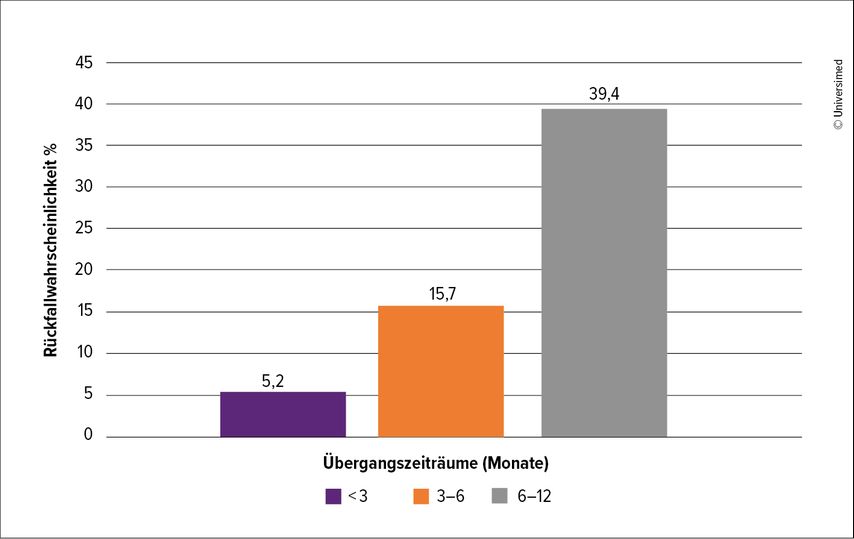
Während der Transition wurden ebenso signifikante Unterschiede festgestellt: 14 (5,2%) Patient:innen in der Gruppe <3 Monaten erfuhren einen Schub, 14 (15,7%) in der 3–6-Monate-Kohorte und 13 (39,4%) in der 6–12-Monate-Gruppe (p<0,001) (Abb. 1). Die Dauer der Switch-Periode hatte keinen signifikanten Einfluss auf ARR, EDSS-Progression und -Regression nach erfolgter Deeskalation.
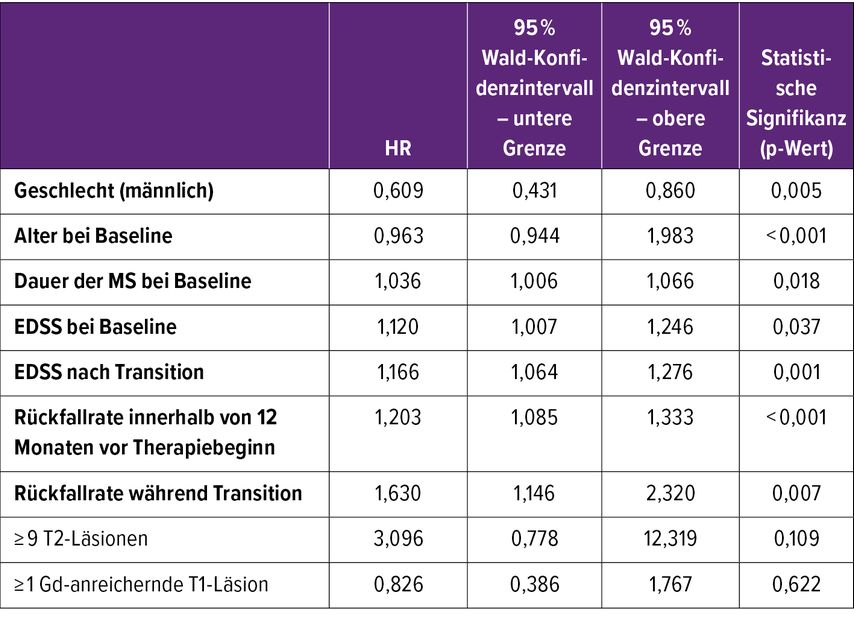
Folgende Prädiktoren zeigten ein herabgesetztes Risiko für Schübe nach der Deeskalation an: männliches Geschlecht, reduzierte ARR zur Baseline und während der Transition, höheres Alter und kürzere Krankheitsdauer zur Baseline und niedriger EDSS-Wert zur Baseline und nach der Transition (Tab. 1). Folgende Risikofaktoren wiesen hingegen auf ein erhöhtes Risiko für EDSS-Behinderung nach der Deeskalation hin: höheres Alter zur Baseline und höherer EDSS-Wert nach der Transition.
Zusammenfassung
Zum einen konnten wir ein erhöhtes Risiko für Schübe und EDSS-Verschlechterung nach der Deeskalation von Natalizumab, Ocrelizumab und Ofatumumab in der sequenziellen Behandlung nachweisen. Zum anderen wurden eine erhöhte Schubrate während der Switch-Periode und ein erhöhter EDSS-Wert nach der Transition als unabhängige Risikofaktoren für Schubaktivität und EDSS-Progression nach der Deeskalation evaluiert. Abschließend untermauern unsere Daten die Wichtigkeit der raschen Umstellung (<3 Monaten) im Rahmen der Deeskalation.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Parkinsonprävention durch Lebensstilmodifikation
Noch bevor die ersten motorischen Symptome der Parkinsonkrankheit auftreten, beginnt die Erkrankung auf biologischer Ebene. Auch wenn bislang keine pharmakologische Neuroprotektion oder ...
Ist die ketogene Diät eine Präzisionsmedizin?
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...