Mögliche Langzeitfolgen neuroonkologischer Therapien
Autorin:
Dr. Waltraud Kleindienst, MBA
Universitätsklinik für Neurologie, Neurologische Intensivmedizin und Neurorehabilitation
Salzburg
E-Mail: w.kleindienst@salk.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Langzeitüberlebende Hirntumorpatienten sind häufig von Folgeerkrankungen betroffen, welche sich oft erst nach Jahren manifestieren oder verschlechtern. Beeinträchtigungen wie zum Beispiel kognitive Veränderungen zeigen sich häufig im Alltag und haben weitreichende Auswirkungen auf die Lebensqualität. Einer frühzeitigen Diagnose von Folgeerkrankungen im Rahmen von Follow-up-Untersuchungen sollte daher besonderes Augenmerk geschenkt werden.
Keypoints
-
Langzeitfolgen neuroonkologischer Therapien treten oft erst Jahre nach erfolgreicher Behandlung auf.
-
50–90% der Langzeitüberlebenden entwickeln kognitive Einschränkungen während und nach der Tumorerkrankung und damit eine reduzierte „quality of life“. Diese Einschränkungen sind meist unterdiagnostiziert und zeigen im Langzeitverlauf einen progredienten Verlauf.
-
Endokrinopathien zählen zu den häufigsten Folgeerkrankungen.
-
Sekundärmalignome gehören zu den am schwersten wiegenden Langzeitfolgen mit einer kumulativen Inzidenz von 6,4% nach 30 Jahren bei behandelten pädiatrischen Hirntumorpatienten.
Infolge einer besseren Behandlung neuroonkologischer Patienten ergibt sich eine hohe Zahl Überlebender von an Hirntumoren Erkrankten. Diese Patienten haben ein erhöhtes Risiko für verschiedene Folgeerkrankungen, auch Jahre nach erfolgreicher Behandlung im Kindesalter, bedingt durch die Tumorerkrankung selbst und die sich daraus ergebende kausale Therapie. Diese Patientengruppe benötigt daher konsequente Follow-up-Untersuchungen für das gesamte Leben, um Sekundärerkrankungen rasch detektieren und die „quality of life“ verbessern zu können.
Langzeitfolgen neuroonkologischer Therapien entstehen infolge der direkten Schädigung durch den Tumor selbst, durch dessen Entfernung und durch die begleitend gesetzten Therapiemaßnahmen, wie Chemotherapie, Radiotherapie und eventuell erforderliche Begleitmedikation wie zum Beispiel Antiepileptika. Junge Patienten stellen eine kritische Patientengruppe dar, da das frühe Auftreten der Erkrankung im Kindesalter die Entwicklung der Betroffenen wesentlich beeinträchtigt. Das Spektrum dieser Langzeitfolgen ist sehr breit und umfasst zentrale fokale und nonfokale ZNS-Komplikationen, periphere Komplikationen und, hochrelevant, sekundäre Neoplasien.
Die hauptsächlich relevanten Patientengruppen haben prognostisch günstige Gliome wie Oligodendrogliome, gutartige Tumoren wie Meningeome, Hypophysentumoren und pädiatrische Tumoren mit einem großen Impact, da sich das Gehirn und die Organe noch in Entwicklung befinden.1
Kognitive Beeinträchtigungen
50–90% der Langzeitüberlebenden entwickeln kognitive Einschränkungen während und nach der Tumorerkrankung mit daraus resultierender reduzierter Lebensqualität. Die Einschränkungen der kognitiven Leistungen sind meist unterdiagnostiziert und treten in einer Frequenz bis zu 62% bei nicht behandelten Gliomen auf. 27% der langzeitüberlebenden Patienten mit oligodendroglialen Tumoren, welche eine Standardtherapie erhielten, zeigten in Studien kognitive Beeinträchtigungen im Sinne eines „mild cognitive impairment“ nach 2–5 Jahren. 39% zeigten schwere Beeinträchtigungen mit Störungen vor allem der Exekutivfunktion und Aufmerksamkeitsstörungen mit MR-topografischen Veränderungen der weißen Substanz und einer Hirnvolumenreduktion. Der Anteil der Patienten mit kognitiven Störungen stieg nach einem Beobachtungszeitraum von >10 Jahren auf 69% an.2
Langzeitüberlebende glialer Hirntumoren zeigen im Verlauf eine progressive Verschlechterung des kognitiven Leistungsprofils. So hatten 39% der behandelten Patienten in einer Follow-up-Studie kognitive Defizite 6,1 Jahre nach Therapie. Der Prozentsatz erhöhte sich auf 53% der Patienten nach 12 Jahren.3
Viele Jahre nach Tumorbehandlung zeigte sich in Untersuchungen bei 39% der Patienten eine schwere Fatigue verbunden mit Konzentrationsstörungen und reduziertem Antrieb, wobei begleitende Dauermedikationen wie z.B. Antiepileptika eine wichtige Rolle spielen.
Risiko für vaskuläre Ereignisse
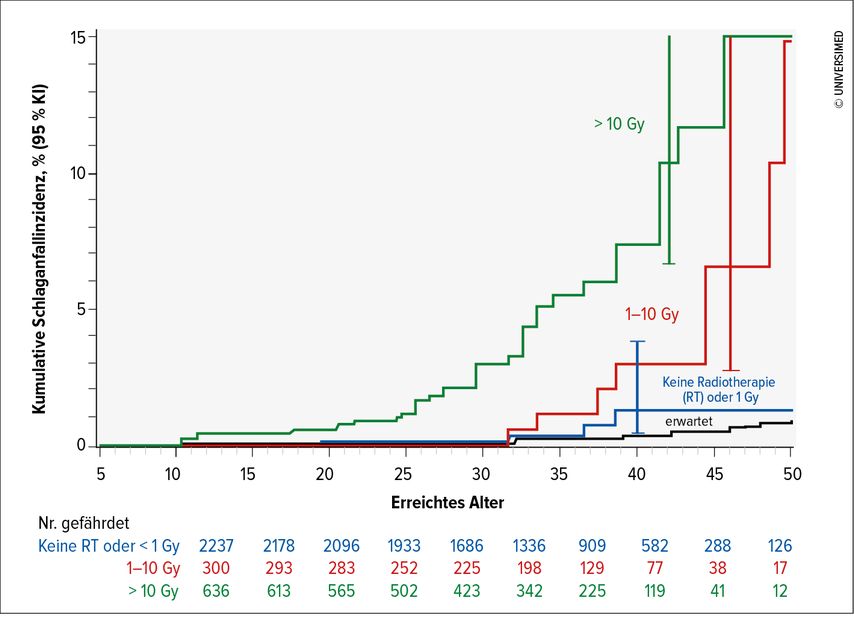
Therapieassoziierte fokale ZNS-Erkrankungen, wie ischämische und hämorrhagische Schlaganfälle, treten doppelt so häufig wie in der Normalbevölkerung auf. Das kumulative Risiko für einen fatal verlaufenden Schlaganfall bei behandelten Hirntumorpatienten liegt bei 11,3% verglichen mit 1% in der gesunden Kontrollgruppe (Abb. 1). Das Risiko für vaskuläre Malformationen ist erhöht mit 5% nach Therapie, ebenso erhöht ist das Auftreten vaskulär okklusiver Erkrankungen wie z.B. Moyamoya.4
Abb. 1: Kumulatives Schlaganfallrisiko nach Radiotherapie in einer Langzeit-Follow-up Serie (mod. nach Di Stefano AL et al. 2019)4
Das SMART(„stroke-like migraine attacks after radiation therapy“)-Syndrom präsentiert sich mit einem Mosaik an Symptomen, reversiblen fokal neurologischen Defiziten verbunden mit Kopfschmerzen, epileptischen Anfällen und MR-Veränderungen in 73%. Das Intervall bis zum Auftreten eines SMART-Syndroms kann sich über Jahre nach der Tumortherapie erstrecken.4 Wichtig ist das Erkennen eines SMART-Syndroms, um Fehldiagnosen zu vermeiden und eine wirksame kausale Therapie anbieten zu können.
Hormonelle Folgen sind häufig
Infolge der Therapie von Hirntumorpatienten gehören Endokrinopathien zu den häufigsten Folgeerkrankungen. Diese spielen eine große Rolle bei Kindern, wobei das Wachstum und die Entwicklung schwer gestört sein können. Die Inzidenz wird mit einer hohen Variabilität mit bis zu 93% angegeben. Im Erwachsenenalter sind hormonelle Störungen nach erfolgter Behandlung signifikant unterdiagnostiziert.
Endokrinopathien sind zeitabhängig und zeigen einen zunehmenden Verlust der hypothalamischen Funktion über Jahre mit Reduktion des Wachstumshormons (GH) sowie von Thyreotropin, LH, FSH und ACTH. Die endokrine Störung mit Reduktion des Wachstumshormons tritt mit einer Häufigkeit von 82,8% auf. Sie hat auch beim erwachsenen Patienten einen Stellenwert und führt bei fehlender Substitution zu Fatiguesymptomatik, Reduktion der Muskelmasse und depressiver Verstimmung.
Häufigkeit von Sekundärneoplasien
Das Auftreten von Sekundärneoplasien ist sicherlich die am schwerwiegendste Langzeitfolge einer onkologischen Therapie. Sekundärneoplasien sind meist maligne. Die häufigsten Folgetumoren sind solide Tumoren wie Meningeome, Gliome, maligne Schwannome und Sarkome sowie hämatologische Erkrankungen. Eine retrospektive Studie mit 3627 eingeschlossenen Patienten zeigte eine kumulative Inzidenz von 6,4% nach 30 Jahren mit Auftreten von Sekundärmalignomen bei pädiatrischen Hirntumorpatienten. Darin fanden sich Hirntumoren unterschiedlicher Dignität (40%), Schilddrüsenkarzinome (11,1%), Leukämien (9,4%), Sarkome (8,5%) und andere Tumoren (30,8%).5
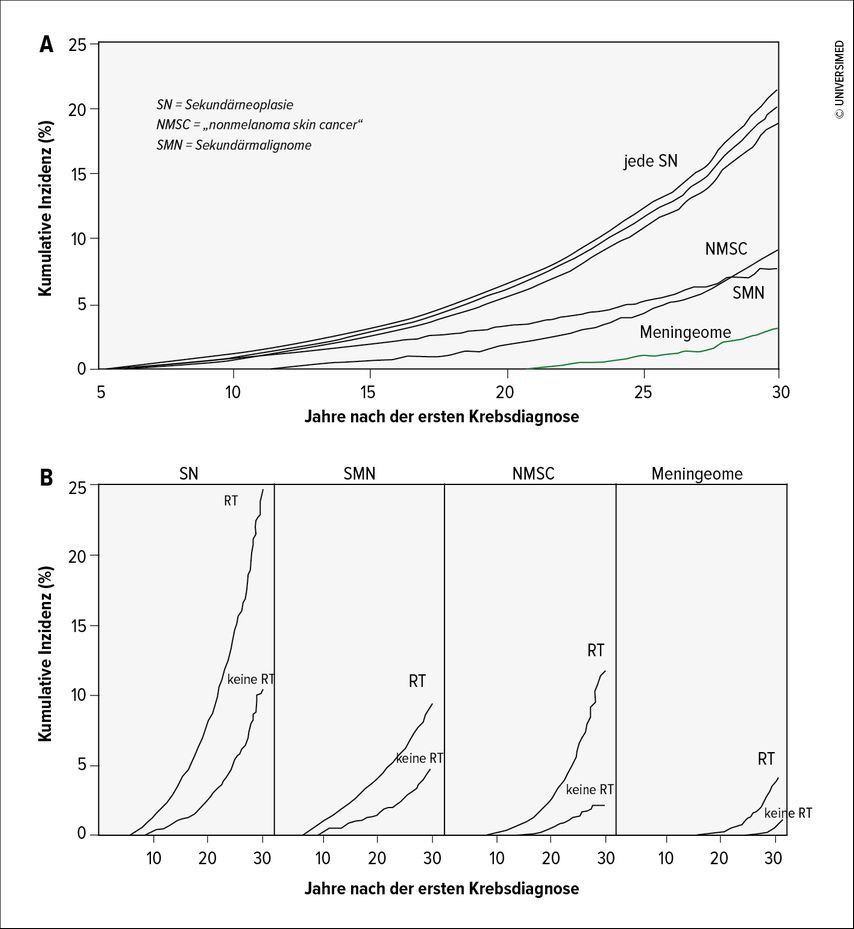
Das Auftreten von Sekundärneoplasien ist nicht nur bedingt durch eine Radiotherapie in der Vergangenheit. Als wichtiger Kofaktor ist die Gabe von alkylierenden Substanzen zu nennen, welche ursächlich für hämatologische Erkrankungen sein können. Das Vorliegen einer genetischen Prädisposition (z.B. Neurofibromatose, NF1) erhöht zudem das Risiko für eine Sekundärneoplasie als Folgeerkrankung im Langzeitverlauf (Abb. 2).
Abb. 2: Kumulative Inzidenz von Sekundärneoplasien (SN) 30 Jahre nach initialer Krebsdiagnose. (A) Alle SN und Meningeome. (B) Alle SN stratifiziert nach Radiotherapie (RT). (mod. nach Friedman et al. 2010)5
Zusammenfassung
Langzeitüberlebende nach Hirntumorerkrankungen entwickeln im Verlauf verschiedenste Folgeerkrankungen. Insbesondere das kindliche Gehirn und die sich entwickelnden Organe sind sehr vulnerabel und bedürfen eines besonderen Augenmerks im Langzeitverlauf. Aufgrund der derzeitigen Datenlage sind Follow-up-Untersuchungen konsequent durchzuführen, um Sekundärneoplasien zum frühestmöglichen Zeitpunkt zu detektieren. Alle hier dargestellten Folgeerkrankungen treten oft erst viele Jahre nach Therapie auf.
Literatur:
1 Alemany M et al.: Late effects on cancer treatment. Consequences for long-term cancer survivors. Neurooncol Pract 2020; 8(1): 18-30 2 Cayuela N et al.: Cognitive and brain structural changes in long-term oligodendroglial tumor survivors. Neuro Oncol 2019; 21(11): 1470-9 3 Douw L, et al.: Cognitive and radiological effects of radiotherapy in patients with low-grade glioma: long-term follow-up. Lancet Neurol 2009; 8(9): 810-8 4 Di Stefano AL et al.: Stroke-like events after brain radiotherapy: a large series with long-term follow-up. Eur J Neurol 2019; 26(4): 639-50 5 Friedman et al.: Subsequent neoplasms in 5-year survivors of childhood cancer: the Childhood Cancer Survivor Study. J Natl Cancer Inst 2010; 102(14): 1083-95
Weitere Literatur bei der Verfasserin
Das könnte Sie auch interessieren:
Asbestbedingtes Larynx- und Lungen-karzinom – Primär- oder Sekundärtumor?
Im Folgenden wird der Fall eines deutschen Facharbeiters vorgestellt, der während seiner Berufstätigkeit asbesthaltigen Stäuben ausgesetzt war und dadurch an einem Plattenepithelkarzinom ...
Die Pollensaison im Temperaturchaos
Die steigenden Temperaturen führen zu einem verfrühten Blühbeginn bei vielen Pflanzenarten und zu einer verlängerten und vermehrten Pollenbelastung für Allergiker:innen. Die ursächlichen ...
Alpha-1-Antitrypsin-Mangel: blinder Fleck auch in der Pneumologie?
Der Alpha-1-Antitrypsinmangel (AATM) gilt als seltene genetische Erkrankung und betrifft überwiegend die Lunge und die Leber,jedoch mithoher klinischer Variabilität. Doch AATM ist nicht ...