Therapie der PAH bei Komorbiditäten
Bericht:
Reno Barth
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In den aktuellen ESC-/ERS-Empfehlungen zum Management der pulmonalarteriellen Hypertonie (PAH) finden Komorbiditäten eine besondere Berücksichtigung im Therapiealgorithmus. Leider sind diese mit einem schlechteren Ansprechen auf die zugelassenen PAH-Medikamente assoziiert, die nur mit dem Therapieziel eines niedrigen Risikos eingesetzt werden sollen – das ist bei Weitem nicht in allen Fällen zu erreichen, weshalb zusätzliche wirksamere Therapien dringend benötigt werden.
Keypoints
-
Medikamentöse Monotherapie wird nur für Patienten mit relevanten Komorbiditäten empfohlen.
-
Patienten ohne Komorbiditäten haben ein besseres Ansprechen auf PAH-Therapien.
-
Die medikamentöse Behandlung soll auf Basis einer Risikoabschätzung erfolgen.
-
Es ist ein niedriges Mortalitätsrisiko von unter 5 Prozent innerhalb eines Jahres anzustreben.
-
Für alle Patienten, die nach 3 bis 4 Monaten nicht im Niedrigrisikobereich liegen, wird eine Therapieeskalation empfohlen.
-
Prostacycline sind in der medikamentösen Therapie der PAH die maximal wirksamste Option.
Im Rahmen der letztjährigen Kongresse der European Society of Cardiology (ESC) und der European Respiratory Society (ERS) wurde die aktualisierte Leitlinie der beiden Gesellschaften zu Diagnostik und Management bei Lungenhochdruck (Guidelines for the diagnosis and treatment of pulmonary hypertension) präsentiert.1 Nach wie vor gilt die lediglich in Details modifizierte Klassifikation der pulmonalen Hypertension (PH) in fünf Gruppen mit unterschiedlicher Genese:
-
Pulmonalarterielle Hypertonie
-
Lungenhochdruck assoziiert mit Erkrankungen des linken Herzens
-
Lungenhochdruck assoziiert mit chronischen Lungenerkrankungen
-
Pulmonale Hypertonie assoziiert mit Obstruktion der Lungenarterie (CTEPD/CTEPH)
-
Lungenhochdruck mit unbekanntem oder multifaktoriellem Hintergrund
Unter den zahlreichen Neuerungen in der aktualisierten Leitlinie findet sich auch ein neuer Therapiealgorithmus für die pulmonalarterielle Hypertonie (PAH), eine der beiden Formen des Lungenhochdrucks, für die spezifisch zugelassene Therapien verfügbar sind. Univ.-Prof. Dr. Gabor Kovacs, einer der Autoren der Leitlinie, unterstreicht, dass die Diagnose einer PAH sowie generell die Abklärung eines Lungenhochdrucks in einem spezialisierten Zentrum erfolgen muss, zumal die Diagnostik und die sich daraus ergebenden Konsequenzen komplex sind. Dies inkludiert einen im Katheterlabor durchzuführenden Test auf Vasoreaktivität, der bei allen PAH-Patienten mit Ausnahme von PAH im Zusammenhang mit Bindegewebserkrankungen indiziert ist. Spricht der Patient auf den Test an, ist er ein Kandidat für eine Therapie mit einem Kalziumkanal-Blocker, dessen Erfolg nach drei bis sechs Monaten evaluiert werden soll. Diese Patientengruppe zu identifizieren, sei insofern wichtig, so Kovacs, als sie bei adäquater Therapie eine sehr günstige Prognose aufweist. Leider sind jedoch rund 90% der PAH-Patienten nicht vasoreaktiv und benötigen eine Therapie mit verschiedenen PAH-Medikamenten. Ist der Test also negativ oder das Ansprechen auf die Therapie nicht zufriedenstellend, so sollen laut Leitlinie in einem nächsten Schritt kardiovaskuläre oder pulmonale Komorbiditäten diagnostiziert oder ausgeschlossen werden. Dieser Punkt steht allerdings aktuell in Diskussion, so Kovacs, da hier noch viele Fragen zu klären sind.
Monotherapie für Patienten mit Komorbiditäten
So sei beispielsweise eine arterielle Hypertonie als Komorbidität zu werten. Fraglich sei allerdings, ob das auch für eine gut eingestellte arterielle Hypertonie gilt. Diese Fragen sind von hoher Relevanz, da Komorbiditäten darüber entscheiden, auf welchem Pfad des Algorithmus die weitere Behandlung des Patienten erfolgt. Medikamentöse Monotherapien werden nämlich nur noch für Patienten mit relevanten Komorbiditäten empfohlen. In dieser Patientengruppe kann im weiteren Verlauf auf eine Kombinationstherapie umgestiegen werden. Hintergrund dieser Empfehlung ist eine Analyse des COMPERA(Comparative, Prospective Registry of Newly Initiated Therapies for Pulmonary Hypertension)-Registers mit 900 Patienten mit idiopathischer PAH, die innerhalb dieser Population drei Cluster identifizierte. Cluster 1 entspricht dabei der klassischen iPAH-Population mit vorwiegend jüngeren Frauen mit guter Lungenfunktion und keinen relevanten Komorbiditäten. Diese Patienten sprachen gut auf PAH-Therapien an und hatten die beste Prognose mit einem Fünfjahresüberleben von 86,6%. Die beiden anderen Cluster waren durch höheres Alter sowie kardiovaskuläre bzw. pulmonale Komorbiditäten charakterisiert (Linksherz- bzw. pulmonaler Phänotyp). In diesen Populationen war das Ansprechen auf PAH-Medikamente schlechter und die Prognose ungünstiger.2 Kovacs betont, dass es sich bei allen drei Clustern um Patienten mit PAH-Diagnose und nicht um Lungenhochdruck der Gruppe 2 und 3 (Lungenhochdruck assoziiert mit Erkrankungen des linken Herzens bzw. assoziiert mit chronischen Lungenerkrankungen) handelte unddass nur etwa 100 der insgesamt mehr als 800 Patienten in dieser Studie in Cluster 1 fielen. Für ein schlechteres Therapieansprechen der Patienten mit Komorbiditäten spricht auch eine Subgruppenanalyse der GRIPHON-Studie, die Selexipag, einen oralen selektiven Agonisten des Prostacyclinrezeptors, mit Placebo verglich.3 Allerdings zeigte diese Analyse auch, dass Patienten mit Komorbiditäten im Sinne einer Verlangsamung der Progression der PAH sehr wohl von der Therapie profitieren, wenngleich sie im Gegensatz zu den Patienten ohne Komorbiditäten keine Verbesserung mehr erreichen. Zu einem sehr ähnlichen Ergebnis kommt eine rezente Analyse von Patienten aus dem COMPERA-Register, die zeigt, dass Patienten ohne Komorbiditäten ein besseres Ansprechen auf PAH-Therapien haben, dass dies jedoch nur beim vollkommenen Fehlen von Komorbiditäten gilt, während sich Patienten mit ein, zwei, drei oder vier Komorbiditäten hinsichtlich der Chancen auf Ansprechen nicht signifikant unterscheiden. Die Studie zeigte auch, dass das in der PAH-Therapie empfohlene System der Risikostratifizierung auch bei Patienten mit Komorbiditäten valide bleibt.4
Therapieerfolg anhand des Risikostatus evaluieren
Aktuell sind für die Behandlung der PAH 14 Medikamente zugelassen, die jeweils in einen von drei für die PAH-Pathologie relevanten Pathways eingreifen: den Endothelin-Pathway, den Prostacyclin-Pathway und den NO-sGC-cGMP-Pathway. Die medikamentöse Behandlung soll auf Basis einer Risikoabschätzung erfolgen, wobei ein Mortalitätsrisiko über 20% innerhalb eines Jahres hohes Risiko bedeutet. Anzustreben ist hingegen niedriges Risiko, was einem Mortalitätsrisiko von weniger als 5% innerhalb eines Jahres entspricht. Bei PAH-Patienten ohne Komorbiditäten beginnt die medikamentöse Therapie in aller Regel bereits mit einer Kombination von zwei Substanzen aus unterschiedlichen Gruppen. Patienten mit niedrigem oder intermediärem Risiko steigen meist mit einer oralen Zweifachkombination aus einem PDE5-Inhibitor und einem Endothelin-Rezeptorantagonisten (ERA) in die Therapie ein.
Die Erfolge der initialen Therapie sollen anhand von drei Parametern, nämlich anhand der WHO-Funktionsklasse, des Sechs-Minuten-Gehtests sowie des BNP oder NT-proBNP, überwacht werden. Daraus ergeben sich vier Risikogruppen, nämlich niedrig, mittel-niedrig („intermediate-low“), mittel-hoch („intermediate-high“) und hoch. Das einzig akzeptable Ziel ist das Erreichen des Niedrigsrisikobereichs nach drei bis sechs Monaten Therapie. Für alle anderen Patienten wird eine Eskalation der Therapie empfohlen. Das bedeutet für Patienten aus dem Risikobereichmittel-niedrig, dass die duale Kombination von PDE5i/ERA entweder mit Selexipag zu einer oralen Dreifachkombination eskaliert werden kann oder der PDE5i durch Riociguat, einen Stimulator der löslichen Guanylatcyclase, ersetzt wird. Beide Empfehlungen beruhen auf klinischen Studien, wie Kovacs ausführt. Für Selexipag konnte in der GRIPHON-Studie gezeigt werden, dass es auch vor dem Hintergrund einer optimierten Zweifachkombinationstherapie den Patienten noch einen Vorteil brachte.5 Die Evidenz für den Ersatz des PDE5-Inhibitors durch Riociguat stammt aus der Studie REPLACE, in der Riociguat die Chancen auf klinische Verbesserung im Vergleich zu einem PDE5-Inhibitor hatte.6
Zufriedenstellende Ergebnisse in High-Risk-Population nur selten erreicht
In den Risikobereichen mittel-hoch und hoch werden die zusätzliche Gabe eines parenteralen Prostacyclins und die Vorstellung an einem Transplantationszentrum empfohlen. Bei hohem Risiko kann auch initial bereits mit einer Dreifachkombination inklusive eines parenteralen Prostacyclinanalogons begonnen werden. Dass Prostacycline die maximal wirksame Option in der medikamentösen Therapie der PAH sind, wurde erst kürzlich wieder in einer Studie aus Deutschland demonstriert.7 Allerdings betont Kovacs, dass auch in dieser Studie nur rund ein Fünftel der Population ein exzellentes Ansprechen hatte, wobei vor allem das jüngere Alter ein guter Prädiktor war. Daher werden dringend neue Therapien benötigt.
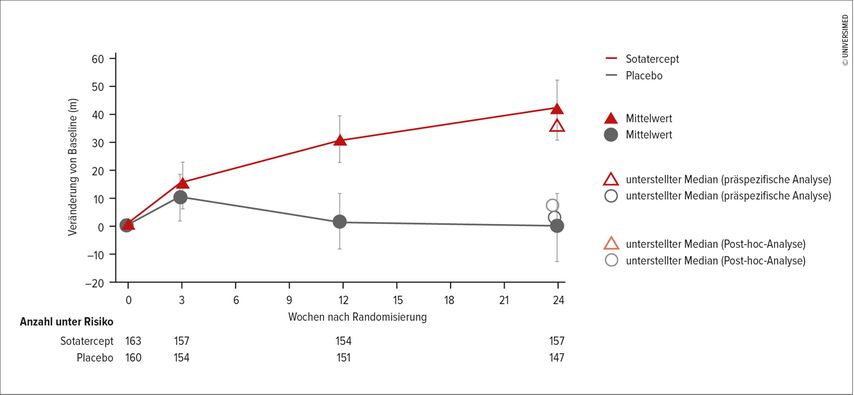
Zwei Substanzen könnten schon in naher Zukunft zur Verfügung stehen. Sotatercept soll durch Inhibition von Activin in das für die PAH typische Remodelling in den Lungengefäßen eingreifen und die Balance zwischen proliferativen und antiproliferativen Pathways wiederherstellen. Sotatercept wurde in der Phase-III-Studie STELLAR in einer Population von 323 Patienten und Patientinnen mit idiopathischer, hereditärer oder mit einer Bindegewebserkrankung assoziierter PAH untersucht. Bei Einschluss in die Studie waren 60% der Population unter maximaler Therapie mit drei Medikamenten schwer symptomatisch. Dabei erwies sich Sotatercept im primären Endpunkt in Veränderungen im Sechs-Minuten-Gehtest sowie in diversen sekundären Endpunkten als überlegen (Abb. 1).8 Ein weiterer Kandidat für einen klinischen Einsatz in der Zukunft ist der inhalative Tyrosinkinaseinhibitor Seralutinib, für den in einer Phase-II-Studie günstige Wirkungen auf den pulmonalen Gefäßwiderstand und das NT-proBNP demonstriert werden konnten.9
Quelle:
Der neue Therapiealgorithmus – hart genug?; Vortrag von Ass.-Prof. Priv.-Doz. Dr. Gabor Kovacs im Rahmen der Jahrestagung der Österreichischen Kardiologischen Gesellschaft am 3.Juni 2023 in Salzburg
Literatur:
1 Humbert M et al.: 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Heart J 2022; 43(38): 3618-731 2 Hoeper MM et al.: Idiopathic pulmonary arterial hypertension phenotypes determined by cluster analysis from the COMPERA registry. J Heart Lung Transplant 2020; 39(12): 1435-44 3 Rosenkranz S et al.: The impact of comorbidities on selexipag treatment effect in patients with pulmonary arterial hypertension: insights from the GRIPHON study. Eur J Heart Fail 2022; 24(1): 205-14 4 Rosenkranz S et al.: The impact of comorbidities on Selexipag treatment effect in patients with pulmonary arterial hypertension: Insights from the GRIPHON study. J Heart Lung Transplant 2023; 42(1): 102-14 5 Sitbon S et al.: Selexipag for the treatment of pulmonary arterial hypertension. N Engl J Med 2015; 373(26): 2522-33 6 Hoeper MM et al.: Selexipag for the treatment of pulmonary arterial hypertension. Lancet Respir Med 2021; 9(6): 573-84 7 Olsson KM et al.: Intravenous treprostinil as an add-on therapy in patients with pulmonary arterial hypertension. J Heart Lung Transplant 2019; 38(7): 748-56 8 Hoeper MM et al.: Phase 3 trial of Sotatercept for treatment of pulmonary arterial hypertension. N Engl J Med 2023; 388(16): 1478-90 9 Frantz RP et al.: Seralutinib treatment in adult subjects with pulmonary arterial hypertension: Results from the TORREY study. präsentiert am ATS 2023
Das könnte Sie auch interessieren:
Genderunterschiede in kardiopsycho-somatischer Rehabilitation
Herz-Kreislauf-Erkrankungen sind lt. dem österreichischen Frauengesundheitsbericht 2022 die häufigste Todesursache bei Frauen. Zudem berichtet das weibliche Geschlecht häufiger über ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...