Tafamidis zur Behandlung der Transthyretin-Amyloid-Kardiomyopathie
Autoren:
Dr. René Rettl
Klinische Abteilung für Kardiologie
Universitätsklinik für Innere Medizin II
Medizinische Universität Wien
E-Mail: rene.rettl@meduniwien.ac.at
Prim. Assoc. Prof. Priv.-Doz. Dr. Diana Bonderman
5. Medizinische Abteilung mit Kardiologie und internistische Aufnahmestation
Klinik Favoriten, Wiener Gesundheitsverbund
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei der kardialen Transthyretin-Amyloidose handelt es sich um eine seltene infiltrative Kardiomyopathie, welche in den letzten Jahren zunehmend in den diagnostischen Fokus getreten ist und den betreuenden Arzt aus therapeutischer Sicht vor große Herausforderungen stellt. Der folgende Artikel soll neue Erkenntnisse über den Einfluss krankheitsspezifischer Therapieoptionen auf die strukturelle und funktionelle Entwicklung des Herzmuskels von betroffenen Patienten vermitteln.
Keypoints
-
In der Zulassungsstudie von Tafamidis konnten signifikante Vorteile hinsichtlich dekompensationsbedingter Hospitalisierungen und der Gesamtmortalität im Vergleich zur Placebogruppe aufgezeigt werden.
-
Neben den klinischen Verbesserungen konnten im Rahmen einer Studie der Medizinischen Universität Wien auch signifikante Vorteile in Bezug auf die kardiale Struktur und Funktion bei ATTR-CM-Patienten beobachtet werden.
-
Die serielle Bildgebung mittels CMR und der Bestimmung des ECV stellt ein geeignetes Tool für die krankheitsspezifische Therapieüberwachung dar.
Pathophysiologie und klinisches Erscheinungsbild
Die Transthyretin-Amyloid-Kardiomyopathie (ATTR-CM) zählt zu den infiltrativen Kardiomyopathien, deren Pathogenese von Transthyretin (TTR), einem hepatisch synthetisierten Transportprotein für Vitamin A und Schilddrüsenhormone, dominiert wird.1 Eine pathophysiologische Schlüsselrolle nimmt dabei die Destabilisierung des TTR-Tetramers und Dissoziation in seine Monomere ein, welche in das umliegende Gewebe diffundieren und durch enzymatische Umwandlungsvorgänge unlösliche Komplexe in Form von Amyloidfibrillen bilden.2 Die Ablagerung von Amyloidfibrillen im Herzmuskel führt zu einer Verdickung des Myokards, welche mit einer erhöhten Steifigkeit mit begleitender diastolischer und systolischer Funktionseinschränkung einhergeht.3
Betroffene Patienten präsentieren sich klinisch oft mit Symptomen der globalen Herzinsuffizienz und nicht selten kommt es zu schleichenden oder akuten kardialen Dekompensationen, die oftmals rezidivierende Hospitalisationen bedürfen. Des Weiteren geht die ATTR-CM im fortgeschrittenen Krankheitsverlauf mit einer schlechten Prognose einher, insbesondere wenn diese unbehandelt bleibt.4 Doch reges Forschungsinteresse führte in den letzten Jahren zu weitreichenden Entwicklungen hinsichtlich therapeutischer Optionen, sodass sich die ATTR-CM von einer unheilbaren zu einer behandelbaren Erkrankung wandelte.
Therapeutische Hoffnung
Da die Dissoziation des TTR-Tetramers in seine Monomere einer der wichtigsten pathophysiologischen Schritte der ATTR-CM darstellt, kann die Stabilisierung des Tetramers als valider therapeutischer Ansatz betrachtet werden. Tafamidis fungiert mittels kleiner Moleküle als kinetischer Stabilisator und wirkt somit der Bildung von Amyloidfibrillen und deren Ablagerungen im Herzmuskel entgegen.5 Dies wiederum trägt womöglich zu einer Verlangsamung der Progression der Erkrankung bei.6 Im Rahmen einer internationalen placebokontrollierten, multizentrischen Phase-III-Studie (ATTR-ACT) mit 441 ATTR-CM-Patienten konnten nicht nur signifikante Vorteile hinsichtlich dekompensationsbedingter Hospitalisierungen (52,3% vs. 60,5%) und der Gesamtmortalität (29,5% vs. 42,9%) im Vergleich zur Placebogruppe aufgezeigt werden, sondern auch klinische Vorteile in Bezug auf die Leistungsfähigkeit und Lebensqualität in der Behandlungsgruppe erfasst werden.7 Ob die positiven Effekte von Tafamidis im Vergleich zur Placebokohorte auf Unterschiede im kardialen Remodeling zurückzuführen sind, ist derzeit jedoch noch unklar.
Kardiale Bildgebung im Kontext einer klinisch-therapeutischen Studie
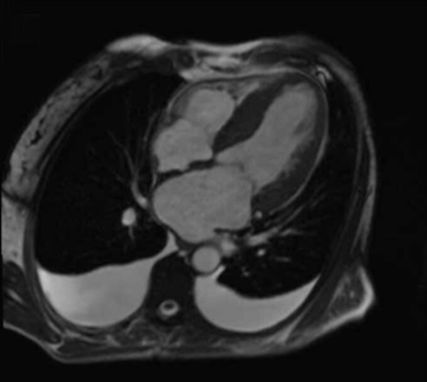
Abb. 1: In der kardialen Magnetresonanztomografie (CMR) zeigt sich im 4-Kammer-Blick eine ausgeprägte linksventrikuläre Hypertrophie mit dem Vollbild einer Transthyretin-Amyloid-Kardiomyopathie (ATTR-CM)
Die Diagnosestellung einer ATTR-CM stellt eine große Herausforderung dar und wird primär von bildgebenden Untersuchungsmethoden dominiert.8 Im Hinblick darauf bieten bildgebende Verfahren wie die kardiale Magnetresonanztomografie (CMR, Abb. 1) unter Verwendung von T1-Mapping-Sequenzen die Möglichkeit zur quantitativen Erfassung der diffusen extrazellulären Ausdehnung, welche zur Beurteilung des extrazellulären Volumens (ECV) bei der ATTR-CM bereits breite Anwendung findet.9,10 Eine Studie der klinischen Abteilung für Kardiologie an der Medizinischen Universität Wien, welche für den Young Investigator Award am Heart Failure Congress 2021 nominiert wurde, setzte sich zum Ziel, mögliche krankheitsmodifizierende Effekte von Tafamidis auf das Fortschreiten der myokardialen Amyloidablagerung bei ATTR-CM-Patienten zu beleuchten und zusätzlich bildgebende Parameter zu identifizieren, die für eine spezifische Therapieüberwachung eingesetzt werden könnten. Im Rahmen der klinischen Studie unterzog sich eine Reihe von ATTR-CM-Patienten bildgebenden Baseline- und Follow-up-Untersuchungen mittels CMR (Abb. 2). In weiterer Folge wurden Patienten, die mit Tafamidis 61mg behandelt wurden, mit einer historischen Kontrollkohorte, welche Tafamidis 20mg erhielt, sowie mit einer historischen, therapienaiven Kontrollkohorte, die den natürlichen Verlauf der Krankheit widerspiegelt, verglichen.
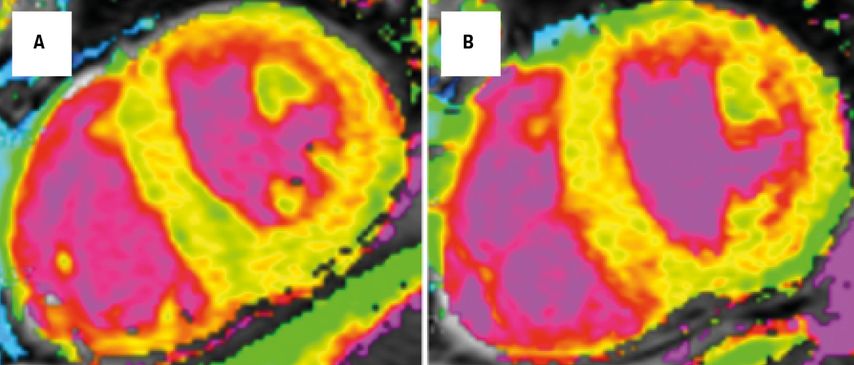
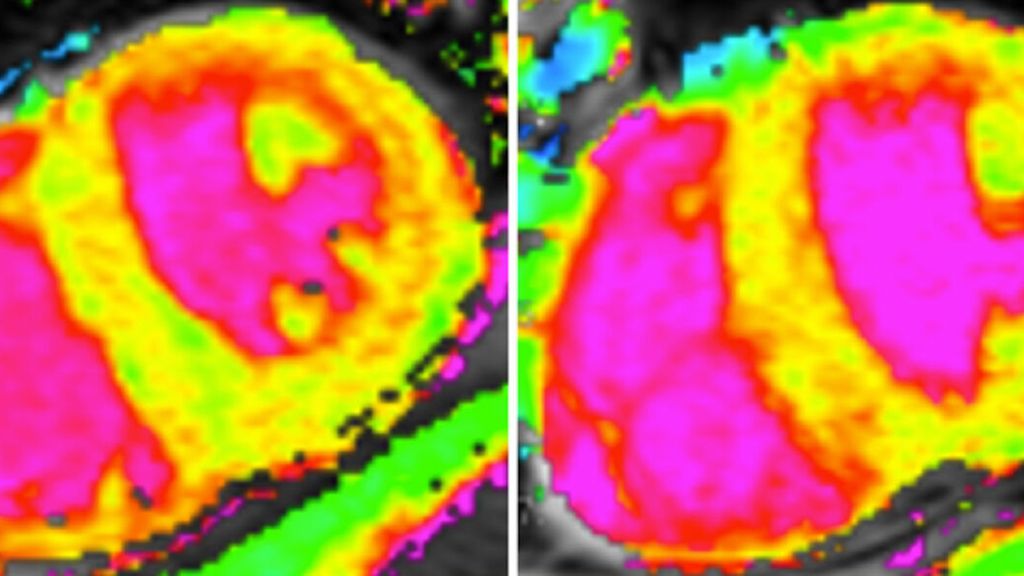
Abb. 2: In der CMR-T1-Mapping-Sequenz finden sich in der kurzen Achse stark erhöhte myokardiale T1-Zeiten, welche auf eine hohe Amyloidlast hinweisen. (A) Baseline-CMR. (B) Follow-up-CMR nach 9-monatiger Behandlung mit Tafamidis
Kardiostrukturelle und -funktionelle Veränderungen
Im Rahmen der Follow-up-Untersuchungen fanden sich bei ATTR-CM-Patienten, die mit Tafamidis 61mg behandelt wurden, signifikant positive Effekte in Bezug auf den linksventrikulären (LV) Masseindex (p=0,036), das ECV (p=0,030) sowie die linksventrikuläre Ejektionsfraktion (LVEF, p=0,035) im Vergleich zu therapienaiven Patienten, die einen Anstieg der LV-Masse und des ECV zu verzeichnen hatten. Im Einklang damit zeigten sich in der mit Tafamidis 61mg behandelten Kohortebeim Vergleich mit der therapienaiven Kohorte positive klinische Effekte hinsichtlich der NYHA-Klassifikation (p=0,004), der 6-Minuten-Gehstrecke (6-MWD: p=0,005) sowie der NT-proBNP-Konzentration im Serum (p=0,002).
Im Gegensatz dazu unterschieden sich die bildgebenden Befunde der ATTR-CM-Patienten, die mit Tafamidis 20mg behandelt wurden, nicht signifikant von denen der therapienaiven Patienten (longitudinale Veränderungen des LV-Masseindex: p=0,287; ECV: p=0,158; LVEF: p=0,120). Beim Vergleich der beiden Kohorten auf klinischer Ebene konnten jedoch ebenfalls Hinweise auf positive Behandlungseffekte zugunsten von Tafamidis 20mg beobachtet werden. Diese spiegelten sich anhand einer Verbesserung der Leistungsfähigkeit (6-MWD: p=0,023) und der kardialen Biomarker (NT-proBNP: p=0,003) wider.
Bei Betrachtung der gesamten Studienpopulation zeigte die Gegenüberstellung der CMR-Parameter und der kardialen Biomarker eine positive Korrelation (Pearson: 0,264; p=0,034) zwischen den longitudinalen Veränderungen des ECV und den longitudinalen Veränderungen der NT-proBNP-Konzentration im Serum. Diesbezüglich deuten die Daten auf eine Stabilisierung des ECV und der kardialen Biomarker bei Patienten, die mit Tafamidis 61mg oder 20mg behandelt wurden hin, während ein Anstieg des ECV und der Biomarker bei therapienaiven Patienten beobachtet wurde.
Resümee
Die Ergebnisse der klinischen Studiezeigten, dass eine Behandlung mit Tafamidis das Fortschreiten der interstitiellen Myokardausdehnung, gemessen anhand des ECV, verzögerte und zu signifikanten Vorteilen in Bezug auf die Herzstruktur und -funktion sowie den klinischen Status im Vergleich zu unbehandelten ATTR-CM-Patienten führte. Ob die Unterschiede in der kardiostrukturellen Entwicklung ursächlich für das bessere kardiovaskuläre Outcome behandelter Patienten sind, gilt es in weiteren Langzeitstudien zu bewerten. Zusätzlich legten die Resultate nahe, dass die serielle Bildgebung mittels CMR und der Bestimmung des ECV ein geeignetes Tool für die krankheitsspezifische Therapieüberwachung bei betroffenen Patienten darstellen könnte.
Literatur:
1 Ruberg F et al.: Circulation2012; 126(10): 1286-1300 2 González-López E et al.: Eur Heart J 2015; 36(38): 2585-94 3 Damy T et al.: Eur Heart J 2016; 37(23): 1826-34 4 Gertz MA et al.: Nat Rev Cardiol 2015; 12(2): 91-102 5 Said G et al.: Nat Rev Drug Discov 2012; 11(3): 185-6 6 Sultan MB et al.: Clin Med Insights Cardiol 2017; 11 7 Maurer MS et al.: N Engl J Med 2018; 379(11): 1007-16 8 Bonderman D et al: Wien Klin Wochenschr 2020; 132(23-24): 742-61 9 Kammerlander AA et al.: JACC Cardiovasc Imaging 2016; 9(1): 14-23 10 Duca F et al.: JACC Cardiovasc Imaging 2018; 11(12): 1924-6
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
Labormedizinische Fallstricke bei kardialen Markern
Bei Schädigung oder Stress des Herzmuskels werden kardiale Marker in den Blutkreislauf freigesetzt. Ihre labormedizinische Bestimmung spielt eine Schlüsselrolle in der Diagnostik, ...