Ergometrie 2022 – Stellenwert in der kardiovaskulären Medizin aktueller denn je
Autoren:
Prim. Priv.-Doz. Dr. Robert Berent1
Prim. Univ.-Prof. Dr. Johann Auer2
Ass. Dr. Theresa Berent3
OA Dr. David Niederseer4
1 HerzReha Bad Ischl, Zentrum für kardiovaskuläre Rehabilitation und Fettstoffwechselstörungen
2 Abteilung für Innere Medizin I mit Kardiologie und Intensivmedizin
A.ö. KH St. Josef Braunau
3 Salzkammergut Klinikum Vöcklabruck
Innere Medizin 3, Kardiologie, Intensivmedizin und Nephrologie
4 Universitätsspital Zürich,Universitäres Herzzentrum, Klinik für Kardiologie
E-Mail: robert.berent@herzreha.at
Die Ergometrie stellt trotz der Verfügbarkeit alternativer Belastungsuntersuchungen mit bildgebenden Verfahren ein weiterhin wichtiges nicht invasives diagnostisches Standardverfahren in der Kardiologie dar. Wir zeigen, was geht, was nicht geht und worauf Sie beim Einsatz achten müssen, um beste Resultate zu erreichen.
Keypoints
-
Auch in der modernen Kardiologie ist die Ergometrie eine sinnvolle und wichtige Untersuchung, wenngleich sie nicht mehr als primäre Diagnostik bei koronarer Herzkrankheit empfohlen wird.
-
Bei der Durchführung der Ergometrie sind Berücksichtigung und Kenntnis von Indikation, Kontraindikation, Einflussfaktoren, Abbruchkriterien und Interpretation wichtig.
-
Die objektive Bestimmung der Leistungsfähigkeit sowie die Erhebung von Daten für die Trainingssteuerung z.B. in der Rehabilitation und Trainingstherapie sind Alleinstellungsmerkmale der Ergometrie.
-
Die Wahl des richtigen Belastungsprotokolls (Stufen vs. Rampenprotokoll) sowie die Belastungsmodalität (Fahrrad vs. Laufband) zum Erreichen einer Belastungsdauer von 8–12 Minuten ist für die Interpretation der Ergometrie von zentraler Bedeutung.
Die ergometrische Belastungsuntersuchung gehört als nicht invasive Untersuchungsmethode zu den häufigen und bewährten Verfahren für Diagnostik, Therapiekontrolle, Prognose und Beurteilung von Leistungsfähigkeit, Belastbarkeit und Beanspruchung in Arbeits- und Sportmedizin, Pneumologie und Kardiologie. Sie gibt Grundlagen zur Trainingsberatung für Gesunde, Sportler und Patienten.
Die Bestimmung der maximalen Belastbarkeit ist für Gesunde und Patienten wichtig zur Prognoseabschätzung von Morbidität und Mortalität. Die Ergometrie ist dosierbar, reproduzierbar und ermöglicht zusätzliche Messungen wie Elektrokardiogramm (EKG), Blutdruck (RR) und Atemgasaustausch. Vor der körperlichen Belastung ist immer eine Voruntersuchung mit Anamnese, klinischem Befund, medikamentöser Therapie und Ruhe-EKG erforderlich, um mögliche Risiken durch latente oder manifeste Erkrankungen zu erkennen. Eine transthorakale Echokardiografie wäre wünschenswert.
Standardisierte Bedingungen im Untersuchungsraum sind nach Möglichkeit anzustreben (Raumtemperatur, Luftfeuchtigkeit). Während der Belastung sind die fortlaufende EKG-Anzeige, Beobachtung des Probanden sowie Herzfrequenz- und Blutdrucküberwachung notwendig, um bei Komplikationen die Ergometrie frühzeitig abzubrechen.
Indikationen und Kontraindikationen
Die Ergometrie ist indiziert oder liefert aussagekräftige Ergebnisse bei1–5
-
Diagnostik: koronare Herzerkrankung (KHK), Arrhythmien, Wirksamkeit von Vitien
-
Prognose: nach Myokardinfarkt (MI), Kardiomyopathie, nach Revaskularisation, antiarrhythmische Therapie
-
Leistung: kardiopulmonal, Schrittmacherfunktion (chronotrope Funktion), implantierbarer Cardioverter - Defibrillator (ICD) -Programmierung, respiratorischer Gasaustausch
-
Therapie: antianginöse Therapie, antihypertensive Therapie, antiarrhythmische Therapie (Frequenzregulation), antiobstruktive Therapie, Therapie bei Herzinsuffizienz (HI), ICD-Programmierung, Resynchronisationstherapie, Trainingssteuerung, Verlaufskontrolle nach aortokoronarer Bypassoperation, perkutaner koronarer Intervention, Vitien, Herztransplantation, Training
Ergometrie-Kontraindikationen1,6,7
-
Absolute: akutes Koronarsyndrom, symptomatische Herzrhythmusstörung mit/ohne eingeschränkte Hämodynamik, symptomatische hochgradige Herzklappenerkrankungen, dekompensierte HI, akute Lungenembolie, akute Phlebothrombose der unteren Extremität, akute Endo-, Myo-, Perikarditis, akute Aortendissektion, akute Extremitätenischämie, akute Infekte mit/ohne Fieber
-
Relative: hämodynamisch wirksame Hauptstammstenose, schlecht frequenzkontrollierte Tachyarrhythmie (Ruheherzfrequenz >110/min), mittel-/hochgradig wirksame Herzklappenerkrankungen mit unklaren Symptomen, Ruheblutdruck >180/100mmHg, hypertrophe obstruktive Kardiomyopathie, höhergradige AV-Blockierungen, Elektrolytstörungen, symptomatische Anämie, manifeste Hyperthyreose, physische und/oder psychische Beeinträchtigungen (wie z.B. fortgeschrittene System- oder Demenzerkrankung)
Die Belastungsuntersuchung ist gerade zur Beurteilung der klinischen Symptomatik, der Hämodynamik und der Einschätzung des Ausmaßes einer mittel-/hochgradig wirksamen Herzklappenerkrankung mit unklaren Symptomen eine viel zu selten angewandte Untersuchungsmethode.6 Eine Echokardiografie unter Belastung kann zusätzliche Informationen für die weitere Therapie liefern.
Fahrradergometrie, Laufband
Belastungsuntersuchungen werden am häufigsten mittels Fahrradergometrie in sitzender oder (halb) liegender Position durchgeführt. Alternativ zum Fahrradergometer wird das Laufbandergometer eingesetzt. Bei Letzterem ist die Sauerstoffaufnahme um 10–15% höher als bei der Fahrradergometrie. Unabhängig von der Methode sollte eine Ausbelastung in 8–12 Minuten erreicht werden. Das Erzielen einer angestrebten Herzfrequenz (HF) oder Wattzahl ist kein Kriterium für einen vorzeitigen Abbruch, sofern keine objektiven Kriterien den vorzeitigen Abbruch der Untersuchung erzwingen.
Ischämiediagnostik
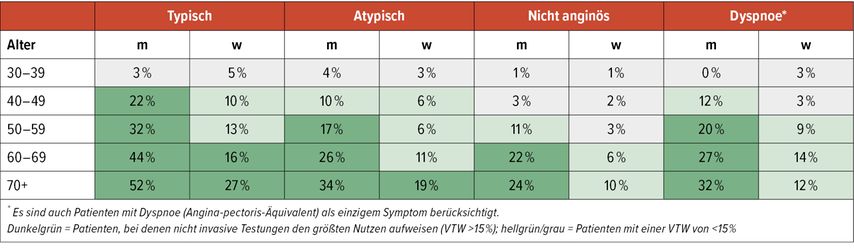
Haupteinsatzgebiet der Ergometrie ist die Ischämiediagnostik, wobei dabei die Sensitivität bei nur 58% und die Spezifität bei nur 62% liegt.8–10 Daher ist die Ergometrie erst ab einer Vortestwahrscheinlichkeit (VTW) von zumindest 15% anzuwenden (Tab. 1).11
Tab. 1: Vortestwahrscheinlichkeit einer koronaren Herzkrankheit (modifiziert nach Knuuti J et al.)11
Weitere diagnostische Testverfahren werden nach Beurteilung der allgemeinen klinischen Wahrscheinlichkeit bei einer VTW von <15% empfohlen.
Keine weitere Diagnostik ist empfohlen
-
bei unauffälligem Belastungs-EKG, wenn kein Koronarkalk im CT (Agatston-Score = 0) vorhanden ist, da dies die Wahrscheinlichkeit für das Vorliegen einer koronaren Herzerkrankung verringert.
Empfohlen ist sie
-
bei Risikofaktoren für eine KHK (Dyslipidämie, Diabetes, Hypertonie, Rauchen, KHK-pos. Familienanamnese), Ruhe-EKG mit neuer Q-Zacke oder ST-Strecken-, T-Wellenveränderungen, linksventrikulärer Dysfunktion, auffälligem Belastungs-EKG, Koronarkalk im CT sowie peripherer arterieller Verschlusskrankheit, da dies die Wahrscheinlichkeit, dass eine KHK vorliegt, erhöht.
Ischämiekaskade
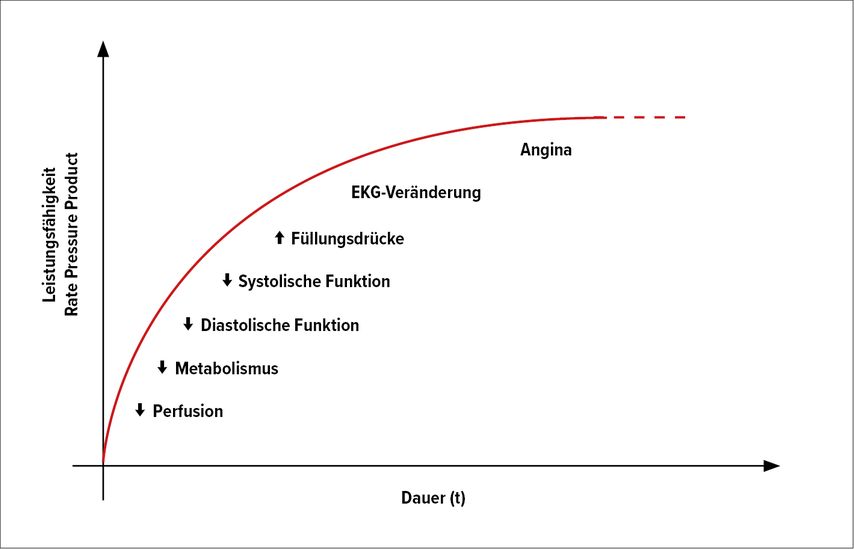
Unter ischämischen Bedingungen manifestieren sich Veränderungen im Myokard zuerst durch Stoffwechselveränderungen, dann durch Änderungen der myokardialen Funktion gefolgt von EKG-Veränderungen und zuletzt durch klinische Beschwerden (Abb. 1).
Ischämie- und ST-Streckenveränderungen12,13
Sensitivität und Spezifität der Ergometrie in der Ischämiediagnostik sind vom Grad der Ausbelastung und der Belastungsdauer abhängig. Es sollte zumindest eine Leistungsfähigkeit von 75% des Sollwertes (oder Anstrengungsempfinden von >17 in der Borg-Skala) erzielt werden, um eine relevante Aussage machen zu können.
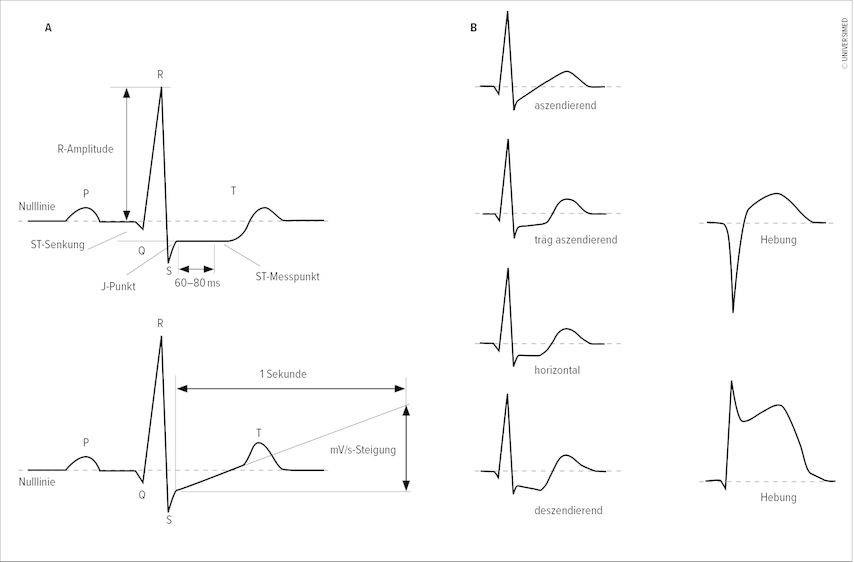
Der Analyse der ST-Strecke im EKG kommt eine besondere Bedeutung in der Ischämiediagnostik unter Belastung zu (Abb. 2A). Je ausgeprägter ST-Streckensenkungen unter Belastung sind und je mehr Ableitungen davon betroffen sind, desto höher ist die Wahrscheinlichkeit einer wirksamen KHK und umso ausgeprägter sind die Koronarveränderungen (Abb. 2B). Die ST-Streckensenkung erlaubt keine sichere Lokalisation des Ortes der Ischämie. Somit ist eine anatomische Zuordnung zur Koronarmorphologie nur eingeschränkt möglich. Bei einer ST-Hebung hingegen kann die transmurale Ischämie je nach Ableitung lokalisiert werden. Bei Patienten unter Digitalistherapie, mit komplettem Linksschenkelblock oder bei ventrikulärem Pacing ist die Veränderung der ST-Strecke unter Belastung nicht als Ischämiehinweis zu werten.
Abb. 2: A) Analyse der ST-Strecke im EKG unter Belastung. Als Bezugspunkt wird der J-Punkt genommen. B) Je ausgeprägter ST-Streckensenkungen unter Belastung sind und je mehr Ableitungen davon betroffen sind, desto höher ist die Wahrscheinlichkeit einer wirksamen koronaren Herzerkrankung und umso ausgeprägter sind die Koronarveränderungen. Bei einer ST-Hebung kann die transmurale Ischämie je nach Ableitung auch lokalisiert werden (modifiziert nach Wonisch M et al.12)
Protokolle
Die zu erzielende maximale Belastung, die innerhalb von 8–12min erreicht werden soll, muss an die individuelle Leistungsfähigkeit des Patienten angepasst werden. Belastungen von kürzerer Dauer führen zu keiner vollen kardiorespiratorischen Ausbelastung. Belastungen über 12 min bringen keinen Informationsgewinn, sondern führen durch muskuläre Erschöpfung zu einem vorzeitigen Belastungsabbruch ohne kardiorespiratorische oder symptomlimitierte Ausbelastung.
Faustformel zur Berechnung der zu erwartenden Sollleistung
Männer: 3 W/kg Körpergewicht (KG)
Frauen: 2,5 W/kg KG
(–1% pro Jahr >30. Lebensjahr)
Individuelles Protokoll
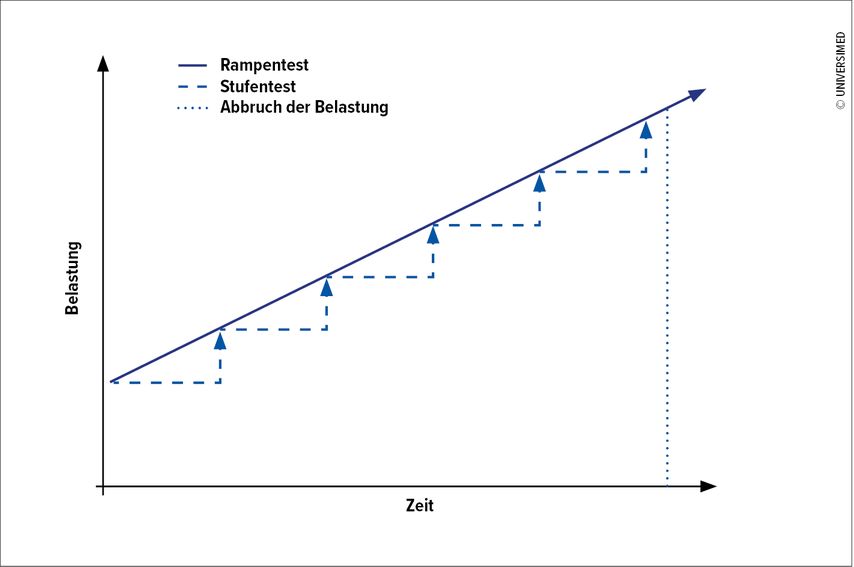
Bei der Fahrradergometrie wird entweder ein individueller Stufentest mit Anstieg in Watt jede Minute oder alle 2 Minuten oder ein individueller Rampentest durchgeführt (Tab. 2). Bei diesem gibt es keine klar definierten Stufen mehr, sondern die Belastung wird kontinuierlich z.B. alle 10 Sekunden um 1–2 Watt bis zum Abbruch erhöht (Abb. 3). Damit eine Belastungsdauer von 8–12min mittels Rampensteigerung erreicht werden kann, muss die erwartete Maximalleistung des Patienten im Voraus abgeschätzt werden. Die Steigerung erfolgt computergesteuert. Der Nachteil ist die unzureichende Vergleichbarkeit auf den einzelnen Belastungsstufen. Rampenbelastungen können aber über Messgrößen des Gasaustausches verglichen werden, speziell über die O2-Aufnahme. Somit wird diese Belastungsform häufig als schneller Rampenanstieg zur Bestimmung der maximalen Sauerstoffaufnahme verwendet.14,15
Bei der Laufbandergometrie werden individuell abgestimmte Protokolle empfohlen. Dabei bieten sich Steigerungen in 1-minütigem Abstand an:
-
Entweder Geschwindigkeit: z.B. 5km/h + 0,3–0,5km/h/min, Steigung 2% konstant oder
-
Steigung: z.B. 5% + 2%/min, 4km/h konstant
-
Alternativ werden standardisierte Protokolle wie das Bruce- oder das modifizierte Bruce-Protokoll verwendet.
Ergometrie zum Ischämienachweis in „Konkurrenz“ zu anderen nicht invasiven Testverfahren11
Die KHK ist eine chronische Erkrankung mit instabilen Phasen (akutes Koronarsyndrom; ACS) und stabilen Phasen (chronisches Koronarsyndrom; CCS). Dazu zählen:
-
Patienten mit Verdacht auf KHK und Angina pectoris und/oder Luftnot,
-
Patienten mit neu aufgetretener HI oder linksventrikulärer Dysfunktion und vermuteter KHK,x
-
asymptomatische und symptomatische Patienten >1 Jahr nach initialer Diagnose,
-
asymptomatische und symptomatische Patienten >1 Jahr nach initialer Diagnose,
-
Patienten mit Angina pectoris und vermuteten epikardialen Koronarspasmen oder mikrovaskulärer Erkrankung,
-
asymptomatische Patienten, bei denen eine KHK im Rahmen einer Screeninguntersuchung entdeckt wurde.
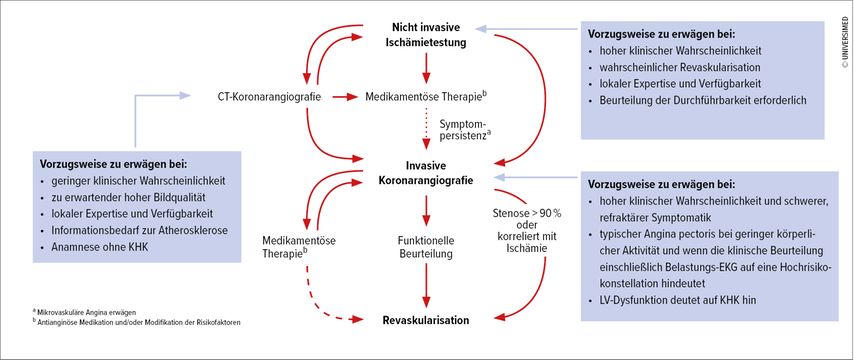
Bei der Auswahl diagnostischer Tests hat das Belastungs-EKG in den neuen Guidelines des CCS eine deutliche Abwertung erfahren. Den Diagnosealgorithmus bei Patienten mit Verdacht auf eine wirksame KHK zeigt Abbildung 4.16
Abb. 4: Diagnosealgorithmus bei Patienten mit Verdacht auf eine wirksame koronare Herzkrankheit (modifiziert nach Leitlinien der DGK)16
Kann anhand der klinischen Untersuchung eine stenosierende KHK nicht ausgeschlossen werden, wird bei symptomatischen Patienten als Primärdiagnostik bei Verdacht auf eine KHK die nicht invasive Ischämietestung durch eine funktionelle Bildgebung (Kardio-MRT unter Belastung, Myokardszintigrafie, Positronen-Emissionstomografie) und/oder ein Koronar-CT empfohlen (Empfehlungsgrad I, Evidenzgrad B).
Bei Patienten mit Verdacht auf eine KHK wird ein Belastungs-EKG zur Beurteilung von Belastungstoleranz, Symptomen, Arrhythmien, Blutdruckverhalten und Risikoabschätzung empfohlen, wenn diese Informationen eine Auswirkung auf das diagnostische Vorgehen oder die Behandlung haben (I C).
Steht keine nicht invasive Bildgebung zur Verfügung, kann ein Belastungs-EKG als alternative Untersuchung angedacht werden, um die Diagnose einer KHK zu stellen oder auszuschließen (IIb B).
Unter einer antianginösen Behandlung kann ein Belastungs-EKG angedacht werden, um die Verbesserung der Klinik bzw. der Ischämie zu beurteilen (IIb C).
Ein Belastungs-EKG für diagnostische Zwecke hat keine Aussagekraft bei Patientenmit ≥0,1mV ST-Streckensenkung im Ruhe-EKG oder bei Patienten, die Digitalis einnehmen (III C). Des Weiteren trifft dies auch bei komplettem Linksschenkelblock, bei ventrikulärer Stimulierung oder bei einem WPW-Syndrom im EKG zu.
Eine Beurteilung bezüglich des Risikos für Koronarereignisse wird empfohlen, um Patienten mit Hochrisikokonstellation bezüglich Mortalität zu identifizieren. Dabei handelt es sich um Patienten, bei denen eine Revaskularisation über eine Symptomverbesserung hinaus zusätzlichen Nutzen bringen könnte: z.B. Patienten mit ST-Senkungen bereits bei niedriger Belastungsstufe in Verbindung mit Symptomen (Angina pectoris, Dyspnoe), schlechter Leistungsfähigkeit, ventrikulärer Extrasystolie oder Tachyarrhythmie unter Belastung oder in der Erholungsphase, überschießender Blutdruckregulation, typischer Angina und einer segmentalen systolischen linksventrikulären Dysfunktion.
Bei Patienten mit vermuteter oder neu diagnostizierter KHK wird eine Risikostratifizierung auf der Grundlage von Belastungsuntersuchungen mit Bildgebung oder eines Koronar-CT empfohlen, falls die Expertise vor Ort und die Verfügbarkeit dies gestatten. Alternativ dazu ein Belastungs-EKG, wenn eine ausreichende Belastung möglich ist und anhand des EKG ischämische Veränderungen erkannt werden können (I B).
Blutdruck und körperliche Belastung
Es besteht kein Konsens über ein normales Blutdruckverhalten unter Belastung.17 Der Anstieg des RRsyst unter Belastung hängt ab vom Ausgangswert, vom Alter (verstärkt mit höherem Alter), von der Gefäßsteifigkeit, der abdominellen Adipositas, dem Geschlecht (Frauen haben einen stärkeren Anstieg) und der Fitness. Unter physiologischen Bedingungen steigt der RRsyst um ca. 10mmHg pro MET (ca. 20W) an.18
Der pathologische Belastungsblutdruck kann abgeschätzt werden:
RR-Grenze = 120mmHg + 0,4x (Intensität [Watt] + Alter [Jahre])
Die „Faustregel“ für den pathologischen Belastungsblutdruck bei Männern und Frauen (20–50 Jahre) ist:
-
>200/>100mmHg bei 100Watt
-
>185/>100mmHg bei 75 Watt
Es gibt Hinweise darauf, dass ein überschießender Blutdruckanstieg unter Belastung, unabhängig vom Ausgangswert, der Entstehung einer arteriellen Hypertonie vorausgeht.19 Nach Ende der Belastung sollte der RR innerhalb von 5min auf den Ausgangswert oder tiefer zurückgehen.18 Ein verzögerter Abfall geht mit einem erhöhten Risiko für eine KHK bzw. HI und somit mit einer Verschlechterung der Prognose einher.20–22
Blutdruck-bedingte Abbruchkriterien bei der Belastungsuntersuchung sind bei untrainierten Gesunden >250 und/oder >115mmHg, ein fehlender Anstieg oder ein Abfall des RRsyst unter den Ausgangswert oder von >10mmHg trotz vorhergehenden Anstiegs.
Herzfrequenz und körperliche Belastung
Damit die körperliche Leistung gesteigert werden kann, kommt es unter Belastung zu einem etwa 5-fachen Anstieg der koronaren Durchblutung und zu einem 4-fachen Anstieg der Sauerstoffaufnahme (VO2). Dies wird durch einen Anstieg der HF um das ca. 2,2-Fache, des Schlagvolumens um das 0,3-Fache und der arteriovenösen Sauerstoffdifferenz um das 1,5-Fache erzielt. Die HF liefert also den stärksten Beitrag zur Leistung.23 Üblicherweise kommt es unter körperlicher Belastung zu einem Anstieg der HF von etwa 10/min pro MET (ca. 20W).18 Die maximal erreichbare Herzfrequenz (HFmax) nimmt mit dem Alter ab und kann durch eine medikamentöse Therapie (Betablocker, Amiodaron) limitiert sein. Das Erreichen der HFmax ist kein Abbruchkriterium, genauso wenig wie die erreichte Sollleistung.
Formeln zur Abschätzung der erzielbaren maximalen Herzfrequenz:
-
HFmax = 208 – 0,7 x Alter (in Jahren) (für gesunde Erwachsene)
-
HFmax = 206 – 0,88 x Alter (in Jahren) (für Frauen ab dem 35. Lebensjahr)
-
HFmax = 220 – Alter (+ 15%) (für den Alltag)
-
Submaximale HF = 200 – Alter
Chronotrope Inkompetenz
Werden <85% der HFmax bei maximaler Ausbelastung ohne eine Betablockertherapie erreicht, so spricht dies für eine chronotrope Inkompetenz. Diese ist mit einer erhöhten Morbidität und Mortalität vergesellschaftet.18 Um die von Patient zu Patient unterschiedliche funktionelle Kapazität und die unterschiedliche Ruheherzfrequenz (HFRuhe) mit zu berücksichtigen, wird das Verhältnis der Herzfrequenzreserve, auch als chronotroper Index bezeichnet, berechnet:24
-
Chronotroper Index = (HFmax – HFRuhe)/(220 – Alter – HFRuhe)
Abnormal und mit einer erhöhten Mortalität verbunden wären <80% (<62% unter Betablockertherapie).24–28
Erholung der Herzfrequenz
Nach dem Belastungsende sollte bei normaler autonomer Funktion die HF um >12/min nach 1 Minute und um >22/min nach 2 Minuten abgefallen sein (Heart Rate Recovery; HRR). Grund ist die parasympathische Reaktivierung, die in den ersten 30 Sekunden nach maximaler Belastung am stärksten ist.29 Van de Vegte et al. konnten zeigen, dass der Abfall der HF in den ersten 10 Sekunden nach maximaler Belastung die größte Aussagekraft bezüglich Mortalität in den nächsten 6 Jahren hat.30 Die HRR ist somit ein unabhängiger Prädiktor für Mortalität, unabhängig von der systolischen Linksventrikelfunktion, der funktionellen Kapazität oder dem Ausmaß der KHK.31 Regelmäßiges Ausdauertraining kann die HRR normalisieren und die Prognose verbessern.32
Rate Pressure Product
Das Produkt aus HF x RRsystistunter den Begriffen Kreuzprodukt, Doppelprodukt, Double Product und Rate Pressure Product (RPP) bekannt. Es ist ein Maß für den myokardialen Sauerstoffverbrauch. Das RPP sollte bei Belastung mindestens um den Faktor 2,4 ansteigen. Bei Ausbelastung gilt ein Wert von >25000mmHg/Schläge/min als gut, >30000–40000 als sehr gut. Myokardiale Ischämien bzw. die Ischämieschwelle lassen sich üblicherweise bei demselben RPP und nicht bei derselben Belastungsintensität nachweisen. Je geringer das RPP, desto schlechter die Prognose bezüglich kardiovaskulärer Ereignisse und desto wahrscheinlicher ist das Vorliegen für eine Mehrgefäßerkrankung.18 Das RPP scheint ein besserer prognostischer Marker zu sein als die HFmax bzw. die HRR.33 Die Einnahme von Betablockern reduziert das RPP.
Beurteilung der Ergometrie
Die Ergometrie sollte symptomlimitiert sein. Die alters-, geschlechts-, gewichts- und größenabhängige Sollleistung und die altersabhängige HFmax sind keine guten Belastungsendpunkte und stellen kein Abbruchkriterium dar. Die Leistung wird üblicherweise als Prozentsatz des Soll ausgedrückt. Eine Leistungsfähigkeit von 100% bedeutet, dass man „nur“ dem Durchschnitt (durchschnittlicher Erwartungswert) entspricht. Während der Belastung und in der Erholungsphase werden drei Parameter beurteilt:
-
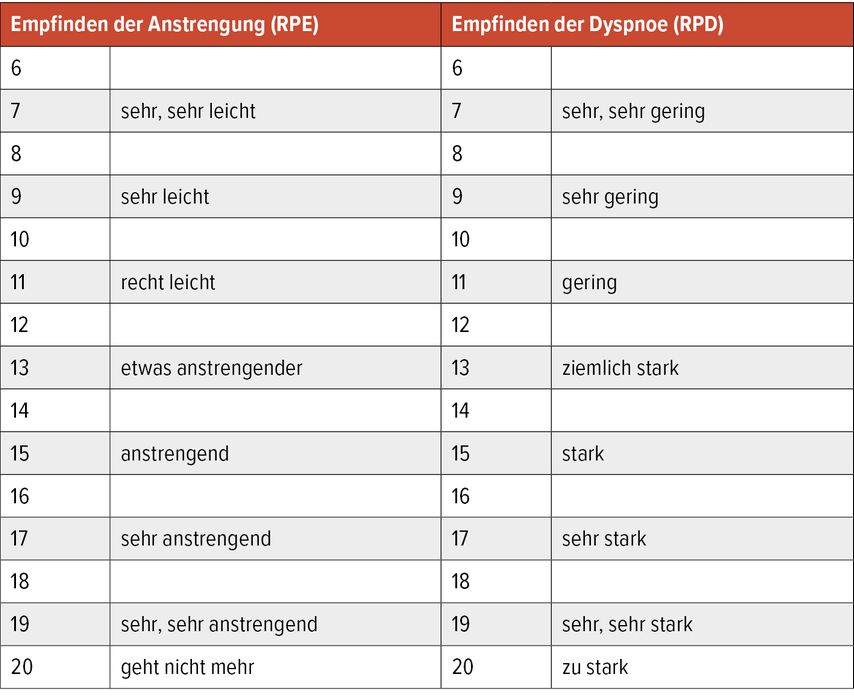
die Klinik, der Grund des Abbruchs, der Erschöpfungs- bzw. Dyspnoegrad durch Beschreibung mithilfe der Borg-Skala (Tab. 3)
-
Hämodynamik mit HF-Verhalten, RR-Verhalten, RPP, Dauer der Belastung, Belastung (Watt), die relative Leistungsfähigkeit (%) und die HRR
-
EKG-Veränderungen wie Repolarisationsstörungen und Rhythmusstörungen
Tab. 3: Borg-Skala: Der Beginn der Skalierung bei 6 beruht auf dem nicht linearen Zusammenhang zwischen Leistung und Leistungsempfinden (RPE = „ratings of perceived exertion“), ebenso die Skala für das Dyspnoeempfinden (RPD = „ratings of perceived dyspnoe“). Die Skalierung von 0–20 ist nicht linear, die von 6–20 verläuft aber linear34
Komplikationen bei der Ergometrie35
Beachtet man Indikationen, Kontraindikationen und Abbruchkriterien, ist die Häufigkeit von Komplikationen bei der Ergometrie gering. Prinzipiell werden kardiale und nicht kardiale Komplikationen unterschieden:
-
Kardiale: akutes Koronarsyndrom, Tachyarrhythmien, Bradyarrhythmien, hypertensive Reaktion, Linksherzinsuffizienz, Hypotonie, Synkope, Schock, thromboembolisches Ereignis, Letalität
-
Nicht kardiale: intrakranielle Blutung, transiente globale Amnesie, thromboembolisches Ereignis, Gelenksbeschwerden, Muskelschmerzen, Lumbalgie, Hypoglykämie
Bei Patienten mit KHK treten bis zu 10 ST-Hebungs-Infarkte und/oder Todesfälle pro 10000 Untersuchungen auf. Das Risiko ist für Patienten mit einem stattgehabten MI größer. MI treten während der Ergometrie 7-mal häufiger auf als ein plötzlicher Herztod (Häufigkeit <0,005%). MI ereignen sich zu 4–20% während der Belastung oder in der 1. Stunde danach. Das Risiko ist für Patienten ohne regelmäßige körperliche Betätigung größer. Tachyarrhythmien oder eine zunehmende ventrikuläre Extrasystolie unter Belastung oder in der Erholungsphase werden als prognostisch ungünstig angesehen.35
Abbruchkriterien
Absolute Abbruchkriterien
-
Kein Anstieg oder Abfall des RRsyst unter den Ausgangswert oder >10mmHg trotz vorhergehenden Anstiegs verbunden mit Ischämiezeichen (Angina pectoris, ST-Senkung)
-
Zunehmende Angina pectoris
-
ST-Hebung >0,1mV in Ableitungen ohne pathologische Q-Zacke (außer in aVR, aVL oder V1)
-
Zunehmende zerebrale Symptomatik (Verwirrtheit, Präsynkope)
-
Zeichen verminderter Perfusion (Zyanose, Blässe)
-
Anhaltende ventrikuläre Tachykardie, AV-Block II° oder III°
-
Wunsch des Patienten
-
Technische Gründe
Relative Abbruchkriterien
-
Abfall des RRsyst >10mmHg gegenüber dem Ausgangs-RR trotz Belastungsanstieg ohne Ischämiezeichen
-
ST- oder QRS-Veränderungen wie horizontale oder deszendierende ST-Senkung (>0,2mV) oder ausgeprägter Lagetypwechsel
-
Arrhythmien mit Gefahr der hämodynamischen Instabilität
-
Erschöpfung, Dyspnoe, Giemen, Beinkrämpfe, Claudicatio
-
Entwicklung eines Schenkelblockbildes oder intraventrikuläre Leitungsverzögerung
-
Abfall der Tretkurbelumdrehungen <40/min
-
Arterielle Hypertonie (>250mmHg und/oder >115mmHg)
Medikamente, die die Ergometrie beeinflussen18,36
-
Betarezeptorblocker senken auf vergleichbarer Belastungsstufe HF und RR. Die Belastbarkeit von Patienten mit koronarer Ischämie steigt (Ischämieschwelle steigt).
-
Nitrate steigern die Belastbarkeit und vermindern die Ischämiereaktion auf vergleichbarer Belastungsstufe.
-
Kalziumantagonisten vom Diltiazem- und Verapamil-Typ senken HF, RR und steigern die Ischämieschwelle, solche vom Nifedipin-Typ wirken ähnlich, steigern jedoch die HF.
-
Digitalis kann eine Ischämiereaktion im Belastungs-EKG vortäuschen (falsch positiver Befund).
-
Diuretika zeigen keine direkte Beeinflussung, eventuell kann es zu Arrhythmien bei Hypokaliämie kommen, bei längerer Einnahme eventuell zu Volumenmangel und erhöhter HF bei Belastung.
-
Vasodilatatoren führen zur Senkung des RR bei vergleichbarer Belastungsstufe (eventuell Steigerung der HF).
-
Antiarrhythmika können zu einer QRS-Verbreiterung und/oder Verlängerung des QT-Intervalls führen. Antiarrhythmika können zu ventrikulären Arrhythmien führen (proarrhythmogene Wirkung).
-
Bronchodilatatoren (β-Mimetika, Theophyllinpräparate) steigern die Herzfrequenz in Ruhe und während Belastung; sie können supraventrikuläre Arrhythmien unter Belastung auslösen.
-
Psychopharmaka: Tranquilizer und Antidepressiva können ein falsch positives Belastungs-EKG hervorrufen (verlängerte QT-Dauer).
-
Antihistaminika (Terfenadin) können Arrhythmien auslösen (Torsade de pointes oder atypische Kammertachykardie).
Literatur:
1 ACSM’s Guidelines for Exercise Testing and Prescription, 11th Edition, 2022 2 Meyer FJ et al.: Belastungsuntersuchungen in der Pneumologie – Empfehlungen der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin e.V. [Exercise Testing in Respiratory Medicine - DGP Recommendations]. Pneumologie 2018; 72(10): 687-731 3 Guazzi M et al.: Cardiopulmonary exercise testing: What is its value? J Am Coll Cardiol 2017; 70(13): 1618-36 4 Corrà U et al.: Role of cardiopulmonary exercise testing in clinical stratification in heart failure. A position paper from the Committee on Exercise Physiology and Training of the Heart Failure Association of the European Society of Cardiology. Eur J Heart Fail 2018; 20(1): 3-15 5 Sinagra G et al.: Risk stratification in cardiomyopathy. Eur J Prev Cardiol 2020; 27(2 Suppl): 52-8 6 Iung B et al.; EORP VHD II Investigators: Contemporary Presentation and Management of Valvular Heart Disease: the EURObservational Research Programme Valvular Heart Disease II Survey. Circulation 2019; 140(14): 1156-69 7 Vahanian A et al.; ESC/EACTS Scientific Document Group; ESC Scientific Document Group: 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J 2021; 28: ehab395 8 Knuuti J et al.: The performance of non-invasive tests to rule-in and rule-out significant coronary artery stenosis in patients with stable angina: a meta-analysis focused on post-test disease probability. Eur Heart J 2018; 39(35): 3322-30 9 Joshi PH, de Lemos JA: Diagnosis and management of stable angina: a review. JAMA 2021; 325(17): 1765-78 10 Ferraro R et al.: Evaluation and management of patients with stable angina: beyond the ischemia paradigm: JACC state-of-the-art review. J Am Coll Cardiol 2020; 76(19): 2252-66 11 Knuuti J et al.; ESC Scientific Document Group: 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J 2020; 41(3): 407-77 12 Wonisch M et al.: Praxisleitlinien Ergometrie. Journal für Kardiologie 2008; 15(Supplementum A – Praxisleitlinien Ergometrie): 3-17 13 Primus C et al.: Praxisleitfaden Ergometrie. Journal für Kardiologie 2020; 27(1-2): 38-42 14 Meyer FJ et al.: Belastungsuntersuchungen in der Pneumologie – Empfehlungen der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin e.V. [Exercise Testing in Respiratory Medicine - DGP Recommendations]. Pneumologie 2018; 72(10): 687-731 15 Primus C et al.: Praxisleitlinien Ergometrie und Spiroergometrie. Journal für Kardiologie 2022; in press 16 Leitlinien der Deutschen Gesellschaft für Kardiologie – Herz- und Kreislaufforschung e.V. ESC Pocket Guidelines. Chronisches Koronarsyndrom, Version 2019. Grünwald: Börm Bruckmeier Verlag GmbH. Kurzfassung der 2019 ESC Guidelines on the diagnosis and management of chronic coronary syndromes 17 Williams B et al.; ESC Scientific Document Group: 2018 ESC/ESH Guidelines for the management of arterial hypertension. Eur Heart J 2018; 39(33): 3021-104 18 Fletcher GF et al.; American Heart Association Exercise, Cardiac Rehabilitation, and Prevention Committee of the Council on Clinical Cardiology, Council on Nutrition, Physical Activity and Metabolism, Council on Cardiovascular and Stroke Nursing, and Council on Epidemiology and Prevention: Exercise standards for testing and training: a scientific statement from the American Heart Association. Circulation 2013; 128(8): 873-934 19 Holmqvist L et al.: Exercise blood pressure and the risk of future hypertension. J Hum Hypertens 2012; 26: 691-5 20 McHam SA et al.: Delayed systolic blood pressure recovery after graded exercise: an independent correlate of angiographic coronary disease. J Am Coll Cardiol 1999; 34(3): 754-9 21 Carneiro HA et al.: Association of blood pressure and heart rate responses to submaximal exercise with incident heart failure: the Framingham Heart Study. J Am Heart Assoc 2021; 10(7): e019460 22 Lee J et al.: Association of blood pressure responses to submaximal exercise in midlife with the incidence of cardiovascular outcomes and all-cause mortality: the Framingham Heart Study. J Am Heart Assoc 2020; 9(11): e015554 23 Brubaker PH, Kitzman DW: Chronotropic incompetence: causes, consequences, and management. Circulation 2011; 123(9): 1010-20 24 Lauer MS et al.: Impaired chronotropic response to exercise stress testing as a predictor of mortality. JAMA 1999; 281: 524-9 25 Dhoble A et al.: Cardiopulmonary fitness and heart rate recovery as predictors of mortality in a referral population. J Am Heart Assoc 2014; 3(2): e000559 26 Khan MN et al.: Chronotropic incompetence as a predictor of death among patients with normal electrograms taking beta blockers (metoprolol or atenolol). Am J Cardiol 2005; 96: 1328-33 27 Dobre D et al.: Association between resting heart rate, chronotropic index, and long-term outcomes in patients with heart failure receiving β-blocker therapy: data from the HF-ACTION trial. Eur Heart J 2013; 34(29): 2271-80 28 Khan MN et al.: Chronotropic incompetence as a predictor of death among patients with normal electrograms taking beta blockers (metoprolol or atenolol). Am J Cardiol 2005; 96: 1328-33 29 Lachman S et al.: The prognostic value of heart rate recovery in patients with coronary artery disease: a systematic review and meta-analysis. Am Heart J 2018; 199: 163-9 30 van de Vegte YJ et al.: Heart rate recovery 10 seconds after cessation of exercise predicts death. J Am Heart Assoc 2018; 7(8): e008341 31 Kligfield P, Lauer MS: Exercise electrocardiogram testing: beyond the ST segment. Circulation 2006; 114(19): 2070-82 32 Jolly MA et al.: Impact of exercise on heart rate recovery. Circulation 2011; 124(14): 1520-6 33 Whitman M, Jenkins C: Rate-pressure product, age predicted maximum heart rate or heart rate reserve. Which one better predicts cardiovascular events following exercise stress echocardiography? Am J Cardiovasc Dis 2021; 11(4): 450-7 34 Borg GA.: Psychophysical bases of perceived exertion. Med Sci Sports Exerc 1982; 14: 377-81 35 Berent R et al.: Komplikationen bei der Ergometrie [Complications during exercise testing]. Herz 2010; 35(4): 267-72 36 Löllgen H, Leyk D: Exercise testing in sports medicine. Dtsch Arztebl Int 2018; 115(24): 409-16
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
(Neue) Blutdruckziele im klinischen Alltag?
Die Diskussion um optimale Blutdruckwerte erhält durch eine aktuelle Analyse aus den USA eine neue Dynamik: Im klinischen Alltag war ein systolischer Blutdruck zwischen 130 und 139mmHg ...