MicroRNAs: neue Einblicke in die Pathophysiologie der Mitralklappeninsuffizienz
Autoren:
Dr. Georg Spinka
Assoc. Prof. Priv.-Doz. Dr. Georg Goliasch, PhD
Medizinische Universität Wien
Universitätsklinik für Innere Medizin II
Klinische Abteilung für Kardiologie
E-Mail: georg.spinka@meduniwien.ac.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Während die sekundäre Mitralklappeninsuffizienz bei Patienten mit Herzinsuffizienz mit reduzierter Linksventrikelfunktion häufig vorkommt und mit einer signifikant erhöhten Mortalität assoziiert ist, sind viele wichtige pathophysiologische Schlüsselmechanismen – besonders auf zellulärer Ebene – derzeit noch unbekannt. MicroRNAs wurden zuletzt mit kardialen Umbaumechanismen in der Herzinsuffizienz in Verbindung gebracht und könnten die pathophysiologischen Veränderungen der Mitralklappeninsuffizienz auf zellulärer Ebene besser charakterisieren.
Keypoints
-
MicroRNAs sind kurzstreckige, nicht-kodierende RNA-Sequenzen, die in die posttranslationale Genregulation involviert sind und eine Vielzahl an bekannten sowie bisher noch unbekannten Auswirkungen auf verschiedenste Erkrankungen haben
-
In der Herzinsuffizienz sind MicroRNAs bereits gut erforscht und dienen als Biomarker, welche in der Beurteilung von Krankheitsverlauf und Prognoseeinschätzung von Bedeutung sind
-
Auch in der sekundären Mitralklappeninsuffizienz scheinen MicroRNAs von Wert zu sein, indem sie Anzeichen für kardiale Umbaumechanismen wie Hypertrophie und Fibrose liefern und speziell durch MicroRNA-133a prognostische Bedeutung erlangen
Hintergrund
Eine zumindest mittelgradige und damit relevante sekundäre Mitralklappeninsuffizienz (SMR) betrifft rund 30% der Patienten mit Herzinsuffizienz mit reduzierter Linksventrikelfunktion (HFrEF). Betrachtet man das gesamte Spektrum der Herzinsuffizienz liegt die Prävalenz der SMR laut einer rezent veröffentlichten Studie sogar bei 40% und ist mit einer signifikant erhöhten Mortalität assoziiert. Dieser sekundär erworbene Klappenfehler entsteht aufgrund von linksventrikulärer Dilatation mit Verlagerung der Papillarmuskeln, welche durch zusätzlichen Zug auf die Mitralklappensegel einen effizienten Klappenschluss verhindern.1–3
Während makroskopische Mechanismen der Pathophysiologie dieser Erkrankung größtenteils geklärt sind, bleiben molekulare oder zelluläre Prozesse weitgehend unbekannt. Die rezente Entdeckung von MicroRNAs konnte nun ein neues Licht auf die mikroskopischen Mechanismen vieler Erkrankungen, darunter die Herzinsuffizienz, werfen. Erstmals 1993 in Nematoden erforscht, sind MicroRNAs kurzstreckige, nicht-kodierende RNA-Sequenzen, die in posttranslationale Genregulation involviert sind. Sie entstehen aus einer primären MicroRNA, welche durch das RNA-Polymerase II Enzym „Drosha“ und das RNAse III Enzym „Dicer“ zu einer doppelsträngigen RNA prozessiert werden. Der „reife“ Strang dieser MicroRNA vermag es an eine Vielzahl verschiedener, komplementärer mRNAs zu binden und somit eine Genexpression zu unterdrücken, was für eine Beteiligung an zahlreichen pathophysiologischen Prozessen spricht.4 Die zunehmende Erforschung dieser MicroRNAs hat zu der faszinierenden Idee geführt, diese als Biomarker für das Voranschreiten einer Erkrankung bzw. zur Risikoeinschätzung zu verwenden, da ihre Expression üblicherweise morphologischen Veränderungen vorangeht.
MicroRNAs in der Herzinsuffizienz
Spezifische MicroRNAs konnten bereits mit kardiovaskulären Erkrankungen und speziell der Herzinsuffizienz in Verbindung gebracht werden. So konnten zum Beispiel die MicroRNA-Superfamilien -1, -133a, -208, sowie -499 als kardiale, muskelspezifische Regulatoren identifiziert werden.5 Speziell die reduzierte Expression von MicroRNA-133a wurde hier mit der Entwicklung von Hypertrophie und Fibrose assoziiert.6 Bei Patienten mit hypertropher Kardiomyopathie konnten erhöhte Konzentrationen von MicroRNA-29a ebenfalls mit Fibrose und Hypertrophie verknüpft werden, was jedoch nicht für die Klappeninduzierte Hypertrophie gilt. Bei Überexpression wurde MicroRNA-let7i als antihypertrophes Agens identifiziert, nicht zuletzt durch die inhibitorische Wirkung auf Angiotensin II. Die Rolle von MicroRNA-21 ist bisher umstritten, es konnte jedoch gezeigt werden, dass Schlüsselmechanismen von wichtigen Signaltransduktionswegen wie Apoptose, Hypertrophie und Fibrose durch sie beeinflusst werden. Die Expression von MicroRNA-132 wirkt antioxidativ sowie antiapoptotisch und ist bei Patienten mit Herzinsuffizienz reduziert. Weniger mit dem Herzen assoziiert, jedoch die am häufigsten vorkommende in der Leber, ist MicroRNA-122 in hohem Maße in den Cholesterin- und Fettsäurestoffwechsel involviert.7,8
MicroRNAs in der sekundären Mitralklappeninsuffizienz
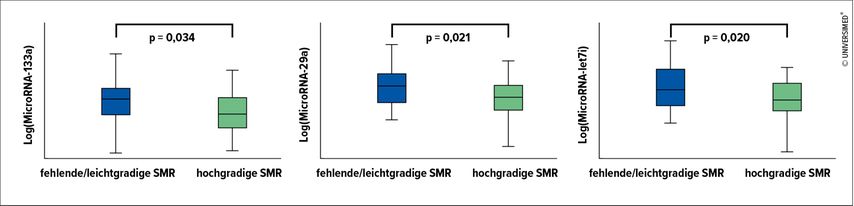
Obwohl in der Herzinsuffizienz mittlerweile eingehend erforscht, existieren kaum Daten über MicroRNAs im Kontext der SMR. Dies hat sich eine rezent veröffentlichte Studie der Medizinischen Universität Wien zum Ziel gemacht und untersuchte die Unterschiede in der Expression verschiedener MicroRNAs bei Patienten mit HFrEF und schwerer SMR im Vergleich zu Patienten mit HFrEF und lediglich leichtgradiger bzw. fehlender SMR.9 Es konnte festgestellt werden, dass MicroRNA-133a, -29a, und -let7i bei Patienten mit hochgradiger Klappendysfunktion im Vergleich zu Patienten mit Herzinsuffizienz ohne relevante SMR signifikant unterexprimiert sind und mit semiquantitativen Messwerten der SMR invers korrelieren (Abb. 1). Verglichen mit bisherigen Ergebnissen von Studien in der Herzinsuffizienz könnten diese Ergebnisse auf die Aktivierung von kardialen Umbaumechanismen in Form von Fibrose und Hypertrophie hinweisen.
Abb. 1: MicroRNA-Profile von Patienten mit HFrEF und fehlender/leichtgradiger SMR verglichen mit Patienten mit hochgradiger SMR.
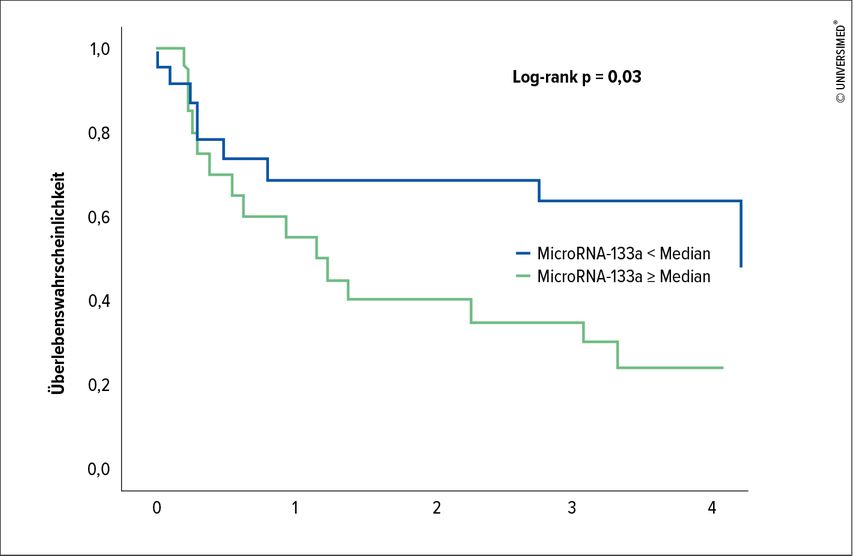
In einer Überlebensanalyse der Studie konnte hingegen interessanterweise gezeigt werden, dass erhöhte Werte von MicroRNA-133a bei Patienten mit HFrEF und hochgradiger SMR mit einem signifikant erhöhten Risiko für den kardiovaskulären Tod oder Hospitalisationen für Herzinsuffizienz assoziiert waren (Abb. 2). Während also über die gesamte Studienpopulation betrachtet die MicroRNA-Konzentrationen mit steigender SMR abnahmen, waren es bei der isolierten Gruppe der Patienten mit schwerer SMR erhöhte Werte, welche ein schlechtes Überleben anzeigten. Eine rezente Studie konnte erhöhte Konzentrationen von MicroRNA-133a bei Patienten mit Herzinfarkt mit einem schlechteren Überleben assoziieren.6 In dieser Hinsicht ist es möglich, dass niedrige Werte von MicroRNA-133a über den gesamten Verlauf der SMR betrachtet protektive Umbaumechanismen anzeigen, während hohe MicroRNA-133a Konzentrationen in der isoliert hochgradigen SMR einen irreversiblen Schaden an den Herzmuskelzellen andeuten. Es sind jedoch weitere Studien notwendig, um diese Theorie zu beweisen.
Abb. 2: Überlebensanalyse bei Patienten mit HFrEF und hochgradiger SMR hinsichtlich der Konzentration von MicroRNA-133a.
Ausblick
Trotz ihrer erst rezenten Entdeckung gewinnen MicroRNAs zunehmend an Bedeutung in der Erforschung vieler Erkrankungen. Ihr Stellenwert konnte auch in kardiovaskulären Erkrankungen bereits aufgezeigt werden, so zum Beispiel in der Herzinsuffizienz und zuletzt in der sekundären Mitralklappeninsuffizienz. Als molekulare Vorboten von morphologischen Veränderungen bieten MicroRNAs nicht nur die Möglichkeit, Einblick in zelluläre Veränderungen verschiedener Erkrankungen zu erlangen, sondern auch als Biomarker zur Risiko- und Verlaufseinschätzung verwendet zu werden. Wir warten mit Spannung auf weitere Ergebnisse in diesem vielversprechenden Forschungsgebiet.
Literatur:
1 Bartko PE et al.: Burden, treatment use, and outcome of secondary mitral regurgitation across the spectrum of heart failure: observational cohort study. BMJ 2021; 373: n1421 2 Bartko PE et al.: Secondary valve regurgitation in patients with heart failure with preserved ejection fraction, heart failure with mid-range ejection fraction, and heart failure with reduced ejection fraction. Eur Heart J 2020; 41: 2799–810 3 Goliasch G et al.: Refining the prognostic impact of functional mitral regurgitation in chronic heart failure. Eur Heart J 2018; 39: 39–46 4 Bartel DP. MicroRNAs: Genomics, Biogenesis, Mechanism, and Function. Cell. 2004; 116: 281–97 5 Wong LL et al.: MicroRNA and heart failure. Int J Mol Sci 2016; 17(4): 502 6 Carè A et al.: MicroRNA-133 controls cardiac hypertrophy. Nat Med 2007; 13: 613–8 7 Roncarati R et al.: Circulating miR-29a, among other up-regulated microRNAs, is the only biomarker for both hypertrophy and fibrosis in patients with hypertrophic cardiomyopathy. J Am Coll Cardiol 2014; 63: 920–7 8 Condorelli G et al.: MicroRNAs in cardiovascular diseases: Current knowledge and the road ahead. J Am Coll Cardiol. 2014; 63: 2177–87 9 Spinka G et al.: Secondary mitral regurgitation-Insights from microRNA assessment. Eur J Clin Invest 2021; 51: e13381–e13381
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
Labormedizinische Fallstricke bei kardialen Markern
Bei Schädigung oder Stress des Herzmuskels werden kardiale Marker in den Blutkreislauf freigesetzt. Ihre labormedizinische Bestimmung spielt eine Schlüsselrolle in der Diagnostik, ...