Ernährung und körperliches Training bei Lebererkrankungen
Autoren:
Prim. Priv.-Doz. Dr. Thomas-Matthias Scherzer
Leiter der Abteilung für Innere Medizin, Kardiologie und Endoskopie
Sanatorium Hera
Krankenanstalt der Bediensteten der Stadt Wien
Leiter des Bereiches Sport und Ernährung im Gesundheits- und Vorsorgezentrum der KFA
Bettina Knabl
Diätologin im Gesundheits- und Vorsorgezentrum der KFA im Sanatorium Hera
Mag. Benedikt Mehl
Sportwissenschafter im Gesundheits- und Vorsorgezentrum der KFA im Sanatorium Hera
Korrespondierender Autor:
Prim. Priv.-Doz. Dr. Thomas-Matthias Scherzer
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Für Patient*innen mit Lebererkrankungen ist nicht nur die medikamentöse Therapie für den Verlauf der Erkrankung entscheidend, auch die Ernährung und körperliche Aktivität spielen eine maßgebliche Rolle. Hier unterscheiden wir vor allem zwischen Patient*innen mit und ohne Leberzirrhose bzw. zwischen Gewichtsverlust im Rahmen einer Malnutrition und/oder einer Sarkopenie und adipösen Patient*innen mit einer Sarkopenie. Bei adipösen Patient*innen handelt es sich zumeist um NASH(„non-alcoholic steatohepatitis“)-Patient*innen.
Keypoints
-
Rechtzeitige Optimierung der Ernährungssituation durch Diätolog*innen im multidisziplinären Team kann Mangelernährung verringern, die Überlebensrate erhöhen und die Lebensqualität verbessern.
-
Patient*innen mit chronischen Lebererkrankungen sollten auf Malnutrition bzw. Sarkopenie gescreent werden.
-
Eine Gewichtsreduktion von >7–10% vom Ausgangsgewicht kann den Leberfettgehalt und die hepatischen Entzündungsprozesse bei der Diagnose Fettleber deutlich reduzieren.
-
Frühe Ernährungs- und Bewegungsmaßnahmen setzen – auch bei ein „bisschen Übergewicht“, „ein bisschen erhöhtem Blutzucker“ und „ein bisschen Fettleber“.
-
Für alle Patient*innen mit Lebererkrankungen gilt: „Move it or lose it.“
In der westlichen Bevölkerung leiden rund 30% an einer Fettlebererkrankung,1 bei hohem BMI und Adipositas kann dies auf bis zu 85% steigen.2 Die nichtalkoholische Fettlebererkrankung (NAFLD) reicht von einer simplen Fettleber (Steatosis hepatis) über die nichtalkoholische Steatohepatitis (NASH) mit oder ohne Fibrose bis hin zur Leberzirrhose. Die NAFLD ist eng mit allen Facetten des metabolischen Syndroms vergesellschaftet.
Ernährung bei Patient*innen mit Fettlebererkrankungen (NAFLD)
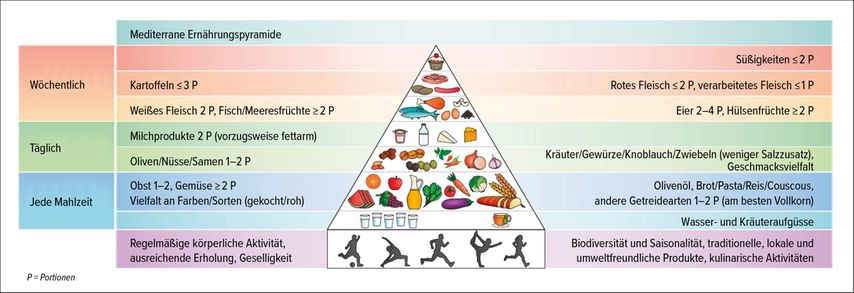
Die wichtigste Maßnahme bei der Therapie stellt eine Lebensstilmodifikation mit Anpassung des Ernährungsverhaltens dar. Durch eine Gewichtsreduktion von >7–10% vom Ausgangsgewicht können der Leberfettgehalt und auch die hepatischen Entzündungsprozesse deutlich reduziert werden. Ziel ist es, eine ausgewogene Kost wie die evidenzbasierte mediterrane Ernährungsform in den Speiseplan zu integrieren. Sie beinhaltet eine ausreichende Proteinzufuhr aus 2/3 pflanzlichen und 1/3 tierischen Eiweißquellen, pflanzliche Öle, Fische mit hohem Anteil an einfach und mehrfach ungesättigten Fettsäuren und reichlich Ballaststoffe (Abb. 1). Zusätzlich sollte die Fruktoseaufnahme gering ausfallen und Alkohol vermieden werden.3
Für einige Patient*innen ist es anfangs sehr schwierig, das Ernährungsmuster und das Ernährungsverhalten zu ändern, da diese zu festgefahren sind oder die Motivation nicht ausreichend vorhanden ist. Auch eine Dysbiose kann einer erfolgreichen Gewichtsreduktion im Wege stehen.4
Patient*innen mit Problemen bei der Lebensstiländerung können positive Effekte nach 2-wöchigem Leberfasten erzielen. Die angewandten Proteinprodukte können mit einer Gesamtenergiezufuhr von 1000−1200 kcal/Tag einen hohen Gewichtsverlust erreichen. Zusätzlich sind diese Proteinshakes neben ihrem hohen Proteingehalt mit leberaktiven Substanzen wie ß-Glucan, Cholin, Taurin und Omega-3-Fettsäuren angereichert.
Leberfasten wird idealerweise ärztlich und diätologisch betreut und sollte sehr individuell auf die Personen abgestimmt werden. Studien bei ausgewählten Steatosepatient*innen zeigen positive Effekte nach 2-wöchigem Leberfasten.5 Zielesind dabei die Optimierung des Stoffwechsels und die Loslösung vom bisherigen Essverhalten. Für nachhaltige Effekte ist eine weitere Umstellung des Ernährungs- und Bewegungsverhaltens von entscheidender Bedeutung.6
Sport und Bewegung bei Patient*innen mit NAFLD
Im Sinne einer ganzheitlichen Lebensstilmodifikation ist körperliche Aktivität zusammen mit einer Ernährungsumstellung eine wichtige Maßnahme bei der Therapie von Fettlebererkrankungen.7 Hauptziel ist die Entfettung der Leber mit konsekutiver Reduktion der Entzündungsprozesse innerhalb der Leber (NASH) bzw. die Abnahme des Viszeralfettes.
Wichtig dabei ist die Unterscheidung von körperlicher Aktivität als Überbegriff für jede Form von (Energieumsatz erhöhender) Bewegung und körperlichem Training als strukturiertem und kontrolliertem Prozess.
Sowohl Ausdauertraining als auch Krafttraining führen zu einer Verbesserung der peripheren Insulinsensitivität, einer Reduktion des intrahepatischen Fettgehaltes (unabhängig von einer Gewichtsreduktion), einer Reduktion inflammatorischer hepatischer Prozesse und einer Verbesserung der Fettsäurenoxidation in der Leber.8 Zusätzlich trägt körperliche Aktivität in Verbindung mit Ernährungsmaßnahmen zur Erzielung einer negativen Energiebilanz bei.7Beide Trainingsformen, das Ausdauertraining und das Krafttraining, sind nach derzeitiger Studienlage ähnlich effektiv, basieren aber auf teils unterschiedlichen Wirkmechanismen.9
Hinsichtlich optimaler Intensität beim Ausdauertraining wird in der Literatur eine moderate Intensität als ähnlich effektiv wie intensives Training beschrieben.10,11 Allerdings ist die Studienlage auch in diesem Bereich nach wie vor nicht zufriedenstellend. Hier scheinen – ähnlich wie bei der Wahl der optimalen Sportart und Trainingsform – die persönliche Präferenz und die körperliche Belastbarkeit wesentliche Faktoren für optimale und nachhaltige Trainingserfolge zu sein.8 Entscheidend ist hier die langfristige Beibehaltung eines gesundheitssportlichen Trainings.
Empfehlenswert ist die Steigerung des Aktivitätslevels im Vergleich zum Ist-Zustand, jedenfalls auf ein Ausmaß von mindestens 150–200 Minuten pro Woche Ausdauertraining oder Krafttraining oder einer Kombination aus beidem, aufgeteilt auf 3–5 Trainingseinheiten (vgl. die Guidelines von EASL-EASD-EASO,12 AASD,13 ESPEN,14 APASL15). Zusätzlich können sich eine Reduktion der Phasen von körperlicher Inaktivität (langes Sitzen, Fernsehzeit) und ein Unterbrechen durchgehender Inaktivitätsphasen durch körperliche Aktivität (Stehen, Gehen) positiv auf das Gewichtsmanagement und den Zucker- und Fettstoffwechsel auswirken.16
Ernährung bei Patient*innen mit Leberzirrhose
Die Unterernährung ist bei Patien-t*innen mit Lebererkrankungen mit dem Schweregrad der Leberfibrose vergesellschaftet. So leiden 20% der Patient*innen mit einer kompensierten Leberzirrhose bzw. bis zu 50% der Patient*innen mit einer dekompensierten Leberzirrhosean einer Malnutrition.
Die Unterernährung äußert sich in einem Verlust von Fett- bzw. Muskelmasse (Sarkopenie), wobei Frauen eher Fett und Männer eher Muskulatur verlieren.17 Eine Ausnahme stellen hier die Patient*innen mit einer NASH dar, die zumeist an einer Adipositas mit Sarkopenie leiden, welche aufgrund des Übergewichtes leicht übersehen werden kann. Die Malnutrition bzw. Sarkopenie stehen mit einer erhöhten Komplikationsrate in Verbindung: So leiden diese Patient*innen häufiger an einer gesteigerten Infektanfälligkeit, einer hepatischen Enzephalopathie, Aszites, Komplikationen im Rahmen der Lebertransplantation und weisen auch eine erhöhte Mortalität auf.
Aufgrund der Wichtigkeit der Therapie der Malnutrition und Sarkopenie sollten Leberzirrhosepatient*innen dahingehend gescreent werden.18 Die EASL gibt eine Guideline vor, welche die Patient*innen in eine Gruppe mit hohem, mittleremoder niedrigem Risiko einteilt. Entscheidend ist hier, auf das CHILD-Stadium zu achten bzw. den BMI (Trockengewicht ohne Aszites) zu bestimmen.
Mangelernährung wird häufig nicht richtig diagnostiziert und tritt, abhängig von den verwendeten Screeningmethoden und den untersuchten Patientenpopulationen, bei 5–92% der Patient*innen auf. Die verringerte Energie- und Proteinaufnahme, Entzündungen, Malabsorption, ein veränderter Stoffwechsel mit Hypermetabolismus, hormonelle Störungen und Dysbiose des Darmmikrobioms können zu Mangelernährung beitragen.19
Eine rechtzeitige Optimierung der Ernährungssituation kann die Prognose verbessern. Für Patient*innen mit fortgeschrittener Leberzirrhose sind eine individuell angepasste Ernährungsoptimierung und eine engmaschige Betreuung essenziell, um den Nährstoffbedarf zu decken. Bei Patient*innen mit Leberzirrhose muss von einem deutlich erhöhten Kalorienbedarf von mindestens 35kcal/kg Körpergewicht über den Tag verteilt ausgegangen werden. Die Proteinaufnahme von 1,2–1,5g/kg Körpergewicht ist besonders wichtig. Ein Ausgleich von Vitaminmangelzuständen sollte zudem unterstützend erfolgen. Lange Nüchternphasen sollten vermieden werden.20
Ernährungstherapeutische Interventionen durch ein multidisziplinäres Team, insbesondere durch Diätolog*innen, können zur Verbesserung der Lebensqualität, Erhöhung der Überlebensrate und Verringerung der Mangelernährung führen.19 Vor allem Patient*innen mit Adipositas bzw. mittlerem und hohem Risiko sollten den Diätolog*innen vorgestellt werden. Dort wird zwischen Leberzirrhosepatient*innen mit oder ohne Adipositas unterschieden.
Sport und Bewegung bei Patient*innen mit Leberzirrhose und Sarkopenie
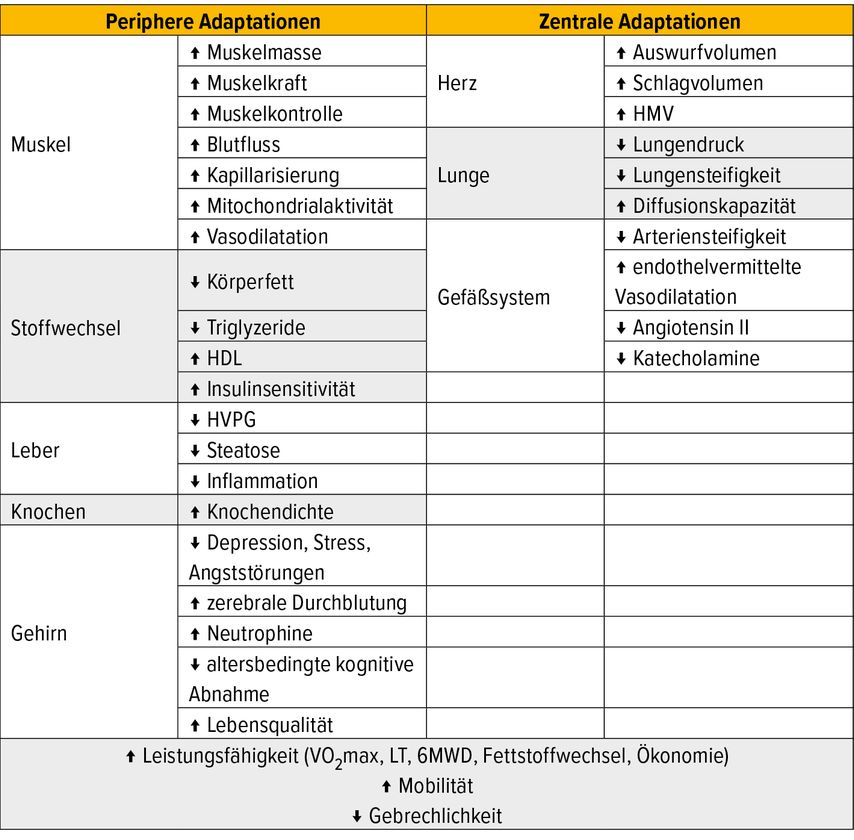
Ein strukturiertes und kontrolliertes körperliches Trainingsprogramm für Personen mit Zirrhose und schwerwiegenden Lebererkrankungen kann wesentliche Parameter körperlicher und psychischer Gesundheit ohne Anzeichen einer erhöhten Komplikationsrate verbessern (Tab. 1).21–24
Tab. 1: Trainingseffekte für Patienten mit Zirrhose (modifiziert nach Jamali T et al. 2022, West J et al. 2021, Tandon P et al. 2018, Tapper EB et al. 2018)21–24
Verbesserungen wurden in der Literatur im Bereich der kardiorespiratorischen Fitness (VO2max, 6-Minuten-Gehtest), Muskelmasse, Muskelkraft, portale Hypertension, Lebensqualität, Mobilität, Gebrechlichkeit/Frailty-Index beschrieben.
Trotz dieser vielversprechenden Ergebnisse liegen noch zu wenige Daten für differenzierte Empfehlungen zur optimalen Gestaltung einer Trainingsroutine hinsichtlich Intensität, Häufigkeit und Trainingsform vor. Auf jeden Fall sollte eine Kombination von Ausdauer- und Krafttraining nach individueller Abklärung der Belastbarkeit und möglicher Risken erfolgen.22,24 Empfehlenswert ist hier ein angeleitetes und individuell gesteuertes Training in enger multidisziplinärer Abstimmung mit Diätologie, Hepatologie und Trainingswissenschaft.25
Fazit
Rechtzeitige Optimierung der Ernährungssituation durch Diätolog*innen im multidisziplinären Team kann Mangelernährung verringern, die Überlebensrate erhöhen und die Lebensqualität verbessern. Ein strukturiertes körperliches Training ist bei der Prävention oder Therapie von Mangelernährung und Sarkopenie mitentscheidend.
Literatur:
1 Rinella ME: Nonalcoholic fatty liver disease: a systematic review. JAMA 2015; 313(22): 2263-73 2 Fabbrini E et al.: Obesity and nonalcoholic fatty liver disease: biochemical, metabolic, and clinical implications. Hepatology 2010; 51(2): 679-89 3 EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver diet. J Hepatol 2016; (4):1388-402 4 Vilar-Gomez E et al.: Weight loss through lifestyle modification significantly reduces features of nonalcoholic steatohepatitis. Gastroenterology 2015; 149(2): 367-78.e5 5 Teufelhart M et al.: A prospective study to evaluate the efficacy of a standardized low calorie diet according to PNPLA3 genotype in patients with non alcoholic fatty liver disease (NAFLD) – 2 months data (interim analysis). J Hepatol 2017; 66(1): 422 6 Interdisziplinäre Leitlinie der Qualität S3 zur „Prävention und Therapie der Adipositas“ der DGE. DGEM 2014 7 Semmler G et al.: Diet and exercise in NAFLD/NASH: beyond the obvious. Liver Int 2021; 41: 2249-68 8 Van der Windt DJ et al.: The effects of physical exercise on fatty liver disease. Gene Expr 2018; 18: 89-101 9 Hashida R et al.: Aerobic vs. resistance exercise in non-alcoholic fatty liver disease: a systematic review. J Hepatol 2017; 66: 142-52 10 Mantovani A, DalbeniA: Treatments forNAFLD: state of art. Int J Mol Sci 2021; 22(5): 2350 11 Zhang HJ et al.: Effects of moderate and vigorous exercise on nonalcoholic fatty liver disease: arandomized clinical trial. JAMA Intern Med 2016; 176: 1074-82 12 EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. J Hepatol 2016; 64(6): 1388-402 13 Chalasani N et al.: The diagnosis and management of nonalcoholic fatty liver disease: practice guidance from the American Association for the Study of Liver Diseases. Clin Liver Dis 2018; 11(4): 81 14 Plauth M et al.: ESPEN guideline on clinical nutrition in liver disease. Clin Nutr 2019; 38(2): 485-521 15 Eslam M et al.: The Asian Pacific Association for the Study of the Liver clinical practice guidelines for the diagnosis and management of metabolic associated fatty liver disease. Hepatol Int 2020; 14(6): 889-919 16 Romero-Gómez M et al.: Treatment of NAFLD with diet, physical activity and exercise. J Hepatol 2017; 67(4): 829-46 17 Alberino F et al.: Nutrition and survival in patients with liver cirrhosis. Nutrition 2001; 17(6): 445-50 18 EASL Clinical Practice Guidelines on nutrition in chronicliver disease. JHepatol 2019; 70(1): 172-93 19 Traub J et al.: Malnutrition in patients with liver cirrhosis. Nutrients 2021; (13): 540 20 Farnque SM et al.: Non-alcoholic fatty liver disease: a patient guideline. JHEP Rep 2021; 3(5): 100322 21 Jamali T et al.: Outcomes of exercise interventions in patients with advanced liver disease: asystematic review of randomized clinical trials. Am J Gastroenterol 2022; 117(10): 1614-20 22 West J et al.: Exercise physiology in cirrhosis and the potential benefits of exercise interventions: a review. J Gastroenterol Hepatol 2021; 36(10): 2687-705 23 Tandon P et al.: Exercise in cirrhosis: translating evidence and experience to practice. J Hepatol 2018; 69(5): 1164-77 24 Tapper EB et al.: Is exercise beneficial and safe in patients with cirrhosis and portal hypertension? Current Hepatol Rep 2018; 17(3): 175-83 25 Duarte-Rojo A et al.: Exercise and physical activity for patients with end-stage liver disease: improving functional status and sarcopenia while on the transplant waiting list. Liver Transpl 2018; 24(1): 122-39
Das könnte Sie auch interessieren:
Sonografie der Leber – aktuelle Entwicklungen, quantitative Verfahren und klinische Bedeutung
Der vorliegende Übersichtsartikel fasst aktuelle technische Entwicklungen sowie klinische Anwendungen und Limitationen der Lebersonografie zusammen und diskutiert deren Stellenwert im ...
11. Hans Popper Lecture an der Medizinischen Universität Wien
Die jährlich im Rahmen der renommierten Hans Popper Lecture der Medizinischen Universität Wien verliehene Auszeichnung ging 2025 an Prof. Dr. Tom Hemming Karlsen, PhD, Oslo. Der führende ...
Fünf Therapien zur Behandlung von MASLD
Mit zunehmendem Übergewicht in der Bevölkerung wird auch die mit metabolischer Dysfunktion assoziierte steatotische Lebererkrankung (MASLD) vermehrt diagnostiziert. PD Dr. Dr. med. David ...