Diagnose der portalen Hypertension bei ausgeheilter chronischer Hepatitis C
Autoren: Dr. Georg Semmler
Ap. Prof. Priv.-Doz. DDr. Mattias Mandorfer
Hepatisches Hämodynamik Labor
Klinische Abteilung für Gastroenterologie und Hepatologie
Universitätsklinik für Innere Medizin III
Medizinische Universität Wien
Korrespondierender Autor:
Ap. Prof. Priv.-Doz. DDr. Mattias Mandorfer
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine Studie analysierte die Genauigkeit von nichtinvasiven Tests zur verlässlichen Diagnose bzw. zum Auschluss einer klinisch signifikanten portalen Hypertension und somit zur Risikostratifizierung der hepatischen Dekompensation nach Heilung der chronischen Hepatitis C.
Keypoints
-
Die portale Hypertension ist der treibende Faktor für Komplikationen fortgeschrittener Lebererkrankung.
-
Da die Therapie die Entwicklung einer hepatischen Dekompensation positiv beeinflusst, ist die verlässliche Diagnose der CSPH bedeutsam.
-
Goldstandard der Diagnostik ist die (minimal) invasive Messung des Lebervenendruckgradienten (HVPG), alternativ werden nicht invasive Tests (NIT) eingesetzt.
-
Beim ILC 2022 wurden praxisrelevante Studiendaten zur Verlässlichkeit von NITs präsentiert.
-
Die Ergebnisse wurden bereits in den rezenten BAVENO-VII-Leitlinien berücksichtigt.
Die portale Hypertension ist der treibende Faktor für Komplikationen der fortgeschrittenen Lebererkrankung (sog. „advanced chronic liver disease“ [ACLD]).1 Da die Therapie der portalen Hypertension erwiesenermaßen die Entwicklung von zukünftiger hepatischer Dekompensation (Aszites, Varizenblutung, hepatische Enzephalopathie) positiv beeinflusst,2 gilt es, die klinisch signifikante portale Hypertension (CSPH) verlässlich zu diagnostizieren und ggf. eine Therapie mit nichtselektiven Betablockern (NSBB; bevorzugt Carvedilol) einzuleiten.3 Dies ist besonders relevant, da im rezenten BAVENO-VII-Konsensus die Diagnose einer CSPH als maßgeblich für die Therapieeinleitung eines NSBB eingestuft wurde, anstatt wie in früheren Leitlinien das Vorhandensein von behandlungsbedürftigen Varizen.3
Nichtinvasive Tests zur Diagnose der CSPH
Da die Messung des Lebervenendruckgradienten (HVPG) zwar den Goldstandard für die Diagnose der CSPH darstellt,4 jedoch aufgrund der (Minimal-)Invasivität und der eingeschränkten Verfügbarkeit nicht bei allen Patienten angewandt werden kann, wurden zahlreiche nichtinvasive Tests (NIT) für die Diagnose der CSPH untersucht.5
Besonders häufig werden hier die Lebersteifigkeitsmessung (LSM) mittels transienter Elastografie sowie laborchemische Tests wie die Thrombozytenzahl eingesetzt, wobei daneben insbesondere der Von-Willebrand-Faktor (VWF) bzw. die Ratio aus VWF und Thrombozytenzahl (sog. VITRO-Score) eine hohe Genauigkeit zur Diagnose der CSPH aufweisen.6,7
Obwohl die Studienlage zur Anwendbarkeit dieser NIT bei Patienten mit aktiver Lebererkrankung gut und eindeutig ist, gab es nach Heilung der chronischen Hepatitis C (CHC, sog. „sustained virologic response“ [SVR]) widersprüchliche Ergebnisse: Während Studien aus Wien die hohe Genauigkeit von LSM und Thrombozytenzahl/VITRO zur Diagnose der CSPH bei kompensierter ACLD, aber auch zur Prognoseeinschätzung nach SVR bestätigten,8,9 postulierten Daten aus Spanien, dass etablierte Cut-offs der LSM, um eine CSPH ein- bzw. auszuschließen (<13,6kPa bzw. ≥21kPa), nach Ausheilung der primären Ätiologie nur ungenügend zutreffend waren, wobei sich diese Studie auf die Subgruppe von Patienten mit CSPH vor Therapie fokussierte.10 Somit ist bei der besagten Studie von einem „spectrum bias“ auszugehen, da bei der klinischen Anwendung in der Regel nicht bekannt ist, ob vor der Therapie eine CSPH vorlag.
Aktuelle Studienergebnisse
Vor diesem Hintergrund wurde die Studie„Non-invasive tests for clinically significantportal hypertension after HCV-cure – pooled analysis and validation“ im Rahmen des BAVENO-VII-Konsensus von Ap.Prof. DDr. Mattias Mandorfer (Medizinische Universität Wien) und Dr. Juan Carlos García-Pagán (Barcelona) initiiert und beim International Liver Congress (ILC) 2022 vorgestellt. Ziel war es, die Genauigkeit der NIT (in diesem Fall LSM und Thrombozytenzahl) vor bzw. nach Heilung der CHC zu untersuchen und durch daraus gewonnene Erkenntnisse Kriterien bzw. Grenzwerte zu definieren, um eine CSPH nach Heilung der primären Ätiologie sicher ein- bzw. auszuschließen. Anhand von 324 Patienten mit gepaarten HVPG und NIT-Messungen vor und nach Hepatitis-C-Therapie konnten folgende zentrale Schlüsse gezogen werden:
-
Die Korrelation des HVPG mit LSM ist nach Heilung der primären Ätiologie stärker als davor, während die Korrelation mit der Thrombozytenzahl vergleichbar ist.
-
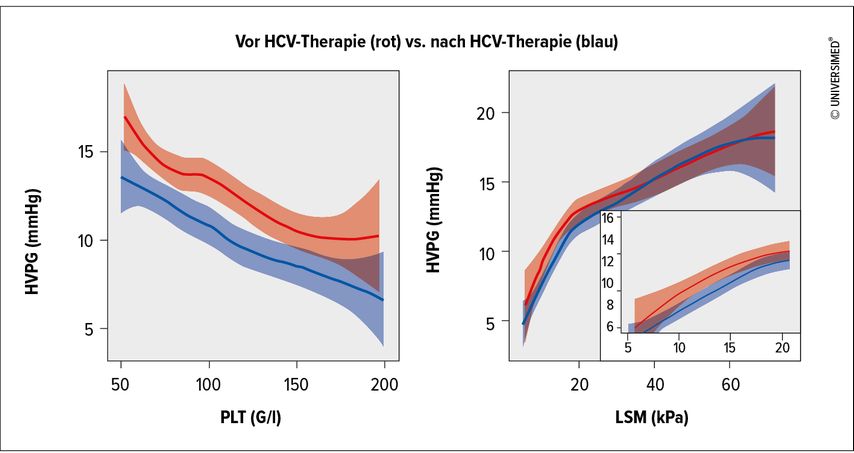
Bei einem gegebenen Wert der Thrombozytenzahl bzw. der LSM (im Bereich bis ∼20kPa) ist der erwartete HVPG-Wert nach Therapie niedriger als vor Therapie (Abb. 1). Dies bedeutet, dass durch die bisher angewandten Cut-offs die Schwere der portalen Hypertension nach Heilung der CHC überschätzt werden würde.
-
Die diagnostische Genauigkeit von LSM und Thrombozytenzahl für CSPH war nach Therapie numerisch höher als vor Therapie.
-
Eine Kombination dieser beiden Parameter erreicht eine sehr hohe Genauigkeit in der Diagnose der CSPH nach Heilung der CHC.
-
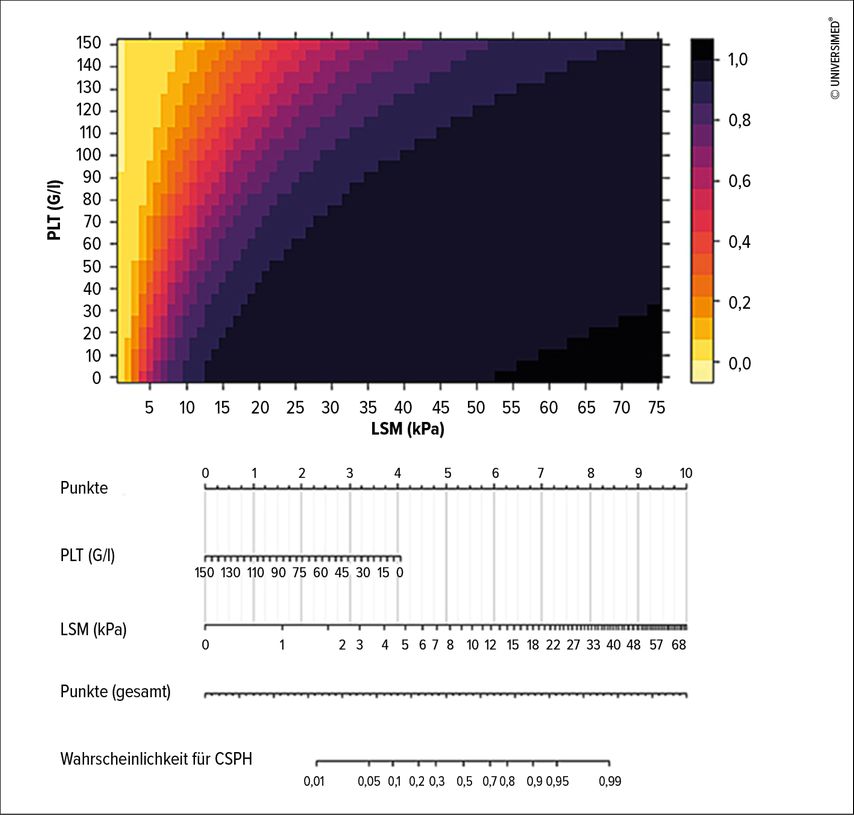
Die Wahrscheinlichkeit für das Vorliegen einer CSPH kann mittels eines Nomogramms bzw. „3-D“-Plots abgeschätzt werden (Abb. 2).
-
Werden Grenzwerte von <12kPa (LSM) und >150G/l (Thrombozytenzahl) kombiniert, kann bei kompensierter ACLD eine CSPH nach Heilung der CHC verlässlich ausgeschlossen werden, wogegen eine LSM ≥25kPa das Vorliegen einer CSPH bestätigt.
Abb. 1: Zusammenhang zwischen Thrombozytenzahl (PLT, links) bzw. Lebersteifigkeit (LSM, rechts) mit dem HVPG vor (rot) bzw. nach (blau) Therapie der Hepatitis C
Abb. 2: Wahrscheinlichkeit für das Vorliegen einer CSPH nach Heilung der CHC anhand der Thrombozytenzahl (PLT) und der Lebersteifigkeit (LSM). Die dargestellten Wahrscheinlichkeiten beziehen sich auf Patienten mit kompensierter ACLD vor Therapie. Eine Thrombozytenzahl >150G/l soll als 150G/l eingesetzt werden
Die zuletzt genannten Kriterien wurden schließlich in einer Kohorte von 755 kompensierten Patienten mit ACLD bezüglich des Auftretens einer hepatischen Dekompensation validiert. Hierbei zeigte sich, dass Patienten, bei denen eine CSPH ausgeschlossen werden konnte, kein Risiko für eine hepatische Dekompensation hatten, während Patienten, bei denen eine CSPH diagnostiziert werden konnte, ein weiterhin relevantes Risiko für zukünftige hepatische Dekompensation aufwiesen.
Weitere Details dieser Arbeit bitten wir der Publikation11 bzw. Vorträgen beim ILC 2022 (on demand) bzw. der UEG(United European Gastroenterology) Week 2022 (Oktober 2022) zu entnehmen.
Für die Praxis und Handlungsempfehlungen
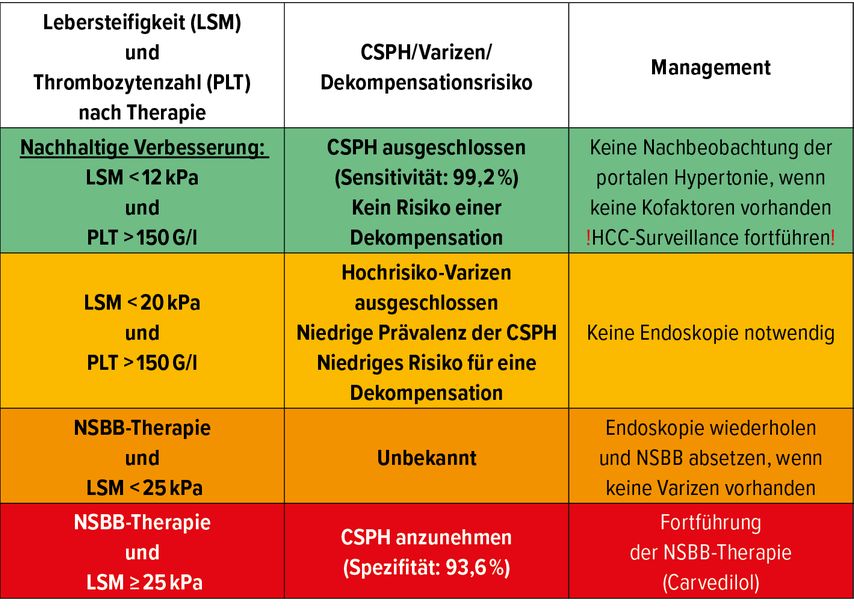
Die vorgestellten Ergebnisse dieser Arbeit haben bereits Einzug in die rezent publizierten BAVENO-VII-Leitlinien gefunden, wobei sich für die Praxis folgende Implikationen ergeben (Tab. 1):
-
Bei kompensierten Patienten mit LSM <12kPa & Thrombozytenzahl >150G/l kann eine CSPH nach Heilung der CHC ausgeschlossen werden. Diese Patienten bedürfen keiner weiteren Überwachung bezüglich der portalen Hypertension (Endoskopie und wiederholte LSM), wenn keine Kofaktoren wie Übergewicht, Diabetes oder (pathologischer) Alkoholkonsum vorliegen.
-
Bei Patienten mit LSM ≥25kPa kann von einem weiteren Vorliegen einer CSPH ausgegangen werden. Diese Patienten bedürfen einer weitergeführtenbzw. neueingeleiteten Therapie mit Carvedilol.
Daneben sind folgende Handlungsempfehlungen essenziell:
-
Die bestehenden BAVENO-VI-Kriterien zum Ausschluss von behandlungsbedürftigen Varizen (LSM <20kPa und Thrombozytenzahl >150G/l) können auch nach Heilung der CHC angewandt werden.
-
Aufgrund des relevanten Risikos für das Auftreten eines hepatozellulären Karzinoms trotz Heilung der CHC sind weiterhin halbjährliche Kontrollen mittels Ultraschall (± α-Fetoprotein) auf unbestimmte Zeit notwendig. Zur individuellen Risikoabschätzung kann eine Kombination aus Alter, α-Fetoprotein, LSM und Albumin (±Alkoholkonsum) nach HCV-Therapie hilfreich sein – Details bitten wir der entsprechenden Publikation zu entnehmen.12
Literatur:
1 Mandorfer M, Simbrunner B: Prevention of first decompensation in advanced chronic liver disease. Clin Liver Dis 2021; 25(2): 291-310 2 Villanueva C et al.: β blockers to prevent decompensation of cirrhosis in patients with clinically significant portal hypertension (PREDESCI): a randomised, double-blind, placebo-controlled, multicentre trial. Lancet 2019; 393(10181): 1597-608 3 de Franchis R et al.: Baveno VII −renewing consensus in portal hypertension. J Hepatol 2022; 76(4): 959-74 4 Reiberger T et al.: Measurement of the hepatic venous pressure gradient and transjugular liver biopsy. J Vis Exp 2020; (160): e58819 5 Mandorfer M et al.: Noninvasive diagnostics for portal hypertension: acomprehensive review. Semin Liver Dis 2020; 40(3):240-55 6 Maieron A et al.: Von Willebrand factor as a new marker for non-invasive assessment of liver fibrosis and cirrhosis in patients with chronic hepatitis C. Aliment Pharmacol Ther 2014; 39(3): 331-8 7 Hametner S et al.: The VITRO score (Von Willebrand factor antigen/thrombocyte ratio) as a new marker for clinically significant portal hypertension in comparison to other non-invasive parameters of fibrosis including ELF test. PLoS One 2016; 11(2): e0149230 8 Mandorfer M et al.: Changes in hepatic venous pressure gradient predict hepatic decompensation in patients who achieved sustained virologic response to interferon-free therapy. Hepatology 2020; 71(3): 1023-36 9 Semmler G et al.: Noninvasive risk stratification after HCV eradication in patients with advanced chronic liver disease. Hepatology 2021; 73(4): 1275-89 10 Lens S et al.: Clinical outcome and hemodynamic changes following HCV eradication with oral antiviral therapy in patients with clinically significant portal hypertension. J Hepatol 2020;73(6): 1415-24 11 Semmler G et al.: Non-invasive tests for clinically significant portal hypertension after HCV cure. J Hepatol 2022; S0168-8278(22)03056-2 (ahead of print) 12 Semmler G et al.: HCC risk stratification after cure of hepatitis C in patients with compensated advanced chronic liver disease. J Hepatol 2022; 76(4): 812-21
Das könnte Sie auch interessieren:
Hepatitis-A-Ausbrüche in den USA
Zwischen 2016 und 2022 kam es in den USA zu einer unerwarteten Häufung von Hepatitis-A-Ausbrüchen. Besonders betroffen waren sozioökonomisch benachteiligte Bevölkerungsgruppen mit ...
Neues aus der Welt der Hepatologie
Kürzlich wurden Arbeiten zu den Risiken nach TIPS-Implantation veröffentlicht und eine neue S3-Leitlinie zu autoimmunen Lebererkrankungen steht nun zur Verfügung. Aktuelles gibt es aber ...
Tumoren der Leber und der Gallenwege
Die Inzidenz von malignen Lebertumoren ist in den vergangenen Jahrzehnten weltweit angestiegen.1 In der westlichen Welt sind Leberfibrosen und -zirrhosen aufgrund von chronischen HCV/HBV ...