Aszites, spontan-bakterielle Peritonitis, hepatorenales Syndrom – wo stehen wir?
Autor:
Dr. Florian Riedl
Assistenzarztfür Innere Medizin
Klinische Abteilung für Innere Medizin 2
Landesklinikum St. Pölten
E-Mail: florian.riedl@stpoelten.lknoe.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das Auftreten von Aszites, einer spontan-bakteriellen Peritonitis (SBP) sowie eines hepatorenalen Syndroms (HRS) sind häufige Manifestationen einer dekompensierten Leberzirrhose. Sowohl die rasche Diagnose als auch die stadiengerechte Therapie sind essenziell zum Erhalt der Lebensqualität und zur Verbesserung der Prognose.
Keypoints
-
Aszites ist die häufigste Erstmanifestation einer dekompensierten Leberzirrhose.
-
Im Falle einer SBP steht die rasche Etablierung einer kalkulierten antibiotischen Therapie im Vordergrund.
-
Ein HRS wird mittels Vasokonstriktoren und Substitution von Humanalbumin therapiert.
-
Alle Patienten mit dekompensierter Leberzirrhose müssen frühzeitig auf die Möglichkeit einer Lebertransplantation evaluiert werden.
Die Leberzirrhose stellt das Endstadium verschiedener chronischer Lebererkrankungen dar.In Österreich sind gesundheitsschädlicher Alkoholkonsum sowie eine Fettleberhepatitis häufige Ursachen. Mit der daraus folgenden Entwicklung einer klinisch relevanten portalen Hypertension (>10mmHg) steigt das Risiko für die Dekompensation der Zirrhose, welche sich u.a. im Auftreten von Aszites, einer spontan-bakteriellen Peritonitis (SBP) und eines hepatorenalen Syndroms (HRS) manifestieren kann. Die Dekompensation stellt einen Wendepunkt des Krankheitsverlaufs mit einhergehender deutlich erhöhter Morbidität und Mortalität dar. Der folgende Artikel soll einen Überblick über die aktuelle Diagnostik sowie Therapiemöglichkeiten der dekompensierten Leberzirrhose geben.
Aszites
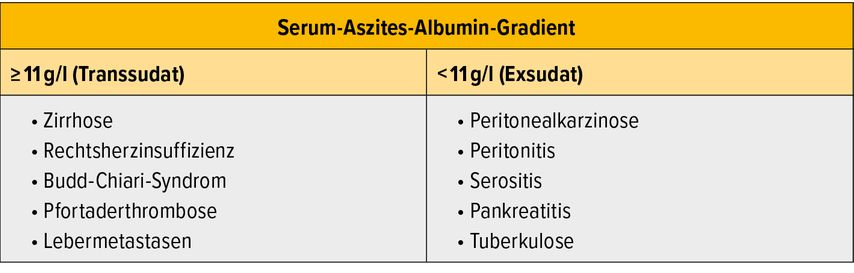
Aszites ist das häufigste Zeichen einer Dekompensation. Daher muss ausnahmslos jeder neu aufgetretene Aszites zur Bestimmung der Genese (portale Hypertension, Malignität, Infektionen etc.) punktiert werden. Doch auch jede klinische Verschlechterung von Patienten mit Leberzirrhose sollte eine Aszitespunktion nach sich ziehen, um potenzielle Auslöser wie zum Beispiel eine SBP zu identifizieren. Neben der Abnahme von Kulturen, Zytologie und Bestimmung der Zellzahl kann die Berechnung des Serum-Aszites-Albumin-Gradienten (SAAG) die Zuordnung der Genese erleichtern (Tab. 1). Bei einem SAAG ≥11g/l kann eine portale Hypertension als Ursache des Aszites angenommen werden. Aktuell wird die Einteilung eines Aszites je nach Ausmaß (Grad I: nur mit Ultraschall detektierbar; Grad II: klinisch erkennbare Abdomendistension; Grad III: deutliche Distension) vorgenommen. Ebenso erfolgt die Unterscheidung zwischen einem unkomplizierten und einem refraktären Aszites. Ein refraktärer Aszites wird definiert durch eine nicht ausreichende Asziteskontrolle trotz maximaler Diuretikadosen, ein rasches Wiederauftreten von Aszites innerhalb von 4 Wochen oder die Unmöglichkeit der Aufdosierung von Diuretika aufgrund des Auftretens von Komplikationen (z.B. Elektrolytentgleisungen, Anstieg der Nierenfunktionsparameter, Entwicklung einer hepatischen Enzephalopathie).
Therapeutisches Vorgehen bei Aszites
Da bei der Entwicklung eines Aszites ein herabgesetzter, systemischer Blutdruck mit daraus folgender Natriumretention und Expansion des extrazellulären Volumens im Vordergrund steht, wird therapeutisch primär eine strikte diätologische Salzrestriktion (5–7g/d) empfohlen. In der Regel gilt es im klinischen Alltag als praktikabel, Patienten dringend zu raten, Fertiggerichte sowie zusätzliches Salzen von Gerichten zu meiden. Im Falle einer dadurch nicht ausreichenden Asziteskontrolle kommen Diuretika (Spironolacton bzw. Furosemid) zum Einsatz, welche schrittweise und in Kombination bis zu einer Maximaldosis (400 bzw. 160mg/Tag) gesteigert werden können. Angestrebt wird ein maximaler Gewichtsverlust von 1kg/Tag mit einem vorab definierten Zielgewicht. Kommt es durch die medikamentöse Therapie zu keiner Verbesserung der Symptomatik, sollten (gegebenenfalls wiederholte) entlastende Aszitespunktionen vorgenommen werden. Hierbei ist ab 5 Litern abgelassenem Aszites auf eine ausreichende Substitution mit Humanalbumin (8g/l) zu achten. Mithilfe dieser Maßnahmen lässt sich ein Aszites Grad II bei 90% der Fälle ausreichend kontrollieren. Die Notwendigkeit der Therapie eines Aszites Grad I ist derzeit noch Gegenstand wissenschaftlicher Diskussionen.
Im Falle der Entwicklung eines refraktären Aszites kann dieser mittels wiederholter Aszitespunktionen oder der Implantation eines „transjugulären intrahepatischen portosystemischen Shunts“ (TIPS) therapiert werden. Ein Fortsetzen der diuretischen Therapie ist nur bei einer Harnnatrium-Ausscheidung von >30mmol/Tag zielführend. Weitere Therapiemöglichkeiten wie die Implantation von Dauerdrainagen oder einer alfapump® kommen in ausgewählten Fällen zum Einsatz und sollten in spezialisierten Zentren vorgenommen werden. Grundsätzlich sind jedoch Patienten frühzeitig – bei der ersten Manifestation einer Dekompensation der Leberzirrhose – in Bezug auf eine Lebertransplantation zu evaluieren.
Spontan-bakterielle Peritonitis
Im Rahmen einer Leberzirrhose kommt es zu Veränderungen des Darmmikrobioms, einer erhöhten Darmpermeabilität und daraus folgender bakteriellen Translokation. Die SBP stellt die häufigste Infektion im Rahmen einer Zirrhose dar und ist mit einer Mortalität von bis zu 20% vergesellschaftet. Als wichtigste Risikofaktoren für die Entwicklung einer SBP gelten Blutungen des oberen Gastrointestinaltraktes, ein niedriger Aszitesproteingehalt (<1,5g/dl) sowie vorausgegangene SBP-Episoden. Durch eine frühzeitige antibakterielle Therapie bzw. Etablierung einer antibiotischen Prophylaxe bei Risikopatienten kann eine deutliche Besserung der Prognose erreicht werden.
Als Goldstandard in der Diagnostik der SBP gilt die Aszitespunktion. Die Diagnose wird mittels Bestimmung der Neutrophilenzahl sowie durch die Abnahme von Asziteskulturen gestellt. Bei Vorliegen einer reinen bakteriellen Besiedelung ohne Entzündungszellen, eines sogenannten Bak-teraszites, ist eine antibiotische Therapie nur im Falle von klinisch-laborchemischen Inflammationszeichen indiziert und ansonsten lediglich mittels Verlaufspunktion zu kontrollieren. Bei einer Neutrophilen-zahl ≥250/mm3 müssen umgehend eine kalkulierte Antibiose sowie die Substitution von Humanalbumin eingeleitet werden. Nach 48Stunden ist der Therapieerfolg (Absinken der Zellzahl ≥25%) mittels neuerlicher Aszitespunktion zu überprüfen. Im Falle eines Therapieansprechens ist die Therapie über 7 Tage fortzusetzen und ansonsten eine Anpassung bzw. Erweiterung der antibiotischen Therapie vorzunehmen. Bei der Auswahl der empirischen Breitbandantibiose sind das Ansprechen auf vorausgegangene Infektionen, Allergien sowie die lokale Resistenzlage zu beachten. In Österreich werden häufig Cephalosporine der 3.Generation, Amoxicillin/Clavulansäure oder Chinolone eingesetzt.
Eine antibiotische Prophylaxe sollte aufgrund von potenziellen Nebenwirkungen, aufgrund von Resistenzentwicklungen und, nicht zuletzt, aufgrund von erheblichen Kosten auf Hochrisikopatienten beschränkt werden. Als Risikofaktoren gelten gastrointestinale Blutungen, ein proteinarmer Aszites (Primärprophylaxe) sowie eine vorausgegangene SBP (Sekundärprophylaxe). Hierbei kann Norfloxacin (400mg/Tag) eingesetzt werden.
Prinzipiell gilt auch für die SBP als Manifestation einer dekompensierten Leberzirrhose, so wie auch bereits für den Aszites, die Notwendigkeit einer frühzeitigen Evaluierung in Bezug auf eine Lebertransplantation.
Hepatorenales Syndrom
Im Rahmen einer Zirrhose kommt es zu einem herabgesetzten systemischen Blutdruck, einer kompensatorischen renalen Vasokonstriktion sowie zur Ausschüttung von antidiuretischen Hormonen. In Kombination mit einer erhöhten, systemischen Inflammation ist häufig eine Verschlechterung der Nierenfunktion bis zu einem akuten Nierenversagen (ANV) anzutreffen, besonders bei hospitalisierten Patienten mit einer deutlich verschlechterten Prognose und einer Mortalität von bis zu 44%. Da bis zum jetzigen Zeitpunkt keine kausale Therapie zur Verfügung steht, sind eine rasche Diagnose, die Beseitigung möglicher nephrotoxischer Einflüsse sowie eine Therapie mit Vasokonstriktoren und Humanalbumin vordergründig.
Zur Diagnosestellung eines ANV werden die international üblichen AKI-Kriterien angewandt (Kreatinin >0,3mg/dl in 48Stunden; ≥50% in 7 Tagen). Therapeutisch werden in einem ersten Schritt alle nephrotoxischen Substanzen pausiert (ebenso nicht-selektive Betablocker). Das Vorliegen von weiteren ungünstigen Einflussfaktoren (Infektionen, Hypovolämie, Schockgeschehen, strukturelle Nierenerkrankungen) sollte ausgeschlossen und wenn möglich therapiert werden. Weiters erfolgt die Substitution von Humanalbumin (1g/kg) über 2 Tage.
Kommt es unter den gesetzten Maßnahmen zu keiner Verbesserung der Nierenfunktion, liegt ein HRS vor. Die bis vor Kurzem übliche Einteilung in HRS-Typ I und HRS-Typ II anhand des Voranschreitens der eingeschränkten Nierenfunktion ist nicht mehr üblich. Unter vasokonstriktorischer Therapie (z.B. Terlipressin) und begleitender Substitution von Humanalbumin kommt es in bis zu 76% zumindest zu einem partiellen Therapieansprechen. Eine Terlipressingabe kann entweder als intravenöse Bolusgabe (initial 0,5mg alle 4Stunden bis max. 2mg alle 4Stunden) oder mittels Perfusor erfolgen (initial 2mg/Tag bis max. 12mg/Tag). Die Therapie soll bis zum Wiedererreichen der initialen Nierenfunktion oder maximal für 14 Tage fortgesetzt werden. Bezüglich des Einsatzes von Nierenersatzverfahren ist die derzeitige Datenlage noch unklar. Primär kommen sie bei Patienten zur Überbrückung bei geplanten Lebertransplantationen oder bei potenziell reversiblen Ursachen des ANV zum Einsatz.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Multiprofessionelle Zusammenarbeit in der Hepatologie am Beispiel der Leberzirrhose
Die Versorgung von Patient:innen mit Lebererkrankungen stellt eine komplexe, multiprofessionelle Herausforderung dar. Besonders bei fortgeschrittener Leberzirrhose mit Komplikationen wie ...
HCC-Update 2026: What’s new, what’s next?
Die Therapie des hepatozellulären Karzinoms (HCC) befindet sich im Umbruch: Immuntherapien haben die Prognose in den letzten fünf Jahren deutlich verbessert und neue Standards gesetzt. ...
Fünf Therapien zur Behandlung von MASLD
Mit zunehmendem Übergewicht in der Bevölkerung wird auch die mit metabolischer Dysfunktion assoziierte steatotische Lebererkrankung (MASLD) vermehrt diagnostiziert. PD Dr. Dr. med. David ...