Kombinationen mit Immuntherapien optimieren Therapien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In den letzten Jahren wurden viele Erfahrungen zu immunonkologischen Strategien mit Checkpoint-Inhibitoren bei verschiedenen Entitäten gesammelt. Eine Optimierung der Wirksamkeit ist bei gastrointestinalen Tumoren durch die Kombination mit etablierten Therapien möglich, wie beim ESMO in diversen Studien gezeigt wurde.
Nivolumab plus Chemotherapie ist neuer Standard beim HER2-negativen Magenkarzinom
Patienten mit fortgeschrittenem HER2-negativem Adenokarzinom von Magen (GC), gastroösophagealem Übergang (GEJC) oder Ösophagus (EC) haben eine schlechte Prognose von <1 Jahr Überleben. Die randomisierte dreiarmige Phase-III-Studie CheckMate 649 untersuchte die Erstlinientherapie mit Nivolumab plus Ipilimumab versus Nivolumab plus Chemotherapie versus alleinige Chemotherapie bei dieser Patientenklientel. 789 Patienten im Nivolumab-Arm wurden mit Nivolumab (360mg) plus XELOX im dreiwöchigen Schema oder mit Nivolumab (240mg) plus FOLFOX im zweiwöchigen Schema behandelt. Im Kontrollarm erhielten 792 Patienten XELOX (q3w) oder FOLFOX (q2w). Die Patienten wiesen in 70% der Fälle ein Magenkarzinom auf. Primäre Endpunkte waren das Gesamtüberleben (OS) und das progressionsfreie Überleben (PFS) bei Patienten mit einem PD-L1-CPS ≥5. Beim ESMO-Meeting wurden die ersten Ergebnisse im Vergleich von Nivolumab plus Chemotherapie versus Chemotherapie mit einer minimalen Nachbeobachtungszeit von 12 Monaten präsentiert.1
Die Studie erreichte ihren primären Endpunkt: Das mediane OS bei Patienten mit PD-L1-CPS ≥5 wurde durch die Hinzunahme von Nivolumab zur Chemotherapie von 11,1 auf 14,4 Monate verlängert (Abb. 1). Das Risiko, zu versterben, wurde um 29% verringert (HR: 0,71; 95% CI: 0,59–0,86; p<0,0001). Auch bei Patienten mit einem PD-L1-CPS ≥1 konnte eine signifikante Verlängerung des Gesamtüberlebens von median 11,3 auf 14,0 Monate beobachtet werden (HR: 0,77; 95% CI: 0,64–0,92; p=0,0001). Für alle in beide Studienarme randomisierten Patienten ergab sich ein Unterschied des medianen OS von 2,2 Monaten (13,8 vs. 11,6 Monate) mit einer Hazard-Ratio von 0,80 (95% CI: 0,68–0,94; p=0,0002). Bezüglich des progressionsfreien Überlebens zeigte sich in der Kohorte der Patienten mit einem PD-L1-CPS ≥5 eine Reduktion des Risikos für einen Progress um 32% (HR: 0,68; 98% CI: 0,56–0,81; p<0,0001). Die Kombination hat das Potenzial für eine neue Standard-Erstlinientherapie bei Patienten mit einem negativen oder unbekannten HER2-Status.
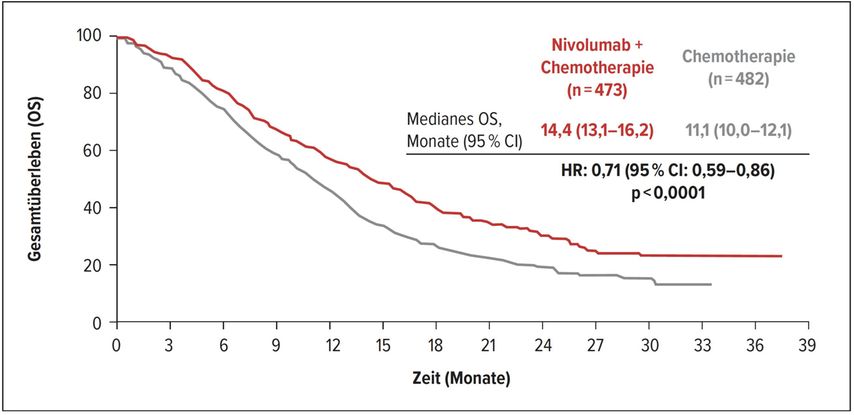
Abb. 1: Gesamtüberleben unter Nivolumab plus Chemotherapie vs. Placebo plus Chemotherapie bei Patienten mit PD-L1-CPS≥51
Auch die asiatische Phase-III-Studie ATTRACTION-4 kam zu der Schlussfolgerung, dass Nivolumab plus Chemotherapie ein neuer Erstlinienstandard bei Patienten mit nicht resezierbarem fortgeschrittenem oder rezidiviertem HER2-negativem GC oder GEJC sein könnte.2 In dieser doppelblinden, randomisierten Studie wurde als Chemotherapie S1 plus Oxaliplatin oder Capecitabin plus Oxaliplatin eingesetzt und insgesamt wurden 724 Patienten aus 130 Zentren in Japan, Korea und Taiwan behandelt. Bei 84% der Patienten lag eine PD-L1-Expression <1% vor. Im Ergebnis wurde das PFS durch die Nivolumab-Gabe von median 8,34 auf 10,45 Monate signifikant verlängert (HR: 0,68; 95% CI: 0,51–0,90; p=0,0007), nicht aber das OS (median: 17,45 vs. 17,15 Monate; HR: 0,90; 95% CI: 0,75–1,08; p=0,257). In der Subgruppenanalyse wurde eine größere Reduktion des PFS-Risikos durch die zusätzliche Nivolumab-Gabe für Patienten mit ≤1 Metastasenlokalität (HR: 0,42) im Vergleich zu ≥2 befallenen Organen (HR: 0,84) gesehen. Dies zeigte sich ebenfalls für das OS (HR: 0,60 bzw. 1,04). Welches der beiden Chemotherapieregime verwendet wurde, schien keinen Einfluss auf das PFS oder OS zu haben. Es sprachen 57,5% versus 47,8% der Patienten auf die Nivolumab-haltige bzw. alleinige Chemotherapie an, die mediane Dauer des Ansprechens betrug 12,91 versus 8,67 Monate.
Erstlinientherapie mit Pembrolizumab plus Chemotherapie beim Ösophaguskarzinom
Mit der Pembrolizumab-Monotherapie wurde bereits Antitumoraktivität bei Patienten mit fortgeschrittenem EC in späteren Therapielinien gezeigt. In der randomisierten, doppelblinden, placebokontrollierten Phase-III-Studie KEYNOTE-590 wurde die Zugabe von Pembrolizumab zur Chemotherapie bei Patienten mit fortgeschrittenem EC auch in der ersten Therapielinie untersucht.3 Primäre Endpunkte der Studie waren das OS sowie das PFS.
Mit der zusätzlichen Pembrolizumab-Therapie konnte das Risiko, zu versterben, gegenüber alleiniger Chemotherapie um 27% signifikant reduziert werden (HR: 0,73; 95% CI: 0,62–0,86; p<0,0001). Das mediane OS wurde durch die Immuntherapie von 9,8 auf 12,4 Monate verlängert. Nach 12 Monaten lebten 51% versus 39% und nach 24 Monaten 28% versus 16% der Patienten. Auch das Risiko für einen Progress wurde um 35% reduziert (HR: 0,65; 95% CI: 0,55–0,76). Im Median lebten die Patienten 6,3 versus 5,8 Monate progressionsfrei. Die 12- und 18-Monats-PFS-Raten betrugen 25% versus 12% bzw. 16% versus 6%. In Subgruppenanalysen zeigte sich ein Benefit insbesondere für Patienten mit einem CPS ≥10 und einer squamösen Histologie (Abb. 2). Pembrolizumab plus Chemotherapie könnte damit ein neuer Standard der ersten Therapielinie bei Patienten mit lokal fortgeschrittenem nicht resezierbarem oder metastasiertem EC einschließlich
GEJC-Tumoren unabhängig von ihrer Histologie oder dem Biomarker-Status sein.
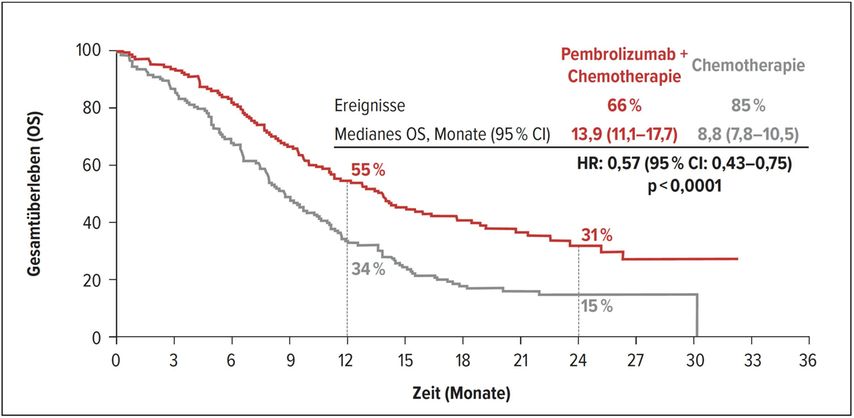
Abb.2: Gesamtüberleben bei Patienten mit squamösem Ösophaguskarzinom und hoher PD-L1-Expression unter Pembrolizumab plus Chemotherapie versus Chemotherapie3
Chemotherapie-freie Rechallenge mit Cetuximab plus Avelumab beim Kolorektalkarzinom
Die Kombination von Immuntherapie und EGFR-Antikörper ist laut der CAVE-mCRC-Studie eine vielversprechende Therapiestrategie für Patienten mit metastasiertem Kolorektalkarzinom (mCRC) und RAS-Wildtyp in der dritten Therapielinie.4 Die einarmige Phase-II-Studie untersuchte die Effektivität von Avelumab plus Cetuximab bei 77 Patienten mit RAS-Wildtyp-mCRC, die in der ersten Therapielinie unter einer Kombination mit Chemotherapie und Anti-EGFR-Antikörper eine komplette oder partielle Remission erreicht hatten. Der primäre Endpunkt der CAVE mCRC-Studie war ein medianes OS von wenigstens 11 Monaten – als 37,5%ige Verlängerung des historischen medianen OS einer Drittlinientherapie von 8 Monaten. Im Ergebnis betrug das OS unter Avelumab plus Cetuximab median 13,1 Monate (90% CI: 8,1–18,0). Das mediane PFS lag bei 3,6 Monaten (95% CI: 3,2–4,1). Ein Ansprechen oder eine Stabilisierung der Erkrankung wurde bei 65% der Patienten gesehen. Die Kombinationstherapie erwies sich als gut verträglich, mit niedriger Inzidenz von Grad-3-Rash (14%) und -Diarrhö (4%). Es wurden keine hämatologischen Toxizitäten festgestellt.
Lebensqualität als prognostischer Marker beim Pankreaskarzinom
In einer deutschen prospektiven, multizentrischen Studie wurde bei Patienten mit metastasiertem Pankreaskarzinom, die in der ersten Therapielinie mit Gemcitabin plus nab-Paclitaxel behandelt wurden, die Lebensqualität mithilfe des EORTC-C30-Fragebogens erhoben und eine Korrelation mit dem Gesamtüberleben untersucht.5 Primärer Endpunkt der Studie war die Patientenzahl ohne Verschlechterung der gesundheitsbezogenen Lebensqualität nach 3 Monaten. 588 Patienten wurden in die Studie eingeschlossen. Die Lebensqualität der Patienten war bei Beginn der Erstlinientherapie bereits stark eingeschränkt, hauptsächlich aufgrund von Verlust der Rollenfunktion und Auftreten von Fatigue. Die mediane Zeit bis zur Verschlechterung der Lebensqualität betrug in der Untersuchung 4,7 Monate (95% CI: 4,0–5,6). Ein relevanter Anteil von 61% bzw. 41% der Patienten gab eine dem Therapiebeginn vergleichbare Lebensqualität nach 3 bzw. 6 Monaten an. Medianes PFS und OS waren mit 5,85 bzw. 8,91 Monaten in den deutschen Zentren gut vergleichbar mit den Ergebnissen der Zulassungsstudie MPACT. In einer univariaten Analyse erwiesen sich die gesamte Lebensqualität und die meisten funktionellen und symptomatischen Variablen als starke Prädiktoren für das Überleben. Die multivariate Analyse identifizierte die körperliche Funktion sowie Übelkeit/Erbrechen als signifikant mit dem Überleben assoziiert. Jede Steigerung der körperlichen Funktion um 10 Punkte ging mit einer 11%igen Reduktion des Sterberisikos einher. Bei um 10 Punkte höheren Werten für Übelkeit/Erbrechen wurde eine 6%ige Steigerung des Sterberisikos beobachtet.
Bericht:
Dr. Ine Schmale
Literatur:
1 Möhler M et al.: Nivolumab plus chemotherapy versus chemo as first-line (1L) treatment for advanced gastric cancer/gastroesophageal junction cancer (GC/GEJC)/esophageal adenocarcinoma (EAC): first results of the CheckMate 649 study. ESMO 2020, Abstr. #LBA6_PR 2 Boku N et al.: Nivolumab plus chemotherapy versus chemotherapy alone in patients with previously untreated advanced or recurrent gastric/gastroesophageal junction (G/GEJ) cancer: ATTRACTION-4 (ONO-4538-37) study. ESMO 2020, Abstr. #LBA7_PR 3 Kato K et al.: Pembrolizumab plus chemotherapy versus chemotherapy as first-line therapy in patients with advanced esophageal cancer: the phase 3 KEYNOTE-590 study. ESMO 2020, Abstr. #LBA8_PR 4 Martinelle E et al.: Avelumab plus cetuximab in pre-treated RAS wild type metastatic colorectal cancer patients as a rechallenge strategy: the phase II CAVE (cetuximab-avelumab) mCRC study. ESMO 2020, Abstr. #397O 5 Götze TO et al.: The QOLIXANE trial – real life QoL and efficacy data in 1st line pancreatic cancer from the prospective platform for outcome, quality of life, and translational research on pancreatic cancer (PARAGON) registry. ESMO 2020, Abstr. #1525O
Das könnte Sie auch interessieren:
Nur eine von vielen Begleiterscheinungen
Warum er MRT-Veränderungen bei unspezifischen Rückenschmerzen wenig Bedeutung beimisst, erklärt Prof. Dr. med. Andreas Seekamp aus Kiel.
Modic Changes bei Rückenschmerzen
Obwohl die Erstbeschreibung fast 40 Jahre her ist, ist immer noch nicht klar, wodurch die MRT-Veränderungen entstehen und welchen Stellenwert sie für Diagnostik und Therapie haben.
Periphere Nervenscheidentumoren
Periphere Nervenscheidentumoren sind eine seltene, aber dennoch bedeutende Tumorentität, die das periphere Nervensystem betrifft. Sie können eine Vielzahl an Symptomen verursachen und ...