Die Osteoporose ist eine gynäkologische Erkrankung
Autor:
Dr. Ewald Boschitsch
Ambulatorium KLIMAX
Ambulatorium für Klimakterium und Osteoporose
Wien
E-Mail: e.boschitsch@klimax.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die häufigste Form der Osteoporose ist die postmenopausale Osteoporose, für die – nomen est omen – der nach der Menopause bestehende Östrogenmangel verantwortlich ist. Alle Gynäkolog:innen wissen das, doch nur wenige ziehen daraus die logische Schlussfolgerung und setzen die menopausale Hormontherapie (MHT) proaktiv zur Frakturprävention ein.
Der Begriff „postmenopausale Osteoporose“ wurde in den 1940er-Jahren geprägt, nachdem der kausale Zusammenhang zwischen Östrogenmangel und Osteoporose aufgedeckt und der osteoprotektive Effekt der Östrogentherapie in mehreren Studien nachgewiesen worden war.1–3 Damals war die Östrogentherapie die einzig wirksame medikamentöse Behandlung der Osteoporose.
Seitdem wurde in einer Vielzahl von Beobachtungsstudien, randomisierten, placebontrollierten Studien und Metaanalysen die signifikante Reduktion von Fragilitätsfrakturen durch Östrogene und Östrogen-Progestogen-Kombinationen bestätigt. Auch im Vergleich mit knochenspezifischen antiresorptiven Medikamenten schneidet die MHT, die das Risiko um circa 30% reduziert, sehr gut ab.4
Die Ergebnisse sämtlicher Studien zu Osteoporose und MHT wurden in die Empfehlungen aller relevanten wissenschaftlichen Gesellschaften aufgenommen, z.B. in die aktuellen Whitepapers5–6 und die neuen Empfehlungen zur MHT der International Menopause Society.7
Während der Adoleszenz und im Erwachsenenalter steuern Östrogene die Auf- und Umbauprozesse der Knochen („modeling“ und „remodeling“). Bis zur Menopause besteht in der Regel eine Homöostase von Knochenresorption und -formation, danach überwiegt wegen der niedrigen Östrogenspiegel die Resorption und führt bereits in den späten peri- und frühen postmenopausalen Jahren zu einem erhöhten Frakturrisiko.8
Fragilitätsfrakturen: Epidemiologie und Kosten
Die Häufigkeit von Fragilitätsfrakturen variiert je nach Alter und Lokalisation: Distale Unterarmfrakturen (Radius- oder Handgelenksfrakturen) treten meist schon in der frühen Postmenopause (PMP) – vor dem 65. Lebensjahr – auf, während die Zahl der Wirbelkörper- und proximalen Oberschenkelfrakturen (Hüftfrakturen) in der späten PMP, mit dem Alter zunehmend, ansteigt.9
Wie wichtig Östrogene für die Frakturprävention sind, führen uns die epidemiologischen Daten eindrücklich vor Augen. In Europa ist bei den über 50-Jährigen die Zahl der an Osteoporose erkrankten Frauen viermal so hoch wie die der Männer (25,5 vs. 6,5 Millionen).10
Jede dritte Frau und jeder fünfte Mann erleidet eine durch Osteoporose verursachte Fraktur. Zusätzlich zu den – teils schwerwiegenden – gesundheitlichen Folgen für die betroffenen Patient:innen entsteht dadurch ein enormer volkswirtschaftlichen Schaden.
Hüftfrakturen spielen dabei die wichtigste Rolle, denn sie müssen im Gegensatz zu anderen Fragilitätsfrakturen, wie Wirbelkörper- oder Unterarmfrakturen, praktisch immer stationär versorgt werden und sind deshalb statistisch und ökonomisch der am besten geeignete Indikator.
Mit einer Inzidenz von 501 Hüftfrakturen/100000 Frauen und 264/100000 Männern liegt Österreich im Spitzenfeld11 und ist im europäischen Vergleich Spitzenreiter in Bezug auf die Kosten für die Akutversorgung dieser Frakturen.12
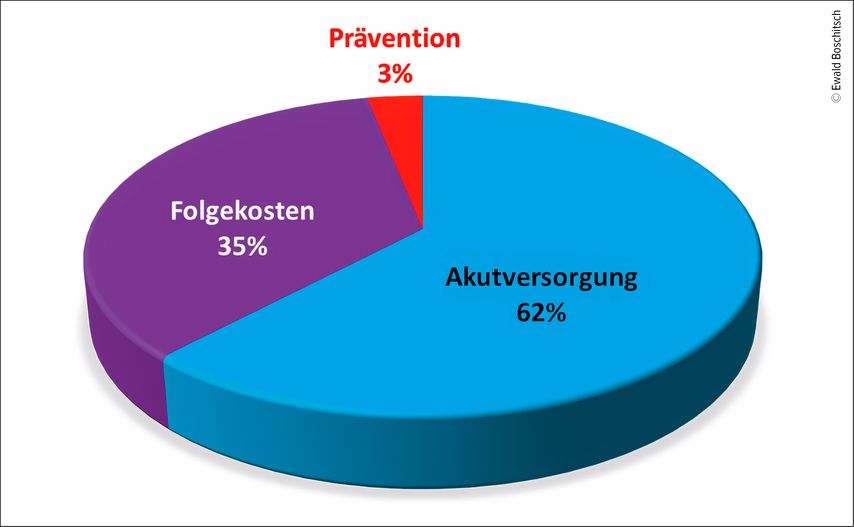
Die direkten Kosten der Osteoporose haben in Österreich im Jahr 2019 1,34 Milliarden Euro betragen (und werden derzeit auf etwa 1,5 Milliarden Euro geschätzt). Davon entfielen im ersten Jahr nach der Fraktur 833,5 Millionen Euro (62%) auf die medizinische Akutversorgung, hauptsächlich die stationäre Versorgung von Hüftfrakturen, und 468,1 Mio. Euro (35%) auf die Folgekosten durch Langzeitbehinderung, hauptsächlich die Betreuung in Pflegeheimen. Nur 41,7 Mio. Euro (3%) wurden für die Frakturprävention, hauptsächlich die pharmakologische Therapie, inklusive Therapiemonitoring, aufgewendet (Abb. 1).13
Die extrem hohen und immer schneller ansteigenden Beträge für Akutversorgung und Langzeitbehinderung sind jedoch nur der direkte Kostenanteil. Dazu kommen indirekte Kosten, die wegen der frakturbedingten verlorenen gesunden Lebensjahre entstehen. Diese „lost quality-adjusted life years (QALYs)“ haben 2019 in Österreich drei Viertel (4,1 Milliarden Euro) der Gesamtkosten von 5,5 Milliarden Euro ausgemacht.10
Heute, im Jahr 2026, kann man von etwa 6 Milliarden Euro Gesamtkosten ausgehen; Kosten, die großteils eingespart werden könnten, weil sie durch vermeidbare Frakturen verursacht werden.
Frakturprävention
Wie es gelingen kann, effektiv Frakturen zu vermeiden, zeigt das Wiener Ambulatorium für Klimakterium und Osteoporose (KLIMAX). Dort wurde die Translation der gynäko-endokrinologischen und osteologischen Kompetenz in die ambulante Betreuung der Patient:innen tagtäglich praktiziert und das Interesse der Zuweiser:innen an der Osteoporose durch begleitende interaktive Fortbildungsveranstaltungen und Publikationen der Daten gefördert.
Im Zeitraum 1990 bis 2011 konnten Patient:innen mittels Überweisung auf Kassenkosten betreut werden. Der Zugang der Bevölkerung zu qualitativ hochwertiger Behandlung war also wesentlich leichter als heute.
Die Daten einer für den Wiener Raum repräsentativen Zahl an Patient:innen zeigen, dass die ambulatorische Betreuung zu bedeutenden Verbesserungen in den Bereichen Diagnostik, Therapie und Prävention führt.9,14–15 Der gezielte Einsatz von MHT-Regimen war auch, mit dem bekannten Verzögerungseffekt, an der zwischen 2005 und 2018 signifikanten österreichweiten Reduktion der Hüftfrakturinzidenz bei Frauen zu beobachten.11 Bei Männern war keine Reduktion der Zahl an Hüftfrakturen festzustellen.
Die von Patient:innen und Zuwei-ser:innen gleichermaßen geschätzten Erfolge wurden von den Kassen nicht honoriert – weder im wertschätzenden noch im wirtschaftlichen Sinn. Im Gegenteil, die Kassen haben 2011 die Honorierung der evidenzbasierten Betreuung von Patient:-innen mit Osteoporose gestoppt und dafür „gewichtige Argumente“ ins Treffen geführt, wie: Es würde Frakturprävention betrieben, für Prävention sei man nicht zuständig und es sei zu teuer (Akutversorgung undFolgekosten vs. Prävention: 97% vs. 3%).
Knochendichtemessung und falsche Therapieentscheidungen
Zufällig zur gleichen Zeit dieses „kassenpolitischen Paradoxons“ übernahmen die Kassen die Honorierung einer einzelnen Untersuchung, der Knochendichtemessung („bone mineral density“; BMD), bei Radiologen und schufen damit ein weiteres Paradoxon. Denn das geschah ausgerechnet, als BMD-Messungen an Bedeutung verloren; generell in der Diagnostik, weil die Aussagekraft Risikofaktoren-basierter Algorithmen und gezielter Labordiagnostik auch ohne BMD deutlich gestiegen war, und besonders im Therapie-Monitoring, wo das Labor den aktuellen Zustand des Knochenstoffwechsels als Spiegel des Therapieerfolges viel genauer und früher abbildet und notwendige Konsequenzen, wie Modifikationen der Therapie, rechtzeitig signalisiert. BMD-Messungen werden deshalb wesentlich seltener empfohlen.
Die jetzige, in der Praxis völlig unkontrollierte Handhabung der BMD-Messungen – ohne Qualitätskontrolle, oft nicht indiziert, noch öfter falsch interpretiert – hat diese wertvolle Untersuchung zu einer inflationären Alibihandlung degradiert und das weitere Management offengelassen oder den damit häufig überforderten niedergelassenen Hausärzten aufgebürdet.
Diese werden allzu oft durch die von den Kassen forcierte Einengung der Diagnose auf Knochendichtewerte zu falschen Therapieentscheidungen verleitet. Die Folge dieser obsoleten Vorgangsweise – Therapieentscheidungen dürfen niemals allein aufgrund der Resultate von Knochendichtemessungen (T-Scores) getroffen werden – ist, dass zwischen 52% („treatment gap“)13 und 75% aller Patient:innen16 keine medikamentöse Therapie erhalten, obwohl sie diese benötigen, und dass etwa zwei Drittel der Patient:innen, die Medikamente für Osteoporose erhalten, diese nicht benötigen.17
Der Großteil der Fragilitätsfrakturen tritt bei osteopenischer (T-Werte –1 bis –2,4) oder normaler BMD auf, und nicht erst, wie oft fälschlich angenommen wird, bei osteoporotischer BMD (T-Wert ≥–2,5). Das ist spätestens seit 2004 bekannt, als in der Studie National Osteoporosis Risk Assessment (NORA) bei 150000 postmenopausalen Frauen in den USA die Inzidenz und Lokalisation von Fragilitätsfrakturen in dem auf eine (periphere) BMD-Messung folgenden Jahr erfasst wurden.18
Studienziel war der Versuch, Schwellenwerte für die pharmakologische Intervention zur Frakturprävention festzulegen. Doch die entscheidende aus den Resultaten gezogene Schlussfolgerung war, dass eine niedrige BMD allein nicht zur Identifikation von Patientinnen mit erhöhtem Frakturrisiko geeignet ist und andere Risikofaktoren in Strategien zur Prävention inkorporiert werden müssen. Wenn man den Schwellenwert bei einem T-Wert von –2,5 ansetzt (nur 6,4% hatten T-Werte von ≥–2,5), würde man nur 18% der Patientinnen, die eine typische osteoporotische Fraktur, und nur 26%, die eine Hüftfraktur erleiden, behandeln.
Das ist eine der Ursachen für die hohe Zahl falscher Therapieentscheidungen und ihre leidvollen und negativen ökonomischen Folgen.
Die Rolle der Gynäkolog:innen
Ein Weg aus dieser irrationalen und kostspieligen Irrfahrt könnte unter gynäkologischer Navigation erfolgreich beschritten werden, denn der Schlüssel eines erfolgreichen Osteoporosemanagements liegt in der möglichst frühen Identifikation von Risikopatientinnen. Rechtzeitig bedeutet peri- oder möglichst früh postmenopausal!
Genau dann beginnt die postmenopausale Osteoporose, verursacht durch die nachlassende osteoprotektive Funktion der Sexualhormone. Auch zahlreiche andere Risikofaktoren sind bereits präsent und können mit Risikokalkulatoren wie FRAXTM standardisiert bewertet werden.
Vor allem aber, und das ist das wichtigste Argument für frühe diagnostische Interventionen, ist die oft vergessene Tatsache, dass auch der Großteil der Fragilitätsfrakturen bereits in diesem Lebensabschnitt, in der Peri- und frühen PMP, d.h. bis zum 65. Lebensjahr, auftritt.
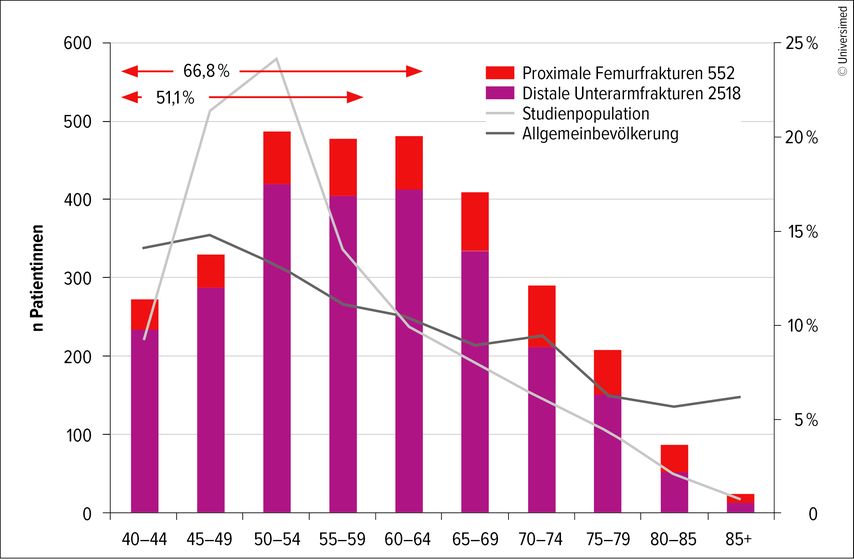
In einer KLIMAX-Studie wurde zwischen 1990 und 2012 bei 99399 Frauen im Alter von ≥40 Jahren (Durchschnittsalter 56,1 Jahre) nicht nur die (zentrale) BMD, sondern auch die altersbezogene Prävalenz von Hüft- und distalen Unterarmfrakturen erfasst: Bei den von niedergelassenen Ärzt:innen zur BMD-Messung überwiesenen Patientinnen waren 66,8% der Frauen mit Fragilitätsfrakturen jünger als 65 Jahre und 51,1 % jünger als 60 Jahre (Abb.2).9
Abb. 2: Altersbezogene Prävalenz von Hüft- und distalen Unterarmfrakturen (modifiziert nach Boschitsch E et al.)9
Zu bemerken ist dabei, dass Frauen mit anamnestisch detektierten Risikofaktoren zu Recht häufiger überwiesen wurden als Frauen ohne erkennbar erhöhtes Risiko und dass, ähnlich wie beim kardiovaskulären Risiko, klimakterische Beschwerden – ein weiterer Überweisungsgrund – wahrscheinlich per se ein erhöhtes Risiko darstellen können. Beides führte zu einer überdurchschnittlich hohen Zahl an Frauen zwischen dem 45. und 60. Lebensjahr in der Studienpopulation gegenüber der Altersverteilung in der weiblichen Allgemeinbevölkerung.
Distale Unterarmfrakturen dominierten in diesem Lebensabschnitt noch deutlich stärker als in fortgeschrittenem Alter über Hüftfrakturen. Wirbelkörperfrakturen, die häufigsten Fragilitätsfrakturen, wurden in dieser Studie nicht berücksichtigt, weil nicht bei allen Frauen Röntgenbefunde der gesamten Wirbelsäule und kaum Beurteilungen mit Genant-Graduierungen19 verfügbar waren; damit konnten morphometrische Frakturen nicht diagnostiziert werden.20
Gynäkolog:innen kommt eine zentrale Rolle im Management der Osteoporose zu, weil sie es sind, die in den Wechseljahren, primär konsultiert werden. Sie sehen Frauen in der für die Frakturprävention entscheidenden Zeit, denn in der Peri- und der frühen PMP tritt der Großteil der Fragilitätsfrakturen auf. Besonders häufig sind distale Unterarmfrakturen. Sie sind keinesfalls als Bagatellfrakturen einzustufen, sondern ein Warnzeichen, das auf ein hohes Risiko für zukünftige Frakturen hinweist.21–22
Die Wechseljahre sind auch der richtige Zeitraum, um bei erhöhtem Risiko therapeutische Interventionen zu empfehlen: Krafttraining, Protein- und kalziumreiche Ernährung, Vitamin-D-Substitution und die MHT haben in dieser Phase Vorrang. Meist erst 15–20 Jahre später können knochenspezifische, antiresorptive oder anabole Substanzen notwendig sein.14–15
Menopausale Hormontherapie (MHT)
Die MHT soll Frauen mit erhöhtem Frakturrisiko innerhalb der ersten 10 postmenopausalen Jahre (oder bis zum 60. Lebensjahr nach Uterusexstirpation) als präventive Maßnahme der ersten Wahl angeboten werden. Bei Frauen mit prämaturer Ovarialinsuffizienz (POI) (<40 Jahre) oder Klimakterium praecox (<45 Jahre) soll sie obligatorisch in Form einer Hormonersatztherapie („hormone replacement therapy“; HRT) eingesetzt werden.23
Eine Begrenzung der Anwendungsdauer gibt es nicht, jedoch ist ein engmaschiges Monitoring – in Abständen von nicht mehr als einem Jahr – notwendig, um das aktuelle Nutzen-Risiko-Verhältnis bewerten und notwendige Änderungen durchführen zu können.
Der durch den Östrogenmangel verstärkte Knochenabbau wird durch eine erhöhte Umbaurate („remodeling“) verursacht, wobei die Resorption die Formation überwiegt. Dabei wird vermehrt Knochenmatrix von Osteoklasten abgegraben und nur unzureichend von Osteoblasten wieder aufgebaut.
Osteoklasten und Osteoblasten kommunizieren auf verschiedenen Signalwegen, wie dem Wnt- und dem OPG-RANKL-RANK-Pfad, mit den Osteozyten, welche die zelluläre Grundsubstanz der Knochenmatrix bilden und als übergeordnete Regulatoren des Knochenstoffwechsels fungieren. Östrogene können über diese Signalwege in die Kommunikation eingreifen, indem sie die Umbaurate hemmen und das Gleichgewicht zwischen Knochenresorption und -formation wiederherstellen.
Prinzipiell wirken alle der heute zugelassenen MHT-Regime osteoprotektiv, doch sollen selbstverständlich Kontraindikationen sowie Nebenwirkungen und Partialwirkungen, z.B. auf die Brust und das Herz-Kreislauf-System, immer berücksichtigt werden, wobei v.a. auf die Wahl des Progestogens und des Administrationsweges geachtet werden soll.24–27
Die MHT hat einen nachhaltigen Effekt auf den Knochen: Schon mit zwei bis drei Jahren der Anwendung während der frühen PMP zeigen sich in randomisiert-placebokontrollierten Studien noch bis zu 15 Jahre später signifikant höhere BMD-Werte und niedrigere Frakturraten.28
Auch die durch die MHT verbesserte Mikroarchitektur des Knochens bleibt noch viele Jahre nach Absetzen der Therapie erhalten, wie in einer großen Querschnittsuntersuchung beim Vergleich von ehemaligen mit gegenwärtigen Anwenderinnen und Frauen ohne MHT mittels des in die BMD-Messung integrierten „trabecular bone score“ (TBS) nachgewiesen werden konnte.29
Für die häufigste Form der Osteoporose, die postmenopausale Osteoporose, ist die MHT eine kausale Therapie und sollte die erste Wahl pharmakologischer Interventionen sein.
Die MHT ist gleichzeitig auch eine systemische Therapie, die Auswirkungen auf praktisch alle Organsysteme hat. Da in MHT-Präparaten verschiedene Wirkstoffe und Wirkstoffkombinationen mit verschiedenen Partialwirkungen und potenziellen Nebenwirkungen enthalten sind, soll deren Anwendung auf die individuelle und persönliche Situation und Konstitution der Patientinnen (Risikofaktoren, Komorbiditäten) abgestimmt werden.
Gynäkolog:innen sollen sowohl in der Diagnostik als auch in der Therapie der postmenopausalen Osteoporose proaktiv das Ruder übernehmen. Sie sind in der Reglen die Ersten, die die Patientinnen in dem für die Frakturprävention entscheidenden Zeitraum, der Peri- und frühen PMP, sehen und sie sind durch ihre Ausbildung am besten qualifiziert, die MHT, als Therapie der Wahl in der Primärprävention, durchzuführen.
Was in diesem Lebensabschnitt versäumt wird, ist später schwer oder nicht mehr aufzuholen. Andere antiresorptive Therapien, wie Bisphosphonate oder Denosumab, sind zur Primärprävention meist erst in der späten PMP (ab 60–65 Jahren) sinnvoll – Ausnahmen bestätigen die Regel, z.B. bei Kontraindikationen oder hohem Risiko der MHT. Doch auch dann wäre mehr Engagement von Gynäkolog:innen wünschenswert. Falls kein Interesse an der Osteologie besteht, sollten sie zumindest die Rolle der „Gatekeeper“ wahrnehmen und ihre Patientinnen an eine kompetente Stelle überweisen.
Was die in der Gesundheitspolitik zuständigen Stakeholder, allen voran die Sozialversicherungsträger, nicht schaffen, kann den Gynäkolog:innen gelingen. Sie haben es in der Hand, das durch die Osteoporose in unnötig hohem Ausmaß bestehende Leiden der Frauen zu lindern und damit auch einen wegweisenden Beitrag zur Reduktion der enormen Kosten, die diese Erkrankung verursacht, zu leisten.
Literatur:
1 Albright F et al.: Post-menopausal osteoporosis: its clinical features. JAMA 1941; 116: 2465-74 2 Albright F et al.: Effect of stilbestrol in post-menopausal osteoporosis. Trans Conf Metab Asp Conval 1946; (14): 99-101 3 Reifenstein EC, Albright F: The metabolic effects of steroid hormones in osteoporosis. J Clin Invest 1947; 26: 24-56 4 Kanis JA et al.: European guidance for the diagnosis and management of osteoporosis in postmenopausal women. Osteoporos Int 2013; 24(1): 23-57 5 de Villiers TJ, Goldstein SR: Update on bone health: the International Menopause Society White Paper 2021. Climacteric 2021; 24(5): 498-504 6 Panay N et al.: Menopause and MHT in 2024: addressing the key controversies – an International Menopause Society White Paper. Climacteric 2024; (5): 441-57 7 Panay N et al.: International Menopause Society (IMS) recommendations and key messages on women’s midlife health and menopause. Climacteric 2025; 28(6): 634-56 8 Manolagas SC et al.: The role of estrogen and androgen receptors in bone health and disease. Nat Rev Endocrinol 2013; 9(12): 699-712 9 Boschitsch E et al.: Age-related prevalence of osteoporosis and fragility fractures: real-world data from an Austrian Menopause and Osteoporosis Clinic. Climacteric 2017; 20(2): 157-63 10 Kanis JA al.: SCOPE 2021: a new scorecard for osteoporosis in Europe. Arch Osteoporos 2021; 16(1): 82 11 Dimai HP et al.: Thirty years of hip fracture incidence in Austria: is the worst over? Osteoporos Int 2022; 33(1): 97-104 12 European Parliament Osteoporosis Interest Group: Sekundärprävention osteoporotischer Frakturen: Ein Modellprojekt gefördert aus Mitteln des Hauptverbandes der österreichischen Soziaversicherungsträger, 2007 13 Willers C et al.: Osteoporosis in Europe: a compendium of country-specific reports. Arch Osteoporos 2022; 17(1): 23 14 Boschitsch E: For how long should osteoporosis treatment continue? Climacteric 2015; 18(5): 675-7 15 Boschitsch E et al.: Long-term persistence with denosumab: real-world data from the Austrian Osteoporosis Clinic (AOC). A retrospective data analysis. Osteoporos Int 2022; 33(1): 263-72 16 Thun M: Zeitgemäße Therapie der Osteoporose. Vortrag KLIMAX-Fortbildung 2015 17 Fenton JJ et al.: Osteoporosis overtreatment in a regional health care system. JAMA Intern Med 2016; 176(3): 391-3 18 Siris ES et al.: Bone mineral density thresholds for pharmacological intervention to prevent fractures. Arch Intern Med 2004; 164(10): 1108-12 19 Genant HK et al.: Vertebral fracture assessment using a semiquantitative technique. J Bone Miner Res 1993; 8(9): 1137-48 20 Boschitsch E: State of the Art: Wann und wie oft messen wir die Knochendichte? J Clin Endocrinol Metabol 2013; 6(3) 21 Seyok T et al.: Future fracture risk in upper extremity fracture and non-fracture patients. Hand (N Y) 2023; 18(7): 1095-101 22 Kanis JA et al.: Characteristics of recurrent fractures. Osteoporos Int 2018; 29(8): 1747-57 23 Maas AHEM et al.: Cardiovascular health after menopause transition, pregnancy disorders, and other gynaecologic conditions: a consensus document from European cardiologists, gynaecologists, and endocrinologists. Eur Heart J 2021; 42(10): 967-84 24 Levy B, Simon JA: A contemporary view of menopausal hormone therapy. Obstet Gynecol 2024; 144(1): 12-23 25 Trémollieres FA et al.: Management of postmenopausal women. Clinical Practice Guidelines. Maturitas 2022; 163: 62-81 26 Jiang X, Kagan R: Hormone therapy for postmenopausal osteoporosis management. Climacteric 2022; 25(1): 50-5 27 Gosset A et al.: Menopausal hormone therapy for the management of osteoporosis. Best Pract Res Clin Endocrinol Metab 2021; 35(6): 101551 28 Bagger YZ et al.: Two to three years of hormone replacement treatment in healthy women have long-term preventive effects on bone mass and osteoporotic fractures: the PERF study. Bone 2004; 34(4): 728-35 29 Papadakis G et al.: The Benefit of menopausal hormone therapy on bone density and microarchitecture persists after its withdrawal. J Clin Endocrinol Metab 2016; 101(12): 5004-11
Das könnte Sie auch interessieren:
„To MESH or not to MESH“?
Das sind die Titelworte eines Themenabschlussvortrags, mit denen sich Ende Jänner 2026, zum vierten Mal in den Tiroler Alpen und Innsbrucks ehrwürdigem Anatomie-gebäude, zwischen ...
Ethische Überlegungen zur Reproduktion am Beispiel der Uterustransplantation
In der Entwicklung der Reproduktionsmedizin gibt es neue Verfahren und Methoden, die, wie die Uterustransplantation, möglicherweise schon auf dem Weg in die klinische Routine sind. Das ...
Von der Rolle des Mikrobioms bis zur Umsetzung der Vakzinierungsprogramme
Im Rahmen des diesjährigen EUROGIN-Kongresses wurde ein Fazit über 20 Jahre HPV-Impfung gezogen und ausführlich über die Implementierung von Screeningmaßnahmen und ...