Varizella-zoster-Meningitis unter JAK-Inhibitor-Therapie bei Morbus Crohn
Autorin:
OÄ Dr. Karin Steidl
Abteilung für Innere Medizin
Krankenhaus der Barmherzigen Brüder
St. Veit an der Glan
E-Mail: karin.steidl@bbstveit.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei Patient:innen mit einer chronisch-entzündlichen Darmerkrankung (CED) besteht ein höheres Risiko für eine Herpes-zoster-Infektion – insbesondere unter JAK-Inhibitor-Therapie. In diesem Beitrag wird ein Patient:innenfall aus dem klinischen Alltag vorgestellt.
Keypoints
-
CED-Patient:innen haben ein 2-fach erhöhtes Risiko für Herpes-zoster-Infektionen, v.a. unter JAK-Inhibitor-Therapie.
-
Da der Krankheitsverlauf aufgrund der Immunsuppression schwerer ist, wird die Impfung vor/während der Therapie empfohlen. Sie ist unter JAK-Inhibitor-Therapie erstattungsfähig.
-
Wichtig vor Therapiebeginn: Aufklärung der Patient:innen bzgl. des Auftretens von Bläschen am Körper und der Notwendigkeit des Beginn einer antiviralen Therapie innerhalb von 72 Stunden.
-
Risikofaktoren für einen schweren Verlauf sind höheres Alter und Nichtanwendung der antiviralen Therapie.
Anamnese und Erstvorstellung
Eine 26-jährige Patientin mit Morbus Crohnwurde am 15.10.2020 erstmals in der CED-Ambulanz vorstellig. Status zum Zeitpunkt der Erstvorstellung: 4x täglich Stuhlgang, keine pathologischen Beimengungen, leichte Bauchschmerzen. Das Gewicht betrug 53kg.
Vorerkrankungen
Die Erstdiagnose eines Morbus Crohn mit kolitischem Befallsmuster wurde 2009 gestellt. Zusätzlich bestanden eine entzündliche Rektumstenose mit analer Inkontinenz sowie eine extraintestinale Begleitsymptomatik (Erythema nodosum) und eine Mitbeteiligung des oberen Gastrointestinaltrakts bei Morbus Crohn und einem anhaltenden chronischen Schubgeschehen sowie ein Z.n. periproktitischem Abszess. Die Nikotinanamnese war negativ. Als Begleiterkrankungen wurden Asthma bronchiale, Z.n. Covid-19-Infektion und Z.n. Appendektomie dokumentiert. Die Familienanamnese ist hinsichtlich chronisch-entzündlicher Darmerkankungen negativ.
Therapieverlauf
Seit August 2019 stand die Patientin unter Therapie mit Infliximab, mit einer Dosierung von 5mg/kg/KG zum Zeitpunkt der Erstvorstellung und einem verkürzten Infusionsintervall von 6 Wochen. Eine gastrointestinale Reevaluierung erfolgte im April 2021, wo sich eine entzündliche Aktivität im Rektum und die entzündliche Rektumstenose zeigten. Eine Ballondilatation wurde abgelehnt. Die Umstellung auf Ustekinumab wurde von der Patientin ebenfalls abgelehnt. Aufgrund des fehlenden Langzeitansprechens wurde Infliximab im Mai 2022 abgesetzt.
Die Umstellung auf Ustekinumab erfolgte im Juni 2022, i.v. Erstgabe mit 260mg. Aufgrund der klinischen Beschwerdesymptomatik und anhaltender Calprotectinerhöhung wurde weiterführend Ustekinumab 90mg s.c. alle 4 Wochen appliziert. Aufgrund eines Schubgeschehens erfolgte eine gastrointestinale Reevaluierung im November 2022, bei der sich koloskopisch eine ausgeprägte, hochgradig aktive linksseitige Kolitis bis 40cm ab ano mit länglichen Ulzerationen und die bekannte distale Rektumstenose zeigten. Die Gastroskopie war unauffällig. Es erfolgte die Einleitung einer Kortisonstoßtherapie, Ustekinumab wurde aufgrund des primären Therapieversagens im Oktober 2022 abgesetzt.
Da es zwischenzeitlich wieder zum Auftreten von Erythema-nodosum-artigen Hautveränderungen an der unteren Extremität beidseits gekommen war, erfolgte die Einleitung einer Adalimumab-Therapie mit Induktion 160/80mg, danach 40mg s.c. alle 2 Wochen.Trotz Intervallverkürzung auf eine 10-tägige Gabe, Reinduktion mit Adalimumab 80mg s.c. und nachfolgend verkürztem Verabreichungsintervall mit Adalimumab 40mg s.c. einmal wöchentlich kam es im Dezember 2023 zu einem neuerlichen Schubgeschehen. Die Therapie mit Kortison wurde initial von der Patientin abgelehnt, im weiteren Verlauf jedoch aufgrund der Aggravierung der klinischen Beschwerdesymptomatik eingeleitet. In weiterer Folge wurde Adalimumab im Mai 2024 bei sekundärem Wirkverlust abgesetzt.
Einleitung einer Therapie mit dem JAK-Inhibitor Upadacitinib
Aufgrund des fehlenden Ansprechens auf Infliximab, Ustekinumab, Adalimumab und des anhaltenden chronischen Schubgeschehens wurde im Mai 2024 eine Therapie mit Upadacitinib eingeleitet.
Es erfolgte die Induktion mit Upadacitinib45mg einmal täglich per os und nachfolgendUpadacitinib 30mg per os ab Juli 2024. Hierunter kam es zu einer Besserung des Stuhlverhaltens und der Stuhlfrequenz, der Calprotectinwert zeigte sich ebenfalls rückläufig.
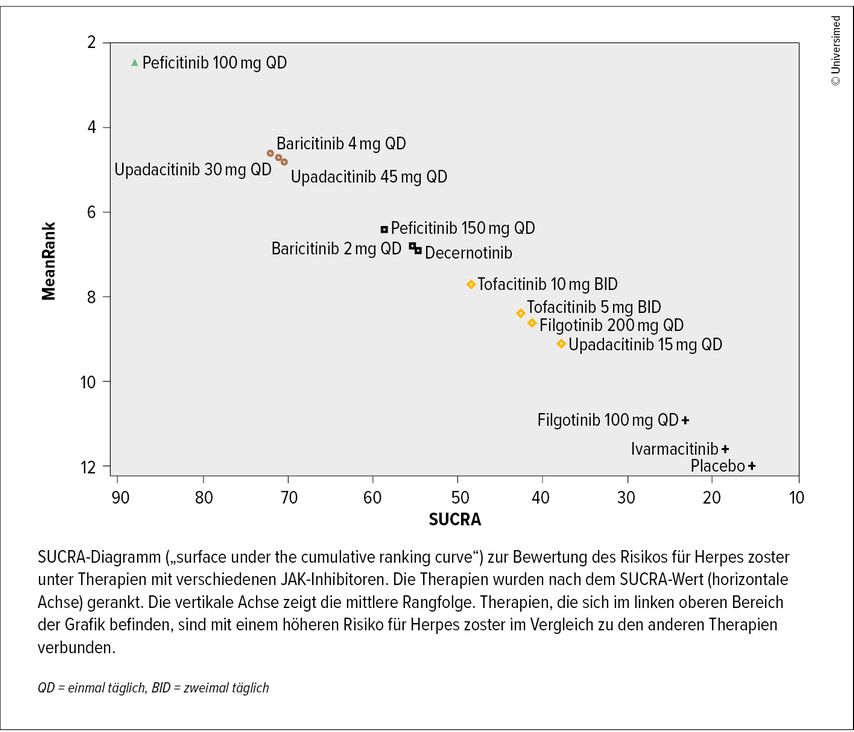
Vor Therapiebeginn wurde mit der Patientin mehrmals eingehend die Notwendigkeit einer Herpes-zoster-Impfung (Shingrix) besprochen, da unter der JAK-Inhibitor-Therapie mit Upadacitinib ein erhöhtes Risiko für das Auftreten einer Herpes-zoster-Infektion besteht (Abb.1). Leider ließ sich die Patientin trotz mehrmaliger Aufforderung nicht impfen.
Abb. 1: Risiko für Herpes zoster im Zusammenhang mit JAK-Inhibitoren bei autoimmunvermittelten entzündlichen Erkrankungen (modifiziert nach Quingling X et al. 2023)
Weiterer Verlauf
Es folgte die Vorstellung auf der Neurologie mit stationärem Aufenthalt im September 2024 aufgrund von Nackenschmerzen beim Beugen nach vorne (kein Meningismus), zudem Kopfschmerzen, Schmerzen in der LWS und starkes Kribbeln im rechten Bein. Es zeigten sich keine fokalen neurologischen Defizite, das Schädel-CT war unauffällig. In der Lumbalpunktion konnte eine lymphozytäre Pleozytose (Zellzahl 40/μl) nachgewiesen werden, die Varizella-zoster-PCR fiel positiv aus.
Somit wurde die Diagnose einer Varizella-zoster-Meningitis und Varizella-zoster-Radikulitis im Bereich L3/L4 unter Therapie mit Upadacitinib gestellt. Als Therapie wurde körpergewichtsadaptiert Aciclovir für 14 Tage verabreicht. Upadacitinib wurde im September 2024 abgesetzt. Eine Shingrix-Impfung wurde der Patientin neuerlich dringendst empfohlen.
Kurze Zeit später im Oktober 2024 erfolgten eine neuerliche neurologische Vorstellung und stationäre Aufnahme bei ausgeprägten Bein- und Hüftschmerzen. Im MR des Schädels und in der gesamten Wirbelsäule war kein entzündliches Geschehen nachweisbar. Die prolongierte Schmerzsymptomatik war im Rahmen der vorhergegangenen Varizella-zoster-Meningitis zu sehen.
Kontrolle in der CED-Sprechstunde
Bei der Kontrolle im Oktober 2024 wurde sonografisch und laborchemisch ein aktiver Morbus Crohn nachgewiesen, worauf aufgrund der multiplen Vortherapien und der vorhergegangenen Varizella-zoster-Meningitis unter Upadacitinib ohne zuvor erfolgte Shingrix-Impfung die Einleitung der Therapie mit Risankizumab 600mg i.v. erfolgte. Zwischenzeitlich kam es auch zum Wiederauftreten von Erythema-nodosum-artigen Hautveränderungen. Die Induktion von Risankizumab wurde abgeschlossen.
Vorstellung in der CED-Ambulanz zur geplanten Erstgabe von Risankizumab 360mg s.c.
Im Jänner 2025 klagte die Patientin über Kopfschmerzen, Müdigkeit, Schwäche und Bläschenbildung links axillär im Bereich von TH2–TH4 sowie brennende Schmerzen, worauf neuerlich eine umgehende neurologische Vorstellung folgte. Mittels Liquorpunktion wurde eine neuerliche Varizella-zoster-Meningitis ausgeschlossen.
Ergänzende dermatologische Vorstellung
Klinisch zeigten sich nicht gruppierte Papeln im Bereich der linken Axilla bis an die linke laterale Brustwand bis zum unteren Rippenbogen reichend, Pseudovesikel und eine scharf begrenzte erythematöse Plaque links axillär. Mittels Abstrich erfolgte eine bakterielle Kulturanlage und eine Varizella-zoster-PCR wurde ebenfalls durchgeführt. Die Patientin erhielt eine prophylaktische Gabe von Aciclovir 500mg i.v. Die Varizella-zoster-PCR fiel negativ aus, der Keimabstrich ergab den Nachweis von Staphylococcus aureus, woraufhin die Diagnose einer Ostiofollikulitis Bockhard gestellt und eine antibiotische Therapie mit Ospexin eingeleitet wurde.
Nochmals wurde der Patientin eine Shingrix-Impfung empfohlen, worauf diese im weiteren Verlauf schlussendlich durchgeführt wurde. Die Erstgabe von Risankizumab 360mg s.c. erfolgte am 6.2.2025.
Literatur:
● Quingling X et al.: Risk of herpes zoster associated with JAK inhibitors in immune-mediated inflammatory diseases: a systematic review and network meta-analysis. Front Pharmacol 2023; 8(14): 1241954 ● Schreiner P et al.: Varicella zoster virus in inflammatory bowel disease patients: what every gastroenterologist should know. J Crohn‘s Colitis 2021; 15(2): jjaa132 ● Shingrix Fachinformation
Das könnte Sie auch interessieren:
Neuroimmunologische Aspekte bei chronisch-entzündlichen Darmerkrankungen
Psychische Belastungssituationen und chronisch-entzündliche Darmerkrankungen sind untrennbar miteinander verbunden, wobei Ursache und Wirkung oft schwer auseinanderzuhalten sind. Die ...
Fallbeispiel: retrograde cricopharyngeale Dysfunktion (R-CPD)
Ein 24-jähriger männlicher Patient stellte sich mit einer Unfähigkeit zu rülpsen sowie ausgeprägtem Meteorismus und anhaltendem abdominellem Spannungsgefühl vor. Die Symptomatik bestand ...
Optimierte Ursachenforschung bei chronischer Diarrhö
Die chronische Diarrhö ist ein Symptom verschiedener Erkrankungen. Wie nach dem Auslöser bestmöglich gesucht wird, erklärte Prof. Dr. Alain Schoepfer, Lausanne, auf dem Jahreskongress ...