Altbewährtes und Neues bei chronisch-entzündlichen Darmerkrankungen
Autor:
Dr. Michael Schleicher
4. Medizinische Abteilung
Abteilung für Gastroenterologie und Hepatologie mit Ambulanz und Endoskopie
Klinik Ottakring
Wiener Gesundheitsverbund
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Durch die Entwicklung neuer Therapieoptionen und Surveillancestrategien in den letzten Jahrzehnten haben sich auch die Therapieziele in der Behandlung der chronisch-entzündlichen Darmerkrankungen geändert.
Keypoints
-
„Ältere“ Medikamente der Prä-Biologika-Ära sind weiterhin in ausgewählten Fällen als Monotherapie bzw. in höherem Ausmaß als Add-On-Therapie indiziert.
-
Die Palette der wirksamen und sicheren Biologika könnte bald mit den vielversprechenden selektiven Interleukin-23-Blockern erweitert werden.
-
Die äußerst potente Substanzklasse der Small Molecules kann nach entsprechender Risikoevaluierung in Betracht gezogen werden. Ob sich diesbezügliche Sicherheitsbedenken in der Praxis bestätigen, wird sich in den nächsten Jahren zeigen.
Mit der Zulassung der ersten Biologika vor mehr als 20 Jahren kam es zu einem regelrechten Aufschwung neuer und personalisierter Behandlungskonzepte, welche den oftmals reflexartigen Griff zu Glukokortikoiden zunehmend ablösen. Während man sich früher, insbesondere bei schweren Verlaufsformen und mangels ausreichender Therapieoptionen, teilweise mit einer reinen Symptomerleichterung zufriedengeben musste, ist das primäre Therapieziel der mukosalen Heilung, also einer endoskopischen und bioptisch verifizierten entzündungsfreien Schleimhaut, heutzutage greifbarer denn je.
Alte Bekannte
Die am häufigsten bereits begonnenen Therapien vor Zuweisung in eine Spezialambulanz für chronisch-entzündliche Darmerkrankungen sind Antibiotika, Probiotika, 5-Aminosalicylate und/oder Glukokortikoide. Während in seltenen Fällen der zeitlich begrenzte Einsatz von darmgängigen Antibiotika im aktiven Entzündungsschub mit entsprechender Dysbiose oder bei Komplikationen wie Abszessen kurzfristig Abhilfe schaffen kann, können Probiotika entgegen der landläufigen Meinung nur wenig ausrichten. Ausnahmen sind das Probiotikum Escherichia coli Stamm Nissle 1917, welches einen möglichen Stellenwert als Add-on-Therapie in der Schubprophylaxe der Colitis ulcerosa hat,1 und die probiotische Mischung VSL#3, die Wirkung in der Remissionserhaltung bei chronischer Pouchitis zeigt.2,3
Dass 5-Aminosalicylate ihre antiinflammatorische Wirkung auch im Darm entfalten können, wurde zufällig entdeckt, nachdem beobachtet worden war, dass Arthritispatient*innen mit gleichzeitig bestehender Colitis ulcerosa, die im Rahmen ihrer Arthritis Sulfasalazin erhielten, auch eine Besserung der Colitis-spezifischen Symptome erfuhren. Bei Morbus Crohn hat der Einsatz von 5-Aminosalicylaten bei fehlender Wirksamkeit im Dünndarm keinen Stellenwert und sollte Patient*innen mit Colitis ulcerosa bzw. mit kolonischem Befall beiM. Crohn vorbehalten sein.4
Die seit den 1980er-Jahren in Verwendung befindlichen Immunmodulatoren wie Thiopurine und Methotrexat haben im Vergleich zu Biologika einen oftmals verzögerten Wirkeintritt bei nicht zu vernachlässigendem (Langzeit-)Nebenwirkungsprofil (z.B. Pankreatitis, Hepatotoxizität, Myelosuppression, Lymphom, nichtmelanozytärer Hautkrebs).4 Daher ist es auch nicht verwunderlich, dass ihr Einsatz, auch vor dem Hintergrund eines immer größer werdenden Armamentariums an alternativen therapeutischen Optionen, immer seltener wird. In ausgewählten Einzelfällen kann Azathioprin in Kombination mit TNF-Alphablockern bei schweren Verlaufsformen bzw. zur Prävention/Aufhebung eines sekundären Wirkverlustes aufgrund einer Immunogenität bei Bildung von „anti-drug antibodies“sinnvoll sein (wobei man hierbei ein potenziell höheres Nebenwirkungsprofil dieser Kombinationstherapie berücksichtigen muss).5,6
In Anbetracht der erheblichen Langzeitrisiken selbst bei kurzzeitigen Gaben systemischer Glukokortikoide (insbesondere Osteoporose und Diabetes mellitus Typ 2)7 sollte die Indikation hierfür sehr streng gestellt werden. Auch sollte überlegt werden, ob nicht stattdessen, je nach Befallsmuster, das Auslangen mit einem topischen Budesonid gefunden werden kann. Während oftmals die sehr schnell einsetzende Wirkung bei fulminantem Entzündungsschub mit Gefahr in Verzug die wesentliche Begründung einer systemischen Glukokortikoidtherapie ist, könnte ihr Einsatz zukünftig durch die kürzlich zugelassenen und ebenfalls sehr schnell wirksamen Januskinase-Inhibitoren8 zunehmend ersetzt werden (auch weil Letztere im Unterschied zu Glukokortikoiden als Erhaltungstherapie geeignet sind).
Personalisierte Medizin
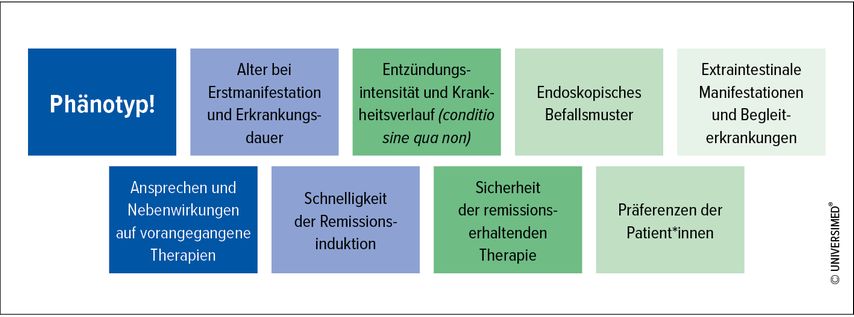
Die stetig wachsende Zahl der uns zur Verfügung stehenden Therapeutika stellt die behandelnden Ärzt*innen auch vor die Herausforderung, das richtige Medikament zum richtigen Zeitpunkt für die richtigen Patient*innen einzusetzen. Nach wie vor gibt es nicht das eine Kochrezept. Vielmehr hängt die Wahl von vielen Faktoren ab, die es zu berücksichtigen gilt, um den äußerst unterschiedlichen Verlaufsformen der Erkrankung gerecht zu werden (Abb.1).
Abb. 1: Entscheidungshilfen zur Therapiefindung bei chronisch-entzündlichen Darmerkrankungen (modifiziert nach Schleicher M 2023)
Zu Beginn ist es ratsam, den Phänotypen und prädiktive Risikofaktoren, wie z.B. Alter (bei Erstmanifestation), Befallsmuster, extraintestinale Manifestationen, Notwendigkeit und Dauer einer Glukokortikoidtherapie, Raucheranamnese, Komorbiditäten, Dringlichkeit einer Remissionsinduktion, aber auch die Präferenzen der Patien-t*innen zu bestimmen. Dieser präzisionsmedizinische Ansatz ermöglicht uns, sowohl eine Unter- als auch eine Übertherapie zu vermeiden.
Strategiewechsel
Der früher oftmals zögerliche Beginn mit Substanzen mit niedriger Wirksamkeit und stufenweiser Therapieeskalation bis zum Erlangen eines Ansprechens (Step-up-Regime) beruhte vor allem auf Sicherheitsbedenken bezüglich etwaiger Langzeitnebenwirkungen der neuartigen Therapien. Um jedoch ein Verschleppen der entzündlichen Aktivität und hierdurch konsekutiv Komplikationen zu vermeiden, empfiehlt es sich bei entsprechendem Phänotyp mit voraussichtlich moderater bis schwerer Verlaufsform, gleich zu Beginn eine potente Substanzklasse zu wählen. Mit nunmehr umfangreicher Evidenz inklusive Real-World-Daten konnte gezeigt werden, dass auch die langfristige Verwendung von Biologika zu keinem signifikant erhöhten Krebsrisiko führt.9–11
Regelmäßige Kontrollen unter Heranziehung multimodaler Surrogatmarker der Entzündungsaktivität erlauben eine frühe Erfassung gesteigerter Krankheitsaktivität selbst bei fehlender Symptomatik. Die Indikation zur Therapieausschöpfung und Eskalation sollte hierbei möglichst großzügig gestellt werden, um den Verlauf der Erkrankung möglichst frühzeitig günstig zu modifizieren und langfristige Komplikationen zu vermeiden.12,13
Das Credo des „hit early and hit hard“ hat sich in den letzten Jahren zunehmend durchgesetzt. Somit empfiehlt sich ein frühzeitiger Einsatz der langjährigbewährten Biologika: TNF-Alphablocker(Infliximab, Adalimumab, Golimumab), Anti-Integrin (Vedolizumab) und Interleukin-12/23-Blocker (Ustekinumab). Darüber hinaus zeigt sich in neuesten Studienergebnissen eine signifikante Wirkung von Vedolizumab bei Patient*innen mit chronischer Pouchitis nach ileopouch-analer Anastomose.14 Somit steht nun auch dieser sonst sehr schwer zu therapierendenPatient*innengruppe eine wirksame Option zur Verfügung.
Neben den gängigen Kontrolluntersuchungen wie CRP, fäkales Calprotektin, Endoskopie und MRT-Enterografie findet in den letzten Jahren der Darmultraschall zunehmend Anwendung. Er kann als einfache, schnelle und nichtinvasive Methode die Entzündungsaktivität darstellen und ist in der Lage, eine Abnahme der entzündlichen Darmwanddicke bereits ab 2 Wochen nach Beginn einer schnell wirkenden Therapie zu erfassen.15 Hierdurch ergibt sich eine prädiktive Qualität des Darmultraschalls, die man in weitere Therapieentscheidungen miteinfließen lassen kann.
„Small molecules“ – Einleitung einer neuen Ära?
Mit einer Molekülgröße, die klein genug für eine enterale Resorption ist, hat die Substanzklasse der Januskinase-Inhibitoren die Palette um dringlich benötigte, gut wirksame perorale Alternativen erweitert. 2018 erhielt Tofacitinib als erster Vertreter die Zulassung für die moderate bis schwere Colitis ulcerosa,16 und die vielversprechenden Daten der Zulassungsstudie konnten im Real-World-Setting bestätigt werden. Selbst Patient*innen, die bislang als „austherapiert“ galten, konnte man hiermit noch eine wirksame Möglichkeit anbieten, und anders als bei TNF-Alphablockern scheint die Zahl der vorangegangenen Biologika-Therapien nicht so sehr ins Gewicht zu fallen. Vorteilhaft wirken sich die fehlende Immunogenität und die kurze Halbwertszeit aus, die ein problemloses Pausieren während Infekten ermöglichen.
Leider gab es in Studien für die rheumatoide Arthritis bei älteren Patient*innen mit kardiovaskulären Vorerkrankungen Sicherheitssignale hinsichtlich thromboembolischer und kardiovaskulärer Ereignisse.17 Diese konnten in den Zulassungsstudien für die nachfolgenden Vertreter, Filgotinib18 und Upadacitinib19,nicht reproduziert werden, was möglicherweise deren präferenziell-selektiver JAK-1-Blockade geschuldet ist. Dennoch kam die Europäische Arzneimittelagentur (EMA) zum Schluss, dass die entsprechenden Risiken auf alle Januskinase-Inhibitoren zutreffen.20 Somit sollte bei entsprechenden Risikofaktoren (z.B. höheres Alter, kardiovaskuläre Vorerkrankungen, Rauchkonsum und Malignome in der Anamnese) jedenfalls Vorsicht geboten sein und potenzielle Alternativen sollten noch ausgeschöpft werden. Um dem erhöhten Risiko für einen Herpes Zoster unter Januskinase-Inhibition prophylaktisch entgegenzuwirken, ist eine Impfung mit dem Totimpfstoff Shingrix empfohlen. Frauen im gebärfähigen Alter sollten im Falle mangelnder Therapiealternativen jedenfalls über eine mögliche teratogene Wirkung (im Tierversuch) aufgeklärt werden und unbedingt eine Verhütung einhalten.
Eine weitere Gruppe der „small molecules“ sind die Sphingosin-1-Phosphat-Rezeptormodulatoren, die in der Neurologie für die Behandlung der multiplen Sklerose bereits seit vielen Jahren erfolgreich eingesetzt werden. Der erste für die Colitis ulcerosa zugelassene Vertreter, Ozanimod,21 ist allerdings in Österreich in der „No Box“ und somit nur nach außerordentlicher Begründung erstattbar. Hierbei sind entsprechende Nebenwirkungen, Kontraindikationen und die EKG-Überwachung bei Induktion zu beachten.
Zukunftshoffnungen
Ustekinumab hat sich in den vergangenen Jahren durch seine Blockade der Zytokine Interleukin12 und Interleukin23 mittels Hemmung der gemeinsamen p40-Untereinheit als eine sehr wirksame und sichere Therapieoption erwiesen.22 Durch Forschungsergebnisse bei anderen chronisch-entzündlichen Erkrankungen, wie z.B. der Psoriasis, konnte jedoch gezeigt werden, dass die antiinflammatorische Wirkung hauptsächlich über die Blockade von Interleukin23 vermittelt wird. Somit wurden mit Risankizumab, Mirikizumab, Guselkumab und Brazikumab Antikörper entwickelt, die eine gezieltere Blockade von Interleukin23 durch Hemmung derzugehörigen p19-Untereinheit ermöglichen.
Anhand bisheriger Studienergebnisse lassen sich exzellente Wirksamkeits- und Sicherheitsprofile voraussagen, sodass einige dieser Vertreter voraussichtlich schon in den nächsten Monaten die Zulassung für die Therapie von Morbus Crohn bzw. Colitis ulcerosa erlangen werden.23
Wohin geht die Reise?
Durch die wachsende Zahl der wirksamen Therapieoptionen muss mehr denn je eine individuelle, für die einzelnen Patient*innen maßgeschneiderte Therapie gefunden werden. Anhand verschiedener Patient*innenmerkmale und Risikofaktoren kann – nach ausführlicher Aufklärung und gemeinsamer Besprechung weiterer Alternativen – das am besten geeignete Medikament eruiert werden. Die Zusammenschau der unterschiedlichen klinischen, laborchemischen und bildgebenden Kontrolluntersuchungen ermöglicht uns eine umfassende Beurteilung der Krankheitsaktivität, nach der sich eine Therapieeskalation bzw. ein Substanzklassenwechsel richten soll.
Hierbei haben „ältere“ Medikamente der Prä-Biologika-Ära in ausgewählten Fällen als Monotherapie bzw. im höheren Ausmaß als Add-on-Therapie weiterhin einen Stellenwert. Allerdings sollte ein zögerliches Herantasten bis zur wirksamen Therapie vermieden werden. Das Verschleppen der Entzündungsaktivität kann zu langfristigen Komplikationen führen, während eine frühe Unterbrechung der entzündlichen Aktivität den Krankheitsverlauf anhaltend günstig beeinflussen kann. Aufgrund der langfristigen Nebenwirkungen von Glukokortikoiden, welche selbst Jahre nach der Verabreichung manifest werden können, ist deren allzu großzügige Verwendung stets kritisch zu hinterfragen.
Derzeit befinden wir uns weiterhin in der Ära der sehr wirksamen und sicheren Biologika, die in naher Zukunft um die sehr vielversprechenden selektiven Interleukin-23-Blocker ergänzt werden. Mit den „small molecules“ kam in jüngster Zeit eine äußerst potente Substanzklasse hinzu, welche man Patient*innen nach entsprechender Risikoevaluierung anbieten kann. Ob sich hierfür die Sicherheitsbedenken in der Real World bestätigen, wird sich in den nächsten Jahren zeigen. Für die Biologika konnte unterdessen anhand von jahrzehntelanger Erfahrung Entwarnung gegeben werden.
Spannend könnten in Zukunft mögliche Kombinationstherapien zweier Immunsuppressiva mit unterschiedlichem Wirkmechanismus sein, insbesondere bei Patient*innen, die trotz mehrerer verschiedener Therapien keine Remission erreichten. Hierfür sind weitere Studien auch hinsichtlich etwaiger potenzierter Nebenwirkungen wünschenswert.
Literatur:
1 Stange EF et al.: Ulcerative colitis-maintanance of remission with the probiotic Escherichia coli strain Nissle 1917.Gastroenterol 2021; 160(7): 2632 2 Gionchetti P et al.: Oral bacteriotherapy as maintenance treatment in patients with chronic pouchitis: a double-blind, placebo-controlled trial. Gastroenterol 2000; 119(2): 305-9 3 Mimura T et al.: Once daily high dose probiotic therapy (VSL#3) for maintaining remission in recurrent or refractory pouchitis. Gut 2004; 53(1): 108-14 4 Lichtenstein GR et al.:ACG Clinical Guideline: Management of Crohn’s Disease in Adults. Am J Gastroenterol 2018; 113(4): 481-517; Erratum in: Am J Gastroenterol 2018; 113(7): 1101 5 Panaccione R et al.: Combination therapy with infliximab and azathioprine is superior to monotherapy with either agent in ulcerative colitis. Gastroenterol 2014; 146(2): 392-400 6 Kothari MM et al.: Strategies for overcoming anti-tumor necrosis factor drug antibodies in inflammatory bowel disease: case series and review of literature. World J Gastrointest Pharmacol Ther 2017; 8(3): 155-61 7 Price DB et al.: Adverse outcomes from initiation of systemic corticosteroids for asthma: long-term observational study. J Asthma Allergy 2018; 11: 193-204 8 Vermeire S et al.: DOP Session 5: The Southern: Small molecules in IBD. ECCO 2022 9 Huss V et al.: Short-and longer-term cancer risks with biologic and targeted synthetic disease-modifying antirheumatic drugs as used against rheumatoid arthritis in clinical practice. Rheumatol 2022; 61(5):1810-8 10 Vedamurthy A et al.: Vedolizumab or tumor necrosis factor antagonist use and risk of new or recurrent cancer in patients with inflammatory bowel disease with prior malignancy: aretrospective cohort study. Clin Gastroenterol Hepatol 2022; 20(1): 88-95 11Hasan B et al.: Ustekinumab does not increase risk of new or recurrent cancer in inflammatory bowel disease patients with prior malignancy. J Gastroenterol Hepatol 2022; 37(6): 1016-21 12 Colombel JF et al.: Effect of tight control management on Crohn’s disease (CALM): a multicentre, randomised, controlled phase 3 trial. Lancet 2017; 390(10114): 2779-89 13 Turner D et al.: STRIDE-II: an update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) initiative of the International Organization for the Study of IBD (IOIBD): determining therapeutic goals for treat-to-target strategies in IBD. Gastroenterol 2021; 160(5): 1570-83 14 Travis S et al.: Vedolizumab for the treatment of chronic pouchitis. N Engl J Med 2023; 388(13): 1191-1200 15 Maaser C et al.: Intestinal ultrasound for monitoring therapeutic response in patients with ulcerative colitis: results from the TRUST&UC study. Gut 2020;69(9): 1629-36 16 Sandborn WJ et al.: Tofacitinib as induction and maintenance therapy for ulcerative colitis. N Engl J Med 2017; 376(18): 1723-36 17 Ytterberg SR et al.: Cardiovascular and cancer risk with tofacitinib in rheumatoid arthritis. N Engl J Med 2022; 386(4): 316-26 18 Feagan BG et al.: Filgotinib as induction and maintenance therapy for ulcerative colitis (SELECTION): a phase 2b/3 double-blind, randomised, placebo-controlled trial. Lancet 2021; 397(10292): 2372-84 19 Danese S et al.: Upadacitinib as induction and maintenance therapy for moderately to severely active ulcerative colitis: results from three phase 3, multicentre, double-blind, randomised trials. Lancet 2022; 399(10341): 2113-28 20 https://www.ema.europa.eu/en/medicines/human/referrals/janus-kinase-inhibitors-jaki ; zuletzt aufgerufen am 14.4.2023 21 Sandborn WJ et al.: Ozanimod as induction and maintenance therapy for ulcerative colitis. N Engl J Med 2021; 385(14): 1280-91 22 Sandborn WJ et al.: Five-year efficacy and safety of ustekinumab treatment in Crohn’s disease: the IM-UNITI Trial. Clin Gastroenterol Hepatol 2022; 20(3): 578-90.e4 23 Parigi TL et al.: Blockade of IL-23: What is in the pipeline? J Crohns Colitis 2022; 16(Supplement_2): ii64-ii72
Das könnte Sie auch interessieren:
Vorsorgekoloskopie und Polypektomienachsorge
In ihrem Vortrag zum Darmkrebs-Screening in Österreich an der SGG-Jahrestagung 2024 ermöglichte Univ.-Prof. Dr. med. Monika Ferlitsch, Wien, einen Blick über den Tellerrand. Sie zeigte ...
Interdisziplinäres Management bei Divertikulitis
Bei der Behandlung der Divertikulitis ist eine enge, interdisziplinäre Zusammenarbeit zwischen Gastroenterologen und Chirurgen unerlässlich. Eine enge Kooperation ermöglicht eine ...
Schwere Pankreatitis – intensivmedizinische Therapiekonzepte
Die schwere akute Pankreatitis geht mit einer hohen Mortalität einher. Da häufig Organversagen und lokale Komplikationen mit ihr assoziiert sind, ist die intensivmedizinische Behandlung ...