Systemische JAK-Inhibitoren liefern aussagekräftige Studiendaten
Bericht:
Dr. Susanne Kammerer
2023 wurde mit Ruxolitinib der erste lokale JAK-Hemmer zur Behandlung der Vitiligo zugelassen. Die Entwicklung steht erst am Anfang: Einige Vertreter dieser Substanzgruppe haben erfolgreich Phase-II-Studien abgeschlossen, sodass bald auch systemische Therapieoptionen zur Verfügung stehen werden.
Bei Vitiligo besteht der erste Schritt der Zerstörung der Pigmentzellen in einer Einwanderung von melanozytenspezifischen CD8+-Zellen, die sich um verbleibende Melanozyten gruppieren.1 Interferon (IF)y ist ein Schlüsselzytokin, das von CD8+-T-Zellen produziert wird und spielt eine zentrale Rolle bei der Pathogenese der Vitiligo. Zudem ist auch IL-15 an der Zerstörung der Pigmentzellen beteiligt. Beide Zytokine nutzen den JAK/STAT-Signalweg, was die Rationale für den Einsatz von JAK-Inhibitoren bei Vitiligo darstellt.1
Nach Ausführung von Prof. Julien Seneschal, Universität Bordeaux (Frankreich), gibt es darüber hinaus einen zweiten Grund, diese Substanzen bei Vitiligo einzusetzen: Studien zeigten, dass sie den Prozess der immunvermittelten Apoptose der Melanozyten unterbrechen können.1,2
Kürzlich wurden nun die Ergebnisse mehrerer Phase-II-Studien zum systemischen Einsatz von JAK-Inhibitoren bei Vitiligo vorgestellt – mit sehr positiven Resultaten.3–5 So wurden in einer multizentrischen, randomisierten, doppelblinden und placebokontrollierten Phase-II-Studie 184 erwachsene Patient:innen mit nicht-segmentaler Vitiligo mit drei verschiedenen Dosen des JAK1/JAK2-Hemmers Upadacitinib (6, 11 und 22mg einmal täglich) in der Doppelblindphase im Placebovergleich behandelt.3
Eine zweite Studienphase wurde ab Woche 24, dem Zeitpunkt der primären Analyse, als verblindete Extension bis Woche 52 fortgeführt. Nach 24 Wochen wurden die zwei Placebogruppen jeweils zur Hälfte mit 11 bzw. mit 22mg Upadacitinib bis Woche 52 behandelt. Primärer Studienendpunkt war die Veränderung des Facial Vitiligo Area Scoring Index (F-VASI) von Baseline bis Woche 24.3Von 185 Proband:innen, die in der ersten Studienphase eingeschlossen wurden, nahmen 165 auch an der anschließenden Studienverlängerung (Studienphase2) teil. Schon aus früheren Studien ist bekannt, dass die Repigmentierung eine gewisse Zeit in Anspruch nimmt.
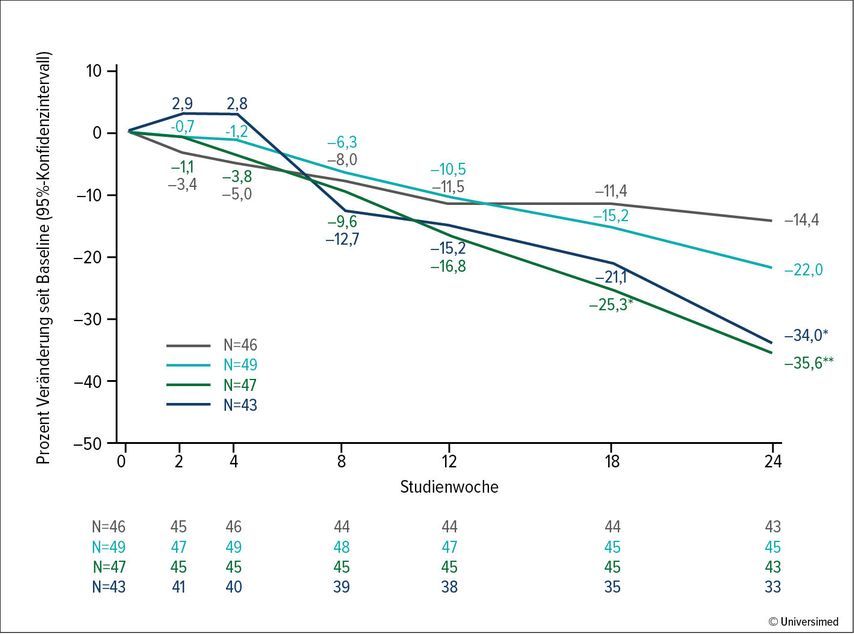
Die in die vorliegende Studie eingeschlossenen Patient:innen wiesen zudem ungünstige Ausgangsvoraussetzungen auf: Die meisten von ihnen litten seit über 15 Jahren an Vitiligo und bei vielen war die Erkrankung aktiv, alles Faktoren, die mit einem schlechteren Ansprechen assoziiert sind. Die Behandlung mit Upadacitinib bewirkte in allen Gruppen eine Verbesserung im F-VASI, die in den beiden höchsten Dosen statistische Signifikanz erreichte. So sank der F-VASI bei Therapie mit 22mg Upadacitinib um 34%, bei Therapie mit 11mg Upadacitinib um 35,6% (siehe Abb. 1).3 Auch bei den Läsionen am Körper gelang eine im Placebovergleich signifikante Repigmentierung mit diesen Dosen.
Abb. 1: Prozentuale Veränderung seit Baseline im F-VASI bis Woche 24 (modifiziert nach Passeron Th.)3
Sowohl im Gesicht als auch am Körper kam es unter Therapie mit Upadacitinib in der Verlängerungsphase zu einer fortschreitenden Verbesserung der Repigmentierung. Nach 52 Wochen war noch kein Plateau erreicht und in der höchsten Dosis sank der F-VASI um 69,8%, mit 11mg Upadacitinib um 60,7%. Auch die Verbesserung der depigmentierten Areale am Körper setzte sich bis Woche 52 fort: Zu diesem Zeitpunkt nahmen depigmentierte Areale bei Therapie mit 11mg Upadacitinib um 45% ab, bei Therapie mit 22mg um 49%.
Hinsichtlich der Verträglichkeit wurde kein Unterschied zwischen den Dosierungen beobachtet. Venöse Thromboembolien kamen nicht vor, allerdings hatte ein Patient mit mehreren kardiovaskulären Risikofaktoren, der mit 11mg Upadacitinib behandelt wurde, einen nichttödlichen ischämischen Schlaganfall in der Verlängerungsphase.
Positive Studiendaten für einen innovativen JAK1-Hemmer
171 Vitiligopatient:innen nahmen an der Studie zur Sicherheit und Wirksamkeit des in der Entwicklung befindlichen JAK-Hemmers Povorcitinib teil, der in Dosierungen von 15mg, 45mg und 75mg mit einem Placebo verglichen wurde. Das Studiendesign sah eine initiale Therapiephase über 24 Wochen vor, an die sich 28 Wochen mit einer Umstellung auf die Höchstdosierung anschlossen. Nur bei Patient:innen im 45mg-Studienarm wurde in diesem Zeitraum die Dosis nichterhöht.
Die Ergebnisse zur Sicherheit von Povorcitinib ergaben eine insgesamt gute Verträglichkeit. Es wurden keine schwerwiegenden unerwünschten Ereignisse im Zusammenhang mit der Behandlung festgestellt, und es wurden keine neuen Sicherheitssignale beobachtet,berichtete Prof. Khaled Ezzedine, Universität Paris Est Créteil (Frankreich).4
Bezüglich des primären Studienendpunkts, der Veränderung im Total Vitiligo Area Scoring Index (T-VASI) für den gesamten Körper in Woche 24, erreichte das Studienmedikament Signifikanz für alle Dosisstärken. Die Depigmentierung verbesserte sich um 19,1% (15mg), 17,8% (45mg) und 15,7% (75mg) gegenüber dem Ausgangswert (p<0,01 versus Placebo). Die ebenfalls signifikanten Ergebnisse für die verbesserte Depigmentierung im Gesicht (F-VASI) lagen bei 27,7%, 36,4% und 29,4% im Vergleich zu 5,1% unter Placebo. Nach 52 Wochen waren die Pigmentierungsergebnisse weiter verbessert und Dr. Ezzedine wies darauf hin, dass zu diesem Zeitpunkt noch kein Plateau der Wirkung erreicht war. Je nach Dosierung stieg der T-VASI auf 40,7–42,7% und der F-VASI auf 63,6–64,4%. Nach einem Jahr wurde eine 50%ige Besserung, d.h. ein T-VASI50 von 37,0–45,2% der Probanden unter Povorcitinib erreicht und ein F-VASI75 von 48,4–58,6%. Sowohl die Repigmentierung im Gesicht als auch am Körper blieb bei den Patient:innen, welche die medikationsfreie Nachbeobachtungsphase der Studie bis Woche 76 abschlossen, erhalten. Zwar befanden sich nur 32 Patient:innen in dieser Gruppe, aber Prof. Ezzedine wertete dies als Hinweis auf ein Anhalten des Ansprechens auch nach dem Absetzen der Therapie.
Geduld ist gefragt und wichtig
Dr. Albert Wolkerstorfer, Universitätsklinik Amsterdam (Niederlande), stellte eine gepoolte Auswertung vor, die sich mit den Non-Respondern innerhalb des TRuE-V-Studienprogramms zu Ruxolitinib-Creme 1,5% bei Vitiligo beschäftigte. Neben den randomisierten Phase-III-Zulassungsstudien beinhaltet TRuE-V auch offene Verlängerungsstudien bis Woche 52 und 104.5 Diese Patientenkohorte mit Vitiligo hatte Ruxolitinib von Beginn an erhalten, erreichte aber in Woche 24 keine oder nur eine geringfügige (<25%) Besserung im Vitiligo Area Scoring Index (VASI) und setzte die Anwendung in der offenen und der Langzeitverlängerung fort, d.h. bis Woche 104. Bei Betrachtung der basalen Charakteristika der Non-Responder findet sich ein durchschnittlicher F-VASI von 0,91 und T-VASI von 6,73 bei den 224 Proband:innen mit einem medianen Alter von 39 Jahren.
Unter den Vitiligopatient:innen, die initial keine VASI-Besserung aufwiesen, erreichten nach einem Jahr 77,8% doch noch eine Verbesserung der Pigmentierung im Gesicht und bei 79,6% kam es zu einer Therapieantwort im T-VASI. Die entsprechenden Raten nach zwei Jahren waren 97,1% und 93,3%.
In der Gruppe derer mit geringfügigem Ansprechen in Woche 24 verbesserte sich der F-VASI bei 64% und der T-VASI bei 64,5% zu Woche 52 bzw. 83,3% und 81,6% zu Woche 104. Das zunehmende Maß an Repigmentierung zeigt zum Beispiel auch der Anstieg der Gruppe mit F-VASI75 von 13,3% in Woche 52 auf 54,9% in Woche 104. Beim T-VASI50 steigerte sich der Anteil der Patient:innen, die diese 50%ige Besserung erreichten, von 23,1% nach einem Jahr auf 50% nach zwei Jahren.
In puncto Sicherheit kam es in der analysierten Kohorte zu keinen schweren therapiebedingten Nebenwirkungen und Ruxolitinib-Creme wurde insgesamt über den Behandlungszeitraum von 104 Wochen als gut verträglich eingestuft.
Zusammenfassend lasse sich sagen, dass diese 2-jährige TRUE-V-Studie die Bedeutung einer verlängerten Behandlung bei Vitiligopatient:innen hervorhebt, selbst wenn nach sechs Monaten der Behandlung nur eine begrenzte oder gar keine Repigmentierung erreicht wird, folgerte Dr. Wolkerstorfer aus diesen Ergebnissen.
Literatur:
1 Seneschal J: Präsentation D1T13.2.C, EADV-Kongress 2023, 11.–14. Oktober, Berlin 2 Qi F et al.: Front Immunol 2021;12:790125.3 Passeron T: Präsentation FC0208, EADV-Kongress 2023, 11.–14. Oktober, Berlin 4 Ezzedine K: Präsentation D1T01.1A, EADV-Kongress 2023, 11.–14. Oktober, Berlin 5 Wolkerstorfer A: Präsentation D1T01.1I, EADV-Kongress 2023, 11.–14. Oktober, Berlin
Das könnte Sie auch interessieren:
Tägliche Tablette gegen Psoriasis
Die US-Arzneimittelbehörde FDA hat mit Icotrokinra ein orales Medikament gegen Schuppenflechte zugelassen, welches die Rezeptoren für Interleukin-23 (IL-23) hemmt. Eine EU-Zulassung ...
Juveniles Polymyositis/Sklerodermie-Overlap-Syndrom
Die Komplexität von Kollagenosen und Autoimmunerkrankungen stellt oft eine diagnostische und therapeutische Herausforderung dar, da viele Patient:innen nicht nur einer einzigen Entität ...
Funktionalisierung bakterieller Nanocellulose
Chronische Wunden unterschiedlicher Ätiologie, etwa bei arterieller und venöser Insuffizienz oder Diabetes mellitus, prägen die tägliche Wundversorgung.Neben chronischen Wunden verlangen ...