Mehr Fleisch am Knochen: Erkennung und Behandlung der Sarkopenie
Autorinnen:
Dr. clin. nutr. Caroline Kiss
Ernährungstherapie/-beratung
Leiterin Klinische Ernährung
Universitäre Altersmedizin FELIX PLATTER, Basel
E-Mail: caroline.kiss@felixplatter.ch
Nadine Beerli
Fachverantwortliche Physiotherapie
Universitäre Altersmedizin FELIX PLATTER, Basel
E-Mail: nadine.beerli@felixplatter.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Im Alter nimmt die Muskelmasse ab und die Muskelkraft lässt nach, dies ist ein physiologischer Vorgang. Geschieht dies jedoch in übermässig starkem Mass, spricht man vom Krankheitsbild der Sarkopenie. Den Betroffenen fehlt die Kraft, um aufzustehen oder Treppen zu steigen, und es kann zum Verlust der Autonomie kommen. Damit die demografische Alterung der Bevölkerung bewältigt werden kann, kommt der Muskelgesundheit eine besondere Bedeutung zu. Deshalb gilt es, Patientinnen und Patienten mit einer wahrscheinlichen Sarkopenie frühzeitig zu erfassen und Massnahmen einzuleiten, um die Selbstversorgungsfähigkeiten möglichst lange zu erhalten. Für die Behandlung einer Sarkopenie sind vor allem zwei Faktoren wichtig: Training der Muskulatur und proteinreiche Ernährung.
Keypoints
-
Für die Behandlung einer Sarkopenie gilt als effektivste Intervention eine Kombination aus Training der Muskulatur und proteinreicher Ernährung.
-
Bei Sarkopenie wird ein individuell angeleitetes Mehrkomponententraining, bestehend aus einem Krafttraining in Kombination mit Gleichgewichts- und Ausdauerkomponenten, empfohlen.
-
Protein für den Muskelaufbau: Mit jeder Hauptmahlzeit 25–35g Protein und zeitnah zur Trainingseinheit zusätzlich Molkenprotein oder leucinangereichertes Molkenprotein.
Der altersbedingte Muskelabbau ist aufgrund seiner Auswirkungen auf die Mobilität und die Selbstständigkeit betagter Personen eine der grossen Komplexitäten für die öffentliche Gesundheit. Insbesondere die sogenannte Sarkopenie, eine Abnahme von Muskelkraft, Muskelmasse und Muskelfunktion, hat ein deutlich erhöhtes Sturzrisiko zur Folge.1 Erst 2016 erkannte die Weltgesundheitsorganisation WHO die Sarkopenie als Krankheitsbild an. 2018 hat die European Working Group on Sarcopenia in Older People (EWGSOP2) eine Revision ihrer bisherigen Konsensusdefinition publiziert.1 Die Sarkopenie ist in der Schweiz (ICD-10-GM, M62.50) kodierbar und wird im Rahmen einer stationären, akutgeriatrischen Komplexbehandlung als «geriatrisches Assessment» berücksichtigt.
Die Ursachen der Sarkopenie sind multifaktoriell: Zu den beeinflussbaren Faktoren gehören die körperliche Inaktivität sowie die Fehl- und Mangelernährung. Nur beschränkt beeinflussbar sind dagegen Faktoren wie endokrinologische Veränderungen im Alter, chronisch-entzündliche Prozesse und neurodegenerative Mechanismen.
Die globale Prävalenz der Sarkopenie variiert je nach verwendeter Definition und untersuchter Population zwischen 10 und 27%.2 Die Inzidenzrate steigt mit dem Alter. In einer Prävalenzstudie der Universitären Altersmedizin Felix Platter (n=305 Patienten/Patientinnen; medianes Alter: 84 Jahre) wurde bei jeder vierten stationär behandelten Person eine Sarkopenie diagnostiziert.3
Fallfindung und Diagnose
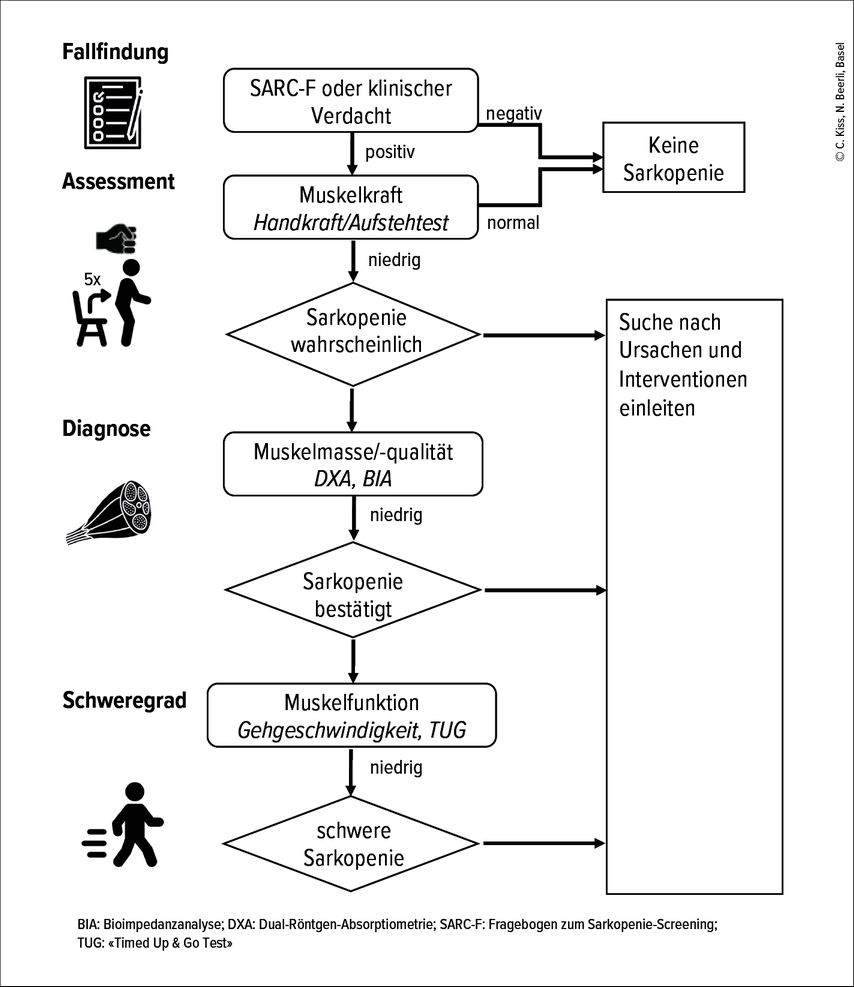
Die aktualisierten europäischen Konsensusempfehlungen sehen einen Diagnosealgorithmus zum Erkennen des Krankheitsbildes der Sarkopenie vor (Abb.1). Empfohlen wird eine Fallfindung bei klinischem Verdacht oder mit dem Screening-Fragebogen SARC-F. In diesem werden fünf Fragen zu möglichen Schwierigkeiten bei alltäglichen Tätigkeiten wie Treppensteigen oder Aufstehen gestellt. Der SARC-F hat eine sehr hohe Spezifität und eine geringe bis mässige Sensitivität.4 Deshalb werden vor allem schwere Fälle erkannt. Bei Berichten über Kraftlosigkeit oder Stürze sowie bei geriatrischen Patientinnen und Patienten sollte die Muskelkraft repräsentativ durch die Evaluation der Handkraft oder das Ausführen des Stuhlaufstehtests («Chair-Stand-Test») erfolgen. Dabei finden sich mit dem Stuhlaufstehtest etwa doppelt so viele Fälle mit wahrscheinlicher Sarkopenie als mit der Bestimmung der Handkraft.5 Für die Messung der Handkraft wird der Martin-Vigorimeter mit Druckball gegenüber dem Jamar-Dynamometer von älteren Personen aufgrund der intuitiven Gebrauchsweise und Schmerzfreiheit bevorzugt.6 Bei reduzierter Muskelkraft ist eine Sarkopenie wahrscheinlich, woraufhin Ursachen identifiziert und Interventionen in die Wege geleitet werden sollen. Um die Diagnose einer Sarkopenie zu bestätigen, benötigt es die Quantifizierung der Muskelmasse. Hierzu werden in der klinischen Praxis DXA (Dual-Röntgen-Absorptiometrie) und BIA (Bioimpedanzanalyse) angewendet. Die Einteilung des Schweregrads der Sarkopenie erfolgt schlussendlich durch die Beurteilung der Muskelfunktion mittels Assessments zur Messung der Gehgeschwindigkeit (beispielsweise mit dem 10-Meter-Gehtest) oder mit dem TUG («Timed Up & Go Test»).
Abb. 1: Algorithmus zur Erkennung und Diagnostik der Sarkopenie in der klinischen Praxis (adaptiert nach Cruz-Jentoft 2019)
Zu den Schwierigkeiten in der Umsetzung der Sarkopeniediagnostik gehören die limitierte Verfügbarkeit apparativer Methoden zur Bestimmung der Muskelmasse sowie fehlende Grenzwerte bei Adipositas. Mittlerweile wurde jedoch gezeigt, dass die Muskelfunktion eine wichtigere Rolle spielt und keine enge Beziehung zwischen der Muskelmasse und dem Auftreten funktioneller Defizite bestehen. Die Muskelmasse erklärt nur 30 bis 70 Prozent der Muskelkraft, und neben der Muskelmasse ist auch die Qualität der Muskulatur bedeutsam. Die Guidelines schlagen als Surrogatmarker die Bestimmung des Wadenumfangs (WU) vor, wenn keine apparativen Methoden verfügbar sind. Der vorgeschlagene Grenzwert von 31cm scheint jedoch zu gering, denn bereits ein WU von <34cm bei Männern und <33cm bei Frauen ist assoziiert mit einer reduzierten Muskelmasse.7 Hier braucht es noch weitere Forschung für die einfach durchführbare Objektivierung der Muskelmasse und der Muskelqualität im klinischen Alltag.
Für die Definition und die diagnostischen Kriterien der sarkopenen Adipositas gibt es einen ersten Konsensus, wobei die Grenzwerte und deren Validierung noch ausstehen.8 Ein hoher Body-Mass-Index geht mit einer höheren Fett- sowie Muskelmasse einher und kann somit das Vorhandensein einer Sarkopenie verschleiern.
Therapie: Muskeltraining und spezifische Ernährung
Das Ziel der Therapie ist die Verbesserung der Muskelfunktion im Alltag. Die am besten untersuchten Ansätze zur Behandlung der Sarkopenie stellen die Trainingsintervention und die ernährungsmedizinischen Massnahmen dar. Eine kürzlich publizierte Übersichtsarbeit kommt zum Schluss, dass ein strukturiertes Training bei älteren Personen mit Sarkopenie zur Verbesserung von Handkraft, Muskelkraft und -masse der unteren Extremität sowie von Gehgeschwindigkeit und Mobilität führt.9 Eine weitere Übersichtsarbeit zu Training in Kombination mit adäquater Proteinmenge bei Patientinnen und Patienten mit Sarkopenie zeigt, dass diese Intervention zu einer Zunahme an Muskelmasse und Kraft führt.10
Muskelabbau und Prävention
Es gilt als allgemein anerkannt, dass der Abbau der Muskulatur über die Zeit zum progressiven Verlust der Fähigkeit führt, Aktivitäten des täglichen Lebens (ADL) selbstständig zu verrichten.1,11 Körperliche Inaktivität verstärkt den Prozess des altersbedingten physiologischen Muskelabbaus. Bereits in jüngeren Jahren trägt ein sedentärer Lebensstil dazu bei, diesen Abbau zu beschleunigen, und dies wird im Alter dann verstärkt. Aus diesem Grund spielt die Prävention, am besten bereits ab dem jüngeren Erwachsenenalter, eine wichtige Rolle. Entsprechend hat die Weltgesundheitsorganisation Richtlinien für körperliche Aktivität und einen aktiven Lebensstil definiert.12 Für Erwachsene werden 150 bis 300 Minuten Alltagsaktivitäten/Sport mittlerer Intensität (ins Schwitzen kommen) oder alternativ 75 bis 150 Minuten Sport oder Bewegung mit hoher Intensität (deutlich erhöhte Anstrengung) pro Woche empfohlen. Kombinationen sind dabei möglich. Zusätzlich soll zweimal pro Woche ein Muskelkrafttraining durchgeführt werden. Erwachsenen über 65 Jahre wird zusätzlich zu diesen Vorgaben an drei oder mehr Tagen pro Woche ein Mehrkomponententraining mit Schwerpunkt auf funktionellen Gleichgewichts- und Kraftübungen als Teil der allgemeinen wöchentlichen Aktivität empfohlen (Tab.1).
Training der Muskulatur bei Sarkopenie
Bei geriatrischen Patientinnen und Patienten mit einem erhöhten Verlust der Muskelkraft wird ein individuelles Mehrkomponententraining empfohlen. Dieses orientiert sich an der allgemeinen Trainingslehre und sollte angeleitet über mindestens zwölf Wochen durchgeführt werden. Bei sarkopenen Patientinnen und Patienten besteht das Training aus einem individuellen moderaten Krafttraining in Kombination mit Gleichgewichts- und Ausdauerkomponenten (Tab.1). Bei älteren Menschen mit Sarkopenie verbessert eine solche Trainingsintervention die Muskelfunktion signifikant.9 Auch im geriatrischen Akutbereich lassen sich bei hochbetagten, hospitalisierten Patientinnen und Patienten durch die Anwendung eines oben beschriebenen individuellen Mehrkomponententrainings deutliche Verbesserungen im Bereich der funktionellen Kapazität erreichen.13 Langfristig wird zwei- bis dreimal pro Woche eine Trainingseinheit (in der Gruppe oder individuell) in moderater Dosis angestrebt.
Als zusätzliche Komponente zum Krafttraining wird die Integration von kognitiv-motorischen Elementen sowie Exergames und virtuelle Realität empfohlen. Diese verbessern die neuronale Muskelansteuerung und somit trainierte Bewegungsabläufe sowie die Motivation und Adhärenz zum Trainingsprogramm.
Proteine im Fokus – Bedarf und Verteilung
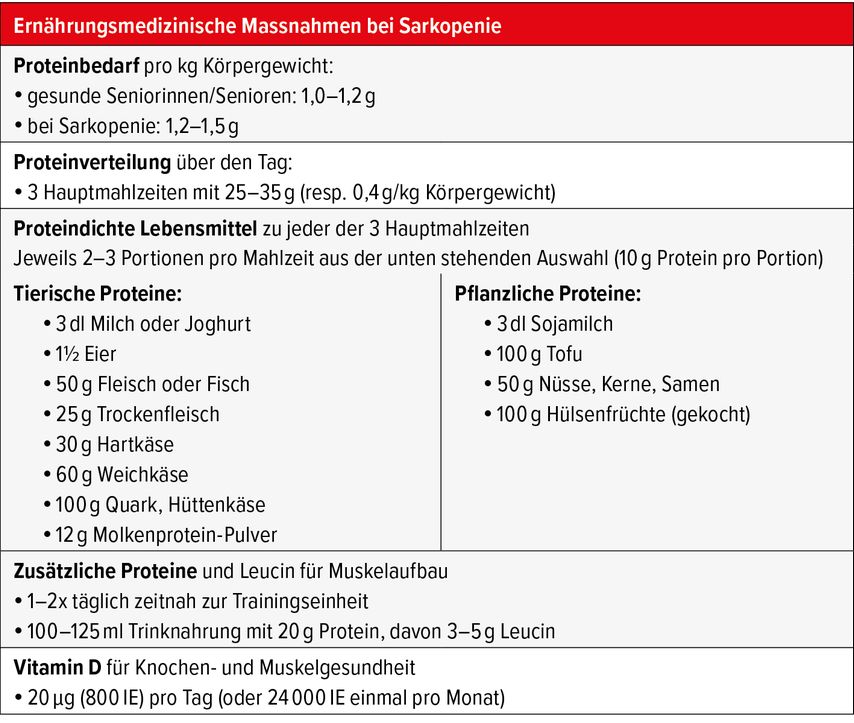
Die empfohlene tägliche Proteinzufuhr für gesunde Seniorinnen und Senioren beträgt 1,0–1,2g/kg Körpergewicht (KG) (Tab. 2). Für einen Muskelaufbau und die Therapie der Sarkopenie liegt der Proteinbedarf bei 1,2–1,5g/kgKG. Bis zum mittleren Alter ist die Bedarfsdeckung mit Protein meist kein Problem. Im Alter wird es jedoch schwieriger, den geforderten erhöhten Bedarf an Protein bei gleichzeitig reduziertem Energiebedarf aufzunehmen. Dieser nimmt vom 25. bis zum 75. Lebensjahr um ein Viertel ab. Gemäss der «MenuCH»-Studie, einer repräsentativen Schweizer Querschnittsstudie, erreichten weniger als die Hälfte der Senioren die Empfehlungen von mindestens 1,0g/kgKG und gar nur 30% die Empfehlungen von 1,2g/kgKG.14 In Situationen von akuter Krankheit und Rekonvaleszenz ist der Proteinbedarf weiter erhöht.15 Aufgrund der krankheitsassoziierten Anorexie ist es jedoch für die Betroffenen noch schwieriger, diesen Bedarf zu decken. In einer grossen Schweizer Studie betrug die Proteinversorgung in der ersten Hospitalisationswoche nur durchschnittlich 0,7g/kgKG.16 Deshalb soll standardmässig ein Screening durchgeführt werden, und sofern ein erhöhtes Risiko für Malnutrition vorliegt, sollen entsprechende individuelle Massnahmen eingeleitet werden.7
Wesentlich neben der Bedarfsdeckung ist auch die Verteilung der Proteinmenge über den Tagesverlauf. Im Vergleich zu jüngeren Erwachsenen braucht es im Alter zur Stimulation der muskulären Proteineigensynthese insgesamt deutlich mehr Protein pro Hauptmahlzeit, weshalb die Tagesmenge am besten gleichmässig auf die drei Hauptmahlzeiten verteilt wird. Jede Mahlzeit mit mindestens 25g Protein wirkt auch im Alter anabol. Jede Hauptmahlzeit sollte also 25–35g Protein (resp. 0,4g/kgKG) enthalten.17 Um dem Proteinabbau in der Nacht entgegen zu wirken, hilft eine proteinreiche Spätmahlzeit.
Molkenprotein und Leucin
Bei geringem Appetit und vorzeitigem Völlegefühl sind Produkte auf der Basis von Molkenproteinen besonders geeignet. Nach heutigem Wissensstand ist vor allem die Aminosäure Leucin wesentlich für den Erhalt einer optimalen Muskelproteinsyntheserate verantwortlich. Ein erhöhter Leucin-Plasmaspiegel begünstigt eine suffiziente Muskelneusyntheserate.18 Idealerweise erfolgt die Proteinaufnahme in zeitlicher Nähe zu einer Trainingseinheit.19 Bewährt hat sich das Molkenprotein als «schnelles Protein», da es leicht verdaulich ist, d.h., es passiert den Magen rasch, wird in einzelne Aminosäuren zerlegt und gelangt innert Kürze in die Muskulatur. Die Aufnahme eines leucinreichen Proteindrinks hilft daher, die trainingsinduzierte Muskelneubildung deutlich zu steigern. Darüber hinaus unterstützt Leucin den Muskel dabei, die durch das Training entstandenen Mikrorisse zu heilen, und fördert den Regenerationsprozess. Es ist deshalb empfehlenswert, innerhalb von 20–30 Minuten vor und/oder nach dem Training einen molkenbasierten Proteindrink (mit 20–30g Protein) oder ein leucinangereichertes Molkenproteinprodukt einzunehmen (mit 10–20g Protein, davon 3–5g Leucin).
Besonders interessant ist, dass durch die Anreicherung von Molkenprotein mit Leucin eine höhere Muskelproteinsynthese erfolgt als mit der doppelten Menge an Protein aus Kasein. Inzwischen gibt es Trinknahrungen auf dem Markt, welche mit Leucin angereichert sind und einen geringen Anteil an Kohlenhydraten und Fetten haben. Mit rund 150kcal, 20g Protein in 100ml, erleichtern sie die Einnahme für altersmedizinische Patientinnen und Patienten. Diese Menge reduziert die Aufnahme der normalen Mahlzeiten kaum und lässt sich mit fünf Schlucken trinken. Sie eignen sich jedoch auch für Personen, die aufgrund von Immobilität oder einer vorbestehenden Adipositas einen reduzierten Energiebedarf bei zeitgleich erhöhtem Proteinbedarf haben. Besteht eine Mangelernährung, haben sich hochkalorische leucinangereicherte Trinknahrungen in kleinen Volumina bewährt, z.B. zweimal täglich 125ml à 300kcal und 20g Protein.
Idealerweise wird die Massnahme nach dem Spitalaufenthalt in der Rekonvaleszenz noch für mindestens drei Monate weitergeführt. Trinknahrungen werden bei definierten medizinischen Indikationen in der Schweiz von der Grundversicherung übernommen. Informationen dazu, Kostengutspracheformulare und Homecare-Anbieter für die Belieferung nach Hause finden sich auf der Website der Gesellschaft für klinische Ernährung der Schweiz ( www.geskes.ch ).
Fazit
Ein strukturiertes, kombiniertes Trainings- und Ernährungsprogramm über mindestens 12 Wochen kann zu einem Muskelzuwachs von 0,5–1kg führen und die Muskelkraft und die Ausdauer um circa 10% steigern. Das scheint auf den ersten Blick nicht viel zu sein. Wenn man aber bedenkt, dass ab dem 50. Lebensjahr die Muskelmasse um 1–2%, die Muskelkraft um circa 1,5% und ab dem 70. Lebensjahr sogar um bis zu 3% pro Jahr abnimmt, dann ist diese Zunahme bemerkenswert und darüber hinaus oft entscheidend für einen suffizienten Erhalt der funktionellen Leistungsfähigkeit im Alter.
Literatur:
1 Cruz-Jentoft AJ et al.: Sarcopenia: revised European consensus on definition and diagnosis. Age Ageing 2019; 48: 16-31 2 Petermann-Rocha F et al.: Global prevalence of sarcopenia and severe sarcopenia: a systematic review and meta-analysis. J Cachexia Sarcopenia Muscle 2022; 13: 86-99 3 Bertschi D et al.: Sarcopenia in hospitalized geriatric patients: insights into prevalence and associated parameters using new EWGSOP2 guidelines. Eur J Clin Nutr 2021; 75: 653-60 4 Beaudart C et al.: Sarcopenia in daily practice: assessment and management. BMC Geriatr 2016; 16: 170 5 Johansson J et al.: Differences in sarcopenia prevalence between upper-body and lower-body based EWGSOP2 muscle strength criteria: the Tromsø study 2015-2016. BMC Geriatr 2020; 20: 461 6 De Dobbeleer L et al.: Martin Vigorimeter assesses muscle fatigability in older adults better than the Jamar Dynamometer. Exp Gerontol 2018; 111: 65-70 7 Gomes F et al.: ESPEN guidelines on nutritional support for polymorbid internal medicine patients. Clin Nutr 2018: 37: 336-53 3 8 Donini LM et al.: Definition and diagnostic criteria for sarcopenic obesity: ESPEN and EASO Consensus Statement. Obes Facts 2022; 15: 321-35 9 Wang Het al.: Efficacy of exercise on muscle function and physical performance in older adults with sarcopenia: an ipdated systematic review and meta-analysis. Int J Environ Res Public Health 2022; 19: 8212 10 Kirwan RP et al.: Protein interventions augment the effect of resistance exercise on appendicular lean mass and handgrip strength in older adults: a systematic review and meta-analysis of randomized controlled trials. Am J Clin Nutr 2022; 115: 897-913 11 Clark BC, Manini TM: Functional consequences of sarcopenia and dynapenia in the elderly. Curr Opin Clin Nutr Metab Care 2010; 13: 271-6 12 WHO guidelines on physical activity and sedentary behaviour. 2020. https://www.who.int/publications/i/item/ 9789240015128 ; zuletzt aufgerufen 9.12.2022 13 Martínez-Velilla N et al.: Effect of exercise intervention on functional decline in very elderly patients during acute hospitalization: a randomized clinical trial. JAMA Intern Med 2019; 179: 28-36 14 Kopf-Bolanz K, Walther B: Proteinkonsum in der Schweiz – Auswertung des menuCH Datensatzes Schweizer Ernährungsbulletin 2021; 130-46 15 Phillips SM et al.: Optimizing adult protein intake during catabolic health conditions. Adv Nutr 2020; 11: 1058-69 16 Schuetz P et al.: Individualised nutritional support in medical inpatients at nutritional risk: a randomised clinical trial. Lancet 2019; 393: 2312-21 17 Rondanelli M et al.: Where to find leucine in food and how to feed elderly with sarcopenia in order to counteract loss of muscle mass: practical advice. Front Nutr 2021; 7: 622391 18 Devries MC et al.: Protein leucine content is a determinant of shorter- and longer-term muscle protein synthetic responses at rest and following resistance exercise in healthy older women: a randomized, controlled trial. Am J Clin Nutr 2018; 107: 217-26 19 Trommelen J et al.: The muscle protein synthetic response to meal ingestion following resistance-type exercise. Sports Med 2019; 49: 185-97
Das könnte Sie auch interessieren:
Was tun bei Medikamentenunverträglichkeit?
Wenn Patientinnen und Patienten in die Praxis kommen und über eine Medikamentenunverträglichkeit klagen, gilt es herauszufinden, ob dies tatsächlich der Fall ist. Wie man dabei vorgeht ...
Physiotherapie bei akuten muskuloskelettalen Schmerzen
Akute muskuloskelettale Schmerzen zählen zu den häufigsten Beratungsanlässen in der Hausarztmedizin und im Notfallsetting. Eine frühzeitige physiotherapeutische Mitbeurteilung kann die ...
Der Tiefenrausch ist eine häufige Ursache für einen Tauchunfall
Atemgase verändern sich in der Wassertiefe physikalisch, was physiologische und medizinische Folgen bei Taucher:innen haben kann. Sauerstoff beispielsweise wird beim Abtauchen in der ...