Du bon usage des antibiotiques au cabinet du médecin de premier recours
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le problème des germes multirésistants en Suisse ne cesse de s’amplifier, ce qui rend le traitement des infections dans le contexte ambulatoire de plus en plus difficile. Dans la lutte contre le développement de résistances, il convient de notamment veiller, dans les soins de base, à une prescription modérée et rationnelle des antibiotiques.
Keypoints
-
Utiliser des antibiotiques uniquement lorsque c’est nécessaire pour minimiser les effets secondaires et le développement de résistances.
-
Les infections simples des voies respiratoires supérieures ne nécessitent pas d’antibiotiques.
-
Une bonne relation médecin-patient est plus importante pour la satisfaction du patient que la prescription d’antibiotiques inutiles.
-
En raison de résistances croissantes, les fluoroquinolones doivent être utilisées avec prudence dans la pratique.
En Suisse, la plupart des antibiotiques sont prescrits en ambulatoire par des médecins de premier recours. Lors de la prescription d’antibiotiques, les effets secondaires potentiels, les interactions et les dommages collatéraux des antibiotiques, tels que le développement de résistances, doivent toujours être pris en compte en plus de l’objectif de guérison de l’infection. Les avantages et les inconvénients potentiels des antibiotiques doivent toujours être soigneusement soupesés les uns par rapport aux autres.
Pour que le traitement des infections soit rationnel et efficace, il convient de se poser dix questions suivantes avant de prescrire des antibiotiques.
1. Un antibiotique est-il vraiment nécessaire?
Les antibiotiques sont de loin les médicaments les plus couramment prescrits en cas d’infections des voies respiratoires, bien qu’une grande partie de ces prescriptions soit inutile. Les antibiotiques ne doivent être prescrits qu’en cas d’infection bactérienne suspectée ou confirmée. L’antibiothérapie ne doit pas être utilisée pour les infections virales.
Dans les situations suivantes, des antibiotiques ne sont généralement pas nécessaires:
-
Infections simples des voies aériennes supérieures, amygdalopharyngite et bronchite aiguë, lesquelles sont généralement virales, bénignes et autolimitées;
-
Bactériurie asymptomatique, c’est-à-dire la détection de bactéries dans l’urine avec ou sans pyurie et sans symptômes cliniques. Exceptions: les bactériuries pendant la grossesse et avant les interventions urologiques avec lésion des muqueuses, qui doivent être traitées par des antibiotiques;
-
Prophylaxie antibiotique chez les patients ayant des articulations artificielles (p.ex. des prothèses de hanche/genou) dans le cadre de la chirurgie dentaire ou de la pose d’une sonde vésicale;
-
Pneumonie par aspiration.
En cas de cystite simple de la jeune femme et d’angine simple avec des streptocoques du groupe A, on peut tenter un traitement principalement axé sur les symptômes et sans antibiotique, étant donné que les deux infections sont généralement bénignes et autolimitées. Cependant, les complications potentielles, les contrôles cliniques et, si nécessaire, le début d’un traitement antibiotique retardé doivent être discutés avec les patients.
Chez les patients qui souhaitent recevoir des antibiotiques, la communication centrée sur le patient permet d’éviter les prescriptions d’antibiotiques inutiles. Des études ont montré que la satisfaction des patients dépend principalement d’une bonne relation médecin-patient et non de la prescription d’antibiotiques en soi, sans qu’il soit nécessaire de prolonger le temps de consultation. Le patient doit se sentir compris par le médecin et comprendre quant à lui le diagnostic, l’évolution naturelle de la maladie ainsi que le plan de traitement. Le patient doit également être informé du problème des résistances et du risque d’effets secondaires.
2. Quel antibiotique couvre le spectre de germes escompté?
Le traitement par antibiotique doit être dirigé aussi étroitement que possible contre le spectre de germes escompté (p.ex. amoxicilline en cas de pneumonie à pneumocoques). Pour les infections simples, les antibiotiques à large spectre tels que les fluoroquinolones (ciprofloxacine, lévofloxacine, moxifloxacine) – dans le cas d’options de traitement alternatives – doivent être utilisés avec retenue dans la pratique étant donné que les dommages collatéraux écologiques (développement de résistances) sont considérables. En 2018, 20% de tous les isolats d’E. coli testés en ambulatoire en Suisse présentaient déjà une résistance aux fluoroquinolones (base de données ANRESIS 2018), ce qui est en partie dû à la consommation considérable de ces antibiotiques ces dernières années.
3. Dois-je m’attendre à des agents pathogènes multirésistants?
Outre le spectre de germes attendu, le risque de pathogènes multirésistants doit également être pris en compte lors du choix des antibiotiques.
Les bases de données sur les résistances, telles que le Centre suisse pour le contrôle de l’antibiorésistance ANRESIS (www.anresis.ch), fournissent des informations précieuses sur la situation locale en termes de résistances d’importants micro-organismes en Suisse.
Les facteurs suivants suggèrent la présence de germes multirésistants:
-
Colonisation connue avec un micro-organisme multi-résistant, tel que le SARM (Staphylococcus aureus résistant à la méticilline) ou les germes producteurs de BLSE (bêta-lactamases à spectre élargi);
-
Antibiothérapie et hospitalisation au cours des trois derniers mois;
-
Comorbidités associées à des hospitalisations et antibiothérapies fréquentes (p.ex. mucoviscidose, maladies hématologiques);
-
Voyages antérieurs en dehors de l’Europe centrale et du Nord (p.ex. voyages en Asie/Inde, en Europe du Sud et acquisition de germes producteurs de BLSE ou de carbapénémase).
4. Quand un diagnostic microbiologique au cabinet s’impose-t-il?
L’antibiothérapie au cabinet du médecin de premier recours est généralement empirique, basée sur un syndrome clinique tel qu’une pneumonie ou une infection urinaire. Dans certains cas, cependant, un diagnostic microbiologique doit être pratiqué avant de débuter une antibiothérapie:
-
Si l’on soupçonne des infections chroniques et associées à des corps étrangers, comme des infections de prothèses articulaires, il est essentiel de consulter d’abord le chirurgien ou un infectiologue. Ces infections sont souvent extrêmement compliquées et longues à traiter et nécessitent généralement une intervention chirurgicale et un long traitement antibiotique, qui dure parfois plusieurs mois. Une seule dose d’antibiotiques peut entraîner des cultures bactériennes négatives, ce qui rend alors impossible tout traitement antibiotique ciblé;
-
Si l’on soupçonne la présence de germes multirésistants (voir ci-dessus);
-
En cas d’infections urinaires pendant la grossesse (résistances croissantes, possibilités limitées d’utilisation des antibiotiques pendant la grossesse);
-
En cas de fièvre peu claire, élévation isolée de la protéine C-réactive.
5. De quoi dois-je tenir compte lors du choix et de la posologie des antibiotiques oraux?
Lors du choix des antibiotiques oraux, il faut tenir compte notamment de la biodisponibilité, du mécanisme d’action (effet dépendant du temps par opposition à l’effet dépendant de la concentration) ainsi que de la nécessité d’ajuster la dose selon les fonctions rénale et hépatique. Les sous-dosages (risque d’échec du traitement, développement de résistances) et les surdosages (risque de toxicité) doivent être évités à tout prix.
Comparée à l’amoxicilline, la pénicilline V orale a une biodisponibilité plus faible (60% contre 80%), de sorte que l’amoxicilline doit généralement être privilégiée pour le traitement oral. En raison du mode d’action dépendant du temps de tous les antibiotiques bêtalactamines, y compris l’amoxicilline, l’administration de trois doses plus faibles (3x 500mg/j) a un meilleur effet que l’administration de deux doses plus élevées (2x 1000mg/j). La co-amoxicilline a un grand index thérapeutique et ne nécessite généralement pas d’adaptation à la fonction rénale lorsqu’elle est administrée par voie orale à une dose standard (3x 625mg à 3x 1000mg par jour).
6. Combien de temps dois-je traiter?
Pour de nombreuses infections simples, des antibiothérapies plus courtes ont fait leurs preuves et se sont révélées équivalentes aux traitements plus longs pratiqués auparavant. De quoi réduire également la toxicité, le développement de résistances et les coûts. Le Tableau 1 présente quelques exemples de la durée d’une antibiothérapie pour des infections non compliquées.
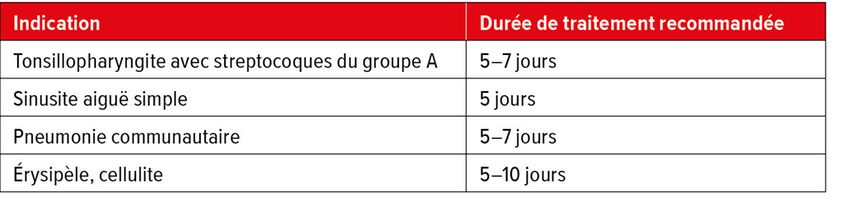
Tab. 1: Exemples de durée de l’antibiothérapie pour certaines infections non compliquées
7. Quand dois-je débuter un traitement antibiotique dans mon cabinet?
Dans le cas d’infections graves, l’antibiothérapie (p.ex. co-amoxicilline ou ceftriaxone) doit être débutée au cabinet dans quelques situations et lorsque le temps de transfert du patient à l’hôpital le plus proche est supérieur à une heure, en effet, en cas de septicémie sévère ou de choc septique, une antibiothérapie retardée augmente rapidement la mortalité (environ 7,4% par heure d’antibiothérapie retardée). Si possible, une ou deux paires d’hémocultures doivent être prélevées avant l’administration des antibiotiques.
Ces urgences infectieuses sont les suivantes:
-
Méningite bactérienne;
-
Infection invasive à méningocoques;
-
Infection bactérienne chez le patient asplénique;
-
Choc septique et toxique.
8. Quels sont les effets secondaires des antibiotiques à attendre?
Les antibiotiques provoquent souvent des effets secondaires tels que des allergies, des effets secondaires gastro-intestinaux, une toxicité hépatique, des allongements de l’intervalle QT, une colite à Clostridium difficile et bien d’autres encore. On estime que 20% de toutes les consultations d’urgence liées aux médicaments sont dues à des effets secondaires d’antibiotiques. Pour ces seules raisons, l’utilisation rationnelle des antibiotiques au cabinet du médecin de premier recours revêt une grande importance.
L’allergie à la pénicilline est l’un des effets secondaires les plus courants. En cas d’allergie de type 1 suspectée ou confirmée de type immédiat (réaction anaphylactique, urticaire, etc.) ou de réaction allergique sévère médiée par les lymphocytes T (syndrome de Stevens-Johnson, DRESS, etc.), un antibiotique non bêtalactamine doit être prescrit et un examen allergologique doit être initié. En cas d’intolérance à la pénicilline (symptômes gastro-intestinaux uniquement, maux de tête, etc.) ou de réaction de type IV clairement bénigne, retardée et à médiation cellulaire (éruption cutanée survenant plusieurs jours après le début du traitement à la pénicilline), un antibiotique bêtalactamine du groupe des céphalosporines peut être utilisé. Le risque d’allergie croisée est d’environ 5%.
En cas d’incertitudes et de situations complexes, il convient de toujours consulter un allergologue.
Le problème de l’allongement de l’intervalle QT avec le risque de tachycardie ventriculaire sous forme de torsade de pointe doit être pris en considération, avant tout lors de l’utilisation de macrolides et de fluoroquinolones, en particulier en association avec d’autres médicaments prolongeant l’intervalle QT (p.ex. méthadone, nombreux neuroleptiques) et des facteurs de risque supplémentaires préexistants (p.ex. trouble électrolytique, insuffisance cardiaque, allongement préexistant de l’intervalle QT).
9. Quand faut-il songer aux interactions?
Lors de la prescription d’antibiotiques, les interactions potentielles avec d’autres médicaments doivent toujours être prises en compte. Les antibiotiques macrolides (inhibition du CYP3A, qui renforce généralement l’effet de diverses substances) et la rifampicine (inducteur du CYP450, qui réduit généralement l’effet de diverses substances) sont particulièrement problématiques. Les fluoroquinolones ne doivent pas être administrées en même temps que des médicaments/produits cationiques (p.ex. aluminium, calcium, fer, zinc, qui sont contenus dans les préparations multivitaminées, les antiacides, les produits laitiers, etc.), étant donné que la chélation peut entraîner une réduction de l’absorption orale des fluoroquinolones et des niveaux plasmatiques insuffisants. Un intervalle de 4 à 6 heures doit être observé entre les prises.
Plusieurs tables d’interaction et calculateurs de qualité sont disponibles sur Internet, certains étant gratuits (p.ex. www.compendium.ch).
10. Quels sont les antibiotiques utilisables pendant la grossesse?
En général, l’indication d’une antibiothérapie pendant la grossesse doit être établie de façon particulièrement stricte.
Les antibiotiques bêta-lactames (pénicillines, céphalosporines, carbapénèmes), les macrolides, la clindamycine, la fosfomycine et le métronidazole peuvent être utilisés pendant la grossesse en cas d’indication. Il convient de noter que ces antibiotiques appartiennent tous à la catégorie de risque B (c’est-à-dire aucun risque dans les études animales, pas de données de qualité chez l’homme). Les fluoroquinolones, les aminoglycosides et les tétracyclines sont contre-indiquées pendant toute la grossesse, le cotrimoxazole et la nitrofurantoïne au troisième trimestre.
En cas d’incertitudes, il convient de consulter un gynécologue ou un infectiologue. Des informations utiles sur les médicaments pendant la grossesse et l’allaitement sont disponibles sur le site www.embryotox.de.
Auteur:
PD Dr méd. Stefan Erb
Facharzt Innere Medizin und Infektiologie
Praxengemeinschaft Warteckhof
Grenzacherstrasse 62, 4058 Basel
Hirslanden St. Anna Klinik
Abteilung Infektiologie und Spitalhygiene
6006 Luzern
E-mail: stefan.erb@hin.ch
Littérature:
● ANRESIS, Antibiotic Resistance Report 2018, www.anresis.ch ●Blaettler L et al.: Secular trend and risk factors for antimicrobial resistance in Escherichia coli isolates in Switzerland 1997-2007. Infection 2009; 37: 534 ● Butler CC et al.: Understanding the culture of prescribing: qualitative study of general practitioners’ and patients’ perceptions of antibiotics for sore throats. BMJ 1998; 317: 637-42 ● Evison J et al.: Der akute infektiologische Notfall beim Erwachsenen in der Praxis. Ther Um 2005; 62: 351-57 ● Gupta K et al.: International clinical practice guidelines for the treatment of acute uncomplicated cystitis and pyelonephritis in women: a 2010 update by the Infectious Diseases Society of America and the European Society for Microbiology and Infectious Diseases. Clin Infect Dis 2011; 52: e103-20 ● Kumar A et al.: Duration of hypotension before initiation of effective antimicrobial therapy is the critical determinant of survival in human septic shock. Crit Care Med 2006; 34: 1589-96 ● Kronenberger A et al.: Symptomatic treatment of uncomplicated lower urinary tract infections in the ambulatory setting: randomised, double blind trial. BMJ 2017; 359: j5268 ● Linder JA et al.: Time of day and the decision to prescribe antibiotics. JAMA Intern Med 2014; 174: 2029-31 ● Little P et al.: Amoxicillin for acute lower-respiratory-tract infection in primary care when pneumonia is not suspected: a 12-country, randomised, placebo-controlled trial. Lancet Infect Dis 2013; 13: 123-9 ● Little P et al.: Information leaflet and antibiotic prescribing strategies for acute lower respiratory tract infection: a randomized controlled trial. JAMA 2005; 293: 3029-35 ● Nicolle LE et al.: Infectious Diseases Society of America guidelines for the diagnosis and treatment of asymptomatic bacteriuria in adults. Clin Infect Dis 2005; 40: 643-54 ● Roden DM: Drug-induced prolongation of the QT interval. N Engl J Med 2004; 350: 1013-22 ● SGINF (Schweizerische Gesellschaft für Infektiologie), Antibiotikarichtlinien. https://ssi.guidelines.ch ● Shehab N et al.: Emergency department visits for antibiotic-associated adverse events. Clin Infect Dis 2008; 47: 735-43 ● Shenoy ES et al.: Evaluation and management of penicillin allergy: a review. JAMA 2019; 321: 188-99 ● Stürchler MS et al.: Diagnosis and antibiotic therapy of infections in outpatients. Schweiz Med Wochenschr 2000; 130: 1437-46 ● Welschen I et al.: Effectiveness of a multiple intervention to reduce antibiotic prescribing for respiratory tract symptoms in primary care: randomised controlled trial. BMJ 2004; 329: 431-3
Das könnte Sie auch interessieren:
Présentations orales sélectionnées
Lors du congrès annuel de la Société suisse d’endocrinologie et de diabétologie (SSED) en novembre 2023, les endocrinologues suisses ont donné un aperçu de leurs nombreuses études. Nous ...
Les innovations numériques transforment la SEP
Les innovations dans le domaine du diagnostic (d’évolution) numérique dans la SEP présentées lors de la conférence annuelle ECTRIMS-ACTRIMS 2023 montrent une multitude d’idées, d’études ...
Verdacht auf berufsbedingtes Asthma: Was muss ich wissen?
Berufsbedingtes Asthma ist die häufigste berufsbedingte Atemwegserkrankung. Die Diagnose hat sowohl für den Patienten als auch für die öffentliche Gesundheit grosse Auswirkungen, die ...