Stehen Standardtherapien in Frage?
Autor:
Dr. Michael Panny
Abteilung für Hämatologie und Onkologie
Hanusch-Krankenhaus, Wien
E-Mail: michael.panny@oegk.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die aktuellen Studiendaten vom Jahreskongress der American Society of Hematology (ASH) 2021 stellen nicht nur die bisherigen Standards in Erst- und Zweitlinientherapie des DLBCL zur Diskussion. Auch die ZNS-Prophylaxe für fitte Patient*innen wird in Frage gestellt.
Erstlinientherapie – POLARIX
Die doppelblinde, placebokontrollierte, randomisierte POLARIX-Studie verglich die Standard-Induktions-Chemoimmuntherapie R/CHOP mit der experimentellen Kombination Polatuzumab-Vedotin plus R/CHP (Pola-R/CHP) bei unbehandelten, fitten Patient*innen mit International Prognostic Index (IPI) 2–5.1 Definierter primärer Endpunkt war das progressionsfreie Überleben (PFS). 879 Patient*innen wurden randomisiert, davon 440 in den experimentellen und 439 in den Standardarm.
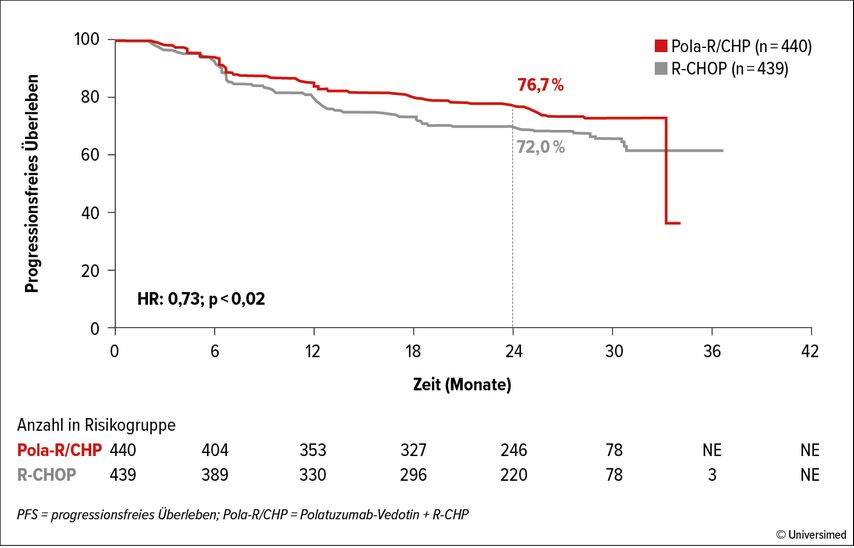
Nach einer medianen Nachbeobachtungszeit von 28,2 Monaten zeigte sich ein signifikanter PFS-Vorteil im Pola-R/CHP-Arm. Der primäre Endpunkt wurde erreicht: Die PFS-Rate nach zwei Jahren lag bei 76,7% unter Pola-R/CHP vs. 70,2% im Standardarm (HR: 0,73; p=0,02; Abb. 1). Zum Zeitpunkt des Data Cut-off benötigten 99 Patient*innen im Pola-R/CHP- und 133 im R/CHOP-Arm eine weitere Lymphom-spezifische Therapie. Sowohl die Rate an kompletten metabolischen Remissionen in der „End of treatment“-PET als auch das Gesamtüberleben (OS) waren ohne signifikanten Unterschied. Die OS-Rate nach zwei Jahren betrug im R/CHOP-Arm 88,6% und im Pola-R/CHP-Arm 88,7% (HR: 0,94; p=0,75). Das Sicherheitsprofil der beiden Studienarme war vergleichbar.
In bereits publizierten Subgruppenanalysen zeigt sich ein nicht ganz schlüssiges Bild – so scheint die experimentelle Therapie zwar bei älteren Patient*innen mit High Risk gemäß IPI und bei Patient*innen mit aktiviertem B-Zell-Typ von Vorteil. Bei Patient*innen mit Stadium IV oder mit „bulky disease“ fand sich allerdings kein signifikanter PFS-Vorteil für den experimentellen Therapiearm.
Fazit
Nach einer Reihe von negativen Phase-III-Studien zur Erstlinientherapie des DLBCL wurde seit vielen Jahren wieder eine positive Erstlinienstudie präsentiert. Trotz signifikanten PFS-Vorteils konnte kein Trend zu einem verlängerten OS detektiert werden. Bedingt durch verbesserte Therapiekonzepte im Rezidiv – das Dogma des DLBCL als „one shot cancer“ ist durchbrochen – scheint sich ein verlängertes PFS beim DLBCL nicht (mehr) automatisch in ein verbessertes Gesamtüberleben umzusetzen. Ob sich die Therapie mit Polatuzumab-Vedotin plus R-CHP als neuer Standard für die Erstlinientherapie etabliert, bleibt daher noch abzuwarten.
Rezidivtherapie – CAR-T vs. ASCT
Drei randomisierte Phase-III-Studien beschäftigten sich mit der Zweitlinientherapie mit CAR-T-Zellen bei primär refraktären Patient*innen mit DLBCL oder Patient*innen mit Rezidiv innerhalb des ersten Jahres nach Therapieabschluss. Die Patient*innen waren für Platin-basierte Hochdosischemotherapie sowie autologe Stammzelltransplantation geeignet. Zwei der Studien konnten hochsignifikante Vorteile für den experimentellen Arm, die Therapie mit CAR-T-Zellen, im Vergleich zur Standardtherapie zeigen. Die dritte Studie BELINDA jedoch fand keinen Unterschied. Hier die Daten im Überblick:
BELINDA
In der BELINDA-Studie wurden 322 Patient*innen randomisiert – 162 in den CAR-T-Arm mit der Verabreichung von Tisagenlecleucel, 160 in den „Standard of care“(SOC)-Arm.2 Der primäre Endpunkt war das ereignisfreie Überleben (EFS) in den ersten 12 Wochen. Ein Ereignis war definiert als stabile oder progressive Erkrankung nach drei Monaten oder Tod. Eine Bridging-Therapie mit Polychemotherapie bis zur CAR-T-Zell-Therapie war erlaubt.
Zwischen experimentellem Arm und Standardarm konnte kein signifikanter Unterschied detektiert werden: Das mediane EFS lag in beiden Armen bei 3 Monaten, die vollständige Ansprechrate in beiden Armen bei 28%.
ZUMA-7
In der ZUMA-7-Studie wurden 180 Patient*innen in den experimentellen Arm mit Axicabtagen-Lisoleucel (Axi-Cel) und 179 in den Standardarm randomisiert.3 Als Bridging-Therapie im CAR-T-Arm waren lediglich Steroide zugelassen. Primärer Endunkt war auch in dieser Studie das EFS. Ein Ereignis war allerdings auch definiert durch Nichtansprechen auf die Platin-basierte Induktionstherapie im Standardarm sowie Progress, Rezidiv oder Tod.
Nach einer medianen Nachbeobachtungszeit von 24,9 Monaten zeigte sich ein hochsignifikanter Vorteil durch die Therapie mit Axi-Cel. Der primäre Endpunkt wurde erreicht: Das mediane EFS im Axi-Cel-Arm lag bei 8,3 Monaten vs. 2 Monate im Standardarm (HR: 0,398; p<0,0001). Der Median in Bezug auf das OS wurde mit der CAR-T-Therapie nicht erreicht und lag im SOC-Arm bei 35,1 Monaten (HR: 0,73; p=0,027). 94% der Patient*innen im experimentellen Arm erhielten die geplante CAR-T-Zell-Therapie und 36% der Patient*innen im SOC-Arm erhielten die geplante konsolidierende autologe Stammzelltransplantation.
TRANSFORM
In der TRANSFORM-Studie wurden jeweils 92 Patient*innen in den SOC-Arm bzw. CAR-T-Arm mit Lisocabtagen-Maraleucel (Liso-Cel) randomisiert.4 Primärer Endpunkt war wiederum das EFS, definiert als Progress, Rezidiv, Tod oder Beginn einer neuen Therapie. Ein Cross-over vom SOC-Arm zur Liso-Cel-Therapie war erlaubt.
In einer Zwischenbeobachtung nach nur 6,2 Monaten im Median zeigten sich signifikant weniger Ereignisse im CAR-T-Arm: 35 Ereignisse unter Liso-Cel stehen 63 Ereignissen im SOC-Arm gegenüber (HR: 0,349; p<0,0001).
Fazit
Zusammenfassend zeigen ZUMA-7 und TRANSFORM ein einheitliches hochsignifikantes Ergebnis zugunsten der CAR-T-Zell-Therapie, während die BELINDA-Studie ein klar negatives Bild zeichnet. Unterschiede in der Definition des EFS, unterschiedliche Bridging-Therapien, Zeitdifferenzen in der Zeit bis zur Reinfusion und Unterschiede im Kollektiv werden als Ursache dieser Divergenz diskutiert. Für Patient*innen mit rezidiviertem/refraktärem DLBCL steht mit der CAR-T-Zell-Therapie eine relevante effektive Therapieoption zur Verfügung.
ZNS-Prophylaxe
Eine multizentrische Analyse von 21 Zentren in Australien, Asien, Nordamerika und Europa bei 2300 Patient*innen mit aggressiven Lymphomen und hohem Risiko für ein ZNS-Rezidiv (definiert als DLBCL mit CNS-IPI 4–6; „high grade“ B-Zell-Lymphome mit MYC- und BCL-2- und/oder BCL-6-Rearrangement und primär testikuläre/mammäre Lymphome) wurde präsentiert.5
Von den insgesamt 2267 Patient*innen mit vorliegenden Daten wurde bei 392 Patient*innen eine prophylaktische systemische Therapie mit Hochdosis-Methotrexat (HD MTX) durchgeführt. Nach einer medianen Follow-up-Zeit von 5,8 Jahren zeigte sich kein signifikanter Unterschied. In der HD-MTX-Kohorte erlitten 7,9% der Patient*innen ein ZNS-Rezidiv. Patient*innen ohne MTX-Prophylaxe erlitten in 9% der Fälle ein ZNS-Rezidiv.
In Subgruppenanalysen (Dosis HD MTX < oder >3g/m2, Anzahl extranodaler Manifestationen, spezifischer extranodaler Befall, CNS-IPI Score, Histologie, isolierter vs. systemischen/synchronen ZNS-Relaps, HD-MTX-Schema, gleichzeitige intrathekale MTX-Therapie) fand sich keine Subgruppe, die signifikant von einer HD-MTX-Prophylaxe profitierte.
Fazit
In Zusammenschau der am ASH 2020 präsentierten und mittlerweile publizierten Daten scheint eine prophylaktische HD-MTX-Gabe für Patient*innen mit aggressivem Lymphom und hohem Risiko für ein ZNS-Rezidiv nicht effektiv. Vor dem Hintergrund einer (toxischen) Übertherapie von 85–90% der Patient*innen (bei Hochrisiko-CNS-IPI: 10–15% Risiko für ZNS-Rezidiv) ist eine prophylaktische MTX-Therapie somit obsolet.
Hinweise auf eine effektivere Prophylaxe durch Kombinationstherapien mit HD MTX und/oder einer konsolidierenden autologen Stammzelltransplantation sollten validiert werden. Gleichzeitig ist es dringend notwendig, das Kollektiv mit hohem Risiko für ZNS-Rezidive besser zu definieren bzw. bei Diagnosestellung einen möglichen ZNS-Befall, z.B. durch Messung von ctDNA im Liquor, zu detektieren.
Literatur:
1 Tilly H et al.: The POLARIX Study: Polatuzumab Vedotin with Rituximab, Cyclophosphamide, Doxorubicin, and Prednisone (pola-R-CHP) Versus Rituximab, Cyclophosphamide, Doxorubicin, Vincristine and Prednisone (R-CHOP) Therapy in Patients with Previously Untreated Diffuse Large B-Cell Lymphoma. ASH-Meeting 2021; Abstr. #LBA-1 2 Bishop M et al.: Tisagenlecleucel vs standard of care as second-line therapy of primary refractory or relapsed aggressive B-cell non-hodgkin lymphoma: analysis of the phase III Belinda study. ASH-Meeting 2021; Abstr. #LBA-6 3 Locke F et al.: Primary analysis of ZUMA-7: aphase 3 randomized trial of axicabtagene ciloleucel (Axi-Cel) versus standard-of-care therapy in patients with relapsed/refractory large B-Cell lymphoma. ASH-Meeting 2021; Abstr. #2 4 Kamdar M et al.: Lisocabtagene maraleucel (liso-cel), a CD19-directed chimeric antigen receptor (CAR) T cell therapy, versus standard of care (SOC) with salvage chemotherapy (CT) followed by autologous stem cell transplantation (ASCT) as second-line (2L) treatment in patients (Pts) with relapsed or refractory (R/R) large B-Cell lymphoma (LBCL): results from the randomized phase 3 Transform study. ASH-Meeting 2021; Abstr. #91 5 Lewis KL et al.: High-dose methotrexate is not associated with reduction in CNS relapse in patients with aggressive B-Cell lymphoma: an international retrospective study of 2300 high-risk patients. ASH-Meeting 2021; Abstr. #181
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...