Technologies dédiées au diabète: une croissance exponentielle
Auteurs:
Dr Marcelo dos Santos Mameda
Dr méd. Giacomo Gastaldib
a Institut de Psychologie et Éducation
Université de Neuchâtel
b Service d’endocrinologie, diabétologie, nutrition et éducation thérapeutique du patient Département de médecine, HUG
1211 Genève 14
E-mail: marcelo.dossantos@unine.c h
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les nouvelles technologies font partie intégrante de notre vie, de la médecine actuelle et de la prise en charge du diabète. Les technologies dédiées au diabète (TdD) désignent l’ensemble du matériel, les dispositifs et les logiciels utilisé par les personnes ayant un diabète.1 Ces technologies sont en phase de croissance exponentielle et ont déjà profondément modifié la prise en charge du diabète. Le présent article passe en revue les TdD disponibles sur le marché helvétique, leurs indications et les challenges à venir avec l’arrivée des systèmes «hybrid closed-loop».
Santé digitale et technologies dédiées au diabète
La «santé digitale» est un domaine en pleine expansion tout particulièrement dans la maladie chronique. Elle inclut les technologies de l’information et celles de la communication, les dispositifs technologiques existant, les systèmes de soins digitaux, la télémédecine, les réseaux sociaux et les applications pour smartphone. Elle est le produit d’une multitude d’acteurs composés notamment de cliniciens, de médecins chercheurs ou de scientifiques issus des sciences de la santé, de l’ingénierie, des sciences sociales et économiques, de la psychologie ou spécialistes dans la gestion des données.2
Les technologies dédiées au diabète sucré (TdD) étaient jusqu’à récemment séparées en deux grandes classes: 1) les systèmes destinés à mesurer le glucose (glucomètres, systèmes de mesure en continu du glucose [CGM]) et 2) les systèmes de délivrance de l’insuline (seringues, stylos et pompes à insuline). Actuellement, la terminologie TdD englobe les systèmes en boucle semi-fermée («hybrid closed-loop») qui sont composés d’un système de CGM, d’une pompe à insuline et d’un algorithme d’intelligence artificielle afin d’adapter la délivrance de l’insuline à la glycémie et l’ensemble des logiciels utiles à l’auto-gestion du diabète (AGDM).1
En Suisse, la majorité des avancées technologiques disponibles sont remboursées en cas de diabète de type 1 (DT1) et chez les patients nécessitant une insulinothérapie intensive (insulinopénie sévère, pancréatectomie, etc.). Le remboursement est lié à la prescription par un spécialiste en endocrinologie/diabétologie. Dans un proche avenir, il est probable que l’indication à la CGM soit étendue à l’ensemble des patients dont le diabète est traité par de l’insuline. Pour l’instant ce n’est pas le cas.
Les systèmes de mesure en continu du glucose (CGM) et de «flash glucose monitoring» (FGM)
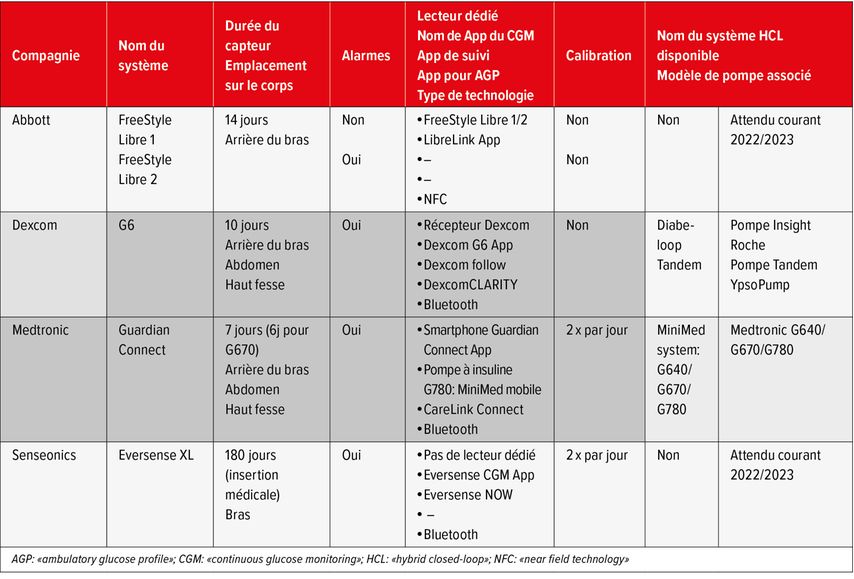
La miniaturisation du glucomètre a permis l’élaboration des systèmes de CGM et de FGM. Ces derniers mesurent le taux de glucose interstitiel à l’aide d’un capteur sous-cutané (<5mm) relié à un transmetteur collé sur la peau. Les capteurs de CGM ou de FGM mesurent l’activité électro-chimique qui correspond au taux de glucose interstitiel. Ce signal est transformé en données analogiques par le transmetteur qui sont lues à l’aide d’un récepteur (l’écran du téléphone, un lecteur dédié ou la pompe à insuline). Il existe pour l’instant trois principaus fabricants de systèmes de CGM sur le marché suisse (Dexcom: modèles G6 et G7 à venir; Medtronic: Guardian Connect et Guardian link couplé aux pompes à insulines G640 670 et 780; et Senseonic: Eversense XL). Un seul fabricant propose du FGM, il s’agit d’Abbott (Freestyle libre) (Tab. 1). Le FGM à la différence des systèmes de CGM nécessite que le patient scanne avec son téléphone ou un lecteur dédié le capteur situé sur la peau pour disposer des données.
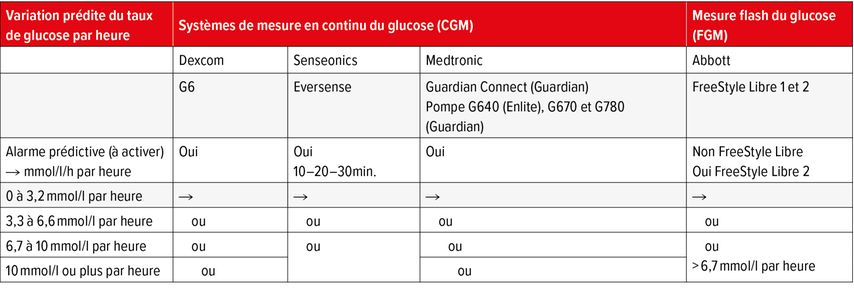
Les dispositifs de CGM/FGM permettent à leur utilisateur de visualiser le taux de glucose interstitiel, la courbe glycémique et sa tendance à l’aide de flèches (Tab. 2). Ces informations sont mises à jour toutes les 3 à 5 minutes, ce qui permet d’afficher le taux de glucose interstitiel en temps réel. Ces trois informations sont précieuses pour la gestion du diabète au quotidien (dosage de l’insulinothérapie, prise de glucides, gestion de l’activité physique etc.). L’utilisation de ces dispositifs en cas de DT1 permet d’améliorer le taux d’HbA1c de 0,5 à 1% en moyenne, réduire significativement la durée et la fréquence des hypoglycémies et limiter le temps en hyperglycémie3
Tab. 2: Signification des flèches de tendance des systèmes de mesure en continu du glucose (CGM) et de «flash glucose monitoring» (FGM)
Les données des systèmes de CGM/FGM sont consultables sur plusieurs supports en parallèle et systématiquement sur le smartphone du patient à l’aide d’une application téléchargeable. En fonction des fabricants, il existe la possibilité d’utiliser un appareil dédié à la lecture des courbes de glycémies (lecteur) ou l’écran d’un des modèles de pompe à insuline (Tab. 3).
Les soignants et les patients ont par ailleurs accès à un rapport contenant l’ensemble des données mesurées. Pour télécharger ce rapport, les fabricants des systèmes de CGM/FGM proposent soit d’accéder à une plateforme online ou via une application mobile. Depuis environ deux ans, il existe une standardisation de ces rapports qui se dénomme «ambulatory glucose profile» (AGP). L’AGP contient de nombreuses données utiles parmi lesquelles: la glycémie moyenne sur 14 jours, le pourcentage de temps passé entre 4 et 10mmol/l («time in range», TIR), les pourcentages de temps passé en hypoglycémie et hyperglycémie et la valeur estimée d’HbA1c. Cette dernière peut être estimées sur la base de 14 jours minimum. La standardisation des données du rapport AGP est récente4 et constitue une avancée réelle pour la pratique clinique quotidienne et la recherche. Notre équipe s’intéresse à l’impact des technologies sur les interactions de soin et nous observons que les soignants s’approprient progressivement ces nouveaux référentiels et qu’ils influencent leur manière d’échanger avec les patients. Le téléchargement et l’interprétation des résultats provenant du rapport AGP fait d’ailleurs partie des recommandations.3 Dans le futur, il est souhaitable que les interactions soignant-soigné autour de la présence des technologies soient mieux étudiées afin de contribuer à l’auto-gestion du diabète et ne pas accentuer la dimension anxiogène liée à leur utilisation et le sentiment d’impuissance face à la maladie.5
Par conséquent, l’utilisation des systèmes de CGM/FGM nécessite une formation technique et pratique des soignants et des patients. Idéalement, pour les patients cette formation devrait couvrir les aspects de manutention technique, les notions de cibles glycémiques (viser 70% du temps entre 4 et 10mmol/l, glycémie >8,0mmol/l avant activité physique, etc.), les limites techniques et de fiabilité (diminution de la précision de la mesure lorsque les valeurs ne sont pas entre 4 et 12mmol/l, problématiser les situations nécessitant le recours à la glycémie capillaire) et une aide à la lecture des flèches de tendance (vérifier après 10–15min. et agir selon un schéma défini). Il est déterminant de continuer à réévaluer et valider périodiquement les compétences d’utilisation (annuellement au minimum) en s’assurant de l’adéquation avec les notions indispensables à l’adaptation des doses d’insuline (insuline-repas et insuline de correction). Les exigences pour les soignants sont élevées car ils doivent maitriser les notions techniques et acquérir des compétences de communication leur permettant de transmettre des informations techniques à des patients très hétérogènes en terme de connaissances et d’accès à ces dernières.6
Les systèmes de CGM/FGM sont de formidables outils pour aider les personnes avec un DT1 à identifier l’influence respective des déterminants de l’équilibre glycémique (charge glucidique des repas, effet de l’activité physique, effet de l’insuline de correction, etc.). Ils sont particulièrement utiles pour apprendre à ajuster l’insulinothérapie. Des recommandations sur la gestion de l’insuline et la prise de glucides en fonction des flèches de tendances sont en cours d’établissement. Il convient donc de revoir régulièrement la manière dont nos patients ajustent leur traitement et leur proposer régulièrement de participer à des séances de formation.4
Les pompes à insuline
Les pompes à insuline constituent un outil de délivrance de l’insuline dont le principal avantage est la précision. Il est possible de déterminer la quantité d’insuline (minimum 0,05UI/h) administrée par tranche horaire sur un cycle de 24 heures (le débit de base = Q/24h) et d’en moduler le débit de base en fonction de besoins en insuline observés. La précision en cas de faible besoin en insuline (dose totale journalière d’insuline <0,3UI/kg/j) et la possibilité d’adapter le débit de base durant la journée s’avèrent particulièrement utile chez les enfants ou en cas de forte variabilité des besoins en insuline (sportifs d’endurance, phénomène de l’aube, etc.). Ces avantages font que l’utilisation des pompes à insuline permet de réduire le nombre d’hypoglycémie et améliorer l’HbA1c lorsque leur utilisation est appropriée.1
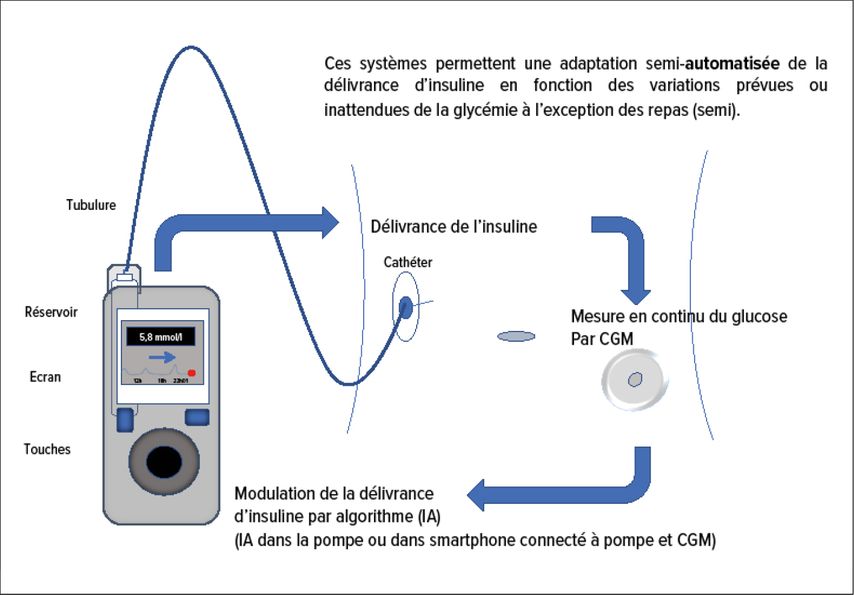
Il existe différents modèles de pompe à insuline externe. Les composants d’une pompe sont le boîtier qui abrite le réservoir, les boutons ou écran tactile servant aux réglages et à l’administration de bolus, le processeur électronique le système de micro-perfusion et une batterie. Les pompes à insuline reliées au corps du patient à l’aide d’un dispositif de perfusion (tubulure + cathéter) (Fig. 1) font partie des pompes à tubulure et il existe des pompes patch (réservoir et cathéter sont collés sur la peau) dont le contrôle et la programmation se fait grâce à un boitier (télécommande).
Les désavantages liés à l’utilisation d’une pompe à insuline sont la nécessité de garder le dispositif constamment relié à son corps. En cas de déconnexion, volontaire ou involontaire (problème technique, décollement du cathéter, etc.), il existe un risque imminent d’acidocétose (quelques heures), la pompe délivrant uniquement de l’insuline rapide dans le tissu sous-cutané. Il convient par ailleurs de bien se rappeler que les pompes à insuline n’adaptent pas la délivrance de l’insuline de manière automatique. Le débit de base est délivré en fonction de la programmation du débit de base et à chaque repas ou situation d’hyperglycémie, l’administration d’un bolus d’insuline dépend de l’action volontaire du patient lui-même.
Boucles semi-fermée ou système «hybrid closed-loop»
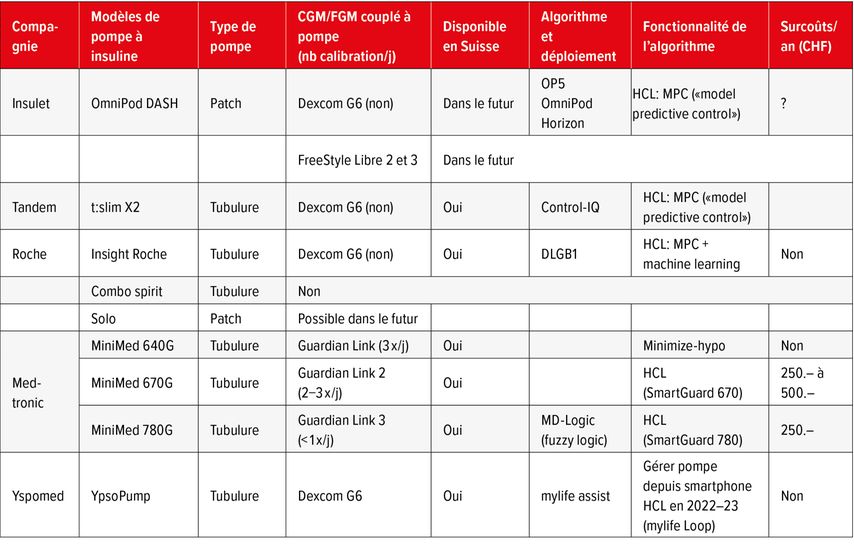
Le couplage entre pompe à insuline, système de CGM et un algorithme d’intelligence artificielle (IA) constitue une boucle fermée (Fig. 1). Ces systèmes ont la propriété d’adapter à la hausse ou à la baisse la délivrance de l’insuline en fonction du taux de glucose. Actuellement, ces systèmes sont au stade de boucle semi-fermée («hybrid closed-loop», HCL); le patient devant injecter de lui-même le bolus au moment des repas (dosage de l’insuline-repas et le timing dépendent totalement du patient). Il existe aujourd’hui trois systèmes sur le marché suisse et très prochainement deux supplémentaires (Tab. 2). Ils permettent de réduire le nombre d’hypoglycémie, améliorer le taux d’HbA1c d’environ 0,3–0,4% et diminuer la charge mentale liée à la gestion du diabète.7 Ces résultats s’observent toutefois principalement chez des individus ayant d’importantes compétences techniques et d’auto-gestion du diabète.1
Limites des technologies
Jusqu’à présent, malgré l’ensemble de ces progrès technologiques, moins d’un tiers des personnes ayant un DT1 atteignent les objectifs glycémiques.8 Il n’y a pourtant aucun doute sur l’efficacité des TdD et particulièrement des systèmes de CGM ou HCL sur les bénéfices en termes d’équilibre glycémique et les progrès technologiques ne vont pas s’arrêter. Une récente étude publiée dans le «Lancet», montre qu’il est déjà possible d’arriver à un contrôle glycémique équivalent à celui obtenu avec les systèmes HCL grâce à un système «fully closed-loop». Ce dernier fonctionne avec de l’insuline et de la pramlintine.9
Pour l’instant, il existe diverses barrières à l’utilisation des technologies, notamment le remboursement, la formation des équipes spécialisées ou la situation psycho-sociale des patients qui semblent expliquer pourquoi en 2010, il y avait, dans le meilleur des cas, seulement 20% des patients avec un DT1 équipés d’une pompe à insuline10 et qu’en Angleterre les systèmes de CGM sont employés par seulement 26% des patients pour des raisons de coûts11 alors qu’aux USA cette proportion peut dépasser 60% lorsqu’ils sont remboursés. La plus importante reste l’envie des patients.1
Il est indiscutable que la technologie facilite la prise en charge tant pour les soignants que pour les personnes vivant avec un DT1, surtout lorsque le recours à la technologie favorise le sentiment d’efficacité vis-à-vis de la maladie. Toutefois, son utilisation peut aussi générer de l’anxiété, une obsessionalisation des gestes de prise en charge et favoriser l’émergence de comportements compulsifs.5 Le rapport au temps et celui au corps sont modifiés en fonction de l’utilisation de la technologie. Cees éléments pourraient également expliquer que seule une minorité de patients souhaite réellement être équipées.
C’est donc bien la gestion du facteur humain qui conditionne encore et à plus d’un titre l’utilisation des nouvelles technologies et donc leur bénéfice sur l’équilibre du diabète. En effet, jusqu’à présent les dispositifs technologiques existants ne se substituent pas à l’utilisateur. Ce dernier reste dans l’obligation quotidienne de s’astreindre à diverses tâches, plus ou moins complexes (par ex.: avoir le matériel nécessaire en suffisance et accessible, remplacer les capteurs périodiquement et en urgence en cas de problème technique, remplir le réservoir de la pompe tous les 2–3 jours, changer le cathéter tous les 2–3 jours, etc.). Il en découle d’importantes contraintes organisationnelles et une réelle charge mentale. C’est pour cette raison que depuis 2021, l’ADA et l’EASD ont entériné dans les recommandations de bonne pratique de considérer cette dernière comme un facteur à part entière de l’équilibre du diabète.1 L’adhésion du patient est cruciale. Elle passe par des interactions soignant-soigné de qualité. Trop de patients acceptent encore à contrecœur le recours aux TdD alors qu’ils y sont réfractaires. Les conséquences sont généralement une sous-utilisation des dispositifs, parfois à l’émergence de problématiques techniques récurrentes voir des situations de mise en danger.
Conclusion
Les défis actuels et à venir vis-à-vis de l’utilisation de la technologie dans le diabète sont nombreux. Nous citerons en tout premier la formation des patients et des soignants, ce d’autant que nous assistons à une multiplication des systèmes et de leurs interconnexions. La meilleure compréhension des mécanismes soutenant les choix, la motivation des patients à utiliser des dispositifs technologiques et leur compréhension vis-à-vis de ces outils est cruciale. Enfin, il y a l’impact de la technologie sur la qualité de vie. Il s’agit donc pour l’instant de rester très rigoureux vis-à-vis des indications médicales existantes et ne pas céder à la tentation de la nouveauté pour la nouveauté. Il s’agit en effet de démocratiser l’emploi de ces dispositifs afin d’améliorer la santé des patients sans conduire à des réactions de rejet ou de mise en danger.
Les challenges du futur sont d’arriver à mettre en place des programmes et des outils favorisant des interactions soignant-soigné structurantes et facilitantes à une meilleure utilisation des TdD. Pour l’instant, il est recommandé de réévaluer régulièrement l’utilisation des dispositifs par les patients afin de les aider à rester en sécurité tout en améliorant la qualité de vie et l’équilibre glycémique.
Littérature:
1 American Diabetes Association: 7. Diabetes technology: standards of medical care in diabetes-2021. Diabetes Care 2021; 44 (Suppl 1): S85-99 2 Rhee SY et al.: Present and future of digital health in diabetes and metabolic disease. Diabetes Metab J 2020; 44: 819-27 3 Danne T et al.: International consensus on use of continuous glucose monitoring. Diabetes Care 2017; 40: 1631-40 4 Battelino T et al.: Clinical targets for continuous glucose monitoring data interpretation: recommendations from the international consensus on time in range. Diabetes Care 2019; 42: 1593-603 5 Fisher L et al.: Addressing diabetes distress in clinical care: a practical guide. Diabet Med 2019; 36: 803-12 6 Walker AF et al.: Barriers to technology use and endocrinology care for underserved communities with type 1 diabetes. Diabetes Care 2021; 44: 1480-90 7 Berget C et al.: Real-world performance of hybrid closed loop in youth, young adults, adults and older adults with type 1 diabetes: Identifying a clinical target for hybrid closed-loop use. Diabetes Obes Metab 2021; 23: 2048-57 8 Foster NC et al.: State of type 1 diabetes management and outcomes from the T1D Exchange in 2016-2018. Diabetes Technol Ther 2019; 21: 66-72 9 Tsoukas MA et al.: A fully artificial pancreas versus a hybrid artificial pancreas for type 1 diabetes: a single-centre, open-label, randomised controlled, crossover, non-inferiority trial. Lancet Digit Health 2021; S2589-7500(21)00139-4 10 Renard E: Insulin pump use in Europe. Diabetes Technol Ther 2010; 12 (Suppl 1): S29-32 11 Roze S et al.: Long-term cost-effectiveness of Dexcom G6 real-time continuous glucose monitoring versus self-monitoring of blood glucose in patients with type 1 diabetes in the U.K. Diabetes Care 2020; 43: 2411-7
Das könnte Sie auch interessieren:
Soleil et prévention cardiovasculaire
Il semble que le moment soit venu de réévaluer la situation: alors que le soleil était autrefois surtout connu pour ses bienfaits, il a fait l’objet d’une diabolisation ces dernières ...
Myocardite aiguë et cardiomyopathies inflammatoires
La myocardite aiguë et les cardiomyopathies inflammatoires sont des maladies complexes du myocarde qui nécessitent une classification étiologique et peuvent avoir des conséquences à long ...
Le rôle de l’imagerie dans la sarcoïdose cardiaque
La sarcoïdose cardiaque est une maladie cardiaque inflammatoire rare, mais importante. Le tableau clinique peut être très variable, allant de manifestations subcliniques à une gêne ...