État actuel des connaissances et nouvelles options de traitement
Auteurs:
Prof. Dr méd. Otto C. Burghuber
Otto-Wagner-Spital und Sigmund Freud Universität
1020 Wien
E-mail: otto.burghuber@med.sfu.ac.at
Prof. Dr méd. Claus Franz Vogelmeier
Klinik für Pneumologie
Universitätsklinikum Marburg
35043 Marburg
E-mail: vogelmei@med.uni-marburg.de
Dr méd.Matthias Urban, PhD
Karl Landsteiner Institute for Lung Research and Pulmonary Oncology
Klinik Floridsdorf
1210 Wien
E-mail: matthias.urban@kages.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Cet article offre une vue d’ensemble résumant le diagnostic de la BPCO ainsi que les options thérapeutiques médicamenteuses et non médicamenteuses. Pour le choix du traitement adéquat, la classification de la BPCO selon les directives GOLD actuelles est cruciale.
Keypoints
-
La bronchopneumopathie chronique obstructive est diagnostiquée par l’anamnèse et l’examen de la fonction pulmonaire; la poursuite de la classification est permise sur la base de la symptomatologie et du taux d’exacerbations.
-
Le traitement non médicamenteux repose sur la réhabilitation, l’entrainement, l’oxygénothérapie, ainsi que la ventilation non invasive en cas d’insuffisance respiratoire.
-
Le traitement médicamenteux de premier choix repose sur les bronchodilatateurs. Les corticoïdes en inhalation doivent être utilisés seulement chez les patients avec des exacerbations fréquentes et une numération d’éosinophiles élevée.
-
Si le succès thérapeutique reste insuffisant, une administration d’appoint à long terme de macrolides ou de roflumilast peut être envisagée.
La bronchopneumopathie chronique obstructive a été définie pour la première fois en 1965 et la compréhension de cette maladie complexe est encore en constante évolution. Les informations proviennent aussi du Global Initiative for Obstructive Lung Disease (GOLD) qui publie chaque année des recommandations reflétant l’état actuel des connaissances sur le diagnostic et le traitement.1 Actuellement, les nouveautés importantes du groupe GOLD concernent l’appréhension du risque d’exacerbation et la symptomatologie, un aspect crucial pour une prise en charge de la BPCO correspondant à l’état actuel des connaissances. Une autre actualisation comprend la numération des éosinophiles circulants permettant de tirer des conclusions sur le traitement médicamenteux.
La BPCO se caractérise par une obstruction respiratoire persistante avec habituellement une aggravation, due à plusieurs années d’exposition à des molécules toxiques inhalées.
Épidémiologie
Concernant la prévalence de la BPCO, les chiffres publiés varient énormément dans le monde et c’est surtout le pourcentage de cas non diagnostiqués de 80% environ à l’échelle internationale qui est impressionnant. Les données les plus probantes sont issues de l’étude internationale BOLD qui indique une prévalence mondiale de 11,7%.2 Dans le cadre de cette étude multinationale, des adultes d’au moins 40 ans ont été examinés. Pour la Suisse, les chiffres d’un échantillonnage (n=6126) de la cohorte SAPALDIA sont connus: chez les 30–73 ans, la prévalence de la BPCO est de 10% pour un stade GOLD >1 et de 5,1% pour un stade GOLD >2.3 La fréquence augmente avec l’âge et atteint son maximum chez les plus de 60 ans. Le pronostic de la PBCO est très influencé par les comorbidités.4 Selon des études d’observation de grande envergure, plus de 50% des patients avec BPCO montrent une ou plusieurs comorbidités (surtout hypertension, maladies cardiovasculaires, diabète, dysfonction musculaire et ostéoporose). En termes de morbidité et de mortalité à l’échelle internationale, la BPCO fait partie des maladies en tête de classement.
Étiologie et pathogenèse
Même si l’étiologie et la pathogenèse de la BPCO ne sont pas totalement élucidées, le principal facteur de risque est le tabagisme avec inhalation de la fumée. Le tabagisme passif est également associé à un risque. La pollution industrielle de l’air et la combustion de biomasse («indoor cooking») dans les pays sous-développés sont aussi des facteurs de risque. Outre les facteurs exogènes, le profil de risque est également influencé par des facteurs endogènes. Un développement pulmonaire insuffisant et un déficit en alpha-1 antitrypsine (DAAT) en font partie, entre autres. En cas d’asthme également, le risque de développer une BPCO est plus de dix fois plus élevé. La réponse physiologique des poumons à l’inhalation de molécules toxiques est une réaction inflammatoire excessive.5 Un déséquilibre entre les protéases et les antiprotéases est considéré comme un facteur de risque supplémentaire se manifestant par un emphysème pulmonaire. La limitation respiratoire qui en découle progresse dans de nombreux cas, même après un arrêt du tabac.
Diagnostic et diagnostic différentiel
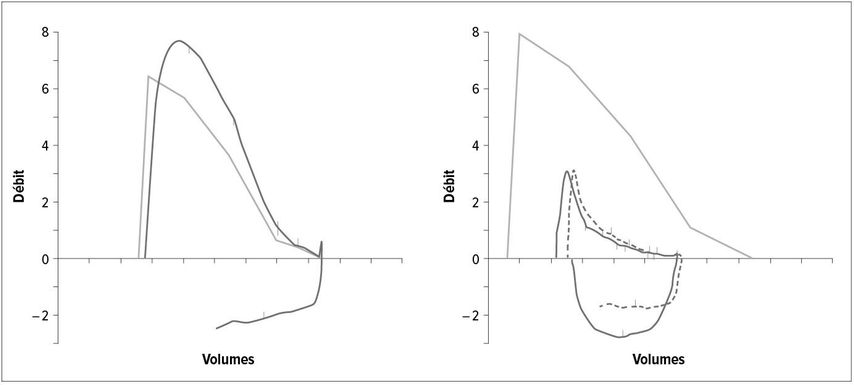
La pose du diagnostic a lieu sur la base de la symptomatologie respiratoire (c.-à-d. toux, expectoration, détresse respiratoire) et l’anamnèse expositionnelle (molécules toxiques inhalées) avec objectivation de l’obstruction par spirométrie. Le rapport entre le volume expiratoire maximal par seconde (VEMS), un marqueur crucial de l’obstruction, et la capacité vitale forcée (CVF) est examiné. Une limitation du débit respiratoire est évidente avec un rapport VEMS/CVF <70% après l’administration d’un bronchodilatateur (Fig. 1). Les dernières observations montrent que le rapport VEMS/CVF peut conduire à des sur-diagnostics chez les personnes âgées et des sous-diagnostics chez les personnes jeunes. C’est pourquoi les «lower limits of normal» (LLN) sont de plus en plus utilisées comme outil de diagnostic valide, surtout dans les études épidémiologiques. Cependant, en raison du manque de données longitudinales jusqu’ici et de l’absence de validation dans la population générale, l’utilisation du rapport VEMS/CVF n’est pas encore totalement évincée. Une augmentation du VEMS >12% ou de 200ml après l’administration d’un bronchodilatateur peut indiquer la présence d’un asthme. D’autres diagnostics différentiels comprennent la bronchite chronique, la tuberculose, des bronchiectasies et le carcinome bronchique.
Fig. 1: Spirométrie avec résultats normaux (gauche: VEMS/CVF = 83%, % VEMS prédit = 100%) et obstruction sévère (droite: VEMS/CVF = 53%, % VEMS prédit = 32%)
Classification
Fig. 2: COPD Assessment Test™ (CAT) ( www.catestonline.org ; disponible dans de nombreuses langues)
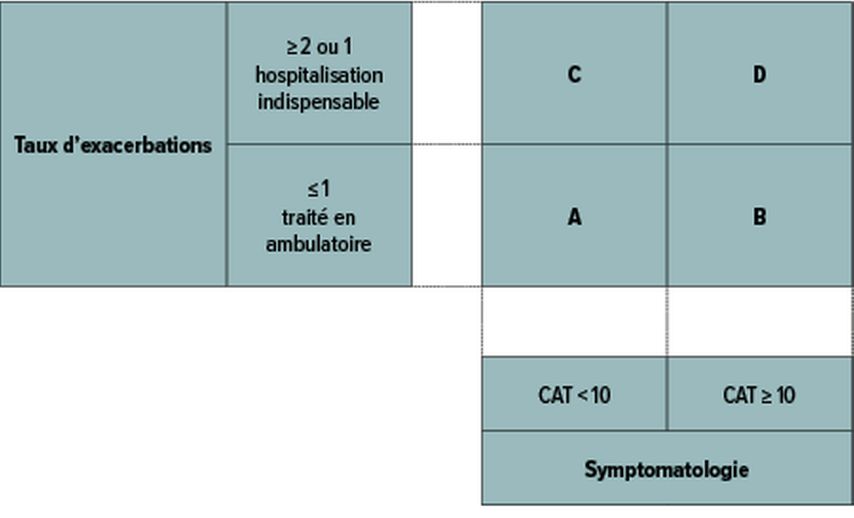
La sévérité de la limitation respiratoire est classée en 4 catégories (>80%: grade1; 50–80%: grade 2; 30–50%: grade 3; <30%: grade 4). De plus, le classement dans l’un des groupes de risque A, B, C ou D se base sur une quantification des symptômes, par ex. avec le COPD Assessment Test™ (CAT, Fig. 2) et le nombre/la sévérité des exacerbations annuelles (Fig. 3). Outre la classification de la BPCO, l’identification d’un phénotype et des maladies associées éventuelles est recommandée. L’anamnèse, une plethysmographie du corps entier, une TD du thorax et une quantification de l’inflammation (paramètres inflammatoires sérologiques, microbiologie des expectorations) peuvent permettre de déterminer si la maladie est dominée surtout par un emphysème ou par une inflammation des voies respiratoires. Les pathologies associées les plus fréquentes (à savoir maladies cardiovasculaires, diabète sucré, ostéoporose, anxiété et dépression) doivent le cas échéant être examinées et traitées.
Prévention
L’arrêt du tabac est de loin la mesure de prévention la plus efficace qui peut éviter un très grand nombre de cas de BPCO et ralentir la progression d’une BPCO existante. Dans le cadre de la prévention secondaire, la protection vaccinale contre l’influenza et les pneumocoques peut réduire le risque d’infection des voies respiratoires inférieures et donc celui d’une exacerbation de la BPCO.
Traitement non médicamenteux
Oxygénothérapie de longue durée (OLD) et ventilation
En cas de trouble chronique de l’oxygénation, l’oxygénothérapie de longue durée (OLD) est associée à un bénéfice en termes de survie bien documenté.6 Une OLD est indiquée lorsque la pression partielle d’oxygène (paO2) est inférieure à 55mmHg ou égale à 55–60mmHg en cas de cœur pulmonaire ou de polyglobulie. L’objectif du traitement par OLD est une paO2 supérieure à 60mmHg. En cas d’hypercapnie chronique, un bénéfice en termes de survie est désormais également prouvé avec la ventilation non invasive (VNI) pendant la nuit.7 L’indication pour cette technique existe à partir d’une pCO2 >50mmHg pendant la journée ou >55mmHg pendant la nuit.
Réduction du volume pulmonaire
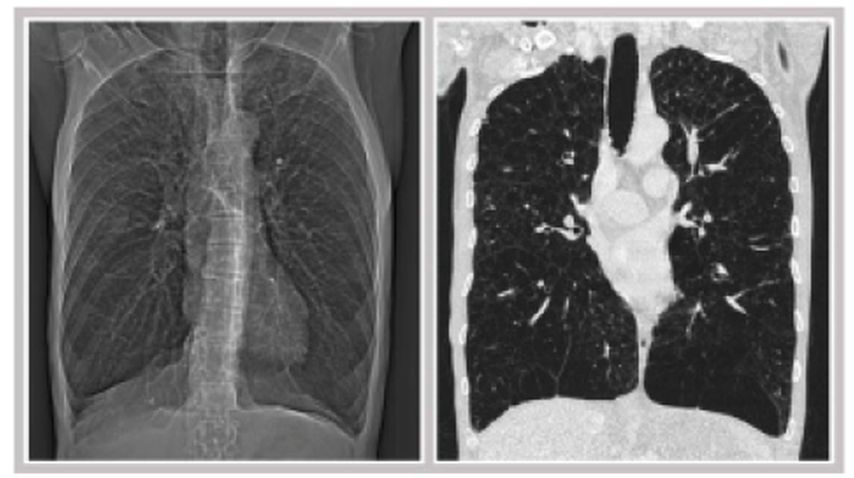
En présence d’un emphysème pulmonaire marqué, il est possible de réduire la dilatation pulmonaire par réduction du volume des poumons par voie chirurgicale et bronchique. En raison du risque associé à l’intervention chirurgicale, des méthodes bronchoscopiques ont été développées dernièrement pour la réduction du volume pulmonaire. La pose sous endoscopie de valves endobronchiques unidirectionnelles est désormais devenue le standard clinique.8 En cas d’emphysème hétérogène (Fig. 4), les valves permettent un dégonflement successif par atélectasie du lobe pulmonaire auparavant excessivement dilaté. Elles peuvent donc de manière avérée améliorer la fonction pulmonaire, les performances physiques et la détresse respiratoire. Il faut cependant garder en tête l’existence d’un taux de pneumothorax post-interventionnel qui peut atteindre 30%, et qui doit, le cas échéant (à savoir à partir de 2cm ou en cas d’augmentation de la taille au cours de l’évolution), être corrigé par un drainage thoracique.
Greffe de poumon
La greffe de poumon représente l’une des rares interventions avec un bénéfice avéré en termes de survie.9 Les conditions requises sont un échec préalable de toutes les options médicamenteuses, une abstinence tabagique stricte ainsi que l’absence de maladies associées sévères (par ex., maladie tumorale, maladies infectieuses systémiques, etc.).
Physiothérapie et réhabilitation
La physiothérapie est une composante cruciale du traitement de la BPCO et cible une amélioration des symptômes et des performances physiques. En cas de rétention des sécrétions, l’expectoration peut être améliorée par compression abdominale ou thoracique ou par une aide respiratoire mécanique. Grâce à des postures corporelles spéciales (position du cocher), il est possible d’utiliser la musculature aidant la respiration en cas de détresse respiratoire aiguë. La technique du «pursed-lip breathing» (expiration contre les lèvres closes) crée lors de l’expiration une pression positive dans les voies respiratoires qui facilite le dégonflement des poumons. La réhabilitation respiratoire comprend l’association de la musculation et de l’entrainement d’endurance qui permet une amélioration de la qualité de vie ainsi qu’une diminution de la détresse respiratoire et de la mortalité.10
Médecine palliative
Le traitement palliatif se concentre sur le soulagement des symptômes jusqu’à l’accompagnement dans la phase terminale de la maladie. L’administration d’oxygène, la substitution calorique, la morphine et des antidépresseurs/anxiolytiques sont disponibles entre autres, en traitement stationnaire ou à domicile via un encadrement palliatif mobile. Il faut aussi songer par avance aux limites du traitement (avec par exemple réanimation, intubation, trachéostomie) et aux documents écrits comme les directives anticipées.
Traitement médicamenteux
Le traitement médicamenteux est surtout destiné au soulagement des symptômes et à une réduction de la fréquence des exacerbations. Les bronchodilatateurs permettent une diminution de la résistance respiratoire et donc une réduction de la détresse respiratoire et de la dilatation excessive des poumons. Cela conduit à une amélioration de la fonction pulmonaire, de la qualité de vie et des performances physiques. En outre, une réduction des exacerbations aiguës est visée.
Bronchodilatation
Les bêta-2 sympathomimétiques induisent une dilatation des voies respiratoires via une activation des bêta-2 adrénorécepteurs. Les bêtamimétiques à action courte (SABA, «short acting beta agonists»; p.ex. salbutamol, fénotérol, terbutaline) sont utilisés comme médicaments on-demand rapides en cas de détresse respiratoire aiguë. Les bêtamimétiques à action longue (LABA, «long acting beta agonists»; p.ex. salmétérol, formotérol) agissent pendant plus de 12h et les principes actifs dits à action ultra-longue (p.ex. olodatérol, indacatérol) jusqu’à 24h et sont donc inhalés 1–2 fois par jour. Les effets indésirables potentiels comprennent les troubles du rythme cardiaque et les tremblements.
Les anticholinergiques dilatent les bronches via une inhibition de la bronchoconstriction parasympathique. Les molécules à action courte (SAMA, «short acting antimuscarinic antagonists»; p.ex. ipratropium) inhibent les récepteurs muscariniques M2 et les composés à action longue (LAMA, «long acting antimuscarinic antagonists»; p.ex. tiotropium, glycopyrronium, aclidinium, umeclidinium) agissent sur les récepteurs M3. Leur fenêtre thérapeutique est large, avec un profil d’effets indésirables avantageux (p.ex. rétention urinaire, sécheresse buccale, etc.).
En termes d’amélioration des symptômes, les LABA et les LAMA ne sont pas vraiment différents. Cependant, les LAMA (surtout le tiotropium) sont meilleurs pour la prévention des exacerbations.1
Corticostéroïdes en inhalation
Les corticostéroïdes en inhalation (CSI) sont efficaces pour réduire les exacerbations. Ils n’induisent pas d’amélioration pertinente de la fonction pulmonaire, mais permettent, en association avec les LABA et les LAMA, un renforcement de l’effet bronchodilatateur et de la prévention des exacerbations. Avec l’association CSI plus LABA plus LAMA (trithérapie), une diminution de la mortalité chez des patients sélectionnés a été notée par rapport au traitement par LABA plus LAMA.
L’utilisation locale réduit le risque d’effets indésirables associés aux corticostéroïdes mais il est impossible d’éviter complètement une certaine sensibilité aux infections respiratoires (à savoir pneumonies, candidoses des muqueuses). Dans les directives GOLD actuelles, la détermination de la numération des éosinophiles dans le sang est recommandée car, à partir de 300 éosinophiles/μl, une réduction du taux d’exacerbation par les CSI peut être prédite.1
Roflumilast et macrolides
En cas d’obstruction plus sévère (VEMS <50% de la valeur théorique), d’exacerbations fréquentes et de symptomatologie de type bronchitique, il est possible de baisser encore de 20% le taux d’exacerbations grâce au roflumilast (inhibiteur de la phosphodiestérase IV).11 Les effets indésirables, à savoir les nausées, la diarrhée, la perte de poids et les insomnies, doivent être prises en compte. Le cas échéant, il est possible de commencer avec une dose initiale réduite (250μg au lieu de 500μg pendant 4 semaines) et d’ajuster la dose ensuite. Chez les patients avec des exacerbations récidivantes en dépit d’un traitement intensif par inhalation, une administration à long terme de macrolides, p.ex. azithromycine (250 ou 500mg p.o. 3x par semaine) peut être envisagée.
Exacerbation
Une exacerbation aiguë se définit par une aggravation des symptômes (toux, détresse respiratoire, expectoration) nécessitant une augmentation du traitement. Elle est associée à une bronchoconstriction, une inflammation des voies respiratoires et, souvent, à une augmentation de la production de sécrétions. Les facteurs déclencheurs peuvent être des virus, des bactéries ou la pollution de l’air. Les exacerbations influencent la charge de morbidité et l’évolution longitudinale de la pathologie. En fonction de la sévérité et de l’intensité, le traitement a lieu par administration forcée de bronchodilatateurs à action courte et de corticostéroïdes systémiques; il ne faut pas dépasser une dose de 50mg d’équivalent prednisolone pendant cinq jours au maximum. En présence de signes cliniques d’infection bactérienne (augmentation de la purulence et de la quantité des sécrétions), il faut aussi instaurer une antibiothérapie.
Traitement correspondant à l’état actuel des connaissances
Le traitement «state of the art» s’oriente en fonction du classement suite à la spirométrie, de la symptomatologie individuelle et de la fréquence des exacerbations en relation avec le groupe de risque auquel appartient le patient (A, B, C ou D). Pour tous les patients, il est recommandé d’utiliser des bronchodilatateurs à action rapide (SABA ou SAMA) pour le traitement on-demand en cas de détresse respiratoire aiguë.
Dans le groupe de risque B (à savoir tableau symptomatique marqué + faible risque d’exacerbation), un bronchodilatateur à action longue, de préférence un LAMA, est recommandé comme traitement initial. En cas de contrôle insuffisant des symptômes lors de l’évolution, il faut compléter le traitement par une association LAMA/LABA.
Dans le groupe de risque C (à savoir faible tableau symptomatique + haut risque d’exacerbation), un traitement initial par LAMA est avantageux en raison de la capacité de prévention des exacerbations prouvée de cette classe de molécules. Alternativement, les associations LAMA + LABA ou LABA + CSI peuvent être utilisées.
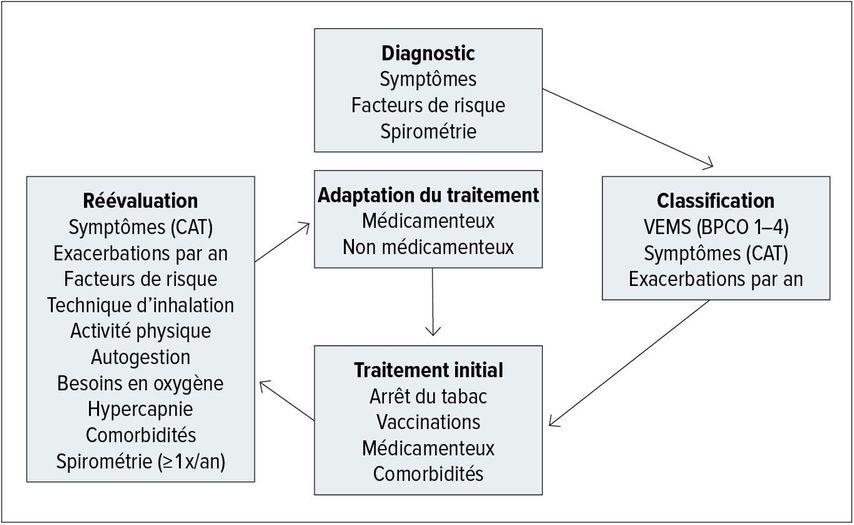
Dans le groupe de risque D (à savoir charge de morbidité élevée + exacerbations fréquentes), l’association LAMA + LABA est a priori recommandée. Si d’autres exacerbations surviennent sous ce traitement, une triple association (LAMA + LABA + CSI) doit être envisagée. Après la mise en place du traitement, il faut réévaluer régulièrement et éventuellement ajuster ce dernier (Fig. 5).
Fig. 5: Recommandation de séquence «diagnostic, classification, traitement initial, réévaluation et adaptation du traitement» en cas de BPCO (modifiée d’après le GOLD Report 2020)1
Littérature:
1 Global Initiative for Chronic Obstructive Lung Disease: Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (2020 report) 2020. www.goldcopd.org ; zuletzt aufgerufen am 28.8.2020 2 Buist AS et al.: International variation in the prevalence of COPD (the BOLD Study): a population-based prevalence study. Lancet 2007; 370: 741-50 3 Bridevaux PO et al.: Prevalence of airflow obstruction in smokers and never smokers in Switzerland. Eur Respir J 2010; 36: 1259-69 4 Divo M et al.: Comorbidities and risk of mortality in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2012; 186: 155-61 5MacNee W: Pathogenesis of chronic obstructive pulmonary disease. Proc Am Thorac Soc 2005; 2: 258-66; discussion 290-1 6Magnussen H et al.: [Guidelines for long-term oxygen therapy. German Society for Pneumology and Respiratory Medicine]. Pneumologie 2008; 62: 748-56 7 Kohnlein T et al.: Non-invasive positive pressure ventilation for the treatment of severe stable chronic obstructive pulmonary disease: a prospective, multicentre, randomised, controlled clinical trial. Lancet Respir Med 2014; 2: 698-705 8 Sciurba FC et al.: A randomized study of endobronchial valves for advanced emphysema. N Engl J Med 2010; 363: 1233-44 9Hosenpud JD et al.: Effect of diagnosis on survival benefit of lung transplantation for end-stage lung disease. Lancet 1998; 351: 24-7 10 Spruit MA et al.: An official American Thoracic Society/European Respiratory Society statement: key concepts and advances in pulmonary rehabilitation. Am J Respir Crit Care Med 2013; 188: e13-64 11 Calverley PM et al.: Roflumilast in symptomatic chronic obstructive pulmonary disease: two randomised clinical trials. Lancet 2009; 374: 685-94
Das könnte Sie auch interessieren:
Soleil et prévention cardiovasculaire
Il semble que le moment soit venu de réévaluer la situation: alors que le soleil était autrefois surtout connu pour ses bienfaits, il a fait l’objet d’une diabolisation ces dernières ...
Myocardite aiguë et cardiomyopathies inflammatoires
La myocardite aiguë et les cardiomyopathies inflammatoires sont des maladies complexes du myocarde qui nécessitent une classification étiologique et peuvent avoir des conséquences à long ...
Le rôle de l’imagerie dans la sarcoïdose cardiaque
La sarcoïdose cardiaque est une maladie cardiaque inflammatoire rare, mais importante. Le tableau clinique peut être très variable, allant de manifestations subcliniques à une gêne ...